基于德尔菲法的传染病诊断试剂遴选评价指标体系的构建
韩 丹,陈一石,任 磊,郭明明,舒丽芯*
(1.海军军医大学药学系军队药材保障论证中心,上海 200433;2.陆军第954 医院药剂科,西藏山南 856099)
0 引言
在突发传染病疫情初期进行快速且准确的病原体诊断,对于控制疫情发展和流行起着决定性作用,而建立及时高效的诊断能力,离不开高质量且能够在短时间内大规模供应的诊断试剂产品。此次新型冠状病毒感染疫情发生初期,普遍出现医疗物资筹措困难的问题,暴露出医疗物资应急储备与管理体系的缺陷[1],例如诊断试剂的生产供应能力不足,导致不能对人群做到早发现、早诊断、早治疗。目前,大多数商品化诊断试剂的研发设计面向医疗条件发达的国家和地区,要求满足基本的实验室条件、有效的维护保障、具有专业知识的卫生人员等条件,不适合在传染病频发、医疗资源有限的国家或地区应用[2]。
笔者根据世界卫生组织(World Health Organization,WHO)发布的优先关注疾病清单[3],对国内传染病诊断试剂生产企业进行相关产品的调研,构建了传染病诊断试剂产品数据库。截至2022 年10 月,国家药品监督管理局已经批准34 个新型冠状病毒抗原检测试剂盒、41 个新型冠状病毒核酸检测试剂盒、39 个新型冠状病毒抗体检测试剂盒,12 个仪器设备,2 个软件产品[4]。这些产品的上市,为有效应对突发传染病疫情提供了坚实的基础,然而我国诊断试剂产品种类较多,制定科学合理的诊断试剂遴选和储备方案是国家卫生行政部门面临的难题。本研究在传染病诊断试剂产品数据库的基础上,使用德尔菲专家咨询法,探讨并构建一套可对传染病诊断试剂进行多维度评价、指标释义清晰的遴选评价指标体系,为传染病诊断试剂的遴选和储备提供参考依据。
1 方法
1.1 专家遴选
专家遴选纳入标准:(1)本科及以上学历;(2)副高及以上职称;(3)从事传染病防治相关工作10 a 以上,能针对本研究提出建设性意见;(4)自愿参加并能确保在规定的时间内参与咨询。
1.2 问卷设计
前期在对诊断试剂遴选相关法律法规、政策文件及文献资料进行收集整理的基础上,通过文献研究,参考国内外文献中影响诊断试剂结果真实性、安全性、可及性等的因素,将敏感性和适用性较好的指标纳入本研究,初步确定专家问卷基本框架及调研内容。设计《传染病诊断试剂遴选评价指标体系咨询问卷》(包括5 个一级指标、30 个二级指标),一级指标包括真实性、安全性、创新性、可及性、勤务适用性,二级指标包括检测灵敏度、检测特异度、可靠性、诊断环境安全等。
咨询问卷采用Likert5 级评分法,将专家对指标的评价分为不重要、不太重要、一般重要、比较重要、非常重要5 个等级,赋值分别为1 分、2 分、3 分、4 分、5 分;专家还可对指标提出修改、增加或删除等意见。
1.3 德尔菲法
本研究于2022 年8—9 月对20 位专家实施2轮德尔菲专家咨询。第1 轮通过电子邮件方式向专家发送《传染病诊断试剂遴选评价指标体系咨询问卷》,要求在2 周内反馈,由2 名工作人员进行数据录入和整理,分别计算各指标专家评分的均值()、标准差(s)、变异系数(coefficient of variation,CV)。第2 轮在第1 轮的基础上构建咨询问卷,并附上第1轮专家咨询结果,再次通过电子邮件方式发送给专家。
1.4 统计学分析
问卷结果采用Excel 2022、SPSS 22.0 软件进行数据整理分析。采用、s、CV 等进行描述性分析。
2 结果
2.1 专家基本情况
本研究共纳入20 名专家,其中男性10 人(50%)、女性10 人(50%);年龄在31~40 岁的4 人(20%),>40~50 岁的12 人(60%),>50 岁的4 人(20%);本科学历1 人(5%),硕士学历2 人(10%),博士及以上学历17 人(85%);工作单位在院校、科研机构的13 人(65%),在医疗机构的6 人(30%),在监管机构的1 人(5%);工作年限为10~20 a 的7 人(35%),20 a 以上的13 人(65%);20 位专家中有3 位专家接受了预调查。
2.2 专家积极程度
专家积极程度用问卷有效回收率表示,回收率>50%可对数据进行分析。本研究2 轮德尔菲专家咨询均发出问卷20 份,回收20 份,有效回收率100%,专家积极系数为1,且专家咨询持续时间在2 周内,说明专家的积极性较高。
2.3 专家权威程度
专家权威程度用权威系数(Cr)表示,由专家判断依据(Ca)、专家熟悉程度(Cs)2 个因素决定,Cr=(Ca+Cs)/2。Ca 分为理论分析、实践经验、同行了解、直觉4 个等级,Cs 分为非常熟悉、比较熟悉、一般熟悉、不太熟悉、不熟悉5 个等级,最终纳入指标需符合Cr≥0.7[5]。第1 轮专家咨询中,Ca=0.78,Cs=0.82,Cr=0.80;第2 轮专家咨询中,Ca=0.80,Cs=0.89,Cr=0.85。2 轮专家咨询中Cr 均>0.70,说明专家对咨询内容的权威程度较高,咨询结果比较可靠。
2.4 专家协调程度
专家协调程度用肯德尔和谐系数W 判断,W 可以检验专家对评价内容的协调程度及意见的一致性,W 取值范围为0~1 之间,以P<0.05 为差异有统计学意义,W 取值越接近1,说明专家的认同度较高,专家协调程度越好,一般要求W>0.4[6]。第1 轮咨询中,一级指标W 为0.554,二级指标W 为0.448,P 值均小于0.05;第2 轮咨询中,一级指标W 为0.569,二级指标W 为0.521,P 值均小于0.05。上述结果表明专家对指标重要性的认识趋向一致,评估意见协调性好,结果可取。
2.5 指标体系的筛选
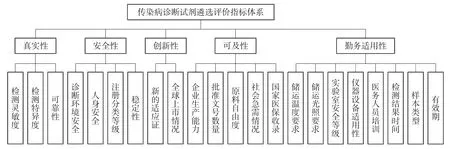
图1 传染病诊断试剂遴选评价指标体系层次结构图
2.6 指标权重的确定
专家对各指标进行重要性评分的同时还对各一级指标的权重进行赋值,一级指标权重合计100%。假设将专家i 对二级指标j 的重要性评分记为Pij(i为专家编号,j 为二级指标编号),专家i 的权威程度系数记为Ci,以权威程度系数为权数,计算每个二级指标得分的加权平均数j,公式为
通过公式计算出各二级指标得分的加权权重,并对其进行归一化处理,得到归一化权重,将二级指标归一化权重与对应的一级指标权重相乘,可得到二级指标的组合权重,即为最终权重[8],详见表1。
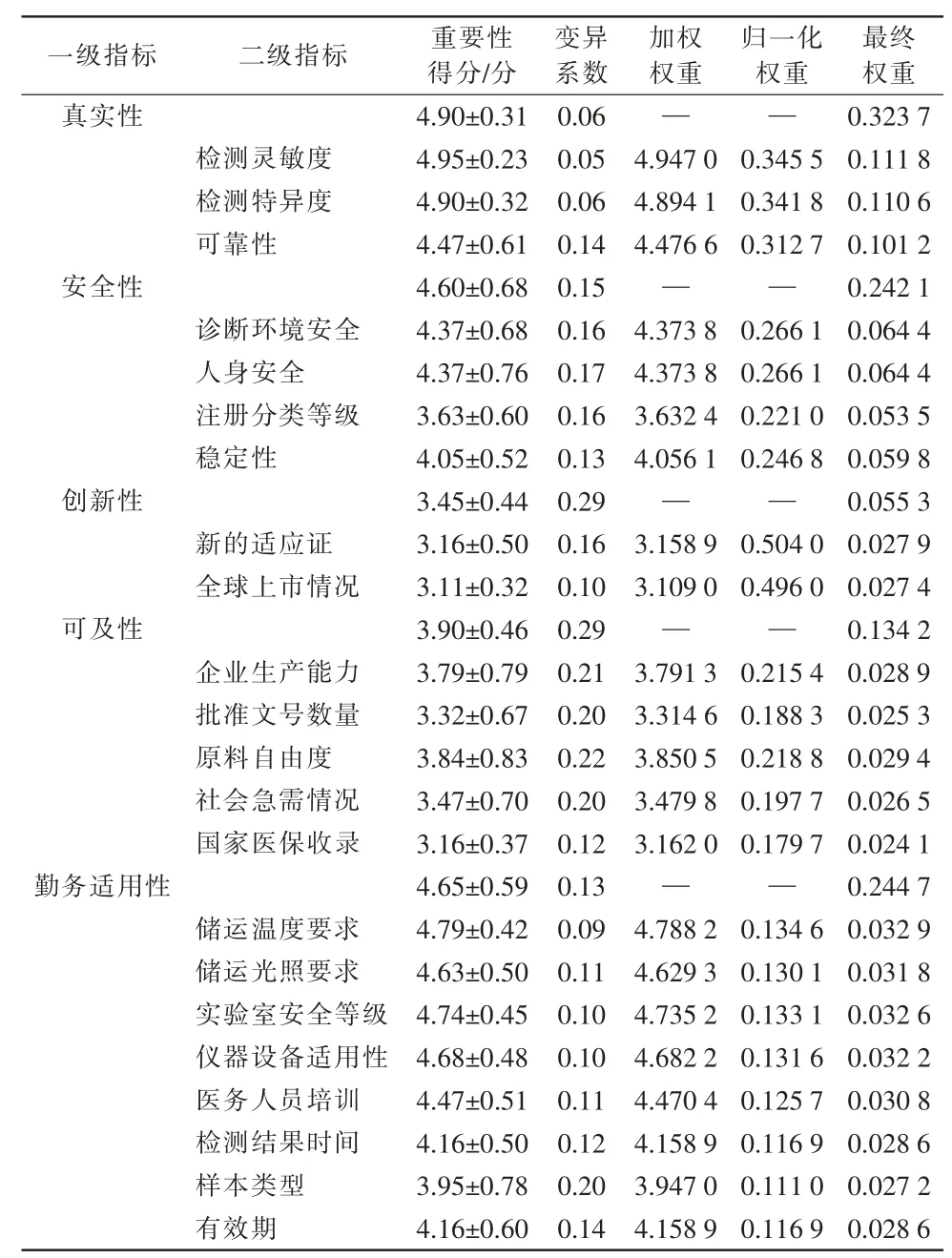
表1 传染病诊断试剂遴选评价指标体系及指标权重
3 讨论
3.1 指标体系的权威性分析
德尔菲法通过咨询问卷与专家建立良好的信息反馈,是广泛征求专家意见的决策方法之一[9]。本次研究共选取20 名专家进行德尔菲专家咨询,从专家基本情况来看,专家的年龄、学历、职称、工作单位、工作年限以及研究领域等能够有效互补,且专家来自院校、科研机构、医疗机构、医疗器械监管机构等不同级别单位,符合德尔菲法对专家的遴选条件。本研究2 轮专家积极系数均为1,Cr>0.70,W>0.4,表明专家对指标体系的积极性较高,研究结果具有较好的权威性和可靠性。
3.2 一级指标的内容分析
WHO 提出了传染病诊断试剂研发的7 项原则,即可负担性、灵敏度高、特异度高、易操作、检测速度快且适应性强、无设备要求和可及性强[7]。本研究结合WHO 研发原则以及文献研究中关于诊断试剂的特点,设计了包含5 个一级指标的指标体系。5 个一级指标的权重分别为:真实性0.323 7,安全性0.242 1,创新性0.055 3,可及性0.134 2,勤务适用性0.244 7,专家对诊断试剂的真实性、勤务适用性、安全性权重赋值相对较高,诊断试剂的这3 个指标是遴选评价的重要组成部分,这与以往的研究和大众的认知相符[10]。本研究将诊断试剂的可及性和创新性纳入诊断试剂遴选评价的指标范畴,可及性指标主要考察诊断试剂的可获得性和可负担性,即当具有相同真实性和安全性数据时,应选择花费较低、经济性较好、容易获得的产品。创新性通常代表着诊断试剂的不可替代性,但诊断试剂属于特殊的商品,真实性和安全性是最基本的要求,虽然创新性和可及性指标纳入评价的标准,但不能强制执行,故创新性和可及性的权重较低。
3.3 二级指标的内容分析
一级指标真实性下权重最高的二级指标是检测灵敏度和检测特异度,这2 个指标较好地解释了诊断试剂真实性的特性。真实性是指测量值与实际值符合的程度,是可以定量的核心技术指标,强调了检测结果的准确程度。灵敏度与正确检出阳性患者的能力密切相关,灵敏度越高,假阴性越少;特异性则代表正确检出阴性患者的能力,特异性越高,假阳性越少[11]。例如某公司生产的新型冠状病毒抗原检测试剂盒灵敏度达到97%以上、特异度达到99%以上时,产品真实性较高,可为疑似人群在早期分流和快速诊断方面提供强有力的保障[12]。
一级指标安全性下包括诊断环境安全、人身安全等二级指标,诊断环境安全即诊断试剂对环境污染的程度,人身安全指诊断试剂虽然不直接作用于人体,但其对操作者或直接接触者健康有影响。例如,针对预防突发传染病的诊断试剂,如果其本身不慎直接接触可能会引起安全问题,或者存在通过污染环境而间接导致安全问题发生的风险,那么在进行遴选时,就必须对其进行限制和谨慎评估。
原料自由度、企业生产能力是一级指标可及性下权重较高的2 个指标,说明诊断试剂的原材料自由度和生产企业生产能力对可获得性尤为重要。自新型冠状病毒感染疫情发生以来,国务院联防联控机制医疗物资保障组发挥了重要的协调和支持作用,促进了疫情防控所需医疗物资的生产和供应,满足了国内疫情防控的需要。
一级指标勤务适用性下,储运温度要求的权重被赋予较高的分值,这是因为不同种类的诊断试剂对温度的敏感性不同,诊断试剂需要在特定的温度条件下储存和运输,以保证试剂的稳定性和检测结果的准确性。另外,实验室安全等级的权重也较高,其重要性体现在诊断试剂在检测不同级别病原体样本时需要在匹配的生物安全实验室中操作,例如新型冠状病毒的样本检测必须在P2 级或以上实验室进行,而埃博拉病毒的样本检测则需要在P4 级实验室进行。诊断试剂分为单独使用、与通用设备组合使用或与特定设备组合使用3 种情况,为满足突发传染病时对人员实施快速检测或应急状态下小型医疗队携行的需要,原则上应尽量选择机动、小型、便携式的诊断试剂。检测速度快也是一项重要指标,例如某公司生产的新型冠状病毒核酸检测试剂盒,采样后30 min 内即可出检验结果[13]。总体来说,在勤务适用性方面,无需特定设备、储存温度可控、样本收集无特殊要求、操作简便且检测结果时间短的诊断试剂,更适合在医疗条件有限的情况下使用。
4 结语
目前,国内关于传染病诊断试剂遴选评价指标体系的研究较少,本研究构建了由5 个一级指标和22个二级指标构成的遴选评价指标体系,该体系采用定性和定量相结合的方法,从多角度体现了诊断试剂的临床价值,符合构建指标体系的基本原则。本研究仅为初步探索,基于诊断试剂遴选评价的影响因素众多,指标的调整与人们的主观认识密不可分,研究具有一定的片面性。研究的统计学结果表明指标体系具有较好的权威性和可靠性,今后将选取2~3 种诊断试剂对该指标体系进行实证研究,进一步测试指标体系的适用性,为传染病诊断试剂的遴选提供参考依据。

