人促红素中二聚体及高分子量物质的质量研究
唐 娜 贾丽华 宋 莉 陈统华 苏超男 王嫦鹤
陕西省食品药品检验研究院,陕西西安 710065
人促红素是用基因重组技术构建CHO 细胞,高效表达并且能刺激红细胞生成的糖蛋白,临床用于肾功能不全所致贫血、非骨髓恶性肿瘤化疗引起的贫血、外科围手术期红细胞动员等症状的治疗[1-6]。高分子量物质是在药物生产和贮存过程中产生的高分子聚合物,在临床中会引起不良反应,也是引起过敏反应的主要原因[7-10]。
《中华人民共和国药典》2020 年版三部并未对人促红素原液及注射液的二聚体及高分子量物质进行控制[11],为确保临床用药的安全性,保证药品的质量,从质量控制角度需增加高分子量物质检查项,本研究参照《英国药典》[12]和《欧洲药典》[13]的方法,建立了体积排阻色谱法测定人促红素原液中的二聚体及高分子量物质,并进行了方法学验证,表明该方法专属性强,灵敏度高,可为人促红素原液及注射剂中二聚体和高分子量物质的质量控制提供参考。
1 仪器与试药
1.1 主要试剂及仪器
无水磷酸氢二钠(批号:20210528)、磷酸二氢钾(批号:20210530)氯化钠(批号:20220616)均购自国药集团化学试剂有限公司。水为高纯水。色谱柱TSKgel G3000SW(7.5 mm×60 cm,10 μm)。Waters/Arc 高效液相色谱仪及Empower 工作站,梅特勒S220 酸度计,梅特勒公司XPR205 电子分析天平。
1.2 供试品及对照品
共收集到9 家国内生产企业(企业A ~I)的人促红素原液共计24 批;处方中不含人血白蛋白的人促红素注射液3 批,其中来自1 家国内生产企业(企业D)的人促红素注射液2 批(D4 和D5),1 家进口生产企业(企业J)的人促红素注射液1 批。EPO-SEC CRS 欧洲标准品(欧洲药品和保健质量理事会,批号:00VdTS)。
1.3 色谱条件
采用TSKgel G3000SW 色谱柱;流动相为磷酸盐缓冲液(磷酸二氢钾0.2 g、无水磷酸氢二钠1.2 g 和氯化钠23.5 g,加水溶解并稀释成1000 ml,调节pH 值至7.4);流速为0.5 ml/min;检测波长为214 nm;进样量为50 μl;柱温为30℃;样品池温度为8℃;保留时间为单体峰保留时间的2 倍。系统适用性要求二聚体与单体峰之间的分离度应>1.5。对照品溶液的单体峰面积为分离度溶液单体峰面积的1.5%~2.5%。
1.4 溶液的配制方法
1.4.1 供试品溶液的配制 取供试品,按照供试品的蛋白质含量用流动相稀释制成含蛋白0.4 mg/ml的溶液,混匀,作为供试品溶液。
1.4.2 分离度溶液 取EPO-SEC CRS 欧洲标准品1 瓶(蛋白含量100 μg),精密加入250 μl 流动相,用流动相溶解并稀释制成0.4 mg/ml 溶液,作为分离度溶液。
1.4.3 对照品溶液 精密量取分离度溶液20 μl,加980 μl 流动相稀释制成0.008 mg/ml 溶液,混匀,作为对照品溶液。
2 结果
2.1 系统适用性
精密量取分离度溶液和对照品溶液各50 μl,分别注入液相色谱仪,记录色谱图,测定分离度和峰面积比。结果显示单体峰的保留时间约为30 ~35 min。对照品溶液的单体峰面积为分离度溶液单体峰面积的1.5%~2.5%,分离度溶液中二聚体与单体峰之间的分离度均大于1.5,见图1,表明方法适用性良好。
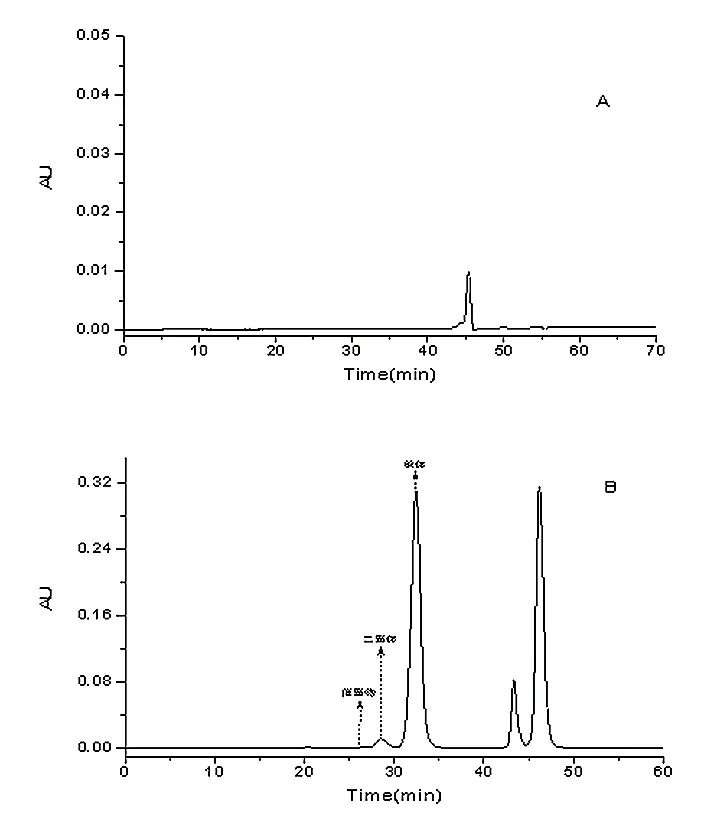
图1 HPLC 色谱图
2.2 专属性
根据生产企业的工艺处方,取枸橼酸、枸橼酸钠、氯化钠等辅料适量,配制辅料空白,称取适量,用流动相溶解并过滤,作为辅料空白溶液。取辅料空白溶液、流动相和对照品溶液各50 μl,分别注入液相色谱仪,按照“1.3”项下的方法进样分析,记录色谱图。结果显示各辅料在主峰出峰位置均无干扰峰,见图1,表明方法专属性良好。
2.3 重复性
取同一批人促红素原液,按照“1.4.1”项下配制6 份供试品溶液,按照“1.3”项下的方法进样分析,记录色谱图。二聚体及高分子量物质含量的RSD 为1.95% ,见表1,表明方法的重复性良好。

表1 重复性测定结果
2.4 检测限
取对照品溶液,加流动相逐步稀释,按照“1.3”项下的方法进样分析,考察检测限。以信噪比S/N ≥3为检测限,结果显示S/N 约为3.4,单体峰浓度为0.002 mg/ml 为检测限。
2.5 稳定性
取同一批人促红素原液,按照“1.3”和“1.4”项下的方法,制备供试品溶液,分别在0、2、4、6、8、12、24 h 进样分析,记录色谱图。峰面积的RSD 值为0.92%,见表2,结果表明供试品溶液在24 h 内稳定。
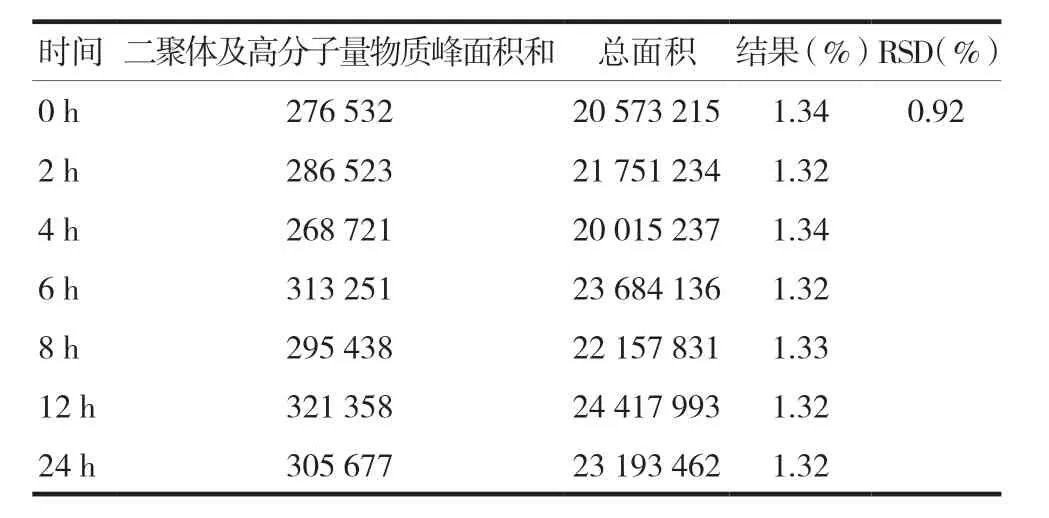
表2 稳定性测定结果
2.6 样品的测定
取24 批人促红素原液和3 批人促红素注射液,按照“1.4.1”项下制备供试品溶液,按照“1.3”项下的方法进样分析,记录色谱图。24 批人促红素原液和3 批人促红素注射液二聚体及高分子量物质的测定结果分析见图2。结果表明除2 个企业的原液未检出外,其余各厂家的原液均有检出,按面积归一化法计算二聚体及高分子量物质的含量均在2.0%以下。3 批人促红素注射液均未检出。其中企业D 的原液和注射液均未检出二聚体及高分子量物质,企业I 原液的二聚体及高分子量物质的含量最高。见图2。
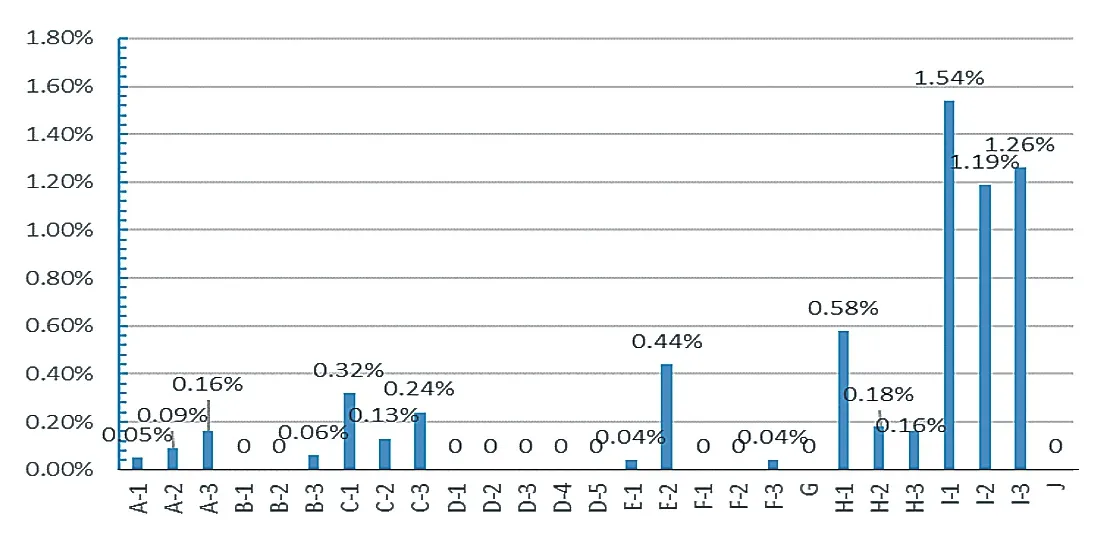
图2 各企业原液中二聚体及高分子量物质统计图
3 讨论
本研究收集了9 家生产企业和1 家进口企业的人促红素原液和注射液共计27 批样品,我国批准的人促红素注射剂(包括注射用和注射液)涉及11 家国内生产企业,本研究收集到的样品共涉及9 家国内生产企业,1 家进口生产企业,样品涵盖了82%的国内生产企业;从数据的结果来看,不同企业的生产工艺不同,可能会导致其产品中二聚体及高分子量物质的残留量的差异,其中企业I 的人促红素原液样品二聚体及高分子量物质含量最高,应引起重视,从生产工艺等各环节考察产生二聚体及高分子量物质的原因。因此有必要从源头开始进行严格的控制,以保证最终注射液产品的安全。建议在人促红素原液标准中增加二聚体及高分子量物质的检查项,参照《英国药典》和《欧洲药典》的限度要求,将该项目的限度暂定为2.0%。
高分子量物质在临床使用中会引起不良反应,是引起过敏反应的主要原因[14-18],有必要在标准中进行控制。目前尚无文献报道人促红素中的二聚体及高分子量物质的测定方法。药品中二聚体的检测方法大多采用排阻色谱法进行测定。现行标准《中华人民共和国药典》2020 年版三部和各个企业的标准均未对人促红素原液的二聚体及高分子量物质进行控制,本研究采用体积排阻色谱法增加了系统适用性试验要求,能够有效地控制人促红素原液中的二聚体及高分子量物质的含量,该方法操作简便、快捷,灵敏度高,重现性好。
综上所述,本研究建立了体积排阻色谱法测定人促红素原液中的二聚体及高分子量物质的方法,能够有效控制人促红素原液中的二聚体及高分子量物质的含量,严把质量标准关,保证用药安全。

