壮药前列舒外洗剂质量标准研究
黄蓓 符军 黄鸿敖 梁国成 韦世民

【摘 要】 目的:建立壮药前列舒外洗剂质量标准,并进行洗剂的常规检查。方法:对壮药前列舒外洗剂进行最低装量及微生物限度检查;采用薄层色谱法鉴别壮药前列舒外洗剂中姜黄、三叉苦;采用紫外可见分光光度法测定壮药前列舒外洗剂总黄酮的含量。结果:壮药前列舒外洗剂最低装量、微生物限度检查均符合2020年版《中国药典》的相关规定;薄层色谱中,姜黄、三叉苦的特征斑点显色清晰,分离效果好,阴性对照无干扰;以HCl-Mg法显色,芦丁为对照品,282 nm波长条件下测定,芦丁在22.18~133.08 μg/mL浓度间呈良好的线性关系好(R2=0.9995,n=6),样品平均回收率98.14%(RSD=1.04%,n=6)。结论:所建立的质量标准操作简单、重复性好,可用于壮药前列舒外洗剂的质量控制。
【关键词】壮药前列舒外洗剂;薄层色谱法;紫外可见分光光度法;质量标准
【中图分类号】R284.1 【文献标志码】 A【文章编号】1007-8517(2023)11-0040-05
Abstract:Objective To establish the quality standard of Zhuang Medicine Qianlieshu lotion and to conduct routine examination of the lotion.Methods The minimum quantity and microbial limit of Qianlieshu lotion were examined,and the turmeric and Trischia in Qianlieshu lotion were identified by Thin layer chromatography The content of total flavonoids in Qianlieshu lotion was determined by UV-Vis Spectrophotometer.Results the minimum loading and microbial limit of Qianlieshu lotion were in accordance with the relevant regulations of Chinese pharmacopoeia (2020 edition),and the characteristic spots of turmeric and trisporia were clearly displayed in TLC,HCl-Mg method was used for the determination of rutin at 282 nm wavelength,rutin showed a good linear relationship between the concentrations of 22.18-133.08μg/mL (R2=0.9995,n=6),and the average recovery was 98.14%(RSD=1.04%,n=6),it can be used for quality control of Qianlieshu lotion.
Keywords:Zhuang Medicine Qianlieshu External Lotion;Thin Layer Chromatography;Ultraviolet Visible Spectrophotometer;Quality Standard
壮药前列舒外洗剂是广西中医药大学附属瑞康医院药物研发中心与男性科结合中医药理论和壮医药理论研制的用于治疗慢性前列腺炎的壮药制剂,用法为外用坐浴。该洗剂由马鞭草、扛板归、了哥王、三叉苦、半枝莲、鬼针草、姜黄等九味壮药材组成,具有清热、祛湿、活血化瘀、缓解疼痛的功效,外洗可用于慢性前列腺炎的治疗,临床应用及实验研究表明其具有确切的疗效[1-4]。为控制制剂质量,研究采用薄层色谱法对其中姜黄、三叉苦进行定性鉴别,采用紫外可见分光光度法测定壮药前列舒外洗剂总黄酮的含量,并对其进行最低裝量及微生物限度检查,建立简便可行的质量控制方法。
1 仪器与试药
1.1 仪器 WHF-205B可见透射紫外反射仪(上海精科实业有限公司);CQ-250超声波清洗剂(上海跃进医用光学器械厂);AL204电子天平(梅特勒-托利多仪器(上海)有限公司);GZX-DH-30×35电热恒温干燥箱(上海跃进医疗器械厂);UV-1800PC紫外可见分光光度计(上海美谱达仪器有限公司)。
1.2 材料 姜黄素对照品(批号:110823-201706中国食品药品检定研究院);三叉苦对照药材(批号:121682-201301,中国食品药品检定研究院);芦丁对照品(批号:100080-201811,中国食品药品检定研究院);水为自制纯化水,其余试剂均为分析纯。壮药前列舒外洗剂(批号:20220104、20220107、20220111,广西中医药大学附属瑞康医院药物研发中心配制)。
2 方法与结果
2.1 薄层鉴别
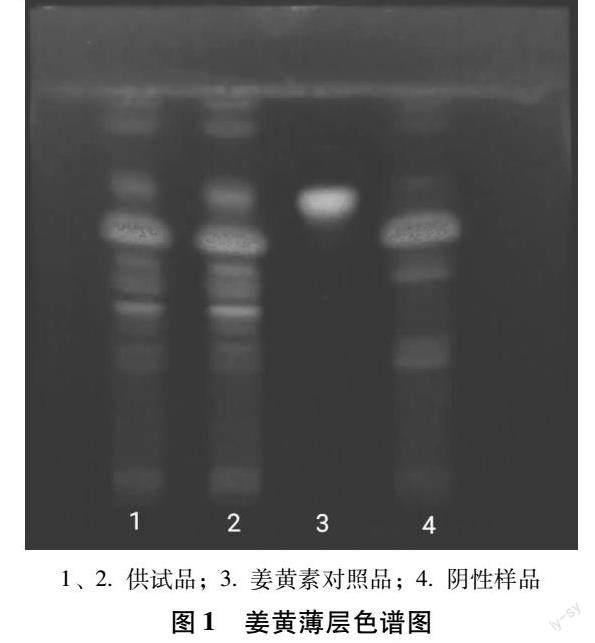
2.1.1 姜黄薄层鉴别 取壮药前列舒外洗剂10 mL,浓缩至5 mL,加入50 mL三氯甲烷,超声30 min后倒入分液漏斗中,待分层后取下层溶液,水浴蒸干,残渣加2 mL三氯甲烷使溶解,作为供试品溶液。取缺姜黄阴性样品,按供试品溶液制备方法同法制得缺姜黄阴性样品溶液。另取姜黄素对照品,加无水乙醇制成每1 mL含0.5 mg姜黄素的溶液,作为对照品溶液。照薄层色谱法(2020年版《中国药典》第四部通则0502)试验[5],吸取供试品溶液和阴性样品溶液各7 μL、对照品溶液2 μL,分别点于同一硅胶G薄层板上,以石油醚-三氯甲烷-甲醇-甲酸(2∶10∶0.7∶0.4)为展开剂,展开,取出,晾干,置365 nm紫外光灯下检视。供试品色谱中,在与对照品色谱相应的位置上,显相同颜色的斑,阴性样品无干扰。如图1所示。
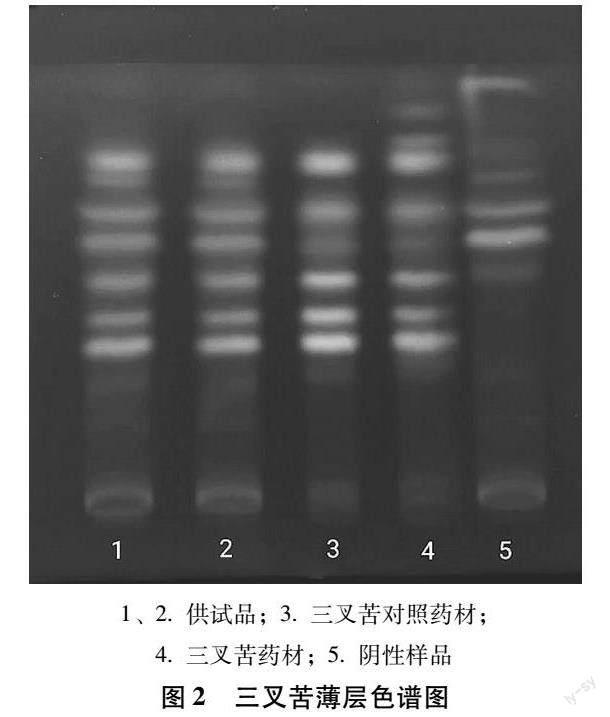
2.1.2 三叉苦薄层鉴别 取壮药前列舒外洗剂15 mL,浓缩至2 mL,加入50 mL乙醇,加热回流1 h,过滤,滤液蒸干,残渣加纯化水40 mL,超声处理20 min,过滤,滤液用乙酸乙酯萃取2次,每次20 mL,合并乙酸乙酯液,蒸干,残渣加2 mL甲醇使溶解,作为供试品溶液。取缺三叉苦阴性样品,按供试品溶液制备方法同法制得缺三叉苦阴性样品溶液。取三叉苦对照药材粉末1 g,加50 mL乙醇,按供试品溶液制备方法同法制得三叉苦对照药材溶液。照薄层色谱法(2020年版《中国药典》第四部通则0502)试验,吸取上述3种溶液各10 μL,分别点于同一硅胶G薄层板上,以甲苯-乙酸乙酯-甲酸-水(5∶5∶1∶ 0.5)静置30 min后的上层溶液为展开剂,展开,取出,晾干,置254 nm紫外光燈下检视。供试品色谱中,在与对照药材色谱相应的位置上,显相同颜色的斑,阴性样品无干扰。结果如图2所示。
2.2 总黄酮含量测定
2.2.1 对照品溶液和供试品溶液制备 精密称取12.0 mg芦丁对照品(供UV法测定,含量为92.4%)置50 mL容量瓶中,加入70%乙醇45 mL,超声溶解后加70%乙醇至刻度,摇匀,制备成含量为0.2218 mg/mL的对照品溶液。精密量取1 mL壮药前列舒外洗剂于50 mL容量瓶中,加70%乙醇至刻度,超声1 h后加70%乙醇补足至刻度,振摇均匀,过滤,收集续滤液即为供试品溶液。
2.2.2 测定方法 取供试品溶液1 mL、对照品溶液 2 mL 置加有0.3 g镁粉的具塞刻度试管中,将试管置冷水浴中缓慢滴加3 mL浓盐酸,并不时振摇试管,最后加入70%乙醇至10 mL刻度处,沸水浴中加热1 h,取出置冷水中迅速冷,用70%乙醇补足至10 mL,以试剂为空白,按照2020年版《中国药典》紫外分光光度法立即在 200~700 nm扫描。结果供试品与芦丁在 282 nm左右皆有最大吸收峰,且峰形对称(如图3所示),与查阅的文献一致[6],故选择以芦丁为对照品在282 nm处测定供试品吸光度。
2.2.3 线性关系考察 精密量取芦丁对照品溶液1 mL、2 mL、3 mL、4 mL、5 mL、6 mL,分别置于加有0.3g镁粉的具塞刻度试管中,按2.2.2的方法测定吸光度A,以芦丁对照品的浓度(mg/mL)为横坐标,以吸光度(A)为纵坐标,绘制标准曲线,得到标准曲线Y=1.6475X-0.0003(R2=0.9995,n=6),结果表明芦丁在 0.02218~0.13308 mg/mL范围内呈良好线性关系(如图4所示)。
2.2.4 精密度考察 取同一供试品溶液经2.2.2项方法处理后,在282 nm波长处重复测定吸光度6次,结果分别为:0.462、0.458、0.459、0.460、0.458、0.463,RSD =0.46%,表明仪器精密度良好。
2.2.5 重复性考察 取平行制备的供试品溶液6份,再分别精密吸取1 mL按2.2.2项下方法在282 nm处测定吸光度,结果分别为:0.460、0.448、0.459、0.451、0.466、0.450,RSD=1.55%,表明本方法重复性良好。
2.2.6 稳定性考察 取同一供试品测定液,放置0 min、30 min、60 min、90 min、120 min、180 min,后在282 nm波长处测定其吸光度,结果分别为:0.462、0.460、0.463、0.461、0.459、0.458,RSD=0.41%,说明供试品溶液在180 min内稳定性良好。
2.2.7 加样回收率试验 精密量取6份已知总黄酮含量(mg/mL)的供试品溶液各1 mL,再分别精密加入0.5mL的对照品溶液( 0.2218 mg/mL),按2.2.2方法测定吸收度A,计算回收率。结果见表1。
2.2.8 样品含量测定 取3批壮药前列舒外洗剂各1 mL共6份,按2.2.1项制备供试品溶液,再取1 mL供试品溶液按2.2.2 项方法在282 nm波长处测定其吸光度,计算样品中的总黄酮含量见表2。
2.3 最低装量检查 按照2020年版《中国药典》四部通则0942“最低装量检查法”检查3批壮药前列舒外洗剂。取每批供试品各3瓶,将内容物转移至预经标化的250 mL干燥量筒中。读出每个容器内容物的装量,并求其平均装量,平均装量应不少于标示装量200 mL,每瓶装量应不少于标示装量的97%(194 mL),结果均符合规定。见表3。
2.4 微生物限度检查
2.4.1 供试液制备 取壮药前列舒外洗剂10 mL,加含5%聚山梨酯80的pH7.0无菌氯化钠-蛋白胨缓冲液,制成1∶10供试液。
2.4.2 检查方法 依照2020年版《中国药典》四部通则1105、1106 “非无菌产品微生物限度检查方法”检查。
2.4.3 需氧菌总数检查 取1∶10供试液1 mL注皿,依法检查。
2.4.4 霉菌和酵母菌总数 取壮药前列舒外洗液原液1 mL注皿,依法检查。
2.4.5 控制菌检查 取1∶10供试液10 mL,接种至胰酪大豆胨液体培养基100 mL中,依法检查金黄色葡萄球菌、铜绿假单胞菌。
2.4.6 三批壮药前列舒外洗剂的微生物限度检查 按上述所建立的微生物限度检查法,对三批壮药前列舒外洗剂进行检验。结果见表4。
3 讨论
3.1 薄层色谱研究 由于壮药前列舒外洗剂由多种壮药水提制成,成分多样复杂,而且各种化学成分相互干扰的情况十分常见,再加上多种药材含有相似的黄酮类成分,薄层鉴别过程中极易出现阴性干扰,阻碍了薄层鉴别研究进程。本实验曾对方中杠板归、了哥王、马鞭草、绞股蓝进行薄层色谱鉴别研究,均出现阴性干扰情况,姜黄、三叉苦的薄层色谱鉴别特征斑点显色清晰,分离效果好,阴性对照无干扰,鉴别方法分离度好,稳定性高,可行性强。
3.2 显色方法选择 紫外分光光度法测定总黄酮含量常用的显色法有直接测定法[7]、NaNO2-AlNO3-NaOH法[8-9]、AlCl3 法[10-11]、HCl-Mg法[6、12]等4种方法。实验对比了以上几种方法,结果表明,直接测定法试剂吸收峰与供试品吸收峰相邻太近,影响大;NaNO2-AlNO3-NaOH 法中,供试品溶液加入4%NaOH溶液立即出现絮状沉淀,且供试品溶液在对照品溶液的最大吸收波长处无吸收峰;AlCl3 法供试品溶液在对照品溶液的最大吸收波长处也无吸收峰;HCl-Mg法供试品溶液与芦丁对照品溶液在282 nm左右有最大吸收,且峰形对称,故选择HCl-Mg法为壮药前列舒外洗液总黄酮含量测定的显色方法。
3.3 供试品溶液提取方法选择 供试品溶液的提取方法曾选用超声波提取法、回流提取法、正丁醇提取法进行比较,结果正丁醇提取法制备的供试液总黄酮含量较低,超声提取和回流提取率差别不大,但超声提取时间快,效率高,故选用超声提取法。
3.4 壮医理论基础 壮医认为毒邪是导致疾病发生的重要原因,慢性前列腺炎发病多为人体受到痧、瘴、毒、火、湿等邪毒侵犯,致天、人、地三气同步失调,从而导致水道、气道病变及龙路和火路功能失调,致咪隆(脾)、咪腰(肾)和咪叠(肝)三脏功能失常为主。基于壮医理论对慢性前列腺炎的认识,广西中医药大学附属瑞康医院研发了壮药前列舒外洗剂对慢性前列腺炎患者进行熏洗治疗,全方由马鞭草、了哥王、杠板归、三叉苦、绞股蓝、姜黄等组成,方中三叉苦祛风湿、除湿毒;了哥王清热解毒、消肿止痛、软坚散结;杠板归利水消肿;绞股蓝清热解毒、补脾益气、调气道;以上诸药合用,作用于龙路、火路,疏通瘀滞,祛湿解毒,恢复“三道两路”同步,从而达到治疗目的。我院男性科自2011年以来,采用壮药前列舒外洗方治疗慢性前列腺炎,取得了很好的疗效,将壮药前列舒外洗方方开发成院内制剂,并制定其质量标准对推动民族壮医药特色疗法治疗慢性前列腺炎具有十分重要的意义。
综上,研究旨在对壮药前列舒外洗剂进行质量标准的研究,为该制剂的质量标准提供一定的科学依据,并将这一经验方开发成院内制剂,以便将壮药理论与临床治疗相结合,方便患者使用,为临床治疗慢性前列腺炎提供一种新的特色壮药制剂。但因方中含有多味壮药材,成分复杂,再加上多种药材含有相似的黄酮类成分,干扰成分较多。研究采用薄层色谱法对姜黄、三叉苦进行定性鉴别,采用紫外可见分光光度法测定壮药前列舒外洗剂总黄酮的含量,建立简便可行的质量控制方法。今后研究可增加其他药味的薄层色谱鉴别及主要药效成分的含量测定,进一步完善壮药前列舒外洗剂的质量标准。
参考文献
[1]戴芳,陆智华,朱闽,等.壮药前列舒外洗剂对ⅢA型前列腺炎患者相关细胞因子表達水平的影响[J].西部中医药,2021(8):136-138.
[2]朱闽,荀建宁,覃兆伟,等.壮药前列舒外洗剂治疗慢性前列腺炎的临床研究[J].西部中医药,2015,28(8):57-59.
[3]朱闽,荀建宁,覃兆伟,等,壮药前列舒外洗剂治疗慢性前列腺炎的临床观察[J].中国性科学,2014,23(9):62-65.
[4]朱闽,荀建宁,覃兆伟.壮药前列舒外洗剂治疗Ⅲ型前列腺炎40例临床观察[J].中国当代医药,2010,17(36):57-58.
[5]国家药典委员会编.中华人民共和国药典(四部)[S].北京:中国医药科技出版社,2020:39-40.
[6]热毛先,热增才旦,周加本,等.藏药甘青青兰总黄酮含量测定方法对比研究[J].中国民族医药杂志,2021(6):49-51.
[7]胥秀英,吉光见稚代,石诚岑,等.红花配方颗粒制备及总黄酮含量测定研究[J].时珍国医国药,2020(1):109-110.
[8]韦瑀龙,黄小鸥,蓝晓庆.固本补肾口服液的总黄酮含量测定方法研究[J].实用药物与临床,2016(10):1287-1289.
[9]郝少君,李文俊,高延玲,等.复方黄栌口服液中总黄酮含量测定方法[J].实用医药杂志,2017(11):1024-1026.
[10]张莹,傅静,王孝勋,等.把天门化学成分预试验及其总黄酮含量测定[J].湖北农业科学,2021(3):137-140,192.
[11]张明,陈华国,赵超,等.杠板归中总黄酮的含量测定[J].中国实验方剂学杂志,2012(18):77-80.
[12]党晓芳,曹飒丽,祁娟娟,等.鬼箭羽总黄酮含量测定方法的建立[J].中国实验方剂学杂志,2014(9):96-98.
(收稿日期:2022-09-29 编辑:陶希睿)

