老化态Pd/Rh基三元催化器的起燃及次生污染物生成特性研究
王朝元, 钱叶剑, 孟 顺, 位晓飞, 谢兆辉, 潘 涛
(合肥工业大学 汽车与交通工程学院,安徽 合肥 230009)
国六排放法规不但提高了排放污染物限值要求,还加严了老化系数,补充了加法老化因子,这对三元催化器(three-way catalytic converter, TWC)的可靠性和耐久性能提出了更高要求[1]。另外,国六排放法规采用新的测试循环,规定了天然气发动机后处理系统次生污染物NH3的排放限值,要求其质量分数不超过1.00×10-5。
TWC通常使用Pd、Rh等贵金属作为活性成分,在高温热老化后,贵金属微观结构的变化会使TWC活性明显降低,催化性能下降[2]。文献[3]指出水热老化会使负载型催化剂的载体和贵金属同时烧结,导致比表面积降低、颗粒尺寸增大,贵金属分散度随之降低;文献[4]发现分散度降低会劣化TWC的催化性能,排放物的转换效率下降,起燃温度增加;文献[5]发现催化剂样品在700 ℃老化5 h后,表面会发生物理变化,虽然分散度仅降低约0.1%,但CO和CH4的起燃温度上升;文献[6]发现Rh/ZrO2催化剂在1 050 ℃老化12 h后,Rh分散度下降约35.8%,NO和CO的起燃温度上升约30 ℃。
贵金属分散度的变化决定了贵金属吸附污染物气体分子的能力以及表面反应时贵金属表面结合位点的数量。次生污染物的生成和消耗与贵金属的吸附能力、活性位点的数量密切相关,因此催化剂老化还会影响次生污染物排放量。文献[7]研究了不同排气温度下新鲜态和老化态TWC次生污染物NH3的生成选择性,与新鲜态相比,排气温度在300~500 ℃区间老化态的NH3生成形成选择性更高。
综上可知,当前研究多集中于催化剂老化对起燃特性的影响,很少涉及不同老化工况对TWC起燃特性的研究,现有研究也很少关注老化对次生污染物N2O生成规律的影响。
因此,本文建立Pd/Rh基(ρPd∶ρRh=5∶1)催化剂催化反应机理模型,利用实验数据验证模型的准确性,理论研究贵金属分散度(0.003 4~0.173 4)对TWC起燃特性以及次生污染物NH3、N2O生成规律的影响,研究结论对提高TWC系统的抗老化性能、降低次生污染物排放量具有重要意义。
1 反应计算模型的建立及验证
1.1 反应模型参数
催化剂计算模型主要包括入口气体属性设置模块、催化剂参数设置模块、出口气体属性设置模块、表面催化反应参数模块、数据输出模块、运行设置模块等。入口气体经过催化剂样品时,在其孔内部发生表面反应,使污染物的浓度显著下降。
模型遵循质量守恒方程、动量守恒方程、能量守恒方程和物质瞬态守恒方程。忽略传热损失,只考虑温度沿轴向变化,反应过程中仅考虑涂覆层和层流之间的传热传质,不考虑涂覆层中的扩散作用。新鲜态和老化态样品的氧化因数采用默认数值。
催化器尺寸及催化剂参数见表1所列。
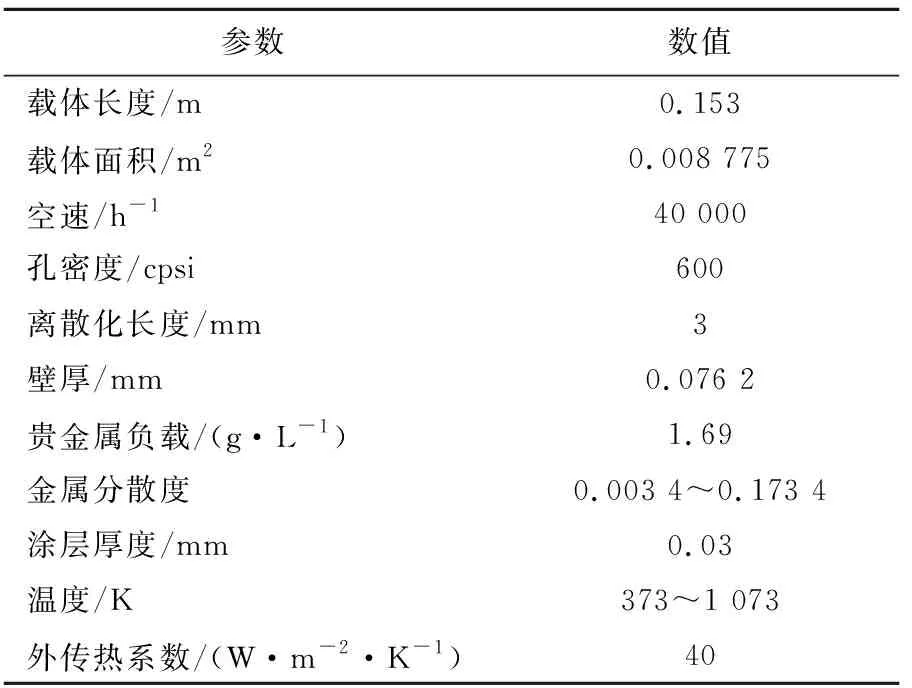
表1 催化剂样品参数
1.2 反应机理
天然气发动机排放物(主要为CH4、CO、NO)的消除主要依靠CH4和CO的氧化反应以及NO的还原反应,本文采用本课题组内建立的Pd/Rh基催化反应机理。
1.3 反应动力学方程
排气各组分的转化效率主要由化学反应速率决定。反应速率常数使用阿伦尼乌斯速率公式表示,具体表达式为:
(1)
催化剂样品老化后,H2氧化的反应速率常数发生变动,表达式为:
(2)
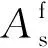
反应速率表达式为:
ω1=KiCFmθi
(3)
其中:C为反应物浓度乘积;θi为覆盖率表达式,指参与反应的载体材料的覆盖程度;Fm(m=1,2,3)为阻聚项。
(4)
F2(X,Ts)=Ts1+Ka,4XCO+
(5)
(6)
其中:XCO、XHC、XNO、XO2分别表示CO、HC、NO、O2的体积分数;Ka,j为速率系数,对应公式中Ka,1~Ka,7;Ts为催化器均温。阻聚项表达式(4)~(6)中Ka,j求解所需动力学参数见表2所列,其中A=lnA1。

表2 阻聚项动力学参数
1.4 模型验证
本文利用文献[8]的实验数据和模拟数据来验证所建模型的准确性。
新鲜态催化剂和老化态催化剂对排放物转化效率的变化规律如图1所示,其中NMOG代表非甲烷碳氢化合物。
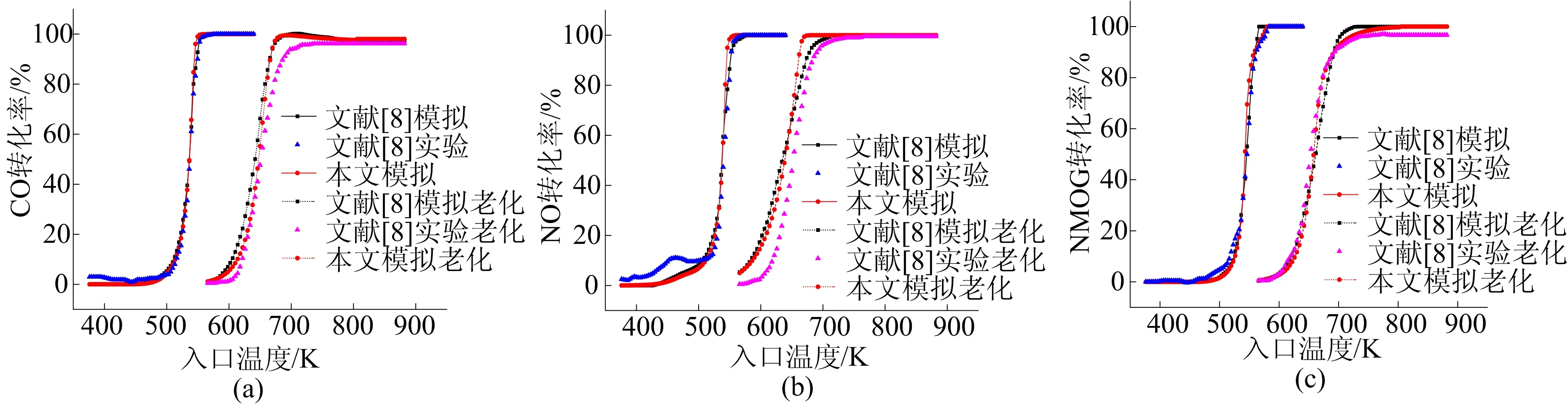
图1 组合Pd/Rh催化剂新鲜/老化状态下模拟验证
从图1可以看出,本文所建模型的计算值与文献[8]的研究结果很接近。虽然文献[8]中的总包反应机理忽略了一些影响较小的反应,使得计算值与实验结果之间存在一定偏差,但此偏差很小,不会影响研究结论的准确性。因此,可以利用构建的模型开展后续研究。
2 结果与讨论
根据标定完成的Pd/Rh基(ρPd∶ρRh=5∶1)机理,设置入口相关参数如下:混合气流量为895.05 L/min;入口气体温度以10 K/min的升温速率从373 K升温至1 073 K;主要配气成分及体积分数为φ(CH4)=1.00×10-3,φ(CO)=4.70×10-3,φ(NO)=8.00×10-4,φ(H2O)=10%,其中平衡气为N2;根据λ的计算公式[9],当量比条件下φ(O2)=3.95×10-3。λ的计算公式为:
(7)
模拟流程采用默认流程,催化剂老化前、后排放物转化率计算公式为:
(8)
其中,ci,f、ci,m分别为进、出口对应i组分浓度。
起燃特性用起燃温度和完全转化温度表征,分别指CH4、CO、NO达到其转化率的50%和90%对应的气体入口温度,通过转化率曲线捕捉各排放物气体的T50和T90。
2.1 贵金属分散度对起燃特性的影响
贵金属分散度是指贵金属在储氧材料表面上的分散程度。老化态催化器的贵金属分散度大大降低,贵金属粒子相互堆叠,部分贵金属无法与气体分子直接接触,导致排放物转化率下降,起燃性能变差。
贵金属负载量在1.69 g/L时不同分散度对CH4、CO、NO的T50、T90影响规律如图2所示。
从图2可以看出,随着贵金属分散度的增加,CH4、CO、NO的T50、T90都有所降低。在分散度为0.003 4~0.043 4范围内下降速率最快,其中CH4的T50由794 K降至689 K,T90由834 K降至739 K;分散度在大于0.043 4~0.113 4范围内,其值每增加0.01,CH4、CO、NO的T50分别降低约5、3、2 K,T90分别降低约7、3、4 K;当分散度大于0.123 4时,分散度对起燃特性的影响逐渐减小。
综上可知,贵金属分散度是影响CH4、CO、NO起燃特性的重要因素。分散度在0.003 4~0.043 4范围内时,增加分散度会明显改善CH4、CO、NO的起燃特性;当分散度大于0.123 4时,分散度的增加对起燃特性的影响变小。由此可以看出,不能一味地通过提高贵金属分散度来提高催化剂的催化能力。
2.2 贵金属分散度对次生污染物生成的影响
为研究在不同老化程度下次生污染物NH3、N2O的生成规律,本文选取贵金属分散度为0.003 4~0.173 4范围内2个等距点进行研究。反应机理中涉及到的次生污染物相关反应见表3所列。
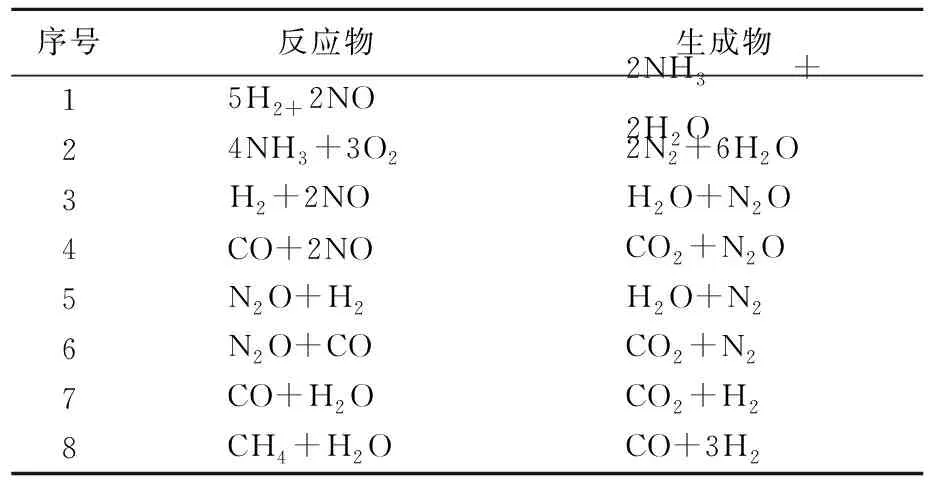
表3 次生污染物相关反应
一般来说,NH3主要来自于NO-H2还原反应,N2O主要来自于H2-NO和CO-NO反应。H2-NO反应的活化能低,因此更易发生。另外,H2-NO反应基本停止后,CO-NO反应才能发生。因为入口组分中未设置H2,所以H2主要来自于水煤气变换(water-gas shift,WGS)和蒸汽重整(steam reforming,SR)反应[10-11]。
在4种不同贵金属分散度下,次生污染物NH3、N2O的生成变化规律如图3所示。

图3 贵金属分散度对次生污染物NH3、N2O生成的影响
从图3a可以看出:贵金属分散度在0.060 1、0.116 7、0.173 4时,NH3在入口温度为530 K时开始生成;当贵金属分散度为0.003 4且入口温度低于570 K时,也没有NH3生成,入口温度大于720 K时,NH3摩尔分数迅速增加;当入口温度在805 K后,NH3生成量高于其他3种贵金属分散度情况。
这是因为:低温下Pd、Rh比表面积的减小会造成排放物吸附不足,抑制WGS和SR反应的发生,导致H2生成量不足,不能进行NO-H2反应,无法生成NH3;入口温度在720~805 K时,贵金属分散度的降低对排放物吸附的影响减小,WGS反应速率加快,H2生成量增加,促进了NO-H2反应,NH3的消耗速率减慢;入口温度大于805 K时,NH3的消耗反应几乎不发生,净生成量大幅增加。
从图3a还可以看出:在贵金属分散度为0.060 1、0.116 7、0.173 4的3种情况中,NH3生成曲线的趋势大致相同,贵金属分散度越低,生成NH3的总摩尔分数越大。催化剂表面NO活性位点随分散度的增大而增加,分散度最大时,吸附的NO最多。分散度为0.173 4、入口温度为570~630 K时,NO-H2反应最快,NH3生成量增加,但此时NH3的消耗量大于生成量,NH3净生成量降低;入口温度为630~860 K时,NH3的生成量大于消耗量,NH3净生成量增加;入口温度大于860 K时,NH3生成和消耗的速率基本一致,NH3净生成量几乎不变。
从图3b可以看出:贵金属分散度为0.003 4时,N2O在入口温度440 K时开始生成,H2-NO反应速率随着入口温度的提高而增加;入口温度大于650 K时,N2O的消耗反应开始进行,直至850 K左右反应停止,CO-NO反应开始进行,N2O摩尔分数略有增加。
从图3b还可以看出:在贵金属分散度为0.060 1、0.116 7、0.173 4的3种情况中,N2O生成量首次达到峰值时对应的入口温度随贵金属分散度的增加而降低,这是由于贵金属分散度较高时,即使入口温度低,WGS和SR反应也可以生成足量的H2,H2可以与吸附在贵金属上的NO反应完全;入口温度为610~650 K时,N2O摩尔分数略有下降,这是由于N2O-CO反应会消耗部分N2O。贵金属分散度越高,有效吸附的CO越多,N2O-CO反应越剧烈,消耗的N2O越多;反应停止后N2O消耗随之暂停,而N2O-H2间的反应继续消耗N2O。3种情况下N2O的消耗大致相同。N2O摩尔分数再次上升时,CO-NO反应开始进行,由于其活化能较高,N2O摩尔分数的上升速率较为缓慢。最终,N2O与剩余的少量H2和CO反应,造成3种情况下N2O摩尔分数均下降。
由此可知,次生污染物NH3、N2O生成的摩尔分数随入口温度波动明显。贵金属分散度的提高能有效降低次生污染物的生成量,对NH3生成的抑制更加明显。另外,贵金属分散度的增加可以使污染物的吸附更加均匀,使次生污染物的消耗增加,总体生成量减少。
3 结 论
本文基于Pd/Rh基(ρPd∶ρRh=5∶1)三元催化剂样品表面反应机理,结合相关物理参数,研究了贵金属分散度对CH4、CO、NO起燃特性以及次生污染物NH3、N2O生成规律的影响,主要研究结论如下:
(1) 合适的分散度有利于贵金属与污染物气体的接触,促使污染物气体在较低的入口温度下实现转化。增加贵金属分散度会提高CH4、CO、NO的起燃特性;CH4、CO、NO的T50和T90在分散度为0.003 4~0.043 4的范围内下降速率快,分散度大于0.043 4时对起燃特性的影响变小。
(2) 贵金属分散度会影响次生污染物NH3、N2O的生成规律。贵金属分散度为0.003 4时,次生污染物NH3、N2O生成加快,消耗缓慢,净生成总量增加;贵金属分散度由0.060 1提高至0.173 4时,由于活性位点的增加,次生污染物的消耗随之增多,导致次生污染物净生成量明显减小。
——庆祝中国共产党成立一百周年贵金属纪念币展

