PRiME HLB固相萃取-高效液相色谱-串联质谱法测定化妆品中的双酚A*
王玉梅,刘 真,姜 星
(南京市食品药品监督检验院,江苏 南京 211198)
化妆品包装除了可以美化外观外,还可以阻止化妆品内部与外界接触,起到抗氧化和防腐的作用[1]。目前,化妆品的包装材料的主要有玻璃、塑料、金属箔等,其中,塑料包装具有方便运输、耐冲击强度大等优点,已经成为化妆品常用的包装材料。双酚A(Bisphenol A,BPA)是用来合成聚碳酸酯、酚醛树脂和不饱和聚酯树脂等材料的重要物质[2],主要用于塑料瓶,食品、化妆品包装的生产。但双酚A属于一种内分泌干扰物质,对人的内分泌、神经系统、生殖系统等有不良影响,严重时会诱发癌症[3]。我国《化妆品技术规范》(2015版)明确规定双酚A是化妆品中的禁用物质[4],但相应的检测方法不完善。目前,化妆品中双酚A的检测标准仅有SN/T 3822-2014和GB/T 30939-2014,两者均使用氨基固相萃取小柱净化,前处理过程复杂,且采用外标法定量,存在基质干扰、定量不准确等现象,不能满足日常的监管检验需求。本研究针对水状、膏霜状和精油状三种性状化妆品基质中双酚A的残留量,采用氨化乙腈提取,通过PRiME HLB固相萃取小柱净化后,采用高效液相色谱-串联质谱法测定化妆品中双酚A,内标法定量,提取净化方法灵敏快捷,以期为化妆品的监管提供技术保障。
1 试验部分
1.1 材料、试剂与仪器
双酚A(100.2μg/mL)、双酚A-d4(100.0 μg/mL),天津阿尔塔科技有限公司;Oasis PRIME HLB固相萃取小柱,200mg/6mL,美国Waters公司;甲醇、乙腈、氨水,色谱级,德国Merck公司;甲酸、氟化铵,色谱级,上海阿拉丁生化科技股份公司;实验用水为市购蒸馏水;其余试剂均为分析纯。
Agilent 6470三重四极杆液质联用仪 (配ESI源),美国安捷伦科技有限公司;Waters ACQUITY UPLC BEH C18,Waters公司;VISIPREP 24TM DL固相萃取装置,Supelco公司;Sorvall LYNX 4000高速离心机,美国赛默飞世尔科技公司;MV5浓缩氮吹仪,莱伯泰科有限公司。
1.2 实验方法
1.2.1 样品前处理
①提取:称取0.5 g试样(精确至0.001 g)于10mL具塞比色管中,加入50μL双酚A-d4标准中间液,加入少量5%氨水-乙腈溶液充分混匀后定容至刻度,超声提取15min后转移至离心管中,10000 r/min离心5 min,取上清液备用。
②净化:取全部上清液,过PRiME HLB固相萃取小柱,收集净化液,40℃水浴中氮气吹至近干,用甲醇溶解并定容至1.0mL,过0.22μm滤膜,供液相色谱-串联质谱测定。
1.2.2 液相色谱条件
色谱柱:Waters ACQUITY UPLC BEH C18色谱柱(100mm×Ø2.0mm,1.7μm);流速:0.4mL/min;柱温:35℃;进样量:5μL;流动相:A(甲醇)、B(0.1%氟化铵水溶液);梯度洗脱程序为0~2.5min,40%~90%A;2.5~4.6min,90%A;4.6~7.0min,90%~95%A;7.0~7.5min,95%A;7.5~7.6min,95%~40%A;7.6~10.0min,40%A。
1.2.3 质谱条件
离子源:电喷雾(ESI)离子源;扫描方式:负离子扫描;检测方式:MRM多反应监测;干燥气温度:300℃;干燥气流速:12 L/min;雾化气压力:275.8 kPa;鞘气温度:350℃;鞘气流速:11 L/min;毛细管电压:3500 V;双酚A及其内标双酚A-d4的保留时间、离子对、碰撞电压和裂解电压见表1。

表1 双酚A及其内标的质谱参数
2 结果与讨论
2.1 色谱质谱条件的优化
参照相关文献[5],色谱柱选用常规的适合小分子类物质分离的Waters ACQUITY UPLC BEH C18(Ø2.1mm×50mm,1.7μm)。实验首先考察了0.1%甲酸溶液-甲醇、水-甲醇和0.1%氨水溶液-甲醇三种流动相体系,结果表明,当使用0.1%甲酸溶液-甲醇流动相体系时,双酚A的相应较弱;使用0.1%氨水溶液-甲醇流动相体系时;双酚A的出峰时间较早,响应也相对较弱,而使用水-甲醇流动相体系时双酚A的响应强度较高,色谱峰形较好。为了使双酚A的响应强度更高,故于流动相中添加0.1%氟化铵,结合前处理步骤中采用甲醇作为定容溶剂,因此本实验确定流动相为0.1%氟化铵水溶液-甲醇。
实验进利用Agilent三重四极杆液质联用仪自带的Masshunter Optimizer软件分析双酚A及其内标的标准溶液,获得目标物质的母离子、子离子及对应的碰撞能和裂解电压。
2.2 提取溶剂的优化
本研究首先对比了乙腈和甲醇的作为提取溶剂的效果,结果表明,在水状、膏霜状、精油状三种性状化妆品基质中,乙腈的提取效率均优于甲醇,回收率均在80%上,故选择乙腈作为提取溶剂。在此基础上,实验考察了1%甲酸乙腈溶液、乙腈和1%氨水乙腈溶液的提取效率,具体结果见图1。实验表明在乙腈中加入氨水后可以增强提取效果。

图1 使用不同提取溶剂对提取效率的影响
实验进一步研究了1%、2%、5%、8%、10%、15%氨水乙腈溶液的提取效果,结果见图2。发现使用5%和8%的氨水乙腈溶液时,三种不同性状基质中双酚A的提取率都比较高。考虑到前处理过程中有氮吹的步骤,实验确定采用5%氨水乙腈溶液作为提取溶液,三种不同形状基质中提取效率均达到95%以上。

图2 不同体积分数的氨水乙腈对提取效率的影响
实验进一步研究了化妆品基质的超声时间的最优条件,于三种性状的化妆品基质中加入20 ng双酚A标准溶液,分别超声5、10、15、20、25min。结果表明,超声时间15min后三种不同性状基质中双酚A的提取率均大于90%以上,且提取效率保持恒定水平。
2.3 定量方式的选择及基质效应的考察
采用质谱分析时需考虑基质效应的影响,一般采用基质效应(ME)=(1-基质匹配标准曲线的斜率/溶剂标准曲线的斜率)×100%的计算方法来评价的基质效应,基质效应在±20%内不显著,结果为正时表示基质抑制,为负表明基质增强[6]。
测定化妆品中的双酚A的相关标准及文献中大部分采用外标法定量,但是实际实验中发现采用外标法定量时受化妆品基质干扰较大,尤其是精油状化妆品,基质效应明显,测定的回收率<50%,结果定量产生的误差较大。本研究改用双酚A-d4内标法定量,内标峰形较好,基线噪音小,无干扰峰,保留时间与双酚A接近。
本实验进一步考察了水状、膏霜状和精油状三种性状化妆品基质于线性范围2~50 ng/mL的基质效应,结果见表2。双酚A在三种基质中基质效应均不明显,进一步说明引入同位素内标后,双酚A的基质效应得到了很好的改善。
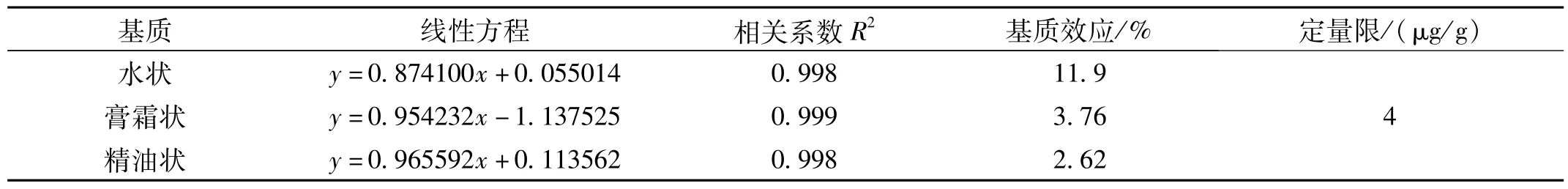
表2 双酚A的基质标准曲线、相关系数、定量限及基质效应
2.4 净化方式的优化
化妆品基质复杂,一般由油脂、乳化剂等成分组成,膏霜状和精油状化妆品基质提取后会出现浑浊难离心的状况[7],需要净化后才能上机分析,否则会污染离子源,影响目标物的响应。
根据双酚A的相关报道[8],本实验分别考察C18、PRIME HLB、MAX、氨基固相萃取小柱的吸附效果。结果发现,采用C18柱净化时,三种基质中的双酚A的回收率都比较低,使用MAX、氨基固相萃取小柱和PRIME HLB固相萃取柱时,双酚A的回收率均能大于80%,但由于使用MAX和氨基固相萃取小柱时需要活化、洗脱等繁杂的实验步骤,考虑到实验的快速和便捷性,PRIME HLB不需要活化等前处理步骤,操作相对简单,因此本实验最终选择PRIME HLB固相萃取小柱作为净化柱。
2.5 方法学考察
2.5.1 线性范围和检出限
在本研究方法确定的前处理及分析条件下,对水状、膏霜状和精油状三种性状化妆品基质中的双酚A的线性范围进行测定,以质量浓度为横坐标,双酚A的峰面积与内标峰面积的比值为纵坐标,绘制标准曲线,并得到相关系数。双酚A在2 ng/mL~50 ng/mL的质量浓度范围内线性关系良好,相关系数均>0.99。具体结果见表2。
2.5.2 精密度与回收率实验
于水状、膏霜状、精油状三种性状化妆品空白基质中,按照定量限的1倍、2倍和10倍定量限的质量浓度水平添加双酚A,进行加标回收率实验。各质量浓度水平均做6个平行,计算双酚A的回收率和相对标准偏差(RSD),结果见表3。由表3可知,水状化妆品基质中的双酚A 的平均回收率为95.6% ~101.2%,相对偏差小于3.2%;膏霜状化妆品基质中的双酚A的平均回收率为93.2%~98.8%,相对偏差小于4.2%;精油状化妆品基质中的双酚A的平均回收率为92.5%~99.0%,相对偏差小于3.9%。
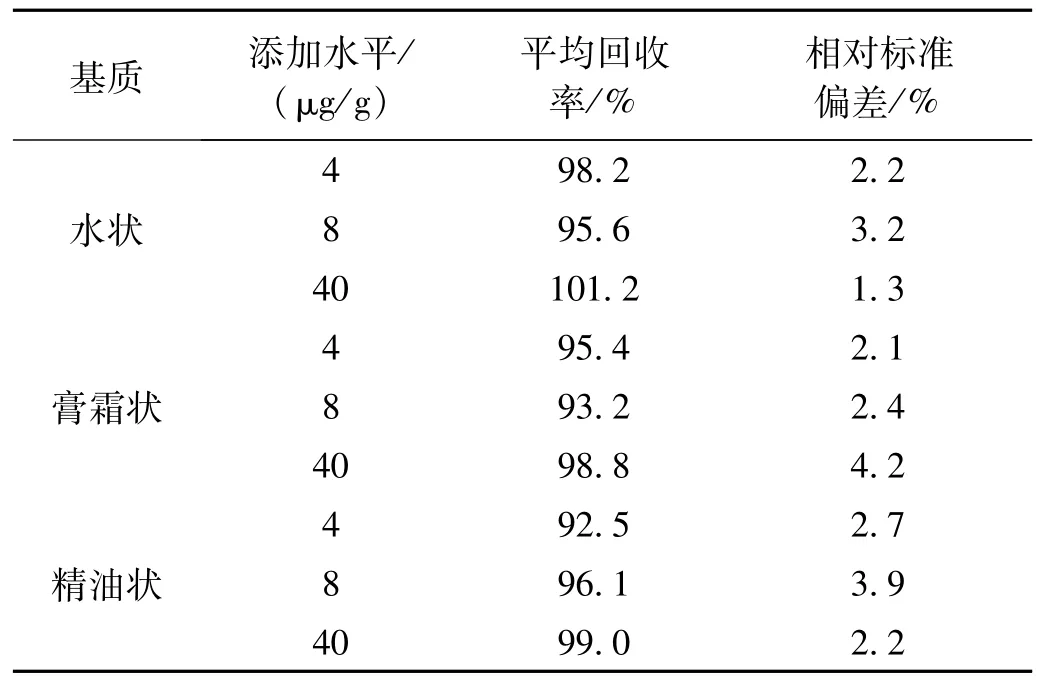
表3 双酚A的回收率和相对标准偏差 (n=6)
2.6 实际样品测定
实验采用建立的方法进行实际样品的检测,分别测定了90批次的样品,包括水状、膏霜状和精油状化妆品各30批。通过保留时间、离子丰度比等信息进行判定,以上样品中均未检出双酚A;样品图谱中无杂质干扰峰,内标出峰正常。可能是因为所检的化妆品均是品牌厂家生产的,具有良好的质量保证。
3 结论
本实验建立了PRiME HLB固相萃取-高效液相-串联质谱法测定水状、膏霜状和精油状三种化妆品基质中的双酚A残留量。本方法前处理快捷简便,定量准确可靠,检测灵敏度和精密度较好,为化妆品的监管和风险监测提供了有力的技术支撑。

