卡瑞利珠单抗治疗霍奇金淋巴瘤的近期疗效及安全性
王 琼,庞迎旭,米瑞华,尹青松
(1.周口市中心医院血液科,河南 周口 466000;2.河南省肿瘤医院血液科,河南 郑州 450000)
霍奇金淋巴瘤是一类来源于淋巴系统的恶性增殖性肿瘤,颈部和锁骨上无痛性淋巴结肿大是其典型的临床症状;成年男性霍奇金淋巴瘤发病率略高于女性[1]。霍奇金淋巴瘤对放化疗高度敏感,标准的一线化学治疗方案阿霉素(adriamycin)+博来霉素(bleomycin)+长春新碱(vincristine)+达卡巴嗪(dacarbazine)(简称ABVD方案)联合局部放射治疗可使80%以上的霍奇金淋巴瘤患者达到缓解并获得长期的疾病控制,霍奇金淋巴瘤也是目前为数不多的可以治愈的恶性肿瘤;但仍有5%~10%的霍奇金淋巴瘤患者对初始化学治疗无反应,还有10%~30%的霍奇金淋巴瘤患者在缓解后出现复发的情况,而中晚期霍奇金淋巴瘤患者的复发率更高[2]。近几年出现的免疫检査点抑制剂类药物为霍奇金淋巴瘤的治疗提供了新的方案。卡瑞利珠单抗为程序性死亡受体1(programmed cell death 1,PD-1)抑制剂,是国家药品监督管理局于2019年5月正式批准用于至少经过二线系统治疗后复发或难治性经典型霍奇金淋巴瘤的治疗[3],但是,目前尚无关于卡瑞利珠单抗治疗霍奇金淋巴瘤的标准方案,其相对标准治疗方案是否有显著的临床疗效仍在研究中。基于此,本研究探讨卡瑞利珠单抗治疗霍奇金淋巴瘤的近期疗效及安全性,以期为卡瑞利珠单抗在霍奇金淋巴瘤治疗的应用提供依据。
1 资料与方法
1.1 一般资料
选择2017年1月至2020年5月周口市中心医院收治的84例霍奇金淋巴瘤患者为研究对象。病例纳入标准:(1)符合《中国淋巴瘤治疗指南(2021年版)》[4]中霍奇金淋巴瘤诊断标准,经病理组织活检及免疫组织化学检查确诊;(2)Ann Arbor分期 Ⅱ~Ⅳ期者;(3)淋巴结肿块最大直径>3 cm;(4)经一线ABVD方案治疗失败;(5)年龄>20岁;(6)临床病历资料及相关实验室检查资料齐全。排除标准:(1)有放化疗禁忌证者;(2)继发性肿瘤者。根据治疗方式将患者分为对照组(n=50)和观察组(n=34)。对照组:男30例,女20例;年龄22~45(35.40±5.44)岁;Ann Arbor分期:Ⅱ期19例,Ⅲ期20例,Ⅳ期11例;病理亚型:结节硬化型20例,混合细胞型22例,富于淋巴细胞型3例,淋巴细胞消减型3例,结节性淋巴细胞为主性2例;淋巴结肿块最大直径4.4~9.7(6.57±1.76)cm;B症状:有27例,无23例。观察组:男24例,女10例;年龄23~44(34.79±5.73)岁;Ann Arbor分期:Ⅱ期15例,Ⅲ期14例,Ⅳ期5例;病理亚型:结节硬化型17例,混合细胞型15例,富于淋巴细胞型1例,淋巴细胞消减型1例;淋巴结肿块最大直径4.2~9.8(6.62±1.85)cm;B症状:有20例,无14例。2组患者的性别、年龄、Ann Arbor分期、病理亚型及淋巴结肿块最大直径等一般资料比较差异无统计学意义(P>0.05),具有可比性。本研究获得医院医学伦理委员会审核批准,患者或家属知情同意并签署知情同意书。
1.2 化学治疗方法
对照组患者接受表柔比星+长春地辛+达卡巴嗪化学治疗方案,第1 天和第15 天静脉注射长春地辛(哈尔滨三联药业股份有限公司,国药准字H20033311)(每日3 mg·m-2)、表柔比星(浙江海正药业股份有限公司,国药准字H20041211)(每日35 mg·m-2)和达卡巴嗪(南京制药厂有限公司,国药准字H32026231)(每日375 mg·m-2),4周为1个化学治疗周期,至少连续进行4个化学治疗周期,若患者身体条件允许,可继续接受化学治疗直至患者病情进展或出现不可耐受的不良反应。
观察组患者接受卡瑞利珠单抗治疗,第1 天和第15 天静脉注射卡瑞利珠单抗(苏州盛迪亚生物医药有限公司,国药准字S20190027),每日200 mg,4周为1个化学治疗周期,若患者身体条件允许,至少连续进行4个化学治疗周期;4个周期后完全缓解的霍奇金淋巴瘤晚期患者接受静脉注射卡瑞利珠单抗维持治疗,每日200 mg,每月1次,直至患者病情进展或出现不可耐受的不良反应。
1.3 观察指标
1.3.1 临床疗效
采用Lugano 2014评价标准[5]评估患者化学治疗4个周期后的临床疗效。基于CT和(或)磁共振成像评估的影像学反应和基于正电子发射计算机断层显像-CT评价的代谢反应分为完全缓解、部分缓解、疾病稳定和疾病进展,计算疾病控制率和客观缓解率,疾病控制率=(完全缓解例数+部分缓解例数+疾病稳定例数)/总例数×100%,客观缓解率=(完全缓解例数+部分缓解例数)/总例数×100%。
1.3.2 不良反应
比较2组患者治疗期间不良反应发生情况,不良反应严重程度参考文献[6]标准进行评估,每个不良反应严重程度均分为0~Ⅳ级,包括血液系统毒性(血小板减少、中性粒细胞减少、白细胞减少、血红蛋白下降等)和非血液系统毒性(恶心、呕吐、出血、腹泻、甲状腺功能减退、黏膜炎、肝功能异常、肺炎、周围神经病、心脏毒性、膀胱炎、反应性毛细血管增生症、乏力、蛋白尿、低钠血症等)。
1.3.3 预后
2组患者均随访2 a,比较2组患者2 a内的生存情况。
1.4 统计学处理
应用SPSS 20.0软件进行数据统计与分析。计数资料以例数和百分率表示,组间比较采用χ2检验;等级资料比较采用秩和检验;P<0.05为差异有统计学意义。
2 结果
2.1 2组患者治疗后近期临床疗效比较
化学治疗4个周期后,观察组患者的疾病控制率和客观缓解率显著高于对照组,差异有统计学意义(χ2=4.019、11.213,P<0.05),见表1。

表1 2组患者治疗后近期临床疗效比较Tab.1 Comparison of short-term clinical efficacy of patients between the two groups after treatment
2.2 2组患者治疗期间不良反应比较
治疗期间,观察组患者血液系统毒性Ⅰ~Ⅱ级发生率及非血液系统毒性Ⅲ~Ⅳ级发生率明显低于对照组,差异有统计学意义(P<0.05),见表2和表3。对照组患者Ⅲ级以上的不良反应中血液系统毒性(血小板减少、中性粒细胞减少、白细胞减少、血红蛋白下降)占10.00%,非血液系统毒性(恶心、呕吐、肝功能异常、乏力、蛋白尿和出血)占18.00%;其中7例患者因严重的血液系统毒性和(或)严重的非血液系统毒性而更改治疗方案,其他均在对症处理后得到有效缓解。观察组患者Ⅲ级以上的不良反应中仅发现中性粒细胞减少和肝功能异常(各占2.94%),其中1例患者因严重的肝功能异常而更改治疗方案,其他均在对症处理后得到有效的缓解。
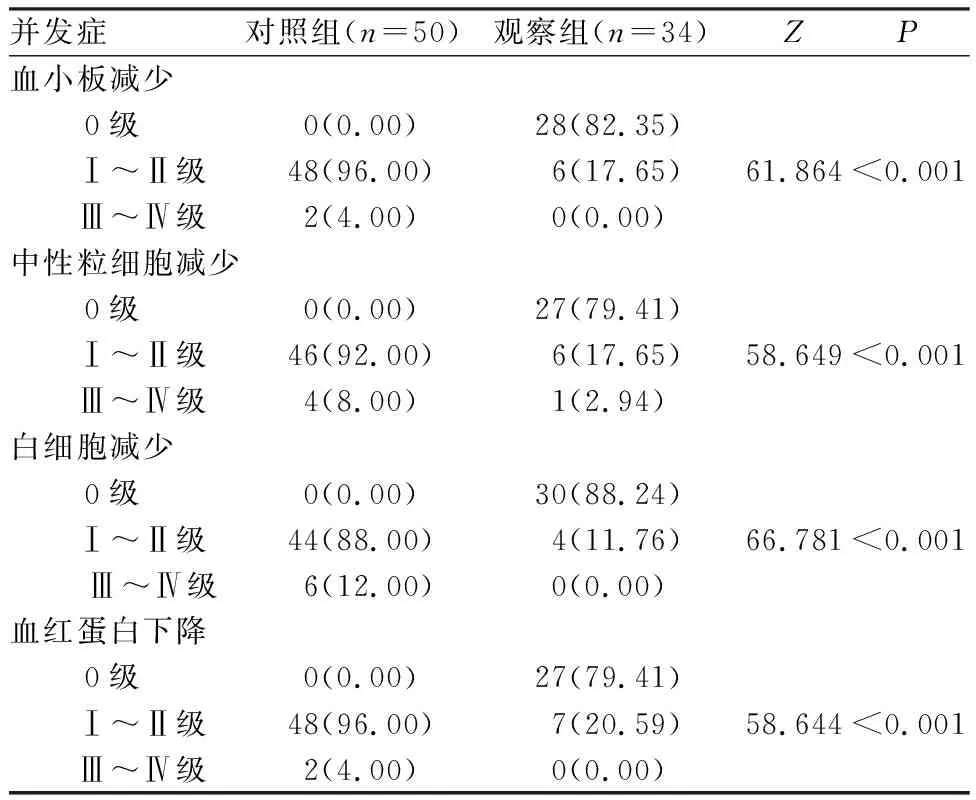
表2 2组患者治疗期间血液系统不良反应比较Tab.2 Comparison of adverse reactions of blood system of patients between the two groups during treatment 例(%)
2.3 2组患者随访2 a生存情况比较
随访2 a期间,对照组患者死亡12例(24.00%),观察组患者死亡2例(5.88%);观察组患者病死率显著低于对照组,差异有统计学意义(χ2=4.783,P<0.05)。
3 讨论
霍奇金淋巴瘤好发于颈部淋巴结,典型表现为颈部和锁骨上无痛性淋巴结肿大,发病年龄呈双峰特征,即15~19岁的青少年及>60岁以上的老年患者为高发人群。霍奇金淋巴瘤是少数临床可治愈的恶性肿瘤,早期霍奇金淋巴瘤的治疗重点是清除病灶、防止复发,晚期霍奇金淋巴瘤的治疗重点主要集中在降低不良反应、延长患者带瘤生存时间[7]。ABVD方案是霍奇金淋巴瘤标准的一线治疗方案,在全世界范围内广泛应用;然而,仍有部分患者对一线化学治疗无明显反应或治愈后复发[8]。霍奇金淋巴瘤二线及以后的化学治疗方案众多,如地塞米松+顺铂+阿糖胞苷方案[9]、吉西他滨+顺铂+地塞米松方案[10]等,但化学治疗引起的不良反应均比较严重,且化学治疗后的疗效仍不尽如人意。
肿瘤免疫逃逸是多数恶性肿瘤发生、发展的重要机制之一,而免疫检查点则是该机制的关键环节[11]。有研究报道,9p24.1染色体扩增可导致 PD-1 在恶性HRS细胞及肿瘤微环境内呈高水平表达,而高水平的PD-1又可消耗大量T细胞,导致T细胞耗竭,从而减弱了机体的抗肿瘤能力[12]。有研究报道,PD-1高表达与肿瘤细胞免疫逃逸密切相关,因而推测抑制PD-1高表达可成为恶性肿瘤治疗的新靶点[13]。近几年,纳武利尤单抗、帕博利珠单抗、信迪利单抗、替雷利珠单抗、维布妥昔单抗等PD-1抑制剂在我国陆续上市,为多种恶性肿瘤的治疗提供了新的治疗方案,延长了患者的生存时间。PD-1/程序性死亡受体配体1(programmed cell death 1 ligand 1,PD-L1)抑制剂通过阻断PD-1/PD-L1信号转导通路,抑制T细胞增殖、活化,进而介导负性免疫调控过程[14]。卡瑞利珠单抗是采用重组技术在中国仓鼠卵巢细胞系中表达的一种人源化IgG4κ型抗PD-1单克隆抗体,与PD-1受体结合后阻断了PD-1与PD-L1结合,激活T细胞而产生抗肿瘤效应[15]。目前,卡瑞利珠单抗仅批准用于至少经过二线系统治疗后复发或难治性经典型霍奇金淋巴瘤的治疗,尚未批准用于其他恶性肿瘤的治疗。本研究结果显示,化学治疗4个周期后,观察组患者的疾病控制率和客观缓解率均高于对照组;随访2 a,观察组患者病死率显著低于对照组;这说明,与表柔比星+长春地辛+达卡巴嗪化学治疗方案比较,卡瑞利珠单抗治疗ABVD方案治疗失败的霍奇金淋巴瘤可增强近期抗肿瘤效果,提高患者生存率,这与赵可等[16]研究结果一致。
PD-1抑制剂可导致免疫功能亢进,促使T细胞攻击机体正常组织细胞,可发生皮疹、瘙痒、甲状腺功能减退等不良反应[17]。但是,本研究结果显示,观察组患者血液系统毒性Ⅰ~Ⅱ级发生率及非血液系统毒性Ⅲ~Ⅳ级发生率显著低于对照组;对照组患者Ⅲ级以上的不良反应中血液系统毒性占10.00%,非血液系统毒性占18.00%,其中有7例患者因严重的血液系统毒性和(或)严重的非血液系统毒性而更改治疗方案,其他均在对症处理后得到有效缓解;观察组患者Ⅲ级以上的不良反应中仅发现有中性粒细胞减少和肝功能异常,各占2.94%,其中1例患者因严重的肝功能异常而更改治疗方案,其他均在对症处理后得到有效的缓解;说明,卡瑞利珠单抗治疗ABVD方案治疗失败的霍奇金淋巴瘤安全性较高,但在临床实际工作中还应早期识别不良反应,并通过抑制淋巴细胞活性或给予类固醇激素治疗有效控制不良反应。
4 结论
卡瑞利珠单抗治疗ABVD方案治疗失败的霍奇金淋巴瘤可增强近期抗肿瘤效果,提高患者生存率,且安全性较高,值得临床进一步研究和推广。但本研究样本量有限,随访时间较短,后期还需扩大样本量,延长随访时间,以更准确地评估卡瑞利珠单抗对霍奇金淋巴瘤患者远期预后的影响。

