Cr 和Ni 对低碳合金钢微观结构和耐蚀性的影响
王 丹,钟庆东
(1.上海工程技术大学高等职业技术学院,上海 200437;2.上海大学材料科学与工程学院,上海 200444)
0 前 言
合金化是优化钢材料的微结构和耐蚀性的重要手段之一[1]。Cr 和Ni 合金化提高钢的耐蚀性是钢材料领域的研究热点之一。Tian 等[2]研究发现在模拟混凝土环境中试验钢添加3%(质量分数,下同)Ni 时,试验钢表面形成具有N 型半导体性质的氧化膜,Ni 能在氧化膜中富集,从而显著降低试验钢的腐蚀速率。程多云等[3]指出添加Ni 元素能使高镍钢表面的锈层更致密,降低其在海洋大气环境中的腐蚀速率,对Cl-的抵抗作用更强。周学俊等[4]发现镍铜质量比与硅含量对试验钢的耐腐蚀性存在一定的交互作用,硅的质量分数为0.9%,镍铜质量比为0.5 时,试验钢的耐蚀性最好。Shi 等[5]研究证明添加Cr 元素能使钢表面形成富含Cr 氧化物/氢氧化物的钝化膜,且Cr 改性钢的外表面主要存在γ-FeOOH。Yong 等[6]研究发现铬钢在高压饱和CO2盐水中的耐蚀性在腐蚀初期和192 h 腐蚀测试后表现出差异性,腐蚀初期材料的耐蚀性随着Cr含量的增加而增加,当192 h 的腐蚀试验结束后,X65钢与含铬钢表面腐蚀层成分的差异反而导致含铬钢的腐蚀速率和腐蚀程度比X65 的更高。Sun 等[7]研究发现Cr 元素能促进α -FeOOH 的转变,而掺入Cr 的α-(Fe,Cr)OOH和FeCr2O4形成的直径为10 nm 左右的球形颗粒能提高锈层的致密性,同时Cr 能促进Cu的富集,在内部锈层中形成CuO。Zhou 等[8]指出同时添加0.24%Cr、0.50%Ni、0.21%Cu 的低碳合金钢在Cl-环境中经过73 次干湿循环后能形成双锈层,其中Cr 分布在内锈层,Ni 均匀地分布在整个锈层中,锈层中不含Cu。由以上文献的研究结论推断,同时添加Cr 和Ni对提高钢的耐蚀性很可能存在叠加效应。本课题组在前期研究[9,10]中发现,当向钢中单独添加Cr 或Ni 时均能优化钢的微观结构并提升钢在Cl-环境中的耐蚀性;本工作通过观察金相组织、物相分析、硬度测试、电化学测试、浸泡试验、XPS 分析等多种方法研究了4 种Cr和Ni 含量不同的低碳合金钢的微观结构及其在Cl-环境中的耐蚀性,探索了同时添加Cr 和Ni 对低碳合金钢的微观结构和耐蚀性的影响。
1 试 验
1.1 试验材料
针对Cr 元素和Ni 元素的含量,在本课题组前期的单因素研究[9,10]的基础上,进行2 因素2 水平正交试验,设计出4 种钢成分。试验所使用的4 种不同成分的钢由真空电弧熔炼炉炼制,钢锭直径25 mm,各试样经PDA-5500S 型直读光谱测定的化学成分如表1 所示。通过线切割工艺截取铸态钢锭截面中心区域钢制成试样,试样尺寸为10 mm×10 mm×2 mm。
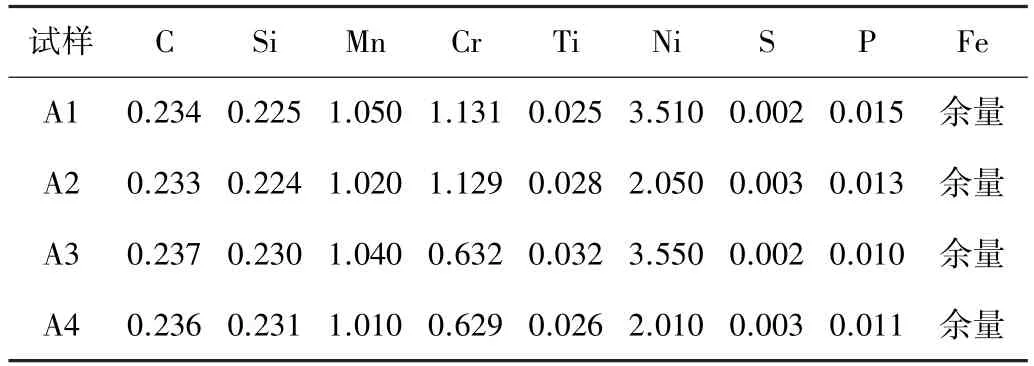
表1 试样的化学成分(质量分数) %Table 1 Chemical composition of samples (mass fraction)%
1.2 形貌、物相结构和显微硬度测试
通过Olympus BC51M 型光学显微镜观察4 种钢的金相形貌,通过Phenom XL 型扫描电子显微镜观察4种钢的微观结构和微观腐蚀形貌。使用600 ~2 000 号水磨砂纸对试样进行打磨后使用粒度为0.25 μm 的抛光剂对试样进行机械抛光,最后使用体积分数为10%的硝酸酒精溶液腐蚀试样后待用。
试样的物相结构由D8 advance BRUKER 型X 射线衍射仪(XRD)检测,测试选用Cu 靶,扫描范围30°~100°,扫描速率为4(°)/min,并利用谢乐公式[式(1)]计算不同钢中的典型碳化物的尺寸:
式中:D表示碳化物的尺寸;K为常数,本工作中取0.89;γ为X 射线波长,本工作中取0.154 08 nm;B表示衍射峰半高宽度;θ表示衍射角。
采用MicroVicker HV 10 型维氏硬度计测试试样的显微硬度。
1.3 电化学测试
将尺寸为10 mm ×10 mm×2 mm 的试样通过导电胶与铜线黏合,通过环氧树脂封装后用SiC 砂纸(800~2 000 号)研磨试样尺寸为10 mm×10 mm 的测试表面,然后用酒精清洗并用凉风吹干试样。
电化学测试采用传统的三电极系统,以铂电极为对电极,饱和甘汞电极(SCE)为参比电极,暴露面积为10 mm×10 mm 的试样为工作电极。极化测试的扫描速率为0.5 mV/s,电位的扫描范围为-1.2~0 V(vs SCE)。电化学阻抗谱分析(EIS)的频率范围为1.0×(10-2~105) Hz,振幅为5 mV,用ZSimpWin 软件对EIS 结果进行拟合。
本工作中采用3.5%(质量分数,下同)NaCl 模拟海水溶液作为测试溶液,温度为室温,本工作中使用的所有溶液均由去离子水和分析纯试剂制备。
1.4 浸泡试验
为了观察4 种钢的宏观腐蚀行为,将尺寸为φ20 mm×2 mm 的试样在3.5%NaCl 溶液中开展为期24.0 h的浸泡试验。浸泡前,将试样通过400 ~2 000 号的水磨砂纸依次打磨后待测。腐蚀过程中间隔4 h 拍摄试样的宏观形貌,24.0 h 后通过扫描电子显微镜(SEM)观察各试样的腐蚀产物的微观形貌,以及经流水冲洗并用毛刷清理腐蚀产物后试样表面的微观腐蚀形貌。为了明确4 种钢的Fe/3.5%NaCl 溶液界面发生的电化学反应随时间的变化,测试4 种钢在3.5%NaCl 溶液中浸泡24.0 h 后的极化曲线。
1.5 腐蚀产物分析
通过Thermo Scientific K-Alpha+型X 射线光电子能谱(XPS)和SmartLab-SE 型X 射线衍射仪(XRD)分析各试验钢在3.5%NaCl 溶液中浸泡24.0 h 后的腐蚀产物。X 射线光电子能谱激发源是1 486.6 eV 的单色Al Kα,在5×10-7Pa 的真空度,通过能量为50 eV 的条件下完成测试,测试结果用284.8 eV 的C 1s 峰校准光谱,由Shirley 背景相减后,用XPS peak41 软件进行分峰。XRD 测试选用Cu 靶,扫描范围为5°~90°,扫描速率为4(°)/min。
2 结果与讨论
2.1 内部形貌和结构分析
试样A1~A4 的金相形貌和微观SEM 形貌如图1、2 所示。图1、2 中的“M”代表马氏体。

图1 试样A1~A3 的金相形貌和微观SEM 形貌Fig.1 Metallographic morphologies and microscopic SEM morphologies of samples A1~A3

图2 试样A4 的金相形貌和微观SEM 形貌Fig.2 Metallographic morphologies and microscopic SEM morphologies of samples A4
图1a,1c,1e,2a 显示了各试样的金相形貌,对比图1a、1e 发现,当Ni 含量相同时,Cr 含量越高试样的晶粒尺寸越细小;对比图1a、1c 发现,当Cr 含量相同时,Ni含量越高试样的晶粒尺寸亦越小;对比图1a、2a 发现,Cr 和Ni 含量同时增加,试样的晶粒尺寸的减小最显著。由划线法计算各试样的晶粒尺寸,可得A1 的晶粒尺寸为50 μm,A2 为80 μm,A3 为65 μm,A4 为100 μm。图1b,1d,1f 及2b 显示了各试样的微观SEM 形貌,对比可知,4 种试样的组织均为马氏体组织,图1b、1f 中马氏体板条均匀致密、碳化物在板条间弥散分布;图1d、2b 中马氏体板条粗大,近似块状、碳化物分布不均。这是因为钢中的Cr 和Ni 含量越多,晶粒和组织长大时的阻碍作用越明显[11],其中Cr 含量越多形成的Cr 碳化物越多,阻碍晶粒长大的效果越显著,而Ni 元素是非碳化形成元素,Ni 通过促进Cr 元素和C 的溶解来改善晶内马氏体组织[12]。综上可知,当含Cr 和Ni最高时,A1 试样的晶粒尺寸最小,马氏体组织最细小,A3 次之,A2 第三,A4 最差。以上结果说明,Cr 和Ni 含量均增加时,改善试样晶粒尺寸和组织的效果高于单独增加Cr 或Ni。
2.2 物相分析
图3 为试样的XRD 谱。将图3 中的衍射峰与α固溶体、Ni 元素和Cr 元素的标准卡进行对比可知,试样中(110)、(200)、(211)和(220)晶面为体心立方(BCC)的Fe-Cr-Ni α 固溶体,各试样中的碳化物主要是FeC 和Cr3C2,且当试样中Cr 含量增加、Ni 含量增加及Cr 和Ni 含量同时增加时,各相衍射峰的强度均增强,表明各物相的相对含量增加。钢中碳化物Cr3C2的相对含量增多、尺寸减小,更有利于晶粒和组织的细化[13],根据式(1)计算得到4 种试样中Cr3C2的尺寸如下:A1 为34 nm,A2 为58 nm,A3 为55 nm,A4 为60 nm,Cr 和Ni 含量均增加时,试样中Cr3C2的尺寸低于单独增加Cr 或Ni 的试样。可见,试样中Cr 含量的增加为Cr3C2的形成提供了更多原材料,而Ni 含量的增加促进了Cr3C2的形成,当试样中Cr 和Ni 含量均增加时,碳化物Cr3C2的尺寸显著降低、相对含量显著增加。
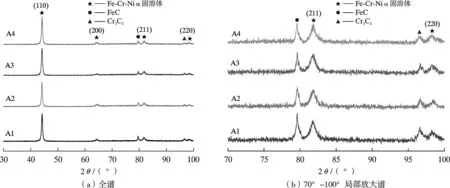
图3 试样的XRD 谱Fig.3 XRD patterns of samples
4 种试样的硬度如表2 所示。由表2 可知,4 种试样的硬度排序为A1>A3>A2>A4,结合表1 和图1、2 分析可知,Cr 含量或Ni 含量单独增加时,试样的晶粒尺寸减小,马氏体组织细化,使试样的硬度增加;当Cr 含量和Ni 含量同时增加时,试样的硬度最高。综合分析可知,Cr 和Ni 含量均增加时,试样中各物相的相对含量、硬度均高于单独增加Cr 或Ni 的试样。

表2 4 种试样的硬度Table 2 Hardness of four kinds of samples
2.3 电化学性能
4 种钢在3.5%NaCl 溶液中的开路电位和浸泡0.5 h 后的极化曲线如图4 所示。由图4a 可知,Cr 和Ni 含量最高的A1 试样的开路电位值最大,对比可知,增加Ni 或增加Cr 均能提高试样的开路电位,且在Ni 含量较低时增加Cr,试样的开路电位降低,说明试样的开路电位受Cr 和Ni 的共同影响。由图4b 可知,A1 的自腐蚀电位最大,自腐蚀电流密度最小。自腐蚀电位是反映材料腐蚀趋势的热力学参数,自腐蚀电流密度是反映材料腐蚀反应快慢的动力学参数[14]。通过3 组平行测试取平均值后得到试样的极化曲线拟合参数如表3所示。表3 显示各试样的极化电阻(Rp)排序为A1>A3>A2>A4,对应的自腐蚀电流密度排序为A1 <A3 <A2<A4,A1 具有最大的极化电阻和最低的腐蚀速率,说明Cr 和Ni 对提高试验钢的电化学腐蚀热力学稳定性和腐蚀动力学稳定性有叠加促进的作用。
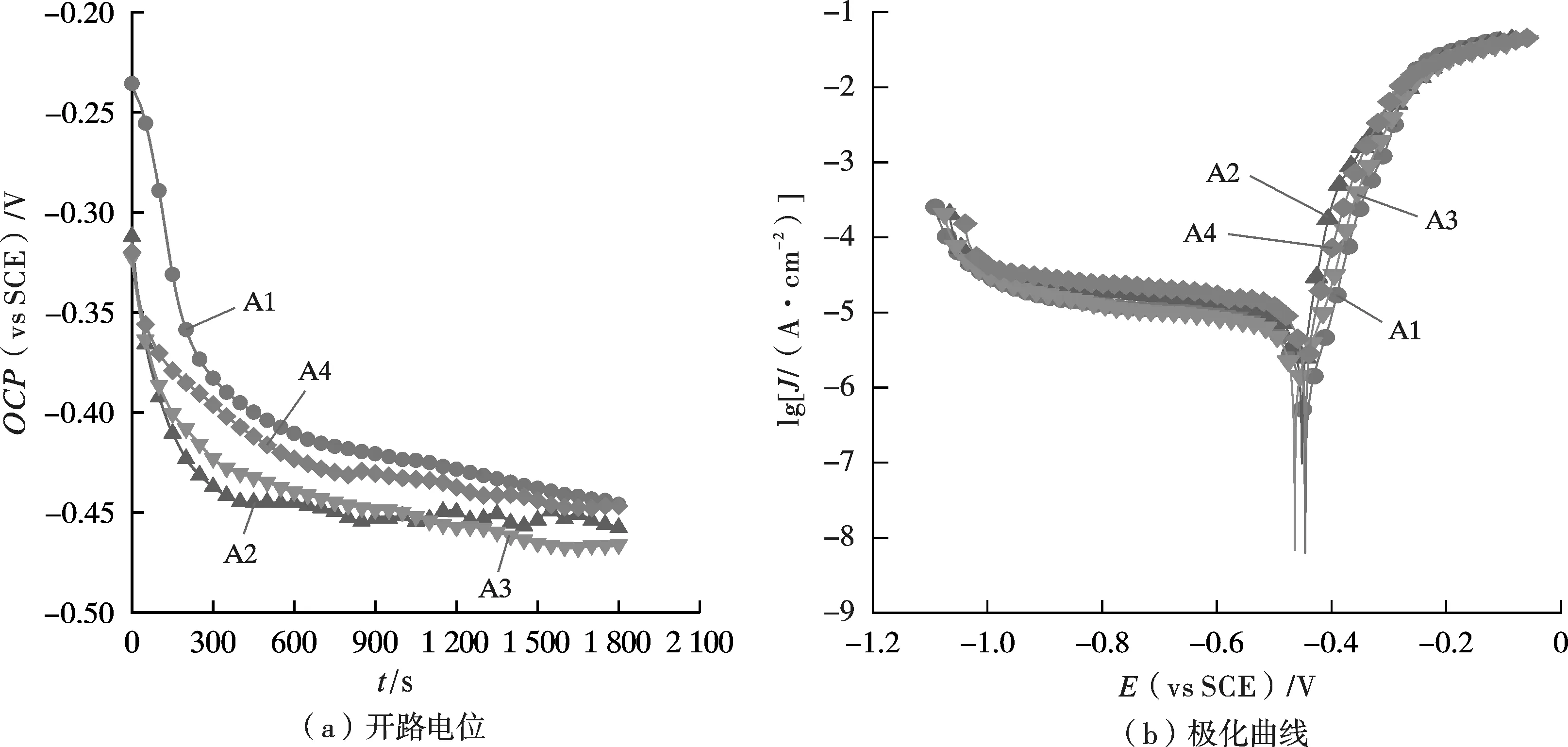
图4 4 种钢在3.5%NaCl 溶液中的开路电位和浸泡0.5 h 后的极化曲线Fig.4 Open circuit potential and potentiodynamic polarization curves of four kinds of steel after immersion in 3.5%NaCl solution for 0.5 h
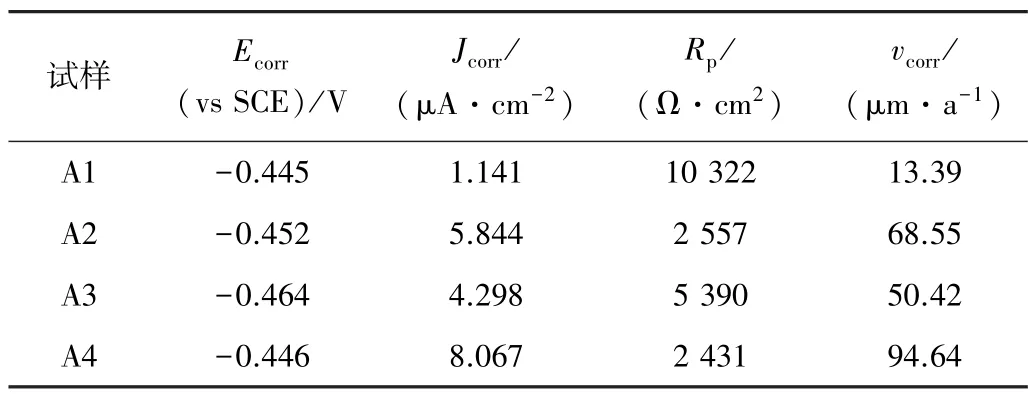
表3 浸泡0.5 h 后试样的极化曲线拟合参数Table 3 Fitting parameters of the polarization curves of samples after immersion for 0.5 h
图5 为试样在3.5%NaCl 溶液中开路电位稳定后的电化学阻抗谱和等效电路。由图5a 可知,各试样的容抗弧半径排序为A1>A3>A2>A4,容抗弧半径大小能反映电荷转移电阻的大小,容抗弧半径越大,材料的耐腐蚀性越好[15];图5b 显示,各试样的最大相位角排序为A1>A3>A2>A4,最大相位角与材料表面的腐蚀损伤程度有关,最大相位角越大,材料抵抗腐蚀损伤的能力越强,材料的耐腐蚀性越好[16]。

图5 试样在3.5%NaCl 溶液中开路电位稳定后的电化学阻抗谱和等效电路Fig.5 EIS and equivalent circuit of the samples after stabilizing their open circuit potential in 3.5%NaCl solution
由图5 分析可知,A1 试样的耐蚀性最好。由图5c可知,各试样的电化学阻抗谱可由等效电路Rs{Qf[Rf(QdlRct)]}拟合,等效电路中,Rs代表溶液电阻,Qf代表腐蚀产物电容,Rf代表腐蚀产物电阻,Rct代表电荷转移电阻,Qdl表示双层电容。试样的电化学阻抗谱拟合参数如表4 所示。表4 中YOf表示腐蚀产物电容Qf的常数,nf表示腐蚀产物电容Qf的指数,YOdl表示双层电容Qdl的常数,ndl表示双层电容Qdl的指数,对比各试样的Rct和Rf可知,Cr 和Ni 含量同时增加时(A1 试样),Rct和Rf的值均最大,说明Cr 和Ni 对提高试验钢的电荷转移电阻和腐蚀产物电阻有叠加促进的作用。电化学阻抗谱显示A1 试样的耐蚀性最高,与极化曲线分析结果相一致。

表4 试样的电化学阻抗谱拟合参数Table 4 Fitting parameters of EIS of samples
2.4 浸泡试验结果
各试样在3.5%NaCl 溶液中24.0 h 浸泡试验结果如下:各试样被置入3.5% NaCl 溶液中后,0.5 h 时,A3、A4 表面出现了不同数量的腐蚀斑点,A1、A2 的表面无宏观腐蚀痕迹;4.0 h 时,所有试样表面均出现不同程度的腐蚀区域,A4 的腐蚀区域最大,A3 表面有较多腐蚀斑点,A2 表面有较深腐蚀沟,A1 表面局部表层发生腐蚀。随着浸泡时间的进一步延长,A1 试样表面的腐蚀区域逐渐扩大,A2 表面的腐蚀沟痕逐渐增多,A3 和A4 表面的腐蚀区域面积快速增加;24.0 h时,A1、A2 表面发生局部腐蚀,A3、A4 基本为全面腐蚀;清理腐蚀产物后,各试样表面宏观腐蚀面积排序为A4>A3>A1>A2,显示各试样腐蚀程度依次为A4>A3>A1>A2。
试样在3.5%NaCl 溶液中浸泡24.0 h 后的腐蚀产物的微观SEM 形貌如图6 所示。在3.5%NaCl 溶液中浸泡24.0 h 并经流水冲洗且用毛刷清理腐蚀产物后试样表面的微观SEM 形貌如图7 所示。

图6 试样在3.5%NaCl 溶液中浸泡24.0 h 后的腐蚀产物的微观SEM 形貌Fig.6 Microscopic SEM morphologies of corrosion products after immersion of samples in 3.5%NaCl solution for 24.0 h

图7 在3.5%NaCl 溶液中浸泡24.0 h 并经流水冲洗且用毛刷清理腐蚀产物后试样表面的微观SEM 形貌Fig.7 Microscopic SEM morphologies of surfaces of samples after immersion in 3.5%NaCl solution for 24.0 h,rinsing with running water,and cleaning the corrosion products with a brush
由图6a、7a 可知,A1 表面的腐蚀产物细小致密,清理后A1 表面平坦,有细小微裂纹;由图6b、7b 可知,A2腐蚀产物结晶尺寸比A1 的粗大,清理后A2 的表面出现局部小块龟裂形貌;由图6c、7c 可知,A3 的腐蚀产物层疏松,有裂纹,清理后A3 表面有较深较长的裂纹;由图6d、7d 可知,A4 的腐蚀产物层的结晶疏松,分布不均,清理后A4 表面的裂纹较A3 更深更长。综合宏观腐蚀情况、腐蚀产物微观形貌和清理腐蚀产物后的微观形貌可知:Cr 相同、增加Ni 或Ni 相同、增加Cr 的情况下,试样的腐蚀产物的尺寸减小,腐蚀产物层的致密度增加,同时基体腐蚀裂纹减少;Cr 和Ni 同时增加,试样的腐蚀产物结晶尺寸细化、清理后基体腐蚀裂纹减少的程度最显著,说明Cr 和Ni 对提高腐蚀产物的致密性有叠加促进作用,进而显著提高腐蚀产物对基体试验钢的保护作用,提高试验钢的耐蚀性。
试样在3.5%NaCl 中浸泡24.0 h 后的极化曲线如图8 所示。表5 列出了浸泡24.0 h 后试样的极化曲线拟合参数。对比图8 和表5 可知,A1 的极化电阻值远远高于其他组,各试样的极化电阻排序为A1>A2>A3>A4,对应的自腐蚀电流密度排序为A1<A2<A3<A4;与浸泡0.5 h 后的极化曲线拟合参数对比可知,浸泡24.0 h 后A1、A2、A4 的极化电阻均增加,自腐蚀电流密度显著减小,而A3 在浸泡24.0 h 后极化电阻减小,自腐蚀电流密度增加。这是因为试样表面的腐蚀产物层致密性越高,腐蚀产物下基体表面腐蚀裂纹数量越少、尺寸越小,对Cl-侵蚀的抵抗作用越强,材料的耐腐蚀性越好[17,18]。

图8 试样在3.5%NaCl 中浸泡24.0 h 后的极化曲线Fig.8 Polarization curves of samples after immersion in 3.5%NaCl for 24.0 h
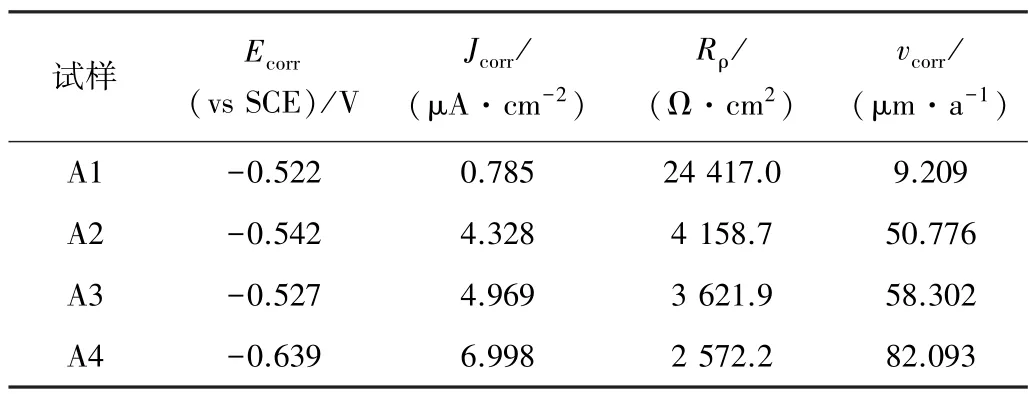
表5 浸泡24.0 h 后试样的极化曲线拟合参数Table 5 Fitting parameters of the polarization curves of samples after immersion for 24.0 h
对比4 种试样浸泡0.5 h 后和浸泡24.0 h 后的耐蚀性可知,4 种钢在浸泡0.5 h 后的电化学行为受Cr 和Ni 总含量的影响较大,而浸泡24.0 h 的腐蚀形貌和电化学行为受腐蚀产物致密性的影响较大。
2.5 腐蚀产物分析
图9 为4 种钢在3.5%NaCl 溶液中浸泡24.0 h 后腐蚀产物的XPS 全谱。
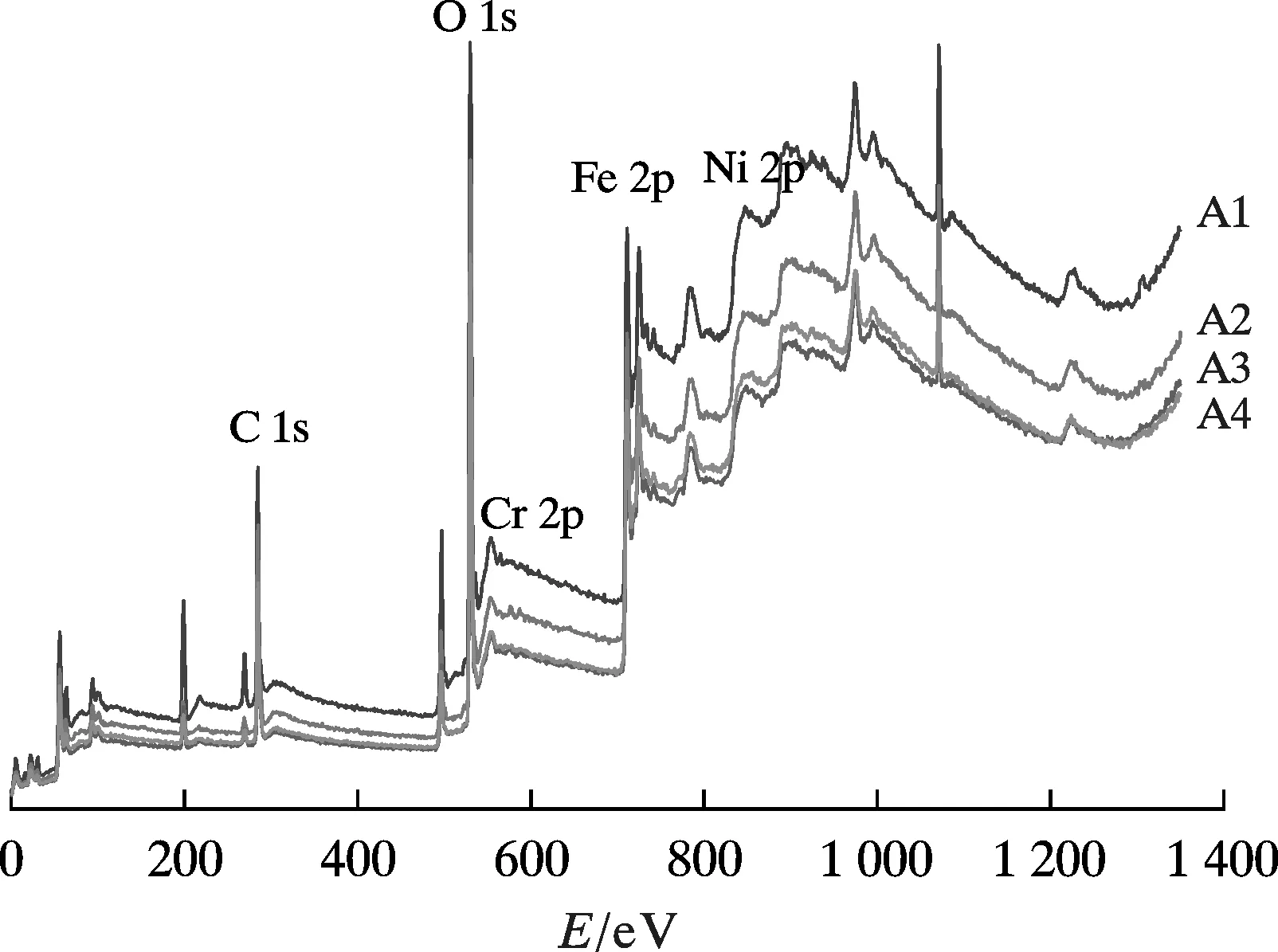
图9 4 种钢在3.5%NaCl 溶液中浸泡24.0 h 后腐蚀产物的XPS 全谱Fig.9 XPS full spectra of corrosion products of four kinds of steels after immersion in 3.5%NaCl solution for 24.0 h
由图9 可知,4 种试样的腐蚀产物中O、Fe、Cr、Ni、C 5 种元素的峰强度较高,其中A1 试样腐蚀产物的各元素的峰强度最高。图9 说明4 种试样的腐蚀产物的主要成分为Fe、O、Cr、Ni 等一种或多种元素组成的化合物。
图10 为4 种钢在3.5%NaCl 溶液中浸泡24.0 h 后的腐蚀产物的Fe 2p 分峰谱及Fe 化合物的主要成分的比例。由图10a ~10d 可知,通过Shirley 算法减除背景后,所有试样表面腐蚀产物的Fe 2p 谱分成FeO(709.5 eV)、α-Fe2O3(710.5 eV)、FeOOH(711.5 eV)、γ-Fe2O3(712.6 eV)共4 个明显的峰,由此可知,各试样表面腐蚀产物主要由Fe2+和Fe3+的化合物组成。各试样的腐蚀产物中Fe 2p 峰强度的对比如图10e 所示,4 种试验钢的腐蚀产物中Fe 2p 峰的强度排序为A1>A2>A4>A3,说明A1 的腐蚀产物的耐蚀性较高[19]。各试样腐蚀产物中Fe化合物的主要成分的比例如图10f。通过各化合物对应的Fe 2p 谱分峰面积计算Fe2+化合物的摩尔分数与Fe3+化合物的摩尔分数的比值,得到A1、A2、A3、A4 的腐蚀产物中Fe2+/Fe3+分别为:0.30、0.24、0.25、0.21;对比可知,Cr相同、增加Ni 试样的Fe2+/Fe3+升高,Ni 相同、增加Cr 试样的Fe2+/Fe3+升高,Ni 和Cr 同时增加时,试样的Fe2+/Fe3+升高最显著;Fe2+含量的增加能提高腐蚀产物层的致密性[20],进而提高材料的耐腐蚀性。因此,同时增加Ni 和Cr 的含量对促进Fe2+/Fe3+值增加的效果更显著,对提高试样表面腐蚀产物层致密性的效果更显著。
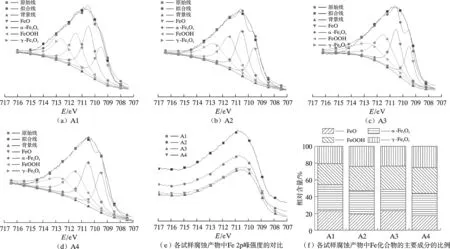
图10 4 种钢在3.5%NaCl 溶液中浸泡24.0 h 后的腐蚀产物的Fe 2p 分峰谱及Fe 化合物的主要成分的比例Fig.10 The Fe 2p peaking spectra of corrosion products of four kinds of steels immersed in 3.5%NaCl solution for 24.0 h and the proportion of main components of Fe compounds
4 种钢在3.5%NaCl 溶液中浸泡24.0 h 后的腐蚀产物的O 1s 分峰谱如图11 所示。通过Shirley 算法减除背景后,所有试样表面腐蚀产物的O 1s 谱分为5 个明显的峰: 529.1,529.5,530.1,530.8,531.4 eV,根据元素/化合物结合能表和文献[21]可知,上述峰位分别对应:NiCr2O4、Fe2O3、FeO、FeCr2O4、FeOOH。由上述分析可知,Fe、Cr、Ni、O 参与了腐蚀反应。
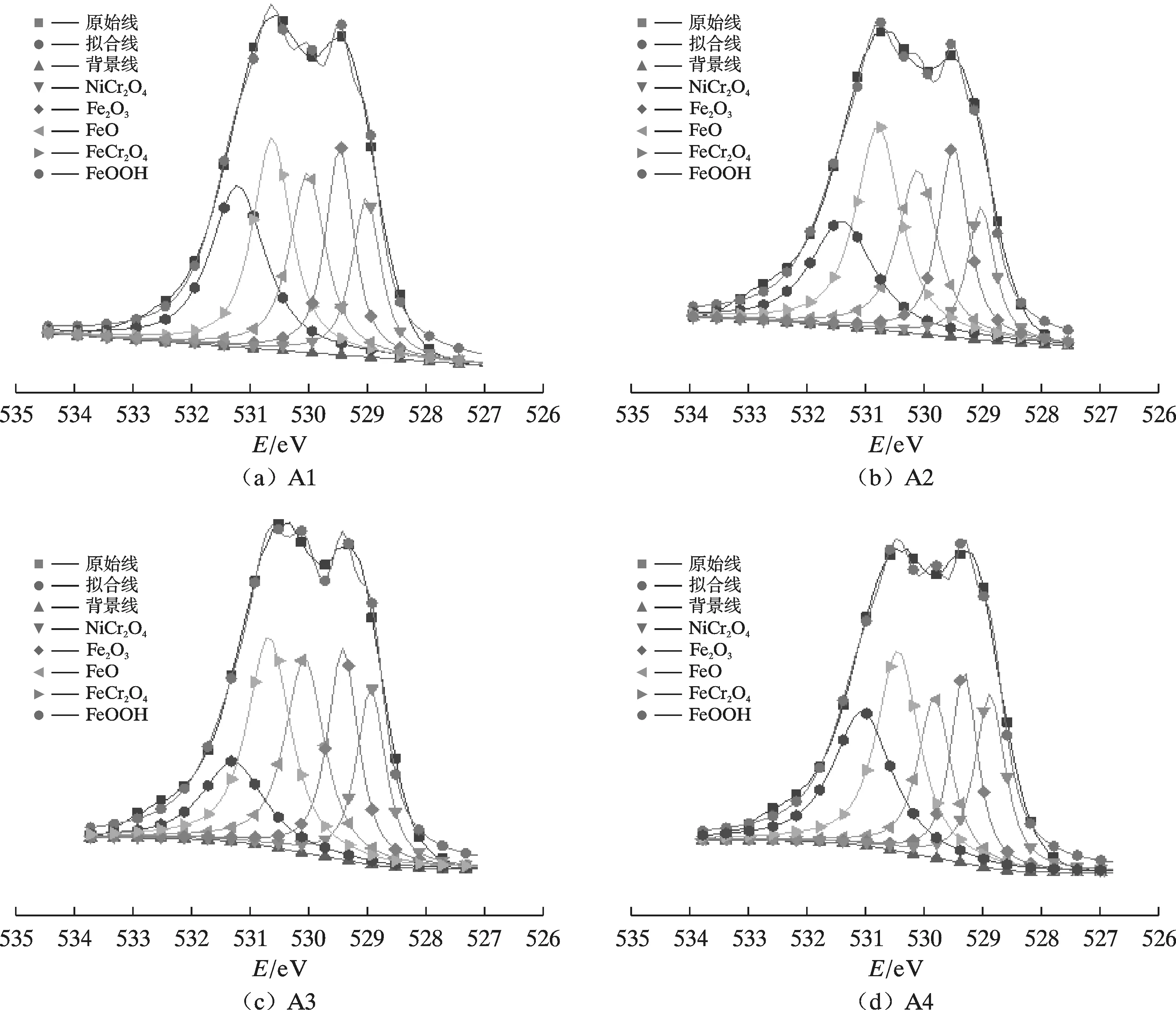
图11 4 种钢在3.5%NaCl 溶液中浸泡24.0 h 后的腐蚀产物的O 1s 分峰谱Fig.11 The O 1s peaking spectra of corrosion products of four kinds of steels immersed in 3.5%NaCl solution for 24.0 h
图12 为4 种钢在3.5%NaCl 溶液中浸泡24.0 h 后的腐蚀产物的Ni 2p 分峰谱。通过Shirley 算法减除背景后,所有试样表面腐蚀产物的Ni 2p 谱分为2 个明显的峰: NiFe2O4(854.3 eV)、Ni(OH)2(855.3 eV )。图13 为4 种钢在3.5%NaCl 溶液中浸泡24.0 h 后的腐蚀产物的Cr 2p 分峰谱。通过Shirley 算法减除背景后,所有试样表面腐蚀产物的Cr 2p 谱分为2 个明显的峰:FeCr2O4(576.6 eV)、CrO3(579.5 eV)。腐蚀产物中的NiFe2O4和FeCr2O4均是由Ni 和Cr 替代Fe3O4中的Fe而形成的,均能提高试验钢腐蚀产物膜的致密性,进而提高试验钢的耐腐蚀性能[22,23]。图14 为4 种钢在3.5%NaCl 溶液中浸泡24.0 h 后的腐蚀产物中Ni 化合物和Cr 化合物的主要成分的比例。由图14 可知,Cr相同,增加Ni 时,试样腐蚀产物中NiFe2O4和FeCr2O4的比例均提高,Ni 相同,增加Cr 时,试样腐蚀产物中NiFe2O4和FeCr2O4的比例也提高;说明增加Ni 能促进试样腐蚀产物中FeCr2O4占比的提高,增加Cr 能促进试样腐蚀产物中NiFe2O4占比的提高,即Ni 和Cr 对提高腐蚀产物的致密性有叠加促进作用。
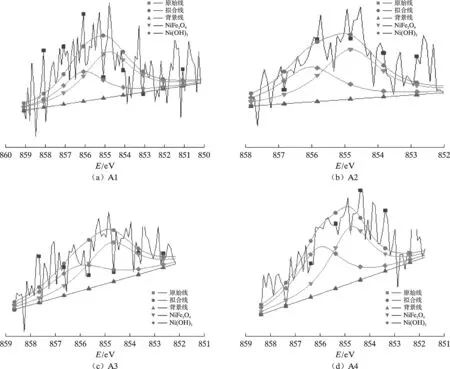
图12 4 种钢在3.5%NaCl 溶液中浸泡24.0 h 后的腐蚀产物的Ni 2p 分峰谱Fig.12 The Ni 2p peaking spectra of corrosion products of four kinds of steels immersed in 3.5%NaCl solution for 24.0 h
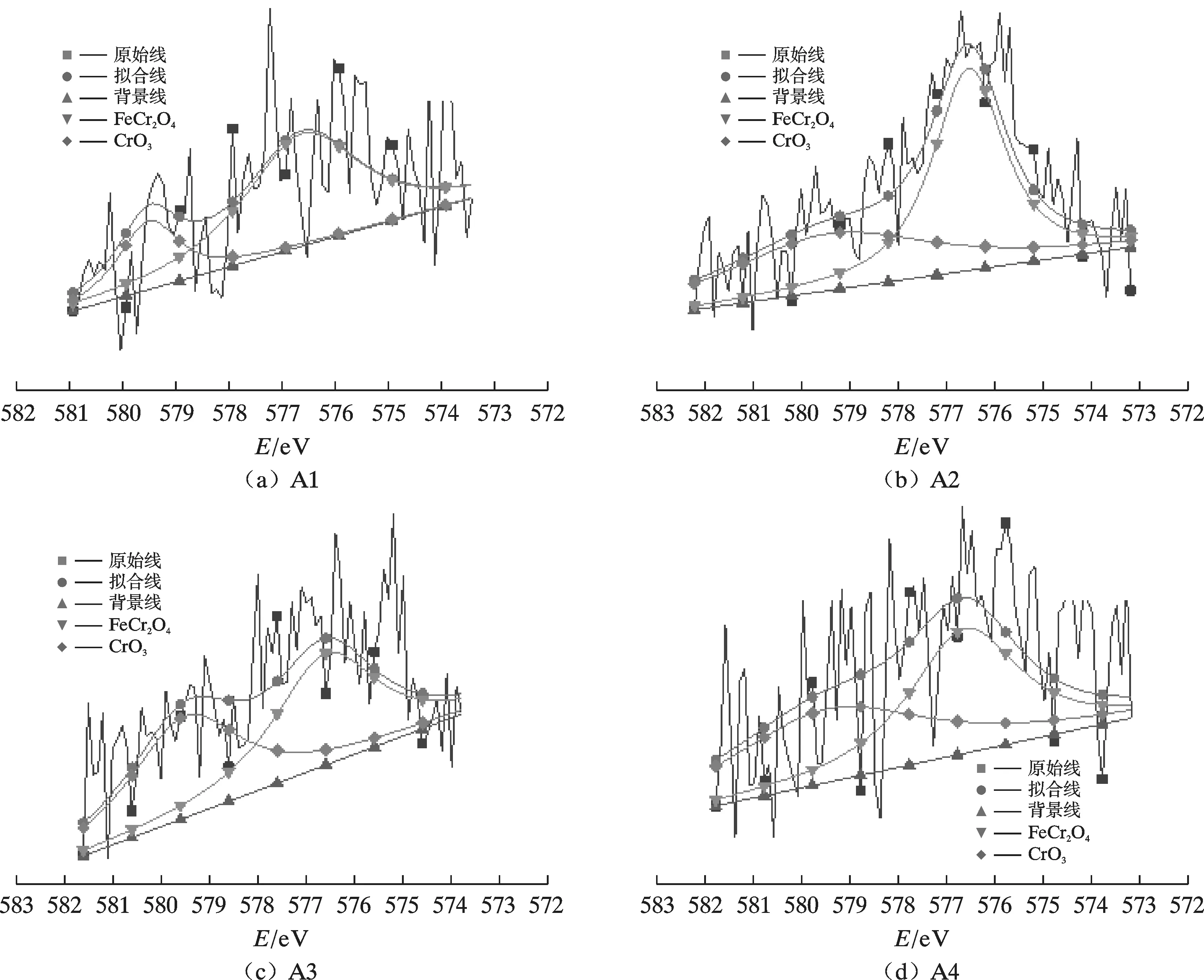
图13 4 种钢在3.5%NaCl 溶液中浸泡24.0 h 后的腐蚀产物的Cr 2p 分峰谱Fig.13 The Cr 2p peaking spectra of corrosion products of four kinds of steels immersed in 3.5%NaCl solution for 24.0 h
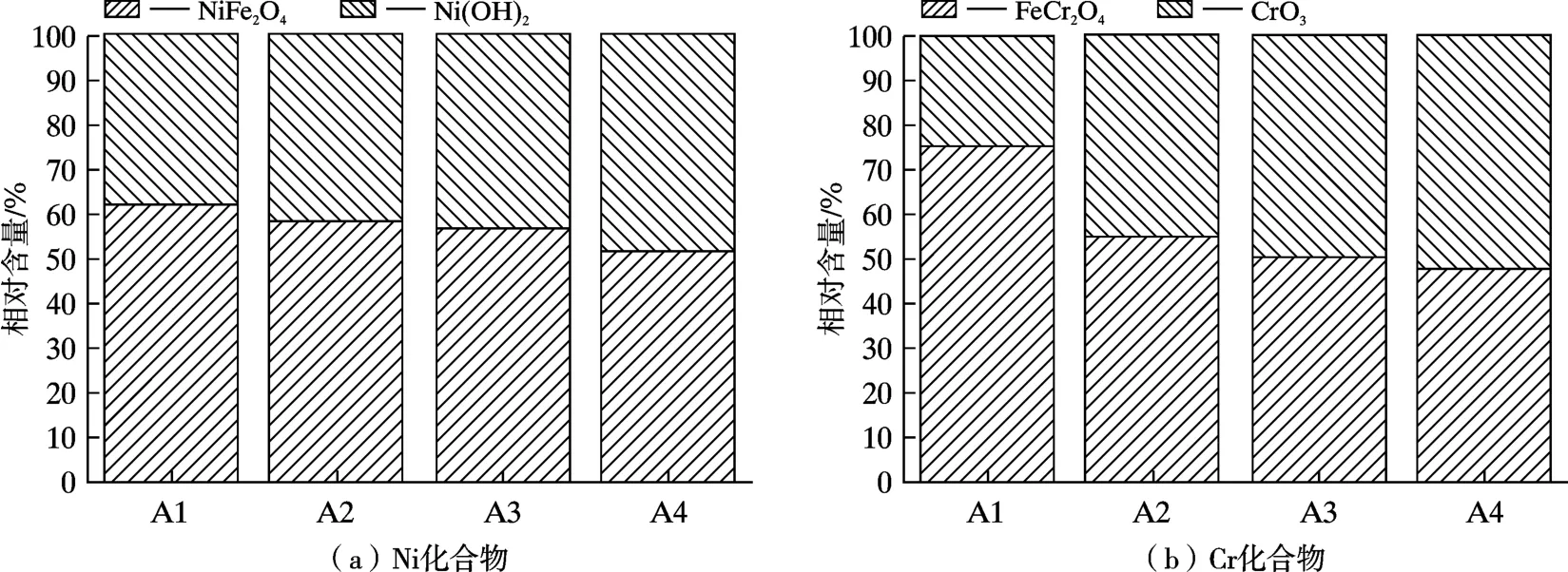
图14 4 种钢在3.5%NaCl 溶液中浸泡24.0 h 后的腐蚀产物中Ni 化合物和Cr 化合物的主要成分的比例Fig.14 The proportion of main compositions of Ni compound and Cr compound in the corrosion products of four kinds of steels after immersing in 3.5%NaCl solution for 24.0 h
4 种钢在3.5%NaCl 溶液中浸泡24.0 h 后的腐蚀产物物相对比如图15 所示。在模拟海水(3.5%NaCl溶液) 环境中,A1 表面腐蚀产物由β - FeOOH,α-FeOOH,Fe3O4和FeO 组成,A2 表面腐蚀产物由β-FeOOH,α-FeOOH,γ-FeOOH,Fe3O4和FeO 组成,A3 和A4 表面腐蚀产物由β - FeOOH,α - FeOOH,γ-FeOOH和Fe3O4组成。结合图10f 和图15,对比A1与A3、A1 与A2 发现,当试样中Cr 或Ni 的含量增加时,腐蚀产物中α-FeOOH,Fe3O4和FeO 的相对含量增加,β-FeOOH,γ-FeOOH 的相对含量减少;对比A1 与A4,当Cr 和Ni 的含量同时增加时,腐蚀产物中α-FeOOH,Fe3O4和FeO 峰的强度增加得最显著,β-FeOOH,γ-FeOOH峰的强度减弱得最显著,说明同时增加Cr 和Ni 对腐蚀产物中各相对应的峰的强度的影响更显著。腐蚀产物中α-FeOOH,Fe3O4和FeO 的致密性较高,对基体表现出较好的保护性[24],β-FeOOH,γ-FeOOH 的电化学活性较高,耐腐蚀性较差[25]。因此可知,在Cr 和Ni 的叠加促进作用下,A1表面腐蚀产物中致密的α-FeOOH,Fe3O4和FeO 的相对含量较高,使其耐蚀性最好。
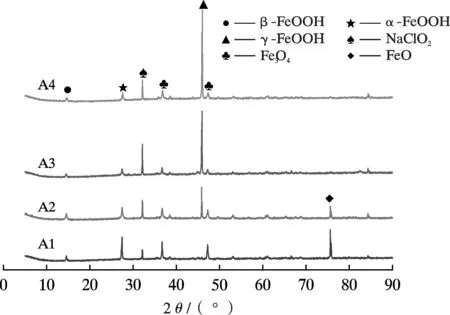
图15 4 种钢在3.5%NaCl 溶液中浸泡24.0 h 后的腐蚀产物物相对比Fig.15 Comparison of the phases of corrosion products of four kinds of steels after immersing in 3.5%NaCl solution for 24.0 h
3 结 论
(1)在试样中增加Cr 含量能促进晶粒尺寸减小,增加Ni 含量能促进马氏体组织细化,同时增加Cr 和Ni 含量时合金钢的晶粒尺寸和微观组织最佳。含Cr和Ni 钢的物相均为Fe-Cr-Ni 固溶体、FeC 和Cr3C2。Cr 和Ni 含量均增加时,试样中各物相的相对含量、硬度均高于单独增加Cr 或Ni 的试样;Cr 和Ni 含量均增加时,试样中Cr3C2的尺寸低于单独增加Cr 或Ni 的试样。Cr 和Ni 合金化对钢的微观结构和相结构的优化有叠加促进作用。
(2)电化学测试显示,同时增加Cr 和Ni 含量时,试验钢在模拟海水环境中的耐蚀性大于单独增加Cr或Ni 的试验钢,说明Cr 和Ni 对钢耐蚀性的提升存在叠加促进的作用。
(3)腐蚀产物分析显示,同时增加钢中Cr 和Ni 含量时,试验钢腐蚀产物中FeCr2O4、NiFe2O4、FeO 等能提高腐蚀产物致密性的成分增加量大于单独增加Cr 或Ni 的试验钢,说明Cr 和Ni 对腐蚀产物致密性的提高有叠加促进作用。

