冠状动脉钙化程度对冠状动脉完全闭塞性病变介入治疗的影响
孔天钟,戴欣彤,侯爱洁,栾波,张晓娇,王永
冠状动脉钙化(CAC)的程度可有效体现冠状动脉(冠脉)粥样硬化斑块负荷程度且与接受经皮冠脉介入治疗(PCI)术后不良心血管病事件及预后有密切关系[1]。流行病学资料显示,约1/3的冠脉病变中可见中重度钙化。而在冠脉CT中显示狭窄程度>75%冠脉节段中,钙化病变占54%[2]。现有研究表明,冠脉内膜钙化是冠脉钙化的主要类型且对于介入手术影响较大,其形成主要与血管内皮细胞损伤和炎症刺激密切相关[3]。相比于无钙化病变患者,钙化在管腔内复杂的分布与形态直接导致了患者在接受PCI期间及PCI术后的临床结局相对更差,患者发生冠脉夹层、靶血管病变血运重建甚至死亡的概率更高[4]。对于冠脉完全闭塞性病变(CTO)患者而言,严重的冠脉钙化所带来的管腔高阻力、成角和迂曲直接影响手术成功率及患者预后[5]。因此,探究冠脉钙化病变的人群特征,病变特点及影响钙化病变介入手术成功与否的因素对于术前筛查高危人群、提高手术成功率、改善预后具有重要的临床意义。
1 资料与方法
1.1 研究对象本研究纳入2019年11月至2021年11月于辽宁省人民医院心内科就诊的经冠脉造影证实为CTO病变且行经皮冠脉支架植入术的患者205例,所有患者均在术前签署知情同意书,并于术中证实CTO病变存在钙化。根据钙化病变的程度分为无钙化/轻度钙化组(n=119)及中度/重度钙化组(n=86),分析所有患者的基线资料与造影结果,探究不同程度的钙化对于CTO介入治疗的影响。
1.2 相关定义CTO病变的定义为:经冠脉造影证实至少有1支血管100%完全闭塞,即远端血流为心肌梗死溶栓治疗血流分级(TIMI)0级,且病史超过3个月[6]。依据冠脉造影的结果将钙化病变的严重程度分为:无钙化及轻度钙化:仅在心脏搏动时看到淡而模糊的高密度影,心脏不搏动时完全看不到钙化影的存在。中度钙化:在心脏搏动时看到较清晰、易看到的高密度影。重度钙化:在心脏搏动与不搏动时均可看到清晰的高密度影[2]。CTO手术的难易程度由J-CTO评分判定[7]。操作成功的定义为:术后管腔内残余狭窄<30%且血流恢复为TIMI3级。手术成功的定义为:在操作成功的基础上不发生术后不良事件:如死亡、卒中、围术期心肌梗死、急性心包填塞、急诊冠脉旁路移植术(CABG)等[9]。
1.3 方法全部纳入人群依照冠脉造影结果所示的钙化程度分为两组:无钙化/轻度钙化组(n=119)和中度/重度钙化组(n=86)。记录患者的基线资料,包括年龄、性别、体质指数、既往病史、手术史等。记录患者的手术及病变相关数据,包括病变血管部位、病变特征、导丝寻径策略等。统计不同组别患者手术成功与否及术后不良事件发生的情况。
1.4 统计学分析采用SPSS 26.0软件进行数据分析。符合正态分布的资料均采用均数±标准差()表示,组间比较采用独立样本t检验。不符合正态分布的资料均采用中位数(四分位数)表示,组间比较采用非参数检验。计数资料采用例数(构成比)表示,组间比较采用χ2检验或Fisher检验。使用单变量logistic回归检验分析钙化病变的程度对手术成功的影响。P<0.05为差异具有统计学意义。
2 结果
2.1 两组患者基线数据的比较205例纳入研究的患者中,存在中度/重度钙化的CTO患者86例(42%),与无钙化/轻度钙化的患者相比,患者在平均年龄(66.9岁vs.63.8岁,P=0.030)、糖尿病史(53.5%vs.30.3%,P<0.001)、高血压史(72.1%vs.49.6%,P=0.003)、1年以上吸烟史(70.9%vs.52.9%,P=0.009)以及CABG史(34.9%vs.8.4%,P<0.001)上有明显统计学差异。相比于与无钙化/轻度钙化组的患者,中度/重度钙化组的患者左室射血分时更低(45%vs.51%,P=0.003),表1。
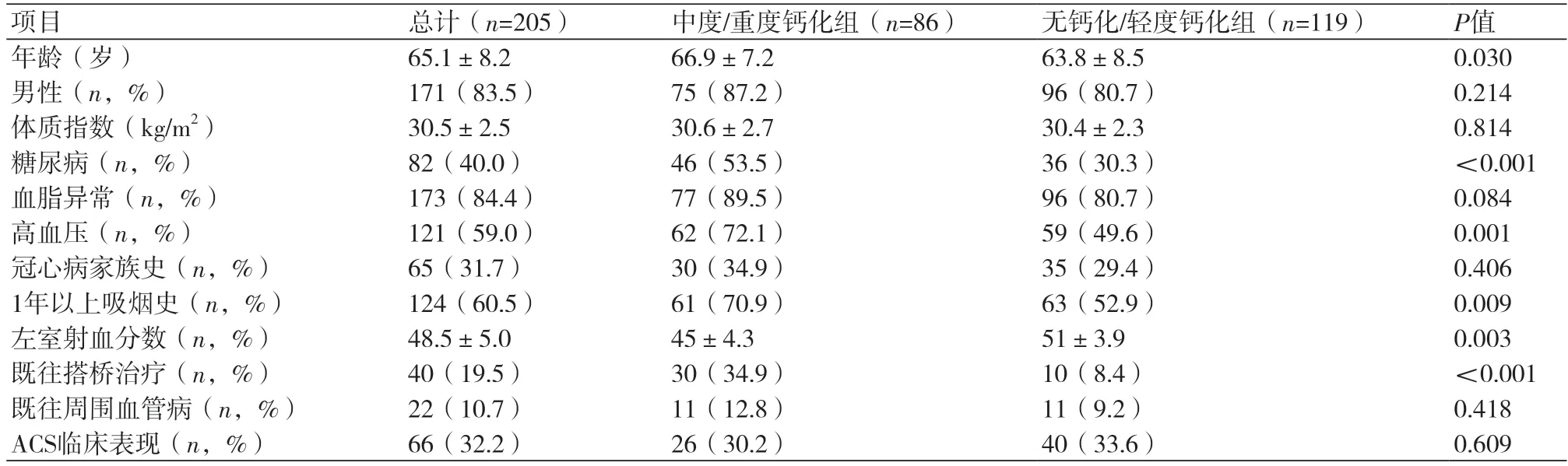
表1 两组患者一般资料的比较

表3 两组患者斑块修饰技术使用的比较
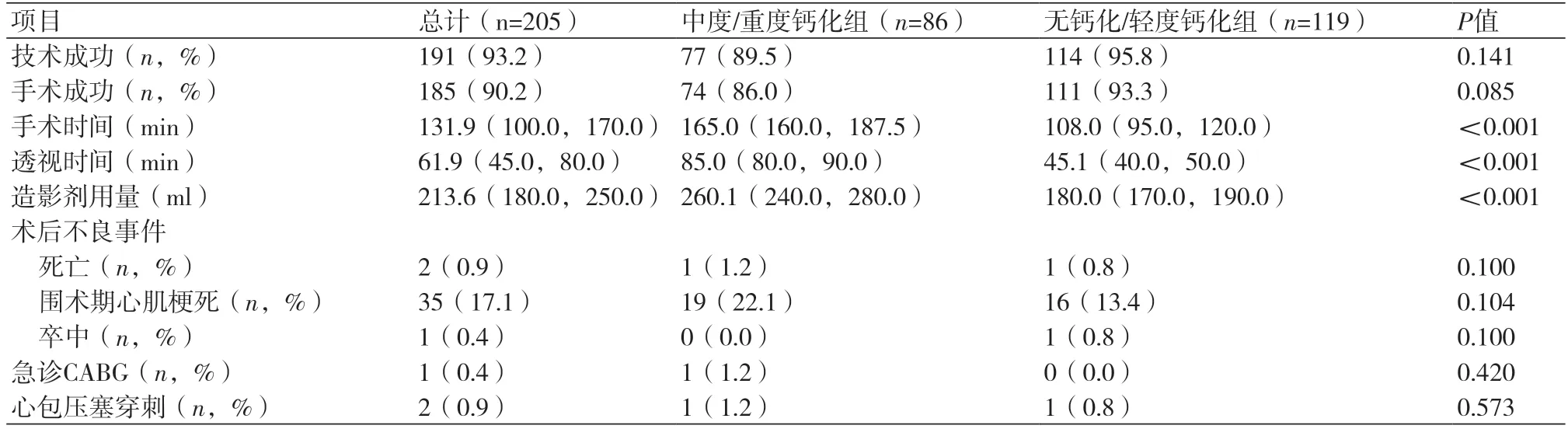
表4 两组患者的手术结局
2.2 两组患者手术策略及造影特征的比较本研究中,最易发生钙化的CTO病变靶血管为右冠脉(51.2%),其次为前降支(33.2%)和回旋支(16.1%)。在血管入路方面,两组患者的差异无统计学意义。相对于无钙化/轻度钙化组的患者,中度/重度钙化组的患者J-CTO评分更高(3.30±1.0分vs.1.90±0.50分,P<0.001),血管直径更大(3.0 mmvs.2.4 mm,P<0.001)、病变更长(30.0 mmvs.26.0 mm,P<0.001)。此外,中度/重度钙化组钝性开口(70.9%vs.21.0%,P<0.001)更多,支架内狭窄更多(25.6%vs.5.9%,P<0.001),中度/重度钙化组的逆向策略更多(81.4%vs.37.8%,P<0.001)、植入支架的数量更多(2.8支vs.2.1支,P<0.001)、使用切割/棘突球囊(74.4%vs.19.3%,P<0.001)以及冠脉旋磨技术(11.6%vs.0.8%,P=0.002)更多。
2.3 两组患者手术结局的比较两组患者在手术成功(89.5%vs.95.8%,P=0.141)与技术成功(86.0%vs.93.3%,P=0.085)上的差异没有统计学意义。中度/重度钙化组患者手术时间(165.0 minvs.108.0 min,P<0.001)和透视时间更长(85.0 minvs.45.1 min,P<0.001),造影剂用量更多(260.1 mlvs.180.0 ml,P<0.001)。而对于术后不良事件的发生情况,两组患者在死亡、围术期心肌梗死、卒中、急诊CABG和急性心包压塞的差异无统计学意义。
3 讨论
冠脉完全闭塞性病变(CTO)指经冠脉造影证实至少有1支冠脉血管100%完全闭塞,即TIMI分级为0级,且病史超过3个月的病变[6]。钙化病变指钙磷复合物在冠脉血管壁上的异常沉积。研究表明,二者均增加了冠脉介入治疗的难度及并发症的发生[8]。本研究发现,中度/重度钙化的CTO病变约占全部钙化CTO病变的41.8%。此类患者年龄更高、射血分数更低、糖尿病史、高血压病史及1年以上吸烟史;其次,中度/重度钙化组的CTO患者手术更加复杂,所需手术时间和透视时间更长,造影剂用量更多。但对于经验丰富的术者,钙化病变的程度对于CTO-PCI的手术成功率及术后不良事件的发生情况并无明显影响。
对钙化病变的病理学研究证实:血脂异常、高血压、免疫系统疾病、糖尿病及肾脏疾病都会影响动脉硬化、血管重塑以及血管内膜钙化的过程[10]。本研究的205例患者中,19.5%的患者有既往CABG史,此类患者更易出现严重钙化。一项基于PROGRESS-CTO注册研究同样报道了相较于既往未行CABG的患者,既往行CABG的患者有更高的J-CTO评分和更低的手术/技术成功率,也易出现更严重的钙化[11]。另一项研究则表明,既往CABG手术史合并CTO的患者更易产生更严重的钙化以及负性重构[12]。此外,CABG还会导致原位血管扭曲和闭塞端钝性出口,给术中导丝通过造成了极大的困难,增加了手术的难度[13]。
通过对两组患者造影结果的比较得出:本研究中,中度/重度钙化组的J-CTO评分更高、病变更长、管腔直径更大、支架内狭窄更多。相关研究表明,冠脉钙化属于高阻力病变,不但增加了器械通过的难度、限制了球囊与支架的充分扩张,且增加了CTO-PCI过程中冠脉夹层与穿孔的风险[14]。此外,J.T.HSU等研究发现钙化病变的长度严重影响CTO-PCI的成功率[15]。但本研究中两组患者在病变扭曲和近端纤维帽模糊上无统计学差异。
本研究中两组患者手术与技术成功率的差异无统计学意义,术者的经验丰富可能是原因之一;此外,逆向策略的应用,板块修饰技术如切割/棘突球囊与冠脉旋磨的使用也很大程度提高了中度/重度钙化组患者的手术成功率。本研究的中度/重度钙化组患者更多使用了切割/棘突球囊和冠脉旋磨术。切割球囊能以较低的压力对钙化斑块进行有序、充分的扩张,减轻对血管内膜的损伤,而棘突球囊表面的特制尼龙棘突则可有效地嵌入斑块[16]。冠脉旋磨术通过打磨钙化斑块改善血管的顺应性,扩大管腔内径,有利于器械通过病变[17]。相关研究表明,使用斑块修饰技术并不会增加CTO-PCI不良事件的发生,且可提高严重钙化病变的手术成功率[18]。本研究的中度/重度钙化组采用了更多的逆向策略。RECTO注册研究证实,对于重度钙化、血管迂曲和长度>30 mm的CTO病变,采用逆向策略可大大增加手术的成功率[19]。
一项来自日本学者的研究发现,J-CTO评分过高的CTO病变,尤其是存在钙化的病变,术者一般很难在30 min内成功通过导丝,极大增加了手术时间、透视时间和造影剂的用量,影响手术的成功率[20]。与既往研究相符,本研究的中度/重度钙化组的患者手术时间更长,透视时间更久,造影剂使用更多;而两组患者术后不良事件的发生情况与钙化程度无关,可能与先进设备的使用与技术的提升有关。
综上所述,相较于无钙化/轻度钙化的CTO病变,中度/重度钙化的CTO病变手术更加复杂,所需的手术时间和透视时间更长,造影剂用量更多,但钙化病变的程度对于CTO-PCI的手术成功率以及术后安全性事件的发生情况并无明显影响。本研究同样存在不足,首先,本研究为单中心研究,纳入患者数量有限;其次,对患者未进行长期随访,无法得知钙化病变的严重程度对于远期预后的影响;最后,本研究对于钙化病变程度的分级依赖于造影,而不是更加精准的血管内超声或光学成像,后续仍需要多中心,大样本的数据来验证。

