结核分枝杆菌表型药物敏感性试验临界浓度设定发展历程
宋媛媛 夏辉 赵雁林
结核分枝杆菌(Mycobacteriumtuberculosis,MTB)的耐药性可以通过表型药物敏感性试验(phenotypic drug susceptibility testing,pDST)或基因型药物敏感性试验(genotypic drug susceptibility testing,gDST)进行检测。商品化gDST检测具有诊断时间更短、易于使用和生物安全风险更低的特点,但目前覆盖的药物有限。全基因组测序(whole genome sequencing,WGS)能够预测更多药物耐药,但当耐药分子机制还不完全清楚时仍然需要pDST方法进行检测。
pDST方法繁多,在当前gDST广泛应用的背景下,部分pDST药物结果的准确性受到挑战,且因方法间报告结果不一致,导致pDST结果解读和应用更加复杂。另外,pDST中MTB的耐药性是基于临界浓度(critical concentration)判断其对药物敏感或耐药的。临界浓度是指抗结核药物在体外能够抑制99%[吡嗪酰胺(pyrazinamide, PZA)为90%]表型野生型(phenotypically wild-type,pWT)MTB菌落生长的最低浓度[1]。先前设定抗结核药物临界浓度的方法不同于其他病原菌使用的方法[2-5],一些药物的准确性和可重复性较差,迫切需要更新临界浓度,且随着一些新型药物如贝达喹啉(bedaquiline,Bdq)、德拉马尼(delamanid,Dlm)等的出现,需要制定针对这些新药的pDST临界浓度以便提供耐药性检测。鉴于抗结核药物临界浓度的复杂性,以及基于现有临界浓度对于结果解读的影响,笔者针对我国常用pDST方法、设定pDST临界浓度方法的历史及进展、在特定临界浓度下临界耐药[borderline resistant;某些耐药相关突变菌株最低抑菌浓度(minimal inhibitory concentration,MIC)分布与pWT MIC分布显著重叠,即其对应的MIC值接近或低于pDST方法的临界浓度]对pDST结果的影响进行系统总结,为结核病实验室技术人员和临床医生合理选择检测方法、正确解读报告检测结果及加强更新临界浓度的研究提供借鉴。
一、目前我国常用的MTB pDST方法
(一)固体比例法DST
1963年Canetti等[6]提出了MTB DST比例法,后几经修改,目前基于改良罗氏(Löwenstein-Jensen,L-J)培养基的传统固体比例法DST是我国最常用的检测MTB药物敏感性的方法。该方法在2支相同临界浓度含药培养基上分别接种高低2个浓度MTB菌液(最终接种菌量约为10-4mg/支和10-6mg/支),同时接种2支空白对照培养基,通过计算含药培养基与对照培养基上生长菌落数量之间的百分比来推断菌株对药物的敏感性。当这一比例≥1%时,该菌株被判为耐药。
(二)液体DST方法
基于分枝杆菌生长指示管(mycobacteria growth indicator tube, MGIT)的快速液体DST方法同样是基于比例法原理,空白对照培养管MTB接种量为含临界浓度药物培养管的1%(PZA为10%)。将稀释后的工作菌液(最终接种菌量约为5×10-2mg)接种至含药培养管中,同时将工作菌液稀释100倍(PZA稀释10倍)接种到空白对照培养管(最终接种菌量约为5×10-4mg,PZA约为5×10-3mg)中。通过仪器定时监测培养管底部发出的荧光信号来预测细菌生长[7]。当空白对照培养管中的生长单位(growth unit,GU)值达到400时(4~13 d,PZA为4~21 d),仪器自动检测含药培养管中的GU值,如果含药管的GU值<100,将自动判为敏感,如果GU值≥100,判为耐药[8-9]。
(三)微量肉汤稀释平板DST法
微量肉汤稀释平板法(常被称为“微孔板法”)[10]是基于微量肉汤稀释法原理的DST方法,使用96孔微孔板通过倍比稀释一系列药物浓度来确定可以抑制99%肉眼可见细菌生长的MIC。每块微孔板可以同时检测多种抗结核药物[11]。除了提供二分类(敏感/耐药)定性结果外,微孔板法还可以确定菌株对抗结核药物的耐药水平(MIC值),为临床医生提供量化的耐药信息。
二、设定MTB pDST折点方法的历史及进展
抗菌药物折点(breakpoint)是用来判断病原菌对药物敏感、中介或耐药的MIC[12],是临床医生选择抗菌药物治疗病原菌感染的一个重要依据。在欧洲抗菌药物敏感性试验委员会(European Committee on Antimicrobial Susceptibility Testing,EUCAST)和一些文献中常被称为临床折点(clinical breakpoint)[13-16],但结核病领域的世界卫生组织(World Health Organization,WHO)指南中针对莫西沙星(moxifloxacin,Mfx)设置了一个高于临界浓度(0.25 μg/ml)的药物浓度(1.0 μg/ml),也被称为临床折点[1],它可以区分Mfx低浓度耐药或高浓度耐药,指导临床通过增加Mfx剂量克服较低剂量时观察到的耐药性。为了避免两者混淆,本文中统一使用“折点”一词,对应于以往MTB pDST中的“临界浓度”一词,而“临床折点”特指MTB pDST中Mfx较高的药物浓度。
(一)既往MTB pDST设定折点的方法
“折点”即“临界浓度”,临界浓度是pDST使用某一方法/培养基获得可解释结果的标准[17]。设定适宜的临界浓度可使pDST结果最大程度反映临床疗效,提高二者相关性。当患者MTB菌株在含临界浓度药物的培养基上有1%(PZA为10%)及以上菌落生长(产生耐药),该药物就不能(或很快不能)用于后续的抗结核治疗。
Canetti[18]首先描述了最初设定临界浓度的方法:选取至少100株来自于从未接受过治疗的新患者的定义为“可能敏感(probable susceptible,PS)菌株”和至少50株来自于接受6个月以上含有相应药物的治疗方案且明显失败的患者的定义为“可能耐药(probable resistant,PR)菌株”,通过比较不同药物浓度下PS和PR菌株的敏感性累积百分比设定临界浓度,将能最大程度区分PS和PR菌株敏感性的浓度设定为该药物的临界浓度[19-20]。药物的临界浓度随使用的培养基(检测方法)不同而变化,这取决于药物在不同培养基中的活性。使用这种方法设定临界浓度也存在一定局限性:(1)结核病的标准治疗是采用联合用药方式,因此,无法获得应用单个药物的临床疗效数据[13],造成选取的PR菌株无法明确是哪个(些)药物耐药造成患者治疗失败;(2)缺乏药代动力学/药效学(pharmacokinetic/pharmacodynamics,PK/PD)数据的支持[21];(3)对于PZA来说,它将高达10%的PZA野生型MTB菌株归类为耐药[13]。因此,目前MTB pDST使用的临界浓度是源于临床实用性和历史原因提出的[2],在很大程度上是基于共识[13,17,22],缺乏坚实的科学基础。
(二)新的MTB pDST设定折点的方法
新的MTB pDST设定折点的方法是参考其他病原菌设定折点的方法,结合pWT菌株MIC分布、临床疗效和PK/PD数据设定[13-14]。这里的pWT菌株必须是基因型野生型(genoypically wild-type,gWT)菌株。然而需要注意的是,并非所有gWT菌株的基因序列都是相同的,因为可能含有与耐药无关的基因突变,而这些突变并不改变菌株的MIC值(如gyrAS95T突变不影响氟喹诺酮类药物的MIC值)[1]。
将一定数量的pWT菌株MIC分布中的最高MIC值称为流行病学临界值(epidemiological cut-off value,ECOFF)[1]。设定ECOFF时[23],需要收集汇总来自多个实验室使用标准化方法获得的足够数量的pWT菌株MIC值,绘制一个单一峰的高斯分布(正态分布)图,即pWT分布,ECOFF对应于通过观察或统计学方法获得的pWT分布的最高MIC值(即通常抑制99%的pWT菌株的值),通常写为Xmg/L(或μg/ml),野生型菌株则写为≤Xmg/L,非野生型为>Xmg/L。ECOFF以最大限度降低了设置折点的风险,从而将pWT菌株MIC分布区分出敏感和耐药。
由于抗结核治疗是联合用药,很难获得单个药物的临床疗效和PK/PD数据。因此,应用其他病原菌设定折点的方法来设定MTB的折点是相对困难的。2004年起一些学者开始使用结核病体外中空纤维系统模型(the hollow fiber system model of tuberculosis)与蒙特卡罗(Monte Carlo)模型相结合进行结核病药物PK/PD研究[24-26]。通过0~24 h浓度-时间曲线下面积(0-24 area under the concentration-time curve,AUC0-24)与MIC的比值,即AUC0-24/MIC来设定临界浓度[25,27]。因此,目前MTB折点可能主要基于野生型菌株患者的临床疗效、体外PK/PD模型和MIC分布中的ECOFF设定。这其中ECOFF显得尤为重要,可以说ECOFF是定义折点的基石[13-14]。
(三)对MTB pDST临界浓度的修订进展
目前,MTB pDST有些药物的临界浓度值将pWT分布一分为二[13],导致DST的可重复性差;有些临界浓度值远高于pWT分布的MIC[13],且缺乏可支持的临床证据,导致一些耐药菌株被判为敏感(假敏感);而2018年以前,一些新药如Bdq、Dlm、氯法齐明(clofazimine,Cfz),WHO尚未推荐临界浓度[1,28]。因此,既往的MTB pDST的临界浓度值亟需系统审核和修订,从而改善MTB pDST的准确性和可重复性[13]。
WHO两项系统综述[28-29]利用已发表的MIC数据评估现有临界浓度是否符合pWT MIC分布上限的ECOFF[2,5],结果发现目前使用的大多数药物-培养基组合的临界浓度值并不符合pWT MIC分布获得的ECOFF[4-5]。面对这种情况,WHO在对现有数据进行系统审查的基础上,2018年[28]对前一版本(2014年[30])推荐的临界浓度进行了修订:(1)建立左氧氟沙星(levofloxacin,Lfx)、Mfx、加替沙星(gatifloxacin,Gfx)在L-J培养基上的临时临界浓度,建立Gfx在MGIT上的临时临界浓度;(2)为尽量减少假敏感结果,将3种二线抗结核药物的临界浓度降低至各自的ECOFF,包括:阿米卡星在米氏7H10培养基(Middlebrook 7H10 medium,7H10)中由4 μg/ml降至2 μg/ml,Lfx在MGIT中由2 μg/ml降至1 μg/ml,Mfx在MGIT中由0.5 μg/ml 降至0.25 μg/ml;Mfx在MGIT中临床折点由2 μg/ml降至1 μg/ml;(3)建立Bdq和Dlm在米氏7H11培养基(Middlebrook 7H11 medium,7H11)和MGIT中的4个临时临界浓度,建立Cfz在MGIT中的临时临界浓度;(4)由于证据有限,3个临界浓度被取消,包括Gfx在7H10上的临界浓度、卡那霉素在7H11上的临界浓度,还有迄今为止只能在L-J培养基上做pDST的环丝氨酸的临界浓度,意味着目前环丝氨酸的pDST不够准确,耐药患者可能会面临无效地使用这种药物并产生严重不良反应的风险[28,31]。同时强调,一旦获得更多数据,应重新评估这些决定[4,28]。
WHO还在2021年[29]根据系统综述的数据,将利福平(rifampicin,RFP)在7H10和MGIT中的临界浓度由1 μg/ml降至暂定ECOFF 0.5 μg/ml。事实上半个多世纪以来7H10培养基的RFP临界浓度是ECOFF的2倍[32],导致一些RFP临界耐药的患者分离株因使用过高的临界浓度值而被判定为对RFP敏感,仍然按RFP敏感患者的标准剂量(10 mg·kg-1·d-1)给予治疗[29,32],这无疑增加了治疗失败和对其他药物产生耐药的可能性[16,29,32-34]。但目前RFP在L-J培养基中的临界浓度依然保持40 μg/ml不变,因为还没有足够的MIC数据来评估罗氏培养基中pWT MIC分布[32]。我国目前常用MTB pDST方法各药物最新折点汇总见表1。
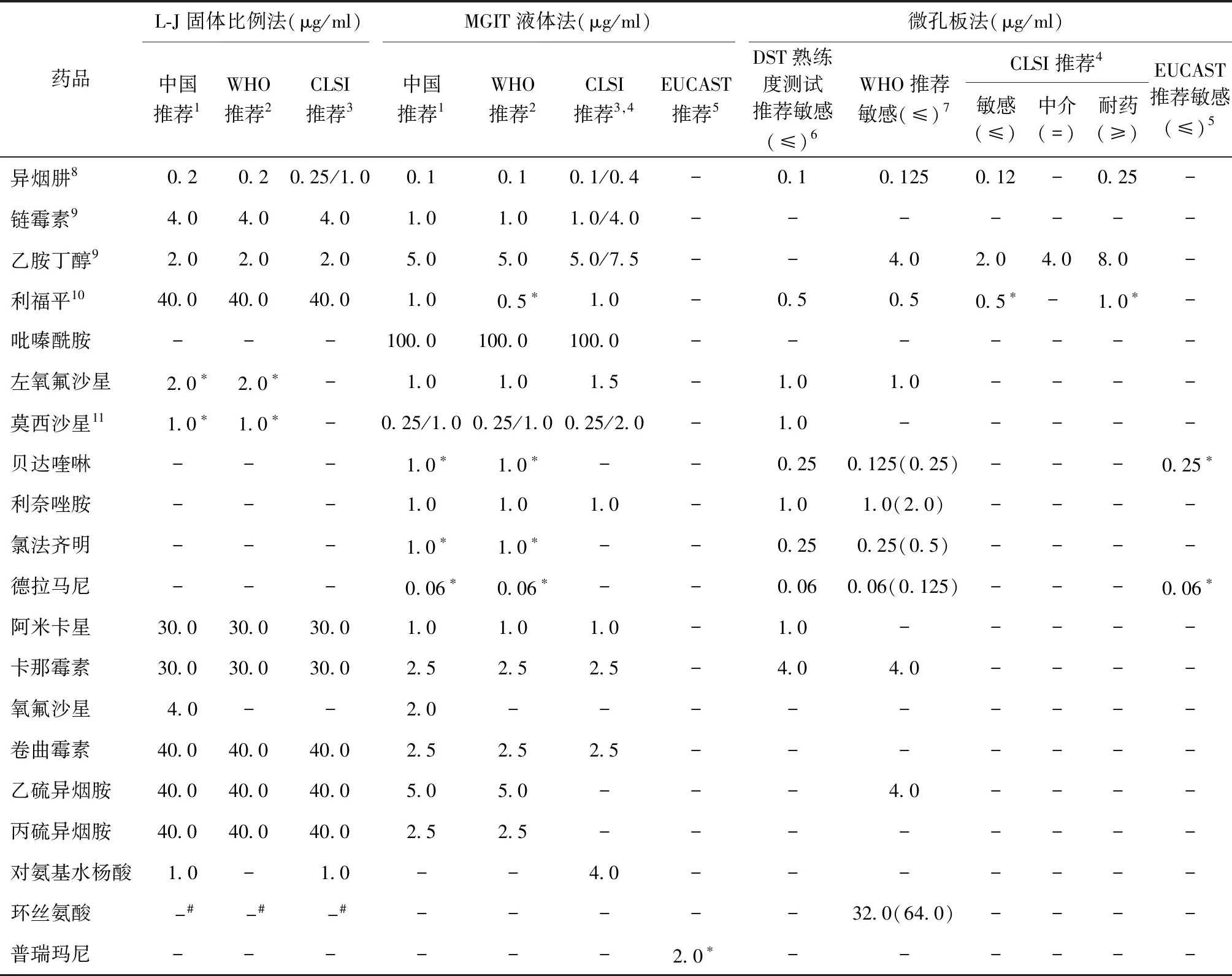
表1 我国常用结核分枝杆菌表型药物敏感性试验方法各药物折点汇总
三、在特定临界浓度下临界耐药对pDST结果的影响
(一)临界耐药对pDST结果的影响
如前所述,通过更加科学的方法和研究建立抗结核药物DST的临界浓度值后可以解决大部分pDST的准确性和可重复性问题,但“临界耐药”菌株仍可能存在一些问题,给实验室技术人员和临床医生造成困扰,如:(1)pDST结果与gDST结果不一致;(2)pDST结果与临床疗效不一致;(3)结果的不确定性,很难报告耐药/敏感等。
“临界耐药”过去也被称为“低水平耐药”,WHO在2022年[10]正式命名为“临界耐药”,指有些耐药基因突变与MIC的低增长相关,导致具有这些突变的耐药株MIC分布与pWT MIC分布显著重叠,依据临界浓度值进行简单的敏感或耐药的二分类结果很难区分这种重叠,增加了敏感或耐药错误分类的可能性,并导致pDST结果的可重复性差。还会出现同一分离株pDST敏感而gDST耐药的情况,使某些药物的耐药相关突变不能通过当前的pDST方法得到可靠的确认,对gDST方法的设计和解释产生不利影响[32-33,36],为临床结果应用带来复杂性。
如乙胺丁醇(ethambutol,EMB),目前设置的临界浓度与耐药相关突变(embB306突变[37-38])菌株的MIC值非常接近,这可能是EMB检测重复性差的主要原因。考虑到重复性不好,2018年WHO不再建议做EMB的简单划分敏感或耐药的二分类pDST,相反MIC结果比二分类pDST结果更有用,它能将具有耐药突变的菌株分辨出来,给出准确的耐药结果,gDST(测序)可能比pDST更可靠,这还需要更多的证据支持[1]。
对于RFP,2021年WHO在系统综述[29]中显示6个RFP耐药决定区域(RFP resistance-determining region,RRDR)突变(L430P,D435Y,H445L,H445N,H445S和L452P)和1个非RRDR突变(I491F)引起耐药的菌株的MIC分布与pWT菌株MIC分布重叠[39],表现出RFP临界耐药,这些耐药类型在使用临界浓度值为1 μg/ml的MGIT 960系统中很大一部分被检测为敏感[4]。因为在较高临界浓度(1 μg/ml)下检测,可能会遗漏临界耐药,此时通过获得具体MIC值和(或)测序突变位点(rpoB)有助于检测临界耐药。虽然证据有限,但依据RFP的PK/PD数据及这7个rpoB突变的有限临床疗效数据(治疗效果不好,失败或复发),WHO在2021年建议将这7个突变类型视为与目前标准剂量RFP(10 mg·kg-1·d-1)治疗具有临床相关性,同时也强调必须根据新的证据对这一建议进行重新评估[29]。因此,2018年WHO推荐采用一种综合判读方法,以确保不遗漏rpoB临界耐药突变,即如果分离株经pDST检测为耐药,或基因型方法确认具有已知的耐药相关突变,均认为该分离株对RFP耐药[29,32-33,39]。然而,对于除RFP外的其他药物,如何在常规临床治疗中解决表型和基因型结果不一致的情况也需要有清晰易行的指导[39]。同时,还提出对于这些RFP临界耐药患者是否能够通过提高RFP剂量改善疗效需要更多的证据支持[29]。
Mfx的gyrA一些突变(如A90V,D94A等)的MIC分布接近临界浓度,导致具有此类突变的菌株pDST结果的可重复性差,与gDST的结果一致性较低[28,40];PZA的pncA也存在2个突变(T47A和I31T)的MIC分布接近临界浓度[41-44],导致其结果可重复性较差[45-46]。目前,MGIT液体法是WHO推荐的唯一一种PZA DST方法,尽管这种方法存在较高假耐药的情况[45,47]。相对于pDST通过DNA测序检测pncA突变是更可靠的方法[1],尽管pncA外的其他基因突变也可能使PZA耐药[48]。
(二)对于临界耐药问题的解决方案
针对临界耐药问题,EUCAST在2018年12月引入了技术不确定区域(area of technical uncertainty,ATU)的概念,用于提示实验室结果存在不确定性,向临床医生报告结果之前需要解决这一问题[49]。ATU通常由一个MIC值定义[10],它不作为结果报告的一部分。目前可用于RFP临界耐药的情况(MIC=1 μg/ml对应于ATU),当MIC≤0.5 μg/ml,报告为敏感; MIC>1 μg/ml,报告为耐药;MIC=1 μg/ml,提示实验室结果不确定[32]。因为由于MIC分布的重叠(仅适用于临界耐药情况,但不适用于高水平耐药情况),基于一次MIC结果不能明确将所检测的菌株归类为敏感或耐药。当遇到这种情况可以通过gDST确定耐药突变类型或本地此类型MIC菌株的流行病学资料协助解决。当无法解决时,需要告知临床医生结果存在的问题。也有学者建议将MIC=100 μg/ml作为PZA的ATU,即MIC≤50 μg/ml报告为敏感,MIC=100 μg/ml 对应于ATU,MIC>100 μg/ml报告为耐药[43]。
同时,EUCAST还将DST结果报告更新为三类[50],分别为敏感、中介、 耐药,并于2019年1月1日生效。具体含义如下:敏感—标准给药方案时敏感(susceptible,standard dosing regimen):当使用药物的标准给药方案治疗成功率很高时,定义为“敏感”;中介—提高药物暴露量时敏感(susceptible, increased exposure):通过调整给药方案或感染部位的药物浓度提高药物暴露量,治疗成功率很高时,定义为“中介”;耐药—即使提高药物暴露量,治疗失败的可能性依旧很高时,定义为“耐药”。药物暴露量是通过调整抗菌药物给药方式、剂量、给药间隔、输注时间及分布和排泄来影响感染部位的病原菌,用AUC来表示[51]。这一报告方式是针对所有病原菌制定的,在结核病领域,比较适合Mfx在MGIT中的结果报告,当低浓度(0.25 μg/ml)耐药,高浓度(1 μg/ml)敏感时,更符合报告“中介”,可通过增加药物剂量(用800 mg/d的Mfx)来治疗。尽管RFP[29]、INH(inhA基因突变)[52-54]、PZA也发现了低水平耐药情况[41-44],WHO在2022年仅提出对于INH低水平耐药使用高剂量INH治疗可能有效[31,52],还没有确定是否可以通过提高RFP和PZA药物剂量来达到良好治疗效果。根据最近的临床试验,增加RFP的剂量是有希望的[55-57]。提高PZA药物剂量可能弥补低水平耐药情况[4,14,43],相信不久的将来随着研究不断深入,这一问题会得到更明确的解决。
美国临床和实验室标准协会(Clinical and Laboratory Standards Institute,CLSI)为解决此类问题,也将DST结果定义为“敏感”“中介”“耐药”[12],但这里的“中介”与EUCAST含义有所不同,指的是不确定(inconclusive)结果,这个“中介”仅仅是针对微孔板法中EMB设置的,其他药物并没有“中介”这个分类。当EMB的MIC≤2 μg/ml,报告为敏感;MIC≥8 μg/ml,报告为耐药;MIC=4 μg/ml,结果不确定。当报告不确定结果时,可以使用MGIT方法或基因型方法重复检测确定敏感或耐药。这个不确定的类别基本对应于ATU。
但对于ATU至今尚无统一的观点或结论,因此,WHO还没有批准ATU的正式使用,主要是为减少对一些病原菌由于MIC分布重叠而产生的重大检测误差[29,49,58-59],但2022年WHO在文件中也提到使用微孔板法时,一些药物可能需要ATU来解释[10]。
笔者建议对于临界耐药分子机制明确的药物,可以应用测序或检测具体位点的商品化试剂盒获得临界耐药结果,也可用MIC方法获得具体MIC值明确是否为临界耐药。对于临界耐药机制不明确的药物,需要利用MIC方法获得更多菌株的MIC分布,结合基因型结果和临床疗效,从而了解临界耐药的表型和基因型表现。且对于临界耐药问题,需要更多地结合用药和血药浓度等综合解读,但在我国尚缺乏统一及明确的解决方案,需要进行更多研究。
四、展望
MTB pDST仍是实验室耐药性检测的重要方法,也有助于其他基因型方法的研究。临界浓度对于pDST结果的准确性至关重要,因而需要采用更加科学的设定折点方法。未来应着重对DST结果不稳定的药物及新药开展更多的关于临界浓度的研究,设定合理的折点,同时对临界耐药问题探索适宜的解决方案。
利益冲突所有作者均声明不存在利益冲突
作者贡献宋媛媛:酝酿和设计实验、实施研究、起草文章、行政/技术/材料支持;夏辉:酝酿和设计实验、实施研究、对文章的知识性内容作批评性审阅、行政/技术/材料支持、指导;赵雁林:获取研究经费、指导、支持性贡献

