经ECMO成功救治1例重症肺出血型钩端螺旋体病
蓝官引 李程 张淑仁 孙雪皎
钩端螺旋体病(简称钩体病)是一种重要的自然疫源性疾病,是世界上发病率和死亡率最高的人畜共患病[1],可由不同型别的致病性钩端螺旋体引起。现总结1例由问号钩端螺旋体引起的重症肺出血型、黄疸出血型钩端螺旋体病,分析该患者的临床资料、影像学及疾病转归,重点介绍重症肺出血型钩端螺旋体病经体外膜氧合(ECMO)治疗好转的过程,以提高临床医师对于ECMO可用于早期支持弥漫性肺泡出血导致的急性呼吸衰竭的认识,提高临床救治成功率。
临床资料
患者,男,61岁,因发热6天于2022年5月27日入院。患者于5月21日无明显诱因下出现发热,体温最高为39.4℃,伴肌肉酸痛、咯血,至当地医院就诊,查血小板:28×109/L,CRP 172mg/L,伴有呼吸困难,遂转入我院,急诊查血常规:白细胞计数10.25×109/L,血红蛋白浓度107g/L,血小板计数9×109/L,中性粒细胞百分数86.1%。C-反应蛋白206.11mg/L。肌酐296.3umol/L。胸部CT提示慢性支气管炎、肺气肿并两肺感染。患者指脉氧急剧下降,经面罩吸氧后呼吸改善不明显,急诊予行经口气管插管、抗感染等对症治疗,拟“肺部感染”收入RICU。既往体健,家中有养鹦鹉史。入院查体:T:38.5℃,P:122次/分,R:30次/分,BP:130/83mmHg (经口气管插管机械通气,模式:PC-BIPAP,氧浓度:80 %,PEEP:8 cmH2O);全身皮肤、巩膜无黄染,浅表淋巴结未及肿大。双肺可闻及干湿性啰音。心率122次/分,律齐。腹部可见散在出血点。入院诊断:1.社区获得性肺炎,重症(CURB-65评分:4分);2.呼吸衰竭;3.脓毒症;4.脓毒性休克(SOFA评分:15分);5.多器官功能障碍综合征;6.电解质代谢紊乱。
诊治经过:入院第1天血常规:白细胞计数11.68×109/L,血红蛋白浓度105g/L,血小板计数8×109/L,中性粒细胞百分数87.7%。C-反应蛋白202.11mg/L。心肌酶谱:乳酸脱氢酶305.9U/L,α羟基丁酸脱氢酶221.6U/L,肌酸激酶1606.9U/L,肌酸激酶同工酶35.8U/L。肾功能:肌酐384.1umol/L,尿素9.89mmol/L,尿酸487.6umol/L。白介素-6测定2875.00pg/mL↑。B型钠尿肽前体(pro-BNP)测定3632.00pg/mL。降钙素原1.990ng/mL。凝血四项+D-二聚体+抗凝血酶:活化部分凝血活酶时间46.0秒,纤维蛋白原9.63g/L,D-二聚体2.40ug/mL,抗凝血酶III74.0%。血清肌钙蛋白I、血浆鱼精蛋白副凝集试验未见异常。肺部CT平扫:1.慢性支气管炎?肺气肿并两肺感染,拟合并肺水肿,病灶较前明显进展,建议治疗后复查; 2.主动脉硬化; 3.扫及:左侧肾盂扩张,建议结合腹部检查(见图1A、B)。考虑患者重症肺炎、脓毒症,家中养鹦鹉史,不除外重症鹦鹉热衣原体肺炎可能,予哌拉西林他唑巴坦4.5g q8h+联合多西环素100mg q12h抗感染,患者肾功能不全,行床边CRRT治疗,辅以抗凝、抑酸护胃、补液、抗炎及对症处理。
5月27日夜间患者呼吸急促,指脉氧下降至82%,完善床边胸片提示肺部病灶明显进展,复查血气分析提示氧合指数63mmHg,紧急行体外膜肺氧合(ECMO)维持氧合(初始血流量3.5L/min、转速约3480 r/min、ECMO氧浓度100%、气流量5L/min、血温36℃),并转至ICU(5月28日)继续治疗。转入后调整抗生素方案为头孢哌酮舒巴坦2g q6h+莫西沙星250mL qd+帕拉米韦0.15g qd抗感染,并持续V-V ECMO治疗,辅以抗凝、激素降低气道反应性、CRRT维持水电解质平衡、输注去白红细胞+血小板、退黄护肝等对症支持治疗。5月29日血常规:白细胞计数13.76×109/L,血红蛋白浓度87g/L,血小板计数48×109/L,中性粒细胞百分数92.1%↑。肌酐229.8umol/L,C-反应蛋白211.39mg/L,总胆红素251 umol/L,外送肺泡灌洗液mNGS回报示:钩端螺旋体(检出序列数49%,置信度99%),结合病史,考虑患者钩端螺旋体感染可能性大,调整抗菌方案为头孢哌酮钠舒巴坦2g q6h+青霉素150万U q6h抗感染,并予激素预防赫氏反应。6月1日查血常规:白细胞计数20.39×109/L,血红蛋白浓度94g/L,血小板计数66×109/L,中性粒细胞百分数83.9%。C-反应蛋白45.77 mg/L,肌酐184.4 umol/L,氧合指数111mmHg。总胆红素245.6 umol/L。患者炎症指标较前下降、氧合较前好转,符合撤机指征,于6月1日(入ICU第5天)停ECMO、CRRT,予文丘里面罩吸氧。6月2日复查肺部CT提示两肺肺出血并感染,病灶较前明显吸收、减少。
6月5日脱呼吸机后患者氧合可,予拔除气管插管。6月5日(入ICU第9天)查体时见患者重度黄疸,复查肝功能提示总胆红素341.3 umol/L,为清除胆红素,予行血浆置换(PE)及双血浆分子吸收系统(DPMAS)(持续时间:4小时),复查胆红素158.5 umol/L,辅以持续退黄、护肝对症。6月8日床边胸片提示病灶较前吸收。至6月9日(入ICU第13天)患者炎症指标趋于稳定,肝肾功能较前好转,病情稳定,遂转至普通病房继续治疗,转入后继续予青霉素钠150万U q6h抗感染,6月11日复查胸部CT病灶较前明显吸收,病情稳定,6月15日(入院第20天)出院。出院后7月7日至我院门诊复查肺部CT提示病灶基本吸收好转(见图1C、D)。起病5个月后电话随访患者其表示现无咯血丝痰等不适。
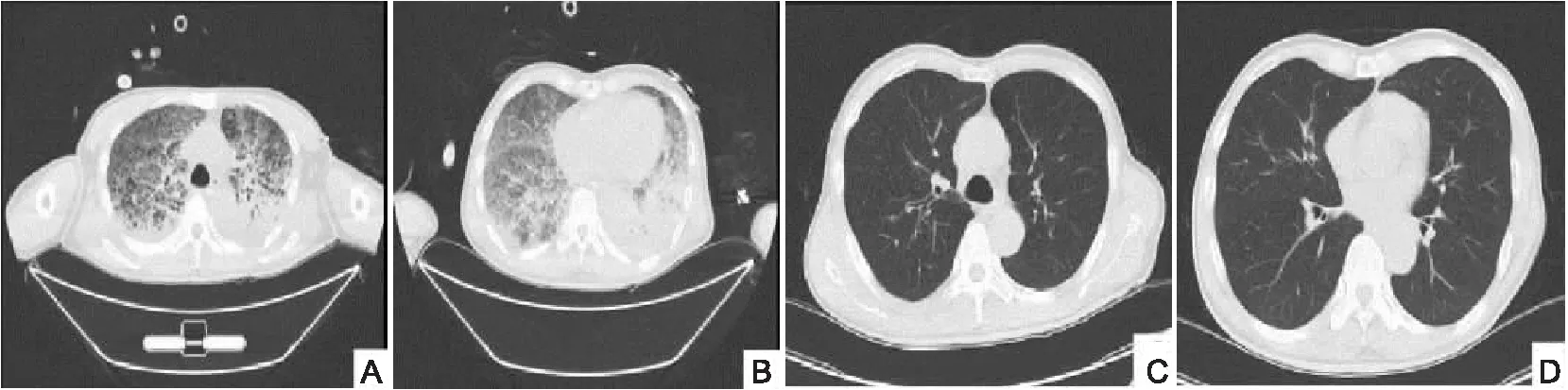
图1 A、B:治疗前肺部CT两肺弥漫性肺出血并感染;C、D:治疗后肺部CT病灶基本吸收好转
讨 论
钩端螺旋体病作为世界上死亡率最高的人畜共患病,其凶险性值得被临床医师所认识。一项以小鼠为研究对象的钩体病动物模型上显示,肺出血是钩体病最早的病理表现[2]。Karpagam K.B.等[3]人指出,约20%~70%的钩端螺旋体病感染患者会累及肺部,从而导致严重肺出血性综合征(SPHS)、急性呼吸窘迫综合征(ARDS)、肺炎和弥漫性肺泡出血(DAH)。据文献报道,不同类型的钩端螺旋体病病死率不一致,黄疸出血型和肺出血型死亡率最高,尽管进行了最大程度的有创通气和充分的治疗,肺出血型钩端螺旋体病死率仍高达74%[4],黄疸出血型会加重肺出血型的死亡率。
肺弥漫性出血主要由肺泡基底膜毛细血管破裂引起,与免疫球蛋白和补体在肺泡表面的线性沉积有关[5],可在短时间内引起严重的呼吸困难,尽管这些DAH患者及时经重症监护治疗,其死亡率也会超过50%[6]。Barnacle J.等[7]人总结了10例使用ECMO治疗钩端螺旋体病的报告,他们发现这些患者应用ECMO后死亡率仅为9.1%,远低于上述在ICU无ECMO支持的死亡率超过50%的报道[6],这说明在患者出现由肺出血导致的严重呼吸衰竭时应用ECMO可改善预后,降低死亡率,本例在入住ICU第5天后即撤机。
近几年不少文献指出ECMO可尽早用于救治肺出血型钩端螺旋体病[7],但其他学者指出活动性出血是使用ECMO的相对禁忌证,在ECMO维持期间使用抗凝药物是否会导致无法控制的肺出血的预测很难确定[8]。因此在治疗过程中要及时调整抗凝药强度,使PT维持在40~50s。肺出血型钩体病在肺部的影像学表现主要以弥漫性小浊片为主,可弥散性合并成较大的实变区域[9]。本病例胸片及肺部CT均提示弥漫性肺间质渗出,与文献报道的肺出血型钩体病表现相符,在治疗后,患者肺部病变最终吸收好转。
钩端螺旋体病由钩端螺旋体属的细菌引起,由>250个已知的致病性血清株钩端螺旋体寄生在受感染哺乳动物的肾脏中,并通过尿液释放到环境中,人或动物通过接触被细菌污染的环境患病[10]。本例感染途径不除外通过接触鹦鹉而患病。急性期钩体病以不典型发热为主,易被误诊为登革热、疟疾和其他急性发热性疾病。明确钩体病的实验室检查方法有多种,包括培养基培养、PCR技术、ELISA检测血清及显微凝集试验等[11]。而宏基因二代测序(mNGS)技术逐渐走进临床,可快速明确病原体,并为精准治疗提供依据。钩端螺旋体近年来的主要检测技术同样是通过mNGS来提供病原学依据[12]。本例在入院后即留取BALF送检mNGS,结果回报后提示钩端螺旋体病(序列数49%,置信度99%)。
根据一项随机对照试验指出,青霉素、头孢菌素、多西环素是治疗钩端螺旋体的常用药物[13]。在使用抗生素过程中,需警惕由抗生素引起的赫氏反应,相关文献显示,在英国,赫氏反应的死亡率达5%[14]。本例患者入院即使用广谱抗生素哌拉西林钠他唑巴坦4.5g q8h+多西环素100mg q12h抗感染,当mNGS结果回报后及时调整为头孢哌酮钠舒巴坦2g q6h+青霉素150万U q6h,辅以激素预防赫氏反应发生,并在患者出现黄疸、胆红素不断升高时及时应用PE改善凝血功能、DPMAS降低胆红素,改善肝功能损害。治疗后复查患者各项实验室结果及影像表现随着用药方案调整得到极大改善,炎症指标明显下降、肺部病灶基本吸收,治疗效果令人满意,预后良好。
综上所述,本例患者起病急骤,入院后即表现为严重的呼吸衰竭,在高水平机械通气下仍有明显的呼吸困难,氧合指数仅为63 mmHg,随后经紧急ECMO救治、辅以PE联合DPMAS改善肝功能、CRRT改善肾功能及抗生素抗感染、激素预防赫氏反应等治疗后呼吸、循环平稳,好转后出院。这提示临床医师,对于出现了严重呼吸衰竭的肺出血型钩体病患者,应尽早考虑应用ECMO等体外生命支持作为一种紧急治疗方案,以此降低重型钩体病患者死亡率。

