水稻土溶解性有机质与Cu2+结合过程及机制研究
周浩,林跃胜,方凤满,阴俐,葛磊,陈辉,李时银,姚有如*
(1.安徽师范大学地理与旅游学院,安徽 芜湖 241003;2.江淮流域地表过程与区域响应安徽省重点实验室,安徽 芜湖 241003;3.南京师范大学环境学院,南京 210023)
伴随着工农业的现代化发展,大量污染物的排放使得土壤重金属污染问题日益突出,越来越受到人们的关注[1]。铜(Cu)是动植物生长发育过程中必不可少的微量元素,作为动植物体内氧化酶的主要成分,对某些酶类具有活化作用。
然而,摄入过量的Cu2+会对生物体造成危害,研究表明,在农业活动过程中,Cu2+的过量摄入会导致作物细胞质膜两侧产生一定的浓度差并且增强膜脂过氧化作用,细胞质膜透性变大,导致生物体内所必需的钾离子流出细胞膜外,从而对细胞质膜产生一定的损害,影响作物的产量。并且累积于作物体内的Cu2+通过食物链过量进入人体会诱发癌症,危害人体健康[2]。因此,洞悉农田土壤环境中Cu2+迁移与转化过程具有重要意义。
有机质作为土壤中的重要组成部分,对Cu2+的迁移转化有着重要的影响。一方面其所具有的基团可以通过键位作用与Cu2+形成络合物,同时其表面所带有的负电荷对于Cu2+起吸附的作用;另一方面,有机质进入土壤后,通过生物的分解作用形成大量的游离态阳离子,这些阳离子会与Cu2+竞争吸附点位,减少土壤胶体对于Cu2+的吸附,从而增加Cu2+的活性[3]。溶解性有机质(DOM)是一类结构复杂且化学活性较强的有机混合物,普遍存在于环境介质中。土壤中的DOM 组分由腐植酸、富里酸、胡敏酸及各种亲水有机酸组成,其所包含的各种游离的氨基酸、有机酸、多酚等物质会影响土壤中营养元素N、P、K 的生物可利用度以及相关污染物的转移能力[4]。研究表明,在不同环境介质中DOM 与重金属之间均存在不同程度相关性,研究人员针对不同季节的湖泊水体,不同类型的土壤以及生物质炭,展开DOM 与金属离子之间的光谱分析,结果表明DOM 的荧光强度随着金属离子浓度的升高发生了淬灭现象,并且各荧光组分均与金属离子有不同程度地络合[5-7]。
在土壤环境中,DOM 既可以直接与重金属离子发生络合作用,也可以通过改变土壤自身的理化性质从而影响其对重金属的吸附作用[8]。另外,土壤DOM中所含有的官能团(羧基、羟基和含硫基官能团等)可与重金属污染物发生吸附-解析、氧化-还原、离子交换、配位络合/螯合等反应[9]。因此,在DOM 的参与下,土壤中重金属的迁移转化过程更加复杂,需要进一步研究探讨。并且,对于高Cu2+含量背景农田土壤,水稻土中的DOM 与Cu2+之间的结合机制还不清楚,需要进一步研究。
安徽省庐江县地处江淮之间,是我国水稻优势产业带,全县稻田种植约10 万hm2,水稻产量位居安徽省首位[10]。同时该县位于郯庐地震带,地区有色金属矿藏丰富[11]。课题组对庐江县土壤中的重金属进行检测(90 个水稻土壤样品),发现土壤中Cu 的平均含量为35.0 mg·kg-1,显著高于当地的背景值(21.65 mg·kg-1)。基于上述原因,开展庐江县稻田土壤中DOM与Cu2+之间的结合过程和机制研究,有利于揭示农田土壤中Cu2+迁移转化行为。
本研究以庐江县的水稻土壤作为研究对象,研究水稻土壤中DOM 的组成、来源以及微观形貌,采用荧光淬灭实验、二维相关光谱以及X 射线光电子能谱(XPS)等方法分析DOM 与Cu2+的络合过程和机制,为进一步了解DOM 参与下农业土壤中Cu2+的迁移特性提供理论依据。
1 材料与方法
1.1 研究区概况
安徽省庐江县水稻种植历史悠久,本研究采样地位于庐江县白湖镇(31°13'07″N,117°22'14″E),采样地水稻种植年限超过20 a,且种植过程中未曾改变土地利用类型。水稻田供肥方式以农用复合肥(磷酸铵、尿素)为主,并少量施用有机肥。另外,该地大部分水稻秸秆被居民回收作为生物燃料,少量用于田间堆肥。
1.2 DOM的提取和分析
供试土壤于2020 年12 月采集,为0~20 cm 表层休耕水稻土壤。经测定样地农田土壤有机质含量为(24.60±10.74)mg·kg-1,pH为6.1±1.1。
将风干磨碎后的水稻土过0.150 mm 筛,筛后的土壤按照1∶10(m∶V)的固/液比与超纯水混合,于25 ℃室温下振荡24 h(220 r·min-1),将振荡完成样品置于4 000 r·min-1转速下离心,离心时间为30 min,取上清液,使用0.45 μm 玻璃纤维滤膜过滤,得到的滤液即为DOM 溶液,将其放置于500 mL 棕色玻璃瓶中,避光保存在4 ℃冰箱中,除了冷冻干燥的DOM 样品,其余上机测定的样品会在24 h内进行测定。使用TOC 分析仪(Multi N/C3100,Analytik Jena,德国)测定溶解性有机碳(DOC)含量,计算样品的DOM 含量,土壤DOM中Cu2+浓度为(0.011±0.005)mg·L-1。
部分DOM 原液离心,经过真空冷冻干燥机(FD-1A-50,长沙巴跃)干燥后,得到一定量粉末,用于后续扫描电镜、透射电镜实验。
1.3 DOM和Cu2+的络合滴定实验
避免内滤作用(当荧光体浓度较大或与其他吸光物质共存时,荧光体或其他吸光物质对于激发光或发射光的吸收,导致荧光减弱的现象),将DOM 溶液进行 稀 释 使 其 浓 度 为10.0 mg·L-1[12],滴 加0.1 mol·L-1NaOH 或HCl 溶液调节溶液pH 为7.0±0.1,防止产生沉淀。滴加浓度为0.1 mol·L-1CuSO4到25 mL DOM溶液中,生成一系列的滴定样品,样品溶液中添加的Cu2+的浓度分别为0、5、10、20、30、50、75、100 μmol·L-1。随后,将滴定样品在25 ℃下避光振荡24 h,使其达到络合平衡,对络合溶液进行动态光散射、三维荧光以及同步荧光等方法展开分析。同时,为了进一步研究DOM 对Cu2+络合能力,通过离子选择性电极法分析了DOM 与Cu2+的结合常数。游离态Cu2+测定采用Cu 离子选择性电极(PCu-1-01,上海雷磁),记录仪为奥立龙Orion Star™A211。在100 mL 蓝色丝口瓶内加入2 mL 的电解质(5 mol·L-1NaNO3),随后加入DOM 母液,并定容使稀释后溶液的TOC 浓度为0.5 mg·L-1。将溶液转移到烧杯中,调节溶液的pH 值为4.0±0.1。在连续搅拌的条件下,用逐步加入CuSO4溶液进行滴定,记录滴加过程中游离态Cu2+的浓度变化。
分别制取200 mL Cu2+浓度为0、100 μmol·L-1的络合溶液进行冷冻干燥,以得到足够的粉末样品用于后续的实验。
1.4 Zeta电位以及粒径的测定
采用动态光散射分析仪(Zetasizer Nano ZS,Mal⁃vern Instruments,英国)测定不同条件下土壤DOM 的粒径分布和Zeta 电位,测定之前使用超声分散30 min。
1.5 光谱测定
对络合溶液进行紫外-可见光谱分析,以2 nm 为间隔,采用紫外-可见分光光度计扫描200~920 nm 波长范围内的吸收光谱,同时以超纯水为空白。
计算SUVA254的值,其可用来表征DOM 的芳香化程度[13],计算过程见公式(1):
式中,a254是样品在波长254 nm 处的吸收系数,m-1;A254是波长254 nm处的吸光度;lL是比色皿的宽度,m。
EET/EBz为253 nm与220 nm处吸光度的比值,其值的大小可用来表征DOM 芳香环上取代基的种类以及取代程度[14]。上述实验均重复3次。
DOM 样品的荧光光谱使用荧光光谱仪(F97Pro,上海棱光)进行测定,激发波长(Ex)波长范围为200~450 nm(增量为5 nm),发射(Em)波长范围为25~550 nm(增量1 nm),扫描速度为2 400 nm·min-1,狭缝均5 nm。同步荧光激发波长为250~550 nm,恒定偏移量Δλ=60 nm,激发和发射狭缝宽度为5 nm,扫描速度为240 nm·min-1。以超纯水为空白,光源为150 W 无臭氧氙弧灯,系统自动校正瑞利和拉曼散射。
荧光指数(FI)为当Ex=370 nm,Em 为450 nm 与500 nm 的荧光强度比值,可以指示DOM 中腐殖质的来源[15],腐殖化指标(HIX)为当Ex=254 nm,Em分别为434~480 nm 区域积分值与300~346 nm 区域积分值的比值,一般指示DOM腐殖化程度[16],自生源指标(BIX)为当Ex=310 nm 时,Em 分别为380 nm 和430 nm 处的荧光强度比值,可以指示DOM自生源特征强弱[17]。
1.6 DOM与Cu2+络合参数拟合
采用改进后的Stern-Volmer络合模型来确定Cu2+与DOM 中不同荧光组分之间的络合能力,为了定量描述络合作用,假设Cu2+与DOM 之间形成1∶1的络合物。改进的Stern-Volmer 方程如公式(2)所示[18]:式中,F0和F代表没有滴加Cu2+以及不同Cu2+浓度CM(mol·L-1)时DOM 组分的荧光强度,KM表示DOM 与Cu2+之间络合的条件稳定常数,f代表DOM 参与Cu2+络合的荧光团比例,KM和f可从线性拟合中获得,对KM取对数得到络合稳定常数lgKM。
基于离子选择性电极法对DOM 与Cu2+络合参数的计算方法如下所示,土壤DOM 与Cu2+以1∶1进行络合反应。根据平衡方程(3)计算得到:
式中,M总为加入的Cu2+总量(μmol);M为游离Cu2+;D总为DOM 中DOC 浓度(mg·L-1);ML为络合物浓度(μmol·L-1)。
1.7 二维(2D-COS)分析
为了研究添加的Cu2+与DOM 结合的具体情况。对不同Cu2+浓度梯度下所发生的络合反应后制得的DOM 样品的同步荧光光谱进行2D-COS 分析。根据Noda 理论和Ozaki 所提供的方法[19],采用“2D Shige 软件”分析。
1.8 SEM、TEM、XPS表征分析
使用扫描电子显微镜(SEM)(Gemini 300,ZEISS,德国)表征干燥后DOM 以及DOM 与Cu2+络合反应之后样品的表面形貌,其中,加速电压为0.02~30 kV。采用透射电子显微镜(TEM)(JEOL 2100F,JEOL 公司,日本)观察DOM 的形貌和粒径,加速电压为200 kV。使用X 射线光电子能谱仪(XPS)(ESCALab250,Thermo Fisher Scientific,美国)对DOM 的表面元素组分及其化学形态进行表征。
1.9 数据分析
使用SPSS 20.0 软件进行数据的分析和检验,图形绘制采用Origin 2019、XPSPEAK41 软件。其中,非参数检验(单样本K-S 检验)被用于数据间的差异性检验。
2 结果与讨论
2.1 水稻土DOM含量和结构特征
水稻土DOM 的含量为(604.2±79.7)mg·kg-1,由紫外-可见光谱参数计算得到SUVA254值为(3.25±0.07)L·(mg·m)-1。SUVA254值的大小与芳香族化合物和腐殖质中的C C 键,CO 键 以及 与DOM 分 子量的大小存在一定的相关性[13]。一般而言,SUVA254的值越大,表明DOM 的分子量越大[20]。此外,SUVA254还与DOM 组分的亲疏水性有关,SUVA254>4 L·(mg·m)-1时,表明此时DOM 中的组分呈现出疏水性特征,且DOM 中含有的芳香物质较多[21]。庐江县水稻土DOM 的SUVA254值低于4 L·(mg·m)-1,表明水稻土DOM 组分主要由亲水性物质构成。土壤腐殖质是非晶态物质,它具有高度的亲水性,说明庐江县水稻土中DOM 以亲水性腐殖质为主。作为结构复杂、性质稳定的特殊性质的高分子化合物,腐殖质的存在直接影响到土壤中的Cu2+的迁移转化过程。同时,EET/EBz的值为0.496±0.005,表明该土壤DOM 的芳香结构中含有一定量的含氧官能团[22]。这些含氧官能团对Cu2+的迁移与转化起着重要作用[14],研究表明,仅酚羟基与Cu2+的络合常数高达7.95[23]。因此,水稻土DOM表面的官能团会加速其与Cu2+的结合行为。
另外,DOM 表面所具有的负电荷也会影响其与Cu2+的结合过程。庐江县土壤DOM 的平均粒径为(174.4±1.5)nm,初始的Zeta 电位为(-17.7±0.8)mV,说明DOM 具有典型的土壤胶体特性,土壤的有机胶体与重金属可以通过静电吸附、阳离子桥接及氢键合等作用联结在一起。并且,DOM 颗粒平均粒径仅174.4 nm。这种稳定的纳米颗粒能够通过表面孔隙吸附和静电作用与Cu2+进行结合。
DOM 中类富里酸和类腐植酸的组分也是实现与Cu2+结合的关键因素。通过分析庐江县水稻土DOM三维荧光光谱可知(图1),土壤DOM存在两个荧光峰值区,分别为类腐植酸荧光峰C1(λEx/λEm=350 nm/440 nm)及类富里酸荧光峰C2(λEx/λEm=270 nm/530 nm)[17]。说明该类型土壤DOM 组分构成以类腐植酸和类富里酸为主,缺乏蛋白质类物质,这可能与庐江县水稻种植年限有关,相关研究表明随着水稻种植年限增加,土壤DOM 中类腐殖物质不断增加而蛋白质类物质累积则会变少,芳香度升高[24]。该结果与上述SUVA254值低于4 L·(mg·m)-1相符合,说明庐江县水稻土DOM中以亲水性腐殖质类物质为主,蛋白质类物质偏少。
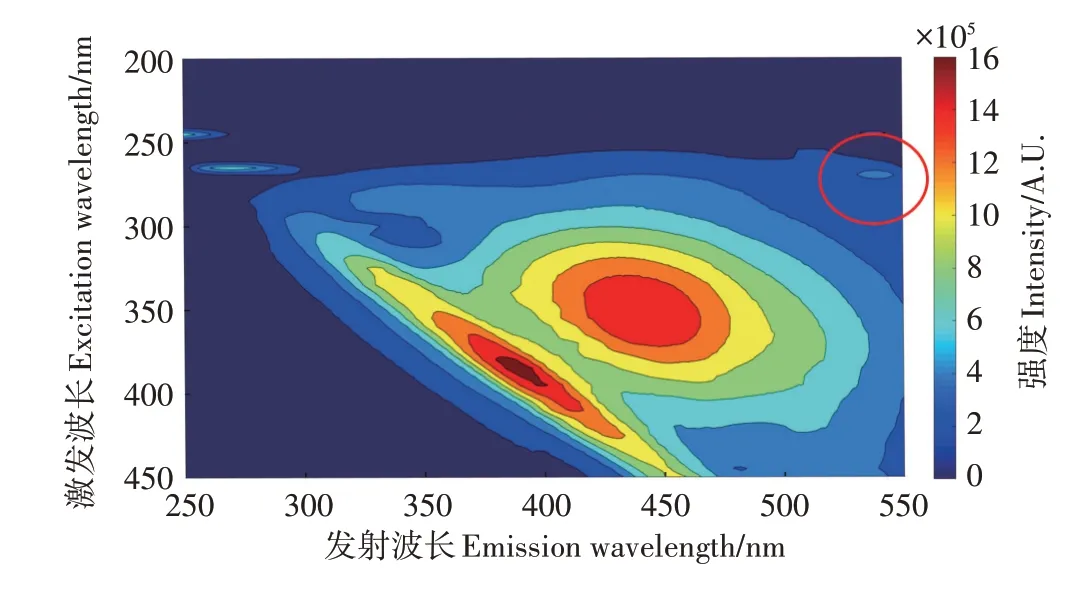
图1 水稻土溶解性有机质组分荧光图谱特征Figure 1 Fluorescence pattern characteristics of dissolved organic matter components of paddy soil
2.2 水稻土DOM的来源分析
目前用来表征DOM 来源的荧光特征参数主要有FI、BIX。其中FI 可以反映环境中类腐殖质的来源情况[15],并且FI 值与富里酸的芳香性存在一定的相关性[25-26]。研究表明,FI 存在两个端源值,FI 为1.4 时,指示DOM 主要为外源输入;FI 为1.9 时,指示DOM 为内源输入。本研究中土壤DOM 的FI 为1.49,表明DOM 来源既有陆源输入,也有内部微生物活动作用。BIX 可以指示DOM 的自生源特征,同时也可以反映生物的可利用性。BIX>1 时,DOM 自生来源特征明显,BIX<1 时,DOM 的自生源特征不显著[17]。本研究中的土壤BIX 为0.68,表明该区水稻土DOM 自生源特征较弱,类蛋白成分较少,土壤DOM 中的生物活性较低。土壤微生物的代谢产物会直接影响土壤腐殖质化程度及其与重金属之间的络合强度[27]。然而,水稻种植过程中土壤的耕作方式、肥料的组成、杀虫剂和其他化学制剂的使用均直接影响了土壤微生物活性[27]。
2.3 水稻土DOM与Cu2+结合过程
2.3.1 添加不同Cu2+浓度下DOM 的粒径与Zeta 电位变化
随着添加Cu2+浓度的升高,DOM 的凝聚现象明显。添加不同Cu2+浓度下,庐江县水稻土DOM 中所测的粒径变化如图2 所示。由图2 可知,随着Cu2+浓度的不断升高,DOM 粒径不断增大。其中,当添加的Cu2+浓度达到75 μmol·L-1和100 μmol·L-1时,DOM 的粒径显著高于其他浓度Cu2+添加时DOM 的粒径。同时,在未添加Cu2+的土壤DOM 中,实验测得其Zeta 电位为(-17.7±0.8)mV,随着添加Cu2+浓度增加至100 μmol·L-1,其Zeta电位上升至(-13.4±0.78)mV。结果表明:Cu2+的添加,使得DOM 的Zeta 电位(绝对值)呈现降低趋势。这是因为DOM 初始状态为负电荷,不断添加带有正电荷的Cu2+会与DOM 表面的负电荷进行结合,从而实现电中和。Cu2+的添加使得DOM表面所带有的负电荷量减少,因此DOM 的Zeta 电位的绝对值减小。另外Cu2+是以CuSO4的形式进入到土壤DOM 中,CuSO4为酸性溶液,添加会使DOM 的pH 值降低,DOM 的H+增加,也导致了土壤DOM 的负电荷被电中和[28]。而Zeta 电位与DOM 分散的稳定性相关[29]。根据DLVO 理论[30],DOM 作为一种典型的胶体物质,其表面Zeta 电位(绝对值)随着Cu2+浓度的增加而减小。说明DOM 胶体的电双层逐渐被压缩,其厚度随着Cu2+浓度的增加而减小,进而降低了Zeta 电位。当DOM 胶体表面的双电层被压缩,胶体颗粒斥力势能降低,导致DOM 胶体更容易呈现出团聚的趋势。而DOM 与Cu2+倾向于结合并呈现团聚的趋势,原因主要来源于两个方面,一方面是DOM 表面的负电荷与Cu2+所携带的正电荷,通过静电斥力相结合。另一方面,DOM 颗粒表面具有多孔结构和众多官能团,这些特性能够吸附游离的Cu2+,导致DOM 粒径呈现增大的趋势(图2)。在不同Cu2+浓度下,DOM 颗粒的粒径和表面电荷的变化,会影响与Cu2+的结合过程和迁移行为。
两种大米淀粉湿热处理前后的核磁共振碳谱图谱出峰位置及其相应的螺旋结构含量如表2所示。其中C1所在的化学位移中102×10-6和103×10-6所对应的区域表示单螺旋的存在,而 101.5×10-6、100.5×10-6和99.4×10-6对应的区域表示有双螺旋的存在[11]。
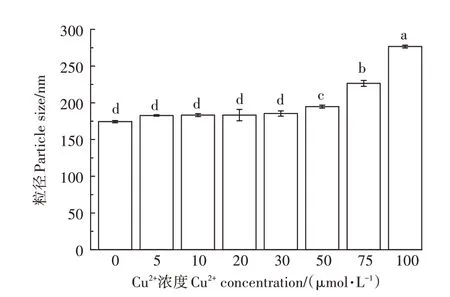
图2 添加不同Cu2+浓度下水稻土溶解性有机质粒径变化特征Figure 2 Particle size variation characteristics of dissolved organic matter in paddy soil under different Cu2+concentrations
2.3.2 添加不同Cu2+浓度下DOM的荧光淬灭过程
在添加Cu2+的条件下,水稻土DOM 荧光峰发生了明显的淬灭(图3),其中,两组荧光峰的荧光强度随着Cu2+添加量的不断增加呈现出下降趋势。表明Cu2+对土壤的DOM 组分有明显的淬灭作用。当DOM溶液中添加的Cu2+浓度从0 μmol·L-1上升至100 μmol·L-1时,C1(类腐植酸)和C2(类富里酸)的Fmax分别降低至原来的54.6%和59.2%(图4)。结果表明水稻土中DOM 所存在的两种组分均可与Cu2+进行结合,导致其荧光强度降低。但是由于不同组分间其所含有的能够与Cu2+结合的官能团种类和数量不同,导致了其淬灭程度呈现出一定的差异[18]。
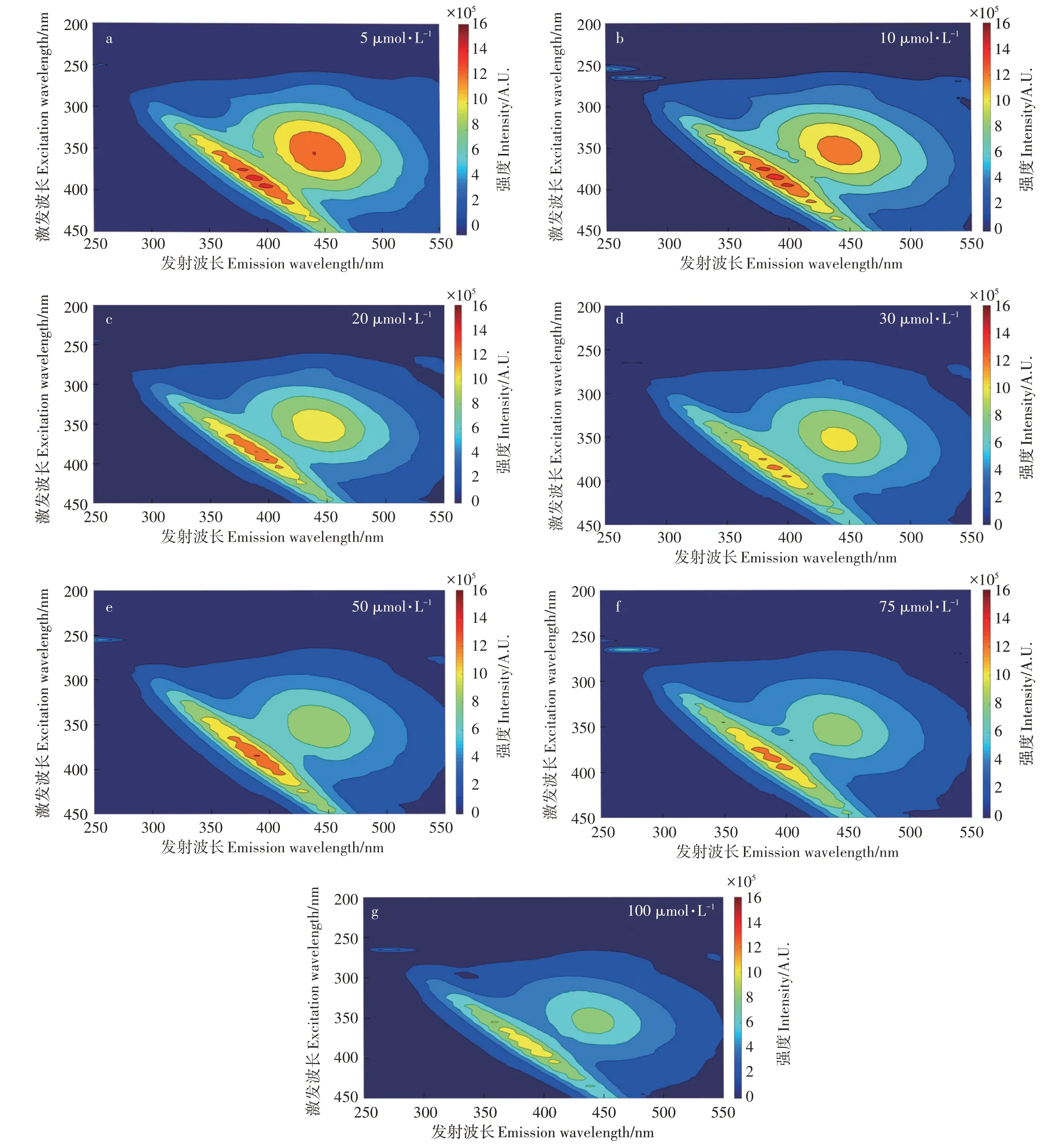
图3 添加不同Cu2+浓度下水稻土溶解性有机质的荧光淬灭过程Figure 3 Fluorescence quenching process of dissolved organic matter in paddy soil with addition of different Cu2+concentrations
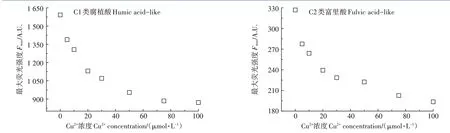
图4 添加不同浓度Cu2+后溶解性有机质不同组分的荧光淬灭曲线Figure 4 Fluorescence quenching curves of different components of dissolved organic matter after dropwise addition of different concentrations of Cu2+
2.3.3 DOM组分与Cu2+的结合参数特征
利用改进的Stern-Volmer 方程,分析DOM 中各类荧光组分与Cu2+作用的络合稳定常数(lgKM),并进一步分析DOM 中与Cu2+结合的各组分荧光基团比例关系。结果如图5a 中所示,DOM 组分的F0(/F0-F)与CM-1之间均有着良好的线性关系(R2=0.95,0.98),表明该方程很好地描述了荧光淬灭过程。并且DOM 中C1、C2 与Cu2+的络合稳定常数lgKM分别为5.07、4.81,表明类腐植酸组分与Cu2+的络合力强于类富里酸组分。因为,类腐植酸的腐殖化程度较高,并且所含有的较多芳香性物质,致使类腐植酸存在着更多与金属离子结合的官能团[12]。从结合荧光团比例(f值)来看,DOM 中C1 组分与Cu2+配位的荧光基团比例为0.51,明显高于C2中的0.39,这是因为土壤DOM 组分中类腐植酸与Cu2+相互作用形成了多齿复合物,或因类富里酸本身具有较少的含氧官能团,难与Cu2+相互结合[31]。
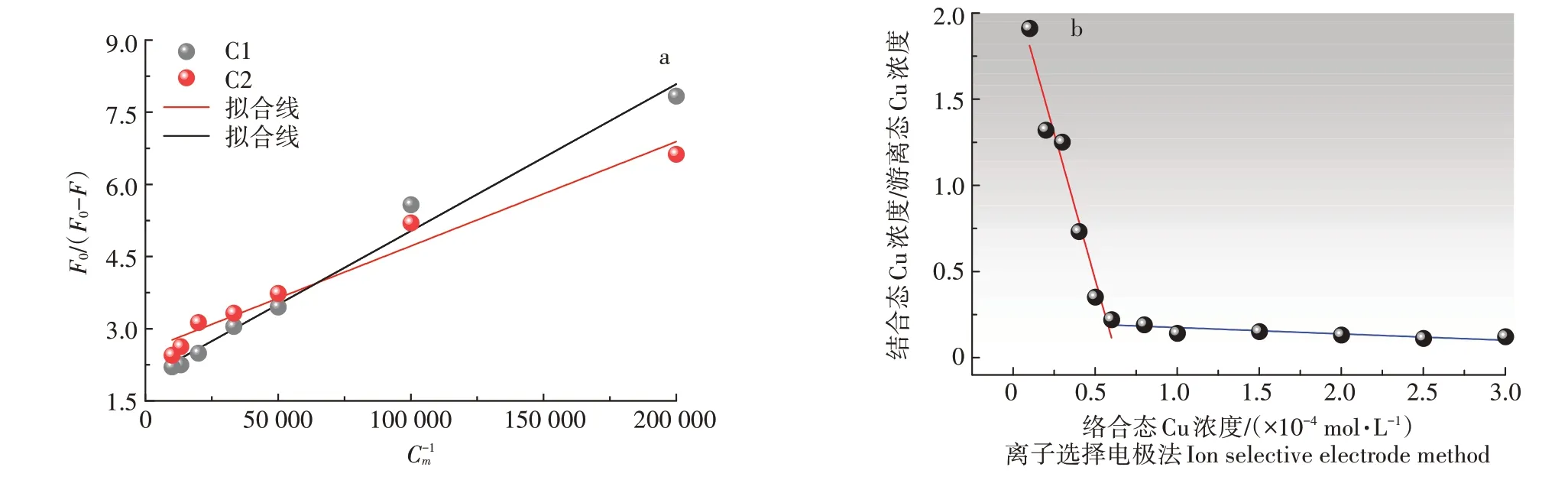
图5 溶解性有机质与Cu2+的结合过程拟合Figure 5 Fitting of complexation process between dissolved organic matter and Cu2+
DOM 中不同组分的络合位点对Cu2+络合能力不完全相同,因此根据对Cu2+的络合能力的不同对曲线进行分段拟合(图5b)。第一组分体现与Cu2+离子有较强络合能力的成分。而第二组分表示对Cu2+络合能力较弱的成分。研究结果表明,两部分络合位的条件稳定常数(lgK)分别5.12 和3.78。该结果与基于荧光强度值拟合得出的络合常数具有一致性。理论上,配位体的条件稳定常数越大,说明其配位体对金属离子的配位能力越强。这也证实了DOM 中类腐植酸组分与Cu2+的配位能力强于类富里酸组分。
2.3.4 DOM与Cu2+结合前后表面形貌变化
DOM 与Cu2+结合前后表面形貌变化特征如图6所示。在DOM 与Cu2+结合之前,其颗粒表面呈现出类蜂窝状特征,孔隙密布、疏松多孔(图6a)。在微观视角下DOM 颗粒呈梭状特征、表面粗糙不平,具有明显的介孔和微孔结构(图6b)。在DOM 与Cu2+结合之后,DOM 颗粒表面形貌发生了巨大变化(图6c 和6d),表面由蜂窝状的形态转变成了针状特征,且表面平滑,多孔结构消失。200 nm 尺度下显示,DOM 与Cu2+结合后的孔隙结构基本消失,平滑状更加明显(图6d),这主要由于DOM 通过表面的孔隙吸附了部分Cu2+,导致其表面变得平滑。

图6 水稻土溶解性有机质及其与Cu2+结合后SEM图Figure 6 SEM diagram of paddy soil dissolved organic matter and its binding with Cu2+
DOM 与Cu2+结合前后表面TEM 图如图7 所示。在DOM 与Cu2+结合之前,其呈现出破碎状态(图7a),微观视角下DOM 的颗粒细小分散且表面粗糙不平(图7b)。在DOM 与Cu2+结合之后,DOM 的形态发生明显改变(图7c 和图7d)。DOM 从原本的破碎状态变成了大块的结晶结合形态,粒径能达到4~5 μm 左右。Cu2+的添加,使其彼此之间发生络合,微粒之间凝聚在一起,粒径增大,并且Cu2+的添加,使得DOM微粒表面平整(图7d)。

图7 水稻土溶解性有机质及其与Cu2+结合后TEM图Figure 7 Paddy soil dissolved organic matter and its TEM diagram after binding with Cu2+
2.4 DOM与Cu2+的结合机制
DOM 与Cu2+结合的同步荧光光谱如图8a 所示。DOM 的同步荧光光谱图的自发峰出现在三个位置,主要位于418、520 nm 和348 nm 处,其中,418 nm 和520 nm 自发峰代表了类腐植酸组分,而348 nm 处自发峰代表了类富里酸组分[32]。且图中所出现均为正交叉峰,表明DOM 中这两组组分的荧光强度与所添加的Cu2+浓度呈负相关关系,并且庐江县水稻土中DOM的各个组分对Cu2+均具有较高的敏感性。
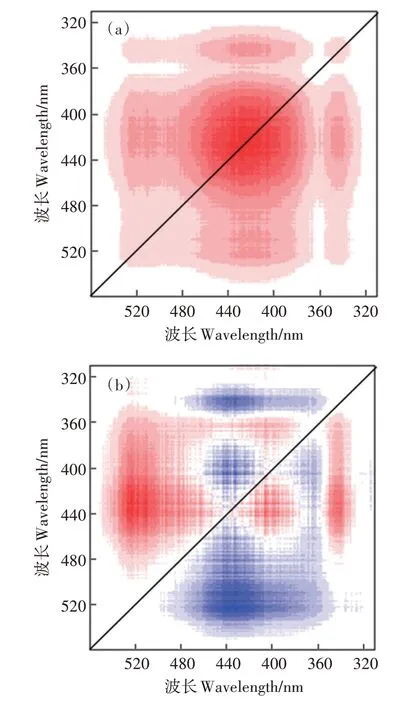
图8 水稻土溶解性有机质与Cu2+络合的同步(a)/异步(b)二维相关光谱图Figure 8 Synchronous(a)/asynchronous(b)two-dimensional correlation spectra of paddy soil dissolved organic matter and Cu2+complex
异步光谱图则可用来表示DOM 不同组分其不同位点在添加Cu2+后其荧光强度的变化趋势,从而揭示DOM 与Cu2+的具体络合位点以及顺序。如图8b 所示,DOM 与Cu2+结合的异步图其对角线左上方存在435 nm/400(350)nm 2 个负交叉峰以及520 nm/435 nm(375)、400 nm/365 nm处3个正交叉峰。根据Noda的规则[19],DOM 组分与Cu2+的络合顺序为350 nm→400 nm→435 nm→375 nm→365 nm→520 nm,即短波类腐植酸→长波类腐植酸→短波类富里酸-长波类富里酸。由此可见,稻田土壤DOM 中的类腐植酸组分优先与Cu2+发生络合反应,尤其以短波类腐植酸其中的酚基、羟基和酚羟基等基团对Cu2+的添加表现得更为敏感。研究表明,由于腐植酸含有较多的羟基、酚羟基和易降解组分,因此,在环境中,其反应活性更高,可以为Cu2+提供更多的结合位点[33]。
2.4.2 X射线光电子能谱(XPS)分析
为了明确水稻土DOM 与Cu2+之间的反应机理,采用XPS 对干燥后的DOM(添加/未添加Cu2+)进行扫描(图9a)。从图9a 中可以看到,未添加Cu2+的DOM的XPS 全谱中,Cu2p 上无响应峰,在添加Cu2+后(图9b)其能谱图中出现了明显的峰值区域,说明DOM 与Cu2+之间发生了结合。添加了Cu2+后(图9c)其有4 个明显峰值区域,分别为Cu O(932.7、934.5、954.3 eV)和O Cu O(952.4 eV)[34]。Cu O 和O CuO 的峰面积占总体面积比例分别为80%和20%。表明在水田土壤中所添加的Cu2+主要以CuO 的形式存在,并且Cu2+会与DOM 中的含氧化合物发生络合反应。另外,XPS 结果显示,Cu 除了发生络合作用外,还发生了氧化还原过程,生成了少量的Cu+。这是因为DOM 中含有的腐植酸具有一定的还原特性。腐植酸中含有醌、酚等氧化还原官能团[35],有研究证实了在现实环境条件下,醌、酚等官能团对可变价金属具有一定的还原能力[35-36]。同时腐植酸还可以与某些金属离子的氧化还原对紧密结合,形成配合物从而间接地还原金属离子[37]。
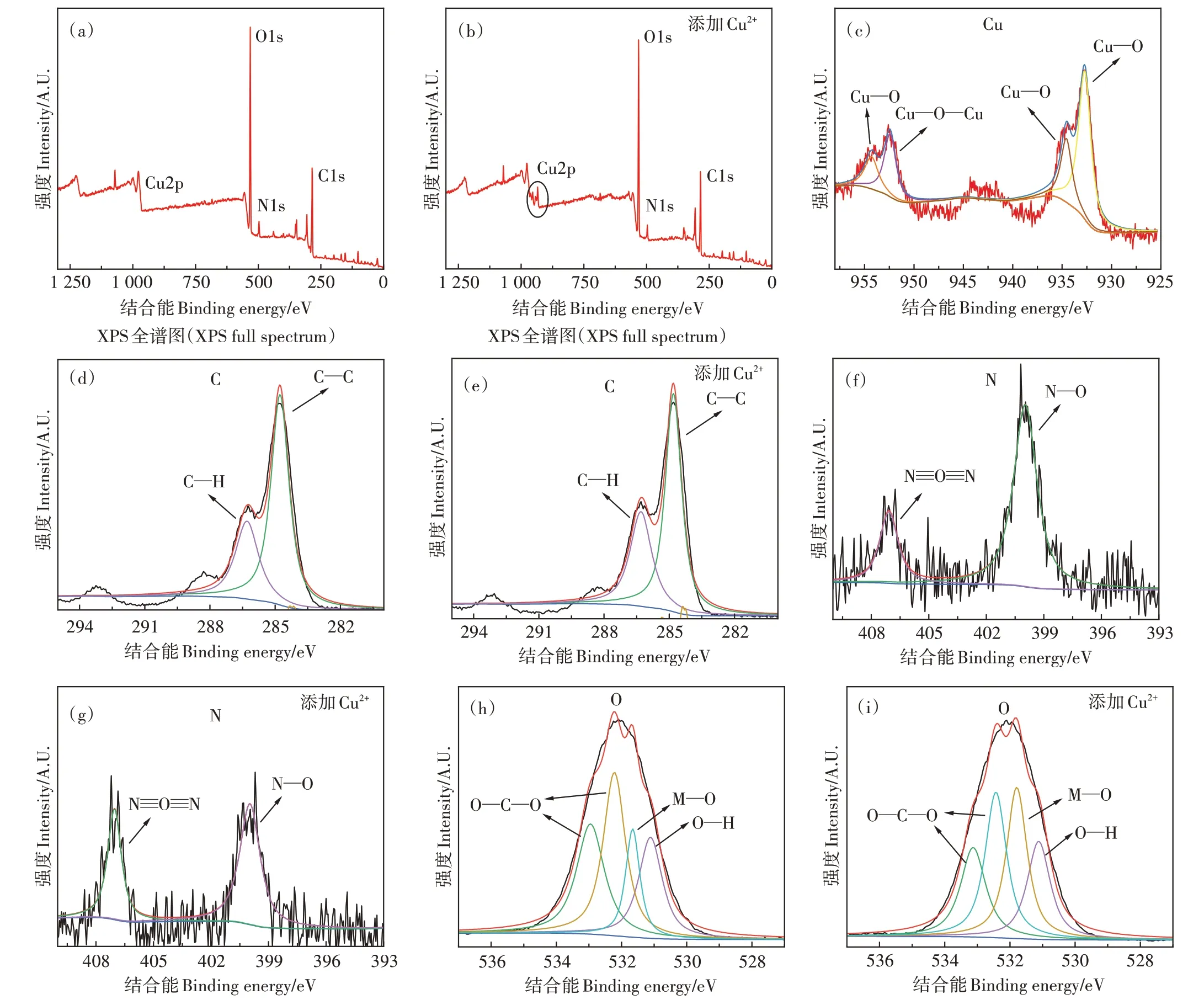
图9 土壤溶解性有机质添加Cu2+前后XPS光谱图Figure 9 XPS spectrum before and after Cu2+addition to soil dissolved organic matter
进一步分析,在C1s(图9d)轨道中存在两个峰值区,分别为C H(286.3 eV)和CC(284.8 eV)[38]。在添加了Cu2+后(图9e),CC由67.9%下降到63.5%,C H 则由32%上升至36.5%,其中CH 的生成表明添加Cu2+后DOM 中的芳香性物质增多。而在N1s 轨道中(图9f),存在的两个峰值区域,NO(399.9 eV),N ON(407.10 eV)[39]。其中在添加Cu2+后(图9g),NO 由76.5%下降至61.6%,N O N 的占比则提高,由23.5%上升至38.4%。在O1s 轨道中存在4 个峰值区域(图9h),除了C O(532.9 eV,532.3 eV),还出现了M O(531.6 eV)以及OH(531.1 eV)[40]。其中CO、OH 峰值的面积在添加Cu2+后其面积明显减小,而MO 的占比则显著提高(图9i)。在N1s 轨道中N O键数量减少而ON键数量增加,在O1s轨道中CO 的数量减少明显且MO 键的数量增加,表明CuO 的形成与Cu2+和含氮、氧的官能团络合形成有关,如羟基、酚羟基以及氨基等。
3 结论
(1)庐江县水稻土土壤溶解性有机质(DOM)中SUVA254的值为(3.25±0.07)L·(mg·m)-1,其主要由亲水性物质组成,芳香性较低且芳香结构中含氧官能团比例较高。DOM 的构成以类富里酸和类腐植酸为主,其中陆源输入所占比重较大,自身组分较少且内部生物活性相对较低。
(2)原本疏散多孔的土壤DOM 在加入Cu2+后,Zeta 电位升高,表面形貌发生了巨大的改变,DOM 的粒径不断增大且生成类似块状结晶的络合物。同时水稻土DOM 组分随Cu2+浓度的增加出现了不同程度的淬灭现象,表明DOM 通过表面疏松的介孔结构、负电荷及官能团与土壤中的Cu2+发生了络合,并且Cu2+与类腐植酸组分的络合力强于类富里酸,同时优先于DOM 中的短波类腐植酸,通过XPS 分析发现,添加的Cu2+主要以Cu O存在。
(3)DOM 通过表面疏松的介孔结构、负电荷以及羟基、酚羟基以及氨基等官能团对Cu2+吸附起到关键作用。因此可以在土壤中施加农家肥等富含腐植酸类肥料,倡导秸秆还田措施,对生物质材料进行有效堆肥,并及时补充微生物含量,从而达到提高土壤DOM中类腐植酸的含量,增加土壤及其胶体对Cu2+的吸附能力,从而降低Cu2+对生物的有效性。

