高血压患者血清25(OH)D、BGP、UA异常表达与血脂异常的相关性
李素芳,朱富佳,李芳奇,刘盈盈
首都医科大学附属北京世纪坛医院:1.干部综合科;2.神经与精神科;3.消化内科,北京 100038;4.北京市石景山医院血管外科,北京 100040
高血压是一种多发性疾病,近年来随着人们生活方式和饮食结构的改变,其发病率逐年升高,已成为威胁我国居民健康的重大公共卫生问题[1]。血脂异常是指机体的脂质代谢或转运过程发生异常,导致血浆中血脂过高,与高血压并存容易增加心脑血管疾病的患病风险[2]。因此,如何防控高血压患者发生血脂异常,是现阶段医护工作者面临的重大挑战。25羟维生素D[25(OH)D]是维生素D在循环中的主要表现形式,能够参与机体的钙磷代谢、骨形成、免疫调节等过程,研究发现,25(OH)D缺乏与血脂异常密切相关[3-4]。骨钙素(BGP)是一种特异性非胶原蛋白,主要由成骨细胞合成与分泌,可反映机体的骨代谢情况,并且能够参与机体的糖脂代谢过程[5]。尿酸(UA)是机体嘌呤代谢的产物,当UA堆积过多可导致高尿酸血症,增加心脑血管疾病的发生风险[6]。目前,关于血清25(OH)D、BGP、UA与血脂异常关系的报道较少。因此,本研究主要探讨高血压患者血清25(OH)D、BGP、UA异常表达与血脂异常的相关性。
1 资料与方法
1.1一般资料 选取2020年2月至2022年4月首都医科大学附属北京世纪坛医院收治的112例原发性高血压患者为研究对象,年龄18~85岁,平均(62.54±7.25)岁;男60例,女52例。纳入标准:(1)符合原发性高血压的诊断标准[7];(2)患者及家属知情同意。排除标准:(1)近期内有服用降血脂药物、维生素D制剂者;(2)合并甲状腺疾病或自身免疫系统疾病者;(3)伴有严重的心、脑、肺功能不全者;(4)合并恶性肿瘤者;(5)有继发性高血压者;(6)依从性差及不能配合本研究者。本研究已获得医院医学伦理委员会的批准。
根据患者是否合并血脂异常分为非血脂异常组(n=77)和血脂异常组(n=35),血脂异常标准[8]:总胆固醇(TC)≥5.2 mmol/L或甘油三酯(TG)≥1.7 mmol/L或高密度脂蛋白胆固醇(HDL-C)<1.0 mmol/L或低密度脂蛋白胆固醇(LDL-C)≥3.4 mmol/L,其中一项指标符合即判断为血脂异常。
1.2方法
1.2.1资料收集 收集所有患儿的临床资料,包括性别、年龄、体重指数(BMI)、吸烟、饮酒、居住地、文化程度、血脂异常家族史、糖代谢异常、血脂指标(TC、TG、HDL-C、LDL-C)等。
1.2.2血清指标检测 患者入院24 h内采集4 mL清晨空腹静脉血,以3 500 r/min离心10 min后,取上层清液,保存于-80 ℃冰箱。采用酶联免疫吸附试验检测血清BGP水平,试剂盒由浙江贝氏生物技术有限公司提供,参照使用说明书进行操作。采用罗氏化学发光法检测血清25(OH)D水平(试剂盒购自瑞士罗氏公司)。采用全自动生化分析仪(山东欧莱博医疗器械有限公司)检测UA、TC、TG、LDL-C、HDL-C水平。
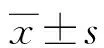
2 结 果
2.1两组患者临床资料比较 两组患者的性别、年龄、饮酒、居住地、文化程度比较,差异无统计学意义(P>0.05);两组患者的BMI、吸烟、血脂异常家族史、糖代谢异常比例及TC、TG、HDL-C、LDL-C水平比较,差异有统计学意义(P<0.05),见表1。
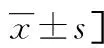
表1 两组患者临床资料比较[n(%)或
2.2两组患者血清25(OH)D、BGP、UA水平比较 非血脂异常组的血清25(OH)D、BGP水平高于血脂异常组,UA水平低于血脂异常组(P<0.05),见表2。
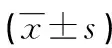
表2 两组患者血清25(OH)D、BGP、UA水平比较
2.3血清25(OH)D、BGP、UA水平与血脂指标的相关性分析 血清25(OH)D、BGP水平与TC、TG、LDL-C呈负相关,与HDL-C呈正相关(P<0.05);血清UA水平与TC、TG、LDL-C呈正相关,与HDL-C呈负相关(P<0.05)。见表3。
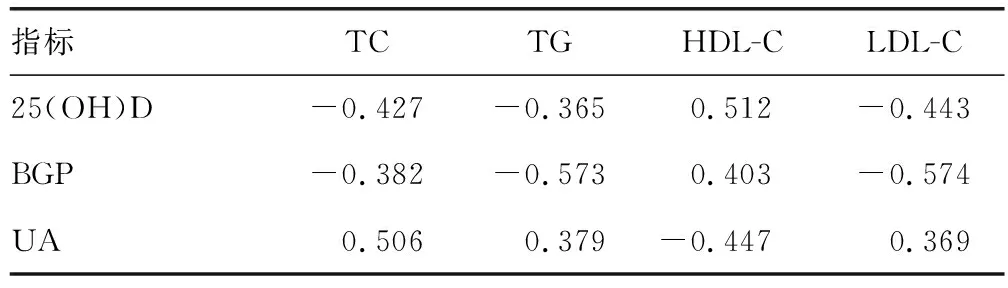
表3 血清25(OH)D、BGP、UA水平与血脂指标的相关性分析(r)
2.4血清25(OH)D、BGP、UA对高血压合并血脂异常的诊断价值 血清25(OH)D、BGP、UA预测高血压合并血脂异常的曲线下面积(AUC)分别为0.903、0.835、0.874,见表4。
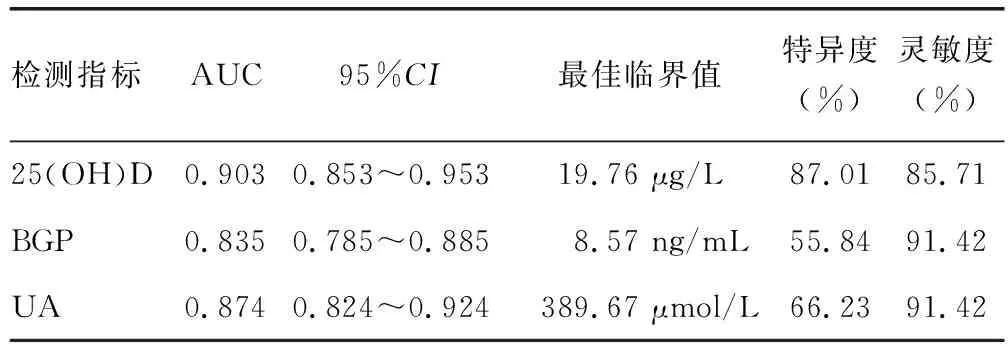
表4 血清25(OH)D、BGP、UA对高血压合并血脂异常的诊断价值
2.5高血压合并血脂异常的多因素Logistic回归分析 本研究将高血压患者是否合并血脂异常作为因变量(否=0、是=1),将单因素分析有意义的指标和25(OH)D、BGP、UA作为自变量进行多因素Logistic回归分析,结果显示,吸烟、糖代谢异常、25(OH)D≤19.76 μg/L、BGP≤8.57 ng/mL、UA≥389.67 μmol/L是高血压合并血脂异常的独立危险因素(P<0.05),见表5。
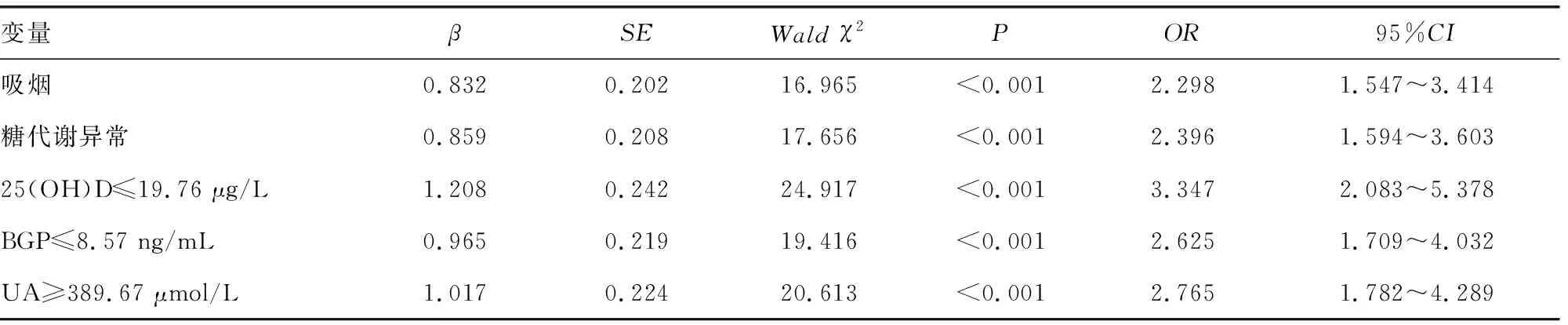
表5 高血压合并血脂异常的多因素Logistic回归分析
3 讨 论
高血压与血脂异常均是导致心脑血管疾病发生的重要病因,而临床上部分高血压患者常伴有血脂异常,据统计我国约有2.7亿人患有高血压,血脂异常的发病率更高[9]。血脂异常是导致高血压发生的危险因素,二者相互联系,互为因果关系,具有协同作用,二者并存后会增加心脑血管疾病的发生风险[10]。因此,防控高血压患者出现血脂异常,对降低心脑血管疾病的发病率具有重要临床意义。
25(OH)D是一种个体生长发育过程中必需的脂溶性维生素,不仅能够参与机体的钙磷代谢、骨形成、免疫调节等过程,且25(OH)D缺乏能够激活肾素-血管紧张素系统,促使血管平滑肌收缩,加速血管钙化,诱发高血压[11]。本研究发现血清25(OH)D水平在高血压合并血脂异常患者中降低,并且与血脂异常有关。分析原因可能是:25(OH)D可以增加钙离子在脂肪细胞中的水平,激活脂肪酸合成酶并抑制脂肪分解,促使脂肪细胞储存,当25(OH)D缺乏时,脂肪细胞的储脂作用受到抑制,大量的脂质释放入血,导致血脂异常[12]。同时25(OH)D缺乏时,单核细胞/巨噬细胞分化过程受到抑制,大量的炎症因子释放入血,导致LDL-C沉积[13]。此外,25(OH)D能够减少LDL-C的摄取,调控泡沫细胞的生成过程,而25(OH)D缺乏能够使细胞外基质受损,泡沫细胞生成增多,促使胆固醇脂类沉积增多[14]。因此认为25(OH)D与血脂异常有关,25(OH)D缺乏时发生血脂异常的风险越高。
BGP是一种由成骨细胞合成与分泌的特异性非胶原蛋白,被认为是骨形成和骨转化的生化标志物,同时BGP能够调控机体的钙磷平衡、血管内皮功能、炎症因子、糖脂代谢等过程[15]。研究发现,BGP能够激活磷脂酰肌醇3激酶/蛋白激酶信号通路,增加一氧化碳合酶(NOS)的活性,进而维持机体血压稳态[16]。本研究发现,血清BGP在高血压合并血脂异常患者中降低,且血清BGP表达异常与高血压患者血脂异常有关。分析原因可能是:BGP根据羧化程度不同可分为羧化和羧化不全两种形式,而羧化不全BGP具有促胰岛素分泌素的活性,可增加胰岛素的分泌,减轻胰岛素抵抗,进而减少脂肪细胞的过度堆积[17]。同时BGP可抑制脂滴包被蛋白、甘油三酯脂肪酶的活性,促使游离脂肪酸和TG水平降低[18]。当BGP缺乏时,机体的胰岛素分泌减少,胰岛素敏感性降低,脂肪细胞分解受阻并堆积,导致血脂异常。
UA是嘌呤代谢的终产物,正常情况下保持动态平衡,当UA生成增多或排出减少时,导致高尿酸血症,同时UA水平升高,可激活肾素-血管紧张素-醛固酮系统或抑制NOS的活性,诱发高血压[19]。本研究发现血清UA水平在高血压合并血脂异常患者中升高,且与高血压患者发生血脂异常密切相关。分析原因可能是UA水平升高,可抑制NOS的活性,使一氧化氮合成减少,血管内皮功能发生障碍,胰岛素的利用率减少,引起胰岛素抵抗,脂肪细胞发生堆积,导致血脂异常。同时UA经相关转运体进入细胞内,可激活p38信号通路,促使促炎症因子合成增多,抗炎症脂联素水平降低,进而加剧机体的炎症反应和胰岛素抵抗,发生血脂异常[20]。本研究还发现血清25(OH)D、BGP、UA预测高血压合并血脂异常的AUC均大于0.8,且25(OH)D≤19.76 μg/L、BGP≤8.57 ng/mL、UA≥389.67 μmol/L是高血压合并血脂异常的独立危险因素,提示血清25(OH)D、BGP、UA对高血压合并血脂异常具有一定的预测价值,且25(OH)D水平降低、BGP水平降低、UA水平升高是发生高血压合并血脂异常的独立危险因素。
综上所述,高血压合并血脂异常患者的血清25(OH)D和BGP水平降低、UA水平升高,且与TC、TG、HDL-C等血脂指标密切相关,是影响血脂异常的独立危险因素。

