基于“聚于胃关于肺”理论的幽门螺杆菌感染与慢性阻塞性肺疾病互作机制探讨
薛倩倩,王益德,徐 丹,李风森
(新疆医科大学第四临床医学院,新疆 乌鲁木齐 830000)
幽门螺杆菌(H.pylori)是一种带有鞭毛的主要定植于胃内的革兰阴性菌,感染该菌可导致胃部炎症、溃疡、胃黏膜相关淋巴瘤、胃癌等多种疾病。H.pylori感染了全球近一半人[1],据报道,我国H.pylori感染的患病率为41.5%~72.3%[2]。一项最新的系统评价结果显示,中国大陆的H.pylori总患病率为44.2%[95%CI(43.4%,5.5%)],估计有5.89亿人感染H.pylori[3]。近年来越来越多的流行病学调查研究发现H.pylori感染除了对消化系统疾病产生影响,还与胃外疾病例如慢性阻塞性肺疾病(COPD)等呼吸系统疾病密切相关[4]。Roussos等[5]研究发现COPD患者和对照组H.pylori感染率分别为77.8%和54.7%。丹麦一项流调显示与未感染的女性相比,H.pylori血清阳性的女性慢性支气管炎或COPD的患病率更高[OR=1.6,95%CI(1.1,2.5)][6]。
“聚于胃关于肺”出自《素问·咳论篇》,该理论高度概括了喘咳的病机,提示肺胃与喘咳关系密切,防治喘咳应注意肺胃并重,从肺胃角度入手分析咳喘的病机对临床防治COPD具有重要指导意义,这与现代医学消化系统常与呼吸系统共病相互契合。多数医家认同H.pylori总属中医“邪气”范畴,并且不同中医证型与H.pylori感染阶段有关,认为此种外邪侵犯是造成脾胃功能受损的重要原因[7]。故笔者拟基于“聚于胃关于肺”探讨H.pylori感染与COPD患病的相关性,现分述如下。
1 现代医学H.pylori与COPD患病相关机制
COPD是一种以肺气肿或慢性支气管炎为临床特征的慢性气流受限性肺部疾病,高龄、烟雾暴露、使用传统生物质燃料或煤等因素均证实是该病的独立危险因素[8]。除此之外,多项研究认为H.pylori感染与COPD患病关系密切[9],另有动物实验发现H.pylori对肺的致病机制可能与促炎因子释放、内皮功能障碍等造成的肺损伤有关[10]。目前,关于H.pylori感染在COPD等呼吸系统疾病发病机制研究日益增加,笔者查阅相关文献并对已明确及有争议的内容进行了汇总整理。
1.1宿主免疫反应 有证据表明,机体会在H.pylori侵犯后产生异己成分做出防御反应,通过分泌白细胞介素(IL)-4、IL-10、肿瘤坏死因子(TNF)-α等促炎因子使得血液中炎症水平升高进而形成非特异性免疫反应[11]。随着肠道菌群研究的深入,愈多证据表明消化系统是机体持续炎症反应的主要来源,并可作为调节炎症轴的驱动器及调制器[12]。上述现象为病原微生物通过全身免疫反应方式参与消化系统以外疾病提供了基本条件。进一步有研究发现H.pylori对宿主的影响不仅局限在消化道和血液,也可通过免疫应答方式影响肺脏等多种重要的靶器官,例如Kienesberger等[13]研究通过观察6个月H.pylori与小鼠宿主的互作关系发现该菌对机体产生的抗体反应可影响到肺组织,使得肺内出现细胞内黏附分子(CAM)-1、CAM-5等金属蛋白酶和内皮功能障碍相关标志物的免疫应答基因表达显著上调。现代医学认为影响COPD病程的关键因素与肺部及全身的慢性炎症反应有关,该病是由多种炎症细胞、促炎介质等共同参与的气道、肺组织、血管及机体的进行性慢性炎症性疾病,炎症细胞可分泌IL-4、IL-10、TNF-α等细胞因子,细胞因子又可反作用于炎症细胞进而构建出细胞因子、炎症细胞的复杂网络系统[14]。因此,宿主对H.pylori感染后诱发的机体免疫反应可诱导肺组织受损进而加重COPD疾病进程。
1.2肺发育不良 肺脏的发育过程分为出生之前的宫内发育及生后发育共两个阶段,上述过程易受到包括遗传、营养、环境等因素的影响,特别是生后发育阶段受到外界微生物环境等因素的影响较大[15]。多项流行病调查研究均发现儿童时期是H.pylori感染的重要年龄阶段,最新柳叶刀的一项包含152 650例儿童的荟萃分析结果显示:全球儿童H.pylori感染的总体患病率为32.3%[95% CI(27.3%,37.8%)],提示H.pylori感染在全球儿童和青少年中仍然非常普遍[16]。我国一项系统评价显示,尽管中国H.pylori感染率近几十年来呈下降趋势,但是在儿童及青少年人群中的负担仍较大[3]。需要注意的是儿童时期正是肺部发育与生长的关键时刻,如果此阶段受到细菌感染等各种因素导致肺发育不良可引发肺功能整体水平的下降,会显著增加COPD的患病风险。究其原因可能分别与铁元素吸收障碍、营养缺乏、机体炎症反应等因素有关:①Darvishi等[17]研究发现缺铁性贫血患儿H.pylori感染率显著高于非缺铁性贫血患儿(81.3% VS 14.3%),而铁元素缺乏与否正是影响肺脏发育及加速COPD疾病进展的重要原因[18],所以H.pylori感染导致的铁元素吸收障碍可能是影响患儿肺脏发育的原因之一。②营养不良与肺脏的发育至关重要,可通过影响其肺泡数量、肺组织胶原和弹性纤维减少等方式对肺发育及支气管发育不良产生影响[19]。波兰的一项前瞻性研究显示H.pylori感染是造成当地青少年营养状况较差的独立危险因素[20],Kopacova等[21]的研究显示,H.pylori感染与较低身高关系密切;另有研究发现,H.pylori感染是影响儿童的生长速度的重要因素,H.pylori阳性患儿其成年后身高较低,而身高是肺活量的主要预测指标[22]。所以H.pylori感染后导致消化系统功能异常引起营养缺乏或不足同样可能是引起肺发育不良重要原因。③Vestbo等[23]研究发现激活NLRP3炎症小体后可上调炎症细胞因子表达,进而通过抑制肺表面活性蛋白表达的方式干扰肺间质发育,此外,炎症反应也可通过激活NF-κB抑制VEGF和VEGFR2以及上调炎症介质影响肺脏发育[24],H.pylori感染引起的宿主免疫应答诱发包括肺脏在内的机体炎症反应已在前面进行阐述,那么我们有理由推测H.pylori感染引起的长期慢性非特异性炎症反应同样是减缓肺发育或诱导肺异常发育的原因之一。
1.3衰老表型 衰老是机体各个组织器官功能随着年龄增长而发生进行性退变的过程,是体内外包括遗传、环境污染等多种因素共同作用的结果。随着全球老龄化的到来,衰老表型的相关研究逐渐成为生命科研领域的热点问题[25]。近年来多项研究均发现COPD是一种加速的肺老化疾病,其疾病进程与机体衰老快慢密切相关,这为该病的发生、发展开辟了视野[26]。多项研究发现了一些与衰老相关标志物参与COPD疾病进程[27-28]。Sirtuins是一种去乙酰化酶,参与包括细胞分化、细胞衰老、炎症反应等多种生物学作用,其中SIRT1作为Sirtuins家族的重要一员,可通过对转录因子、组蛋白等多种蛋白修饰的赖氨酸残基方式进行乙酰化进而调控相关基因的表达。Shin等[29]使用褪黑色素诱导SIRT1高表达可降低炎症介质水平,进而对COPD发挥潜在治疗作用。同样,Klotho也是抗衰老的重要潜在作用靶点,其在衰老及抗衰老相关疾病进程中发挥极为重要的调控作用[30]。Gao等[31]研究发现在COPD患者肺组织中抗衰老基因Klotho表达显著减低,并通过动物实验观察到COPD患者气道上皮细胞Klotho表达降低与氧化应激、炎症和凋亡增加相关,这为COPD疾病进展与肺老化加速相关的机制提供了新的见解。Li等[32]采用体外实验发现Klotho激动剂对于COPD的治疗可能与其抑制CSE刺激细胞中的ERK、Akt和IGF-1的磷酸化进而减弱自噬表型发挥抗衰老作用有关。H.pylori感染同样是造成机体衰老的重要原因,并且参与调控Klotho、SIRT1等多个衰老相关基因的表达:自噬是一种保护细胞和生物免受细菌感染的进化保守过程,Wang等[33]观察到H.pylori可以通过下调SIRT1抑制自噬通量的方式促进其细胞内生存和定植,因此通过靶向SIRT1上调其表达减缓衰老的途径对于降低H.pylori感染对机体造成的损伤具有重要意义。而且,Wang[34]观察到H.pylori感染等多种原因造成胃部肿瘤患者中抗衰老基因Klotho表达下调,提示通过高表达Klotho进而参与调控衰老进程方式可能对于减缓或抑制H.pylori感染向肿瘤发生发展具有潜在应用价值。
1.4胃内容物误吸 伴有食管外症状的胃食管反流病,尤其是伴有咳喘等表现的胃食管反流病越来越受到人们的关注[35],H.pylori可以通过胃内容物误吸而移植到呼吸道的方式引起呼吸系统及全身的免疫反应;而且,食管内的酸性物质可激活神经轴锁反射这种引起局部神经反射方式诱导IL-5、IL-6、IL-8等促炎物质的释放引起炎症连锁反应;此外,H.pylori影响气道也可通过免疫细胞、神经源介质等直接引起呼吸道上皮组织的损伤[36]。可见,比邻关系造成反流H.pylori移植至呼吸道引起气道慢性炎症、气道重塑、损伤肺组织同样可能在诱发或持续性加重COPD临床表现方面发挥一定作用,见图1。
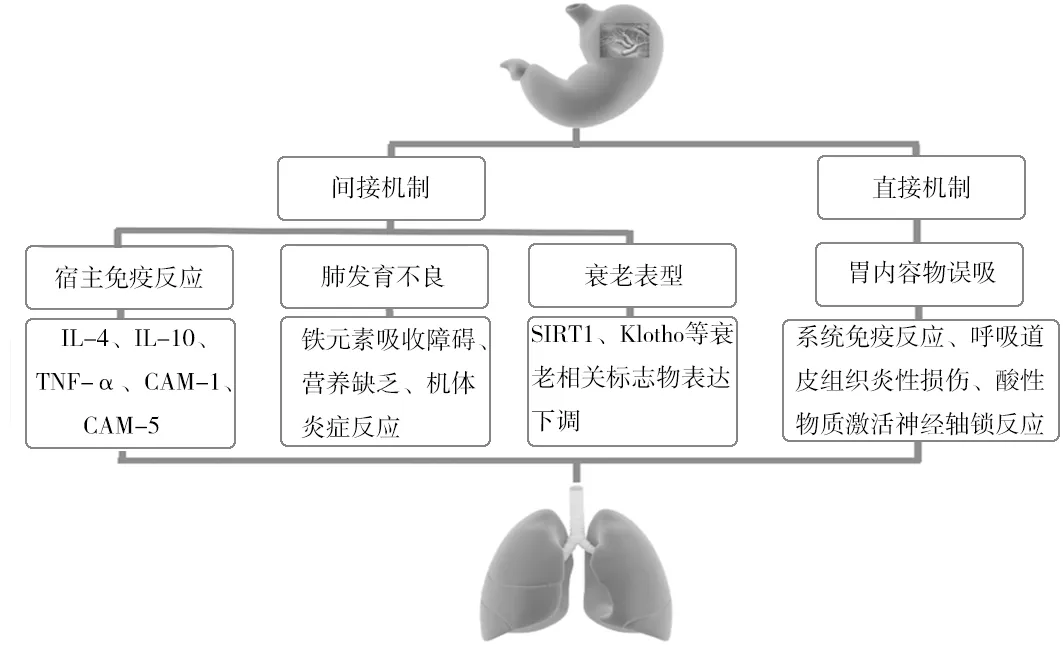
图1 现代医学关于H.pylori暴露与COPD患病的作用机制
2 中医学“聚于胃关于肺”理论探讨H.pylori侵袭脾胃与COPD关系
COPD是临床常见的呼吸系统疾病,属于中医学“喘证”“肺脏”等范畴,其病因多样,机制复杂,受到众多古今医家广泛讨论。《黄帝内经》中关于喘咳“聚于胃关于肺”的认识对后世影响深远。无论西医学还是祖国医学对于咳喘的认知与“关于肺”相关,自不待言。虽然中医学认为“五脏六腑皆令人咳”,那么单将胃放到如此醒目的总结位置其重要程度可见一斑,故有“聚于胃”之说。内经中常以脾胃并论,揭示脾胃共作才能体现其意义[37],目前大多医家也认为此处的“胃”指的是广义之胃,即脾、胃,而“关于肺”则是指的是胃中之邪进入或影响及肺脏。不揣浅陋,笔者现将“聚于胃关于肺”相关理论进行梳理并探讨H.pylori侵袭脾胃与COPD关系,兹浅析如下。
2.1“盖胃为水谷之海……而精气先输脾归肺” 中医学的藏象学说提到脾胃位于中焦,亦被认为“后天之本”,其在五行之中属土,具有生化气血之功,或作“气血生化之源”。《冯氏锦囊秘录》述:“至于脾胃……化源生发之机。”《玉机真藏论》曰:“五脏者,皆禀气于胃,胃者,五脏之本也。”所以饮食入胃,经其腐熟,配合脾之运化之功,脾气散精上归于肺,精微得以营养肺脏及全身,对于维持肺脏功能及机体的生命活动至关重要。《脾胃论》提到:“若胃气之本弱,饮食自倍,则脾胃之气既伤,而元气亦不能充,而诸病之所由生也。”H.pylori感染属于祖国医学“邪气”范畴,邪气旺盛,侵犯脾胃,脾胃之气虚弱或中气亏虚,经现代胃镜检查结果可多见慢性胃炎、慢性萎缩性胃炎等表现,长期可损害消化系统的营养功能。故而胃之受纳腐熟之功受损,则精微不足,肺脏失于濡养而疾病内生。
2.2“脾为生痰之源,肺为贮痰之器” 在生理状态下肺脏的功能得以实现需要精气之濡养,而精气需要脾之运化产生,故脾可益气助肺。在中医五行学说中肺脏属金,脾脏属土,土生金即表现在肺之宣降行水、输散津液之功需要脾之健运,运化水饮进行保障,两者协调,相互为用。《脾胃论》著:“肺金受邪,由脾胃虚弱不能生肺,乃所生受病也。”所以在病理状态下如若受到H.pylori等外邪侵扰后可致脾胃虚损,脾失健运,则水谷精微难归正化,反而酿生湿浊、痰邪,浸渍肺脏则生咳喘。本课题组前期的一项系统评价研究结果显示对于此类脾肺脏腑虚损所致喘咳,基于“培土生金”理论在西医常规治疗基础上辅以益气健脾方药相较于单纯常规治疗在改善COPD患者肺功能、减少临床症状等方面具有明显优势[38]。
2.3“胃主通降,肺主肃降” 《庄子·天运篇》曰:“意者有机缄而不得已耶。”“气机”即气的运动或包括“升降出入”运动的形式,其中机体又以“升”“降”这两种方式多见。具体到脏腑,脾胃位于中焦,通连上下,故有“脾胃为气机升降之枢纽”之论。肝主疏泄可辅脾升胃降之气机正常运行,同时,肺主肃降与肝之升发相互协作,从而调理脾胃与肺脏气机的升降运行。五脏六腑皆令人咳,其中肝火犯肺所致咳嗽的肝咳较为常见,叶天氏在治疗肝咳时常以泄肝通胃法治之;现代医家牟重临针对喘嗽等肺部疾病,常采用“通腑而降肺气”“肃降肺气以通腑”之法调畅肺气郁胃腑之气机,常获卓效[39]。
2.4“手太阴之筋,起于大指之上……散贯贲,合贲下抵季胁” 《黄帝内经》言:“经脉者,所以行血气而营阴阳,濡筋骨,利关节者也。”中医经络学说与精气血精液学说、藏象学说等理论互相辅翼,贯穿于医学体系中的生理、病理、疾病诊治等多个方面,在祖国医学之中占有重要地位。脾脏与胃腑在经络体系中存在联属关系,两者表里并行,足阳明胃经属胃而络脾,足太阴脾经属脾而络胃,《灵枢经》提到:“太阴阳明为表里,脾胃脉也。”《素问》同述:“四肢者皆禀气于胃,而不得至经,必因于脾,乃得禀也。”此外,脾脏与肺脏同样存在经络联系,关系密切:两者皆属太阴,功能互用,经气相同、气血互贯;而且肺经与胃相关联,手太阴肺之经筋循行至胃之贲门,《灵枢经》述有:“手太阴之筋,起于大指之上……散贯贲,合贲下抵季胁。”在上述联属关系下,胃脏受H.pylori等外邪侵扰,循足阳明胃经系到足太阴脾经,进而络与同属太阴之肺经,影响其经气及气血运行可影响到手太阴肺经正常功能的运作。
可见,医学对于“聚于胃关于肺”的认识可从其营养疏布、健运化痰、气机通降、经络联属这四个方面去理解,见图2。生理状态下胃发挥腐熟营养之功,脾之健运,将水谷精微物质经过经络联属疏布肺脏及全身,津液得以疏布,气机达畅,则喘咳自消。如若受到H.pylori感染等外邪侵扰,在病理状态则会出现胃失通降,脾失健运,痰浊自现,则咳喘内生;《医贯·喘》认为“真元损耗,喘出于肾气之上奔……及气不归元也。”咳伤肺气,久病肺弱,加之脾胃营养疏布之功受损,也会加重其“本虚”之机。

图2 基于“聚于胃关于肺”理论的H.pylori侵袭脾胃与COPD相关性
3 小 结
综上,基于“聚于胃关于肺”理论,中医学主要从“营养疏布、健运化痰、气机通降、经络联属”四个方面重点阐述了脾胃与喘咳等肺部疾病的密切关系,并认为H.pylori感染在中医病因学说中属由口而入的外邪,现代医学则分别从宿主免疫反应、反流H.pylori移植、肺脏发育、衰老表型等方面对H.pylori感染诱导或加重COPD的可能机制进行了初步探讨。当然,尚有一些问题未得到阐明:首先,由H.pylori感染诱导或加重COPD的研究类型仍多属于横断面研究或回顾性分析,因果推论较差、证据等级偏低,因此两者的具体关系仍有待大样本多中心的前瞻性队列及相关的高质量系统评价进一步证实;其次,中医药现代化是传统中医学发展的必然要求,而关于经典中医理论的研究对于指导临床诊断与防治具有重要的临床意义,目前“聚于胃关于肺”理论相关的肺脏与脾胃的关联基础研究仍然较少,其背后客观物质基础和科学内涵的尚未完全阐明;最后,需要注意的是,目前关于H.pylori感染与COPD患病的基础研究多是基于体内外实验的间接机制探讨,研究内容相对表浅,随着系统生物学、多组学等现代生物科学技术的迅速发展,对于深入了解宿主基因组和微生物基因组之间的相互联系和相互作用、高通量方式筛选关键靶点及后续针对性开发相关药物具有重要意义,从而为制定预防或治疗该病提供新策略。
利益冲突:所有作者均声明不存在利益冲突。

