老年衰弱综合征与躯体化症状及焦虑抑郁的相关性
全 英,胡晓月,刘 红
躯体化症状表现为变化不定、品类繁多、反复性发生的症状,受心理和社会因素影响,也就是说即便患者已经被确定为存在某些疾病,但所罹患的疾病不能全面阐述相关症状的性质以及程度[1]。老年衰弱综合征主要指的是60岁以上的人群出现的系列性症状,但这些患者并未表现出显著器质性改变的综合征。老年衰弱综合征患者往往会表现出肢冷畏寒、气喘咳嗽、夜尿频多、腰酸腿痛、失眠健忘、食欲不佳等问题,医院检查时会发现特别明显的器质性疾病,易出现焦虑、抑郁等问题。相关文献证实[2],老龄人群内发生衰弱的概率大约为10%,85岁以上老年人群体约有50%存在老年衰弱综合征,上述群体还没有取得系统化诊治和评估。为了全面探讨老年衰弱综合征与躯体化症状及焦虑抑郁相关性,本文对上述问题加以分析。
1 资料与方法
1.1 一般资料:本研究选取2020年6月至2021年6月在石嘴山市第二人民医院住院的老年患者为研究样本。共计300例。男183例、女117例。年龄61.33~83.55岁,平均年龄(74.44±5.11)岁。结合Fried得分标准,分成衰弱组(120例)、前期衰弱组(95例)、非衰弱组(85例)。
1.2 纳入标准:①资料完整;②>60岁;③知情同意、认知正常;④预计生存时间高于6个月。
1.3 排除标准:①近6个月内存在感染症状、重度创伤;②肿瘤终末期病患,生存时间半年以下;③当前使用精神类药物者;④慢性疾病急性加重期者;⑤其他不适合参与实验调查者。
1.4 方法:本实验通过创建数据库的方式,记录好受试者基础资料。其中包含文化水平、年龄、性别、BMI指数等等。有效记录患者疾病发生情况,受试者在入组后第2天清晨接受取血检查。测定各项生化指标。
1.5 诊断标准
1.5.1 冠心病(CHD):结合ACC/AHA标准进行诊断[3]。
1.5.2 心律失常:按照病患心电图检查资料/疾病史情况开展诊断。
1.5.3 高血压(EH):参考《中国高血压防治指南2018年修订版》内相关条目[4]。
1.5.4 2型糖尿病(T2DM):参考WHO在1999年制定的标准[5]。
1.5.5 脑血管疾病(CVD):依照迅速出现有关体征和突然性发病的特点,同时参照脑血管病理改变引发疾病的具体证据。
1.6 评估标准
1.6.1 衰弱评估:实验应用Fried量表对受试者开展衰弱评估,共计5个项目,每项积分1分。结合该量表标准,符合0项视为非衰弱者,符合2项以内视为前期衰弱者,符合3项以上视为衰弱者。以此为依据对受试者开展分组。
1.6.2 躯体化症状严重程度分析:应用PHQ-15问卷量表分析受试者躯体化症状严重程度。该量表信效度良好,操作性强。具体结合病患症状严重程度分为3级。0级为不存在困扰;1级为当前困扰比较少;2级为当前困扰比较多。30分为满分,0~4分为无躯体症状,分数越高表明患者躯体症状越严重。
1.6.3 焦虑评估:应用SAS量表评价焦虑详情。临界分值为50分,分数和焦虑状态呈正比。
1.6.4 抑郁评估:应用SDS量表评价抑郁详情。临界分值为53分,分数和抑郁状态呈正比。
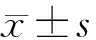
2 结果
2.1 不同衰弱程度患者基线资料对比情况:3组间的CHD、年龄、性别比较差异有统计学意义(P<0.05);3组间的心律失常、脑血管疾病、DM、EH、学历、BMI比较差异无统计学意义(P>0.05),见表1。
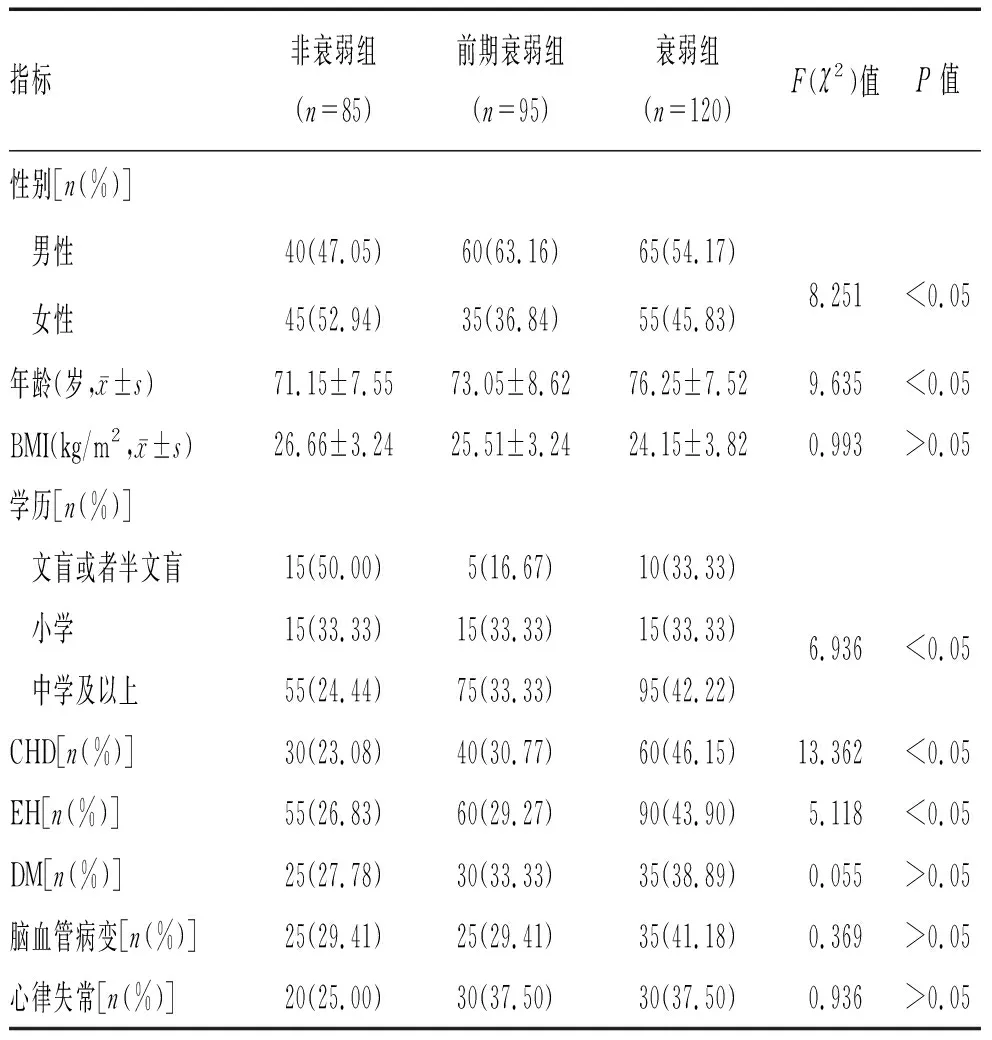
表1 不同衰弱程度患者基线资料对比
2.2 不同衰弱程度患者各项生化指标比较:3组间的IL-6、CRP、Scr、ALB水平比较差异有统计学意义(P<0.05);3组间的BNP、UA、 BUN、CysC、FPG、TG、TC、HDL-C、LDL-C、WBC、HGB、PLT水平比较差异无统计学意义(P>0.05),见表2。
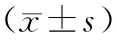
表2 不同衰弱程度患者各项生化指标比较
2.3 不同衰弱程度患者的焦虑、抑郁及躯体化症状对比:衰弱组和前期衰弱组SAS评分、SDS评分和PHQ-15评分明显高于非衰弱组,衰弱组SAS评分、SDS评分和PHQ-15评分明显高于前期衰弱组,随着衰弱程度加重,SAS评分、SDS评分和PHQ-15评分呈升高趋势(P<0.05),见表3。
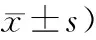
表3 不同衰弱程度患者的焦虑、抑郁及躯体化症状对比(分,
2.4 老年衰弱综合征高危因素回归分析结果:抑郁、焦虑、躯体化症状、冠心病、年龄是导致老年人出现衰弱症的独立性高危因素(P<0.05),见表4。

表4 老年衰弱综合征高危因素回归分析结果
3 讨论
老年衰弱综合征主要指的是当老年人生理储备降低之后,引发机体抗体水平下降、受损性增加的不正常状态。老年人生理储备降低或者多类异常为老年衰弱疾病的重要核心[6]。即便患者受到外界小刺激时,也有可能出现临床不良事件。可以说老年衰弱为系列性慢性疾病以及单次急性不良事件或者重症疾病的结局。相关文献表明[7-8],失眠、焦虑抑郁情绪、活动功能降低、合并用药、多病共存、肌少症、营养不良、意外跌倒以及高龄和老年衰弱疾病发生存在极大关联性。
诸多疾病共存有可能加速老年衰弱的发展,且这些疾病所造成的激素改变以及人体生理病理变化也与衰弱症的发生发展存在极大关联性。老年衰弱综合征发生的重要途径为系统调节和功能失衡[9]。尤其体现于代谢紊乱、凝血功能活动性加强、机体释放炎性物质、神经内分泌大幅度变化以及免疫系统失衡等诸多方面。本研究对300例住院的老年人进行分析,开展衰弱评估工作,探讨老年衰弱综合征与躯体化症状及焦虑抑郁的相关性,依照具体的衰弱程度分为衰弱组(120例)、前期衰弱组(95例)、非衰弱组(85例)。结果表明,前期衰弱组、非衰弱组年龄比衰弱组低(P<0.05),且和男性相比,女性更容易出现衰弱综合征。冠心病为导致我国老年人因病致残致死的重要原因。同时罹患衰弱综合征的老年冠心病患者比未发生衰弱综合征的人群预后更差,可使伤残和跌倒的风险明显增高,更容易受到医源性伤害。其中,曾经接受过心脏冠脉旁路手术、心力衰竭、急性心肌梗死、稳定性心绞痛以及导管介入治疗的群体,若发生老年衰弱综合征,其冠心病死亡的风险会增加2倍左右。本研究中,衰弱组冠心病检出率比其他2组更高(P<0.05)。提示心血管疾病的出现和衰弱存在相关性,导致这一情况发生的原因很可能和炎症通路被激活有关。值得说明的是,衰弱综合征的出现与消化系统疾病病理过程有着极多相似之处。与另外2组相比,衰弱组CRP、IL-6差异有统计学意义。提示在心血管疾病老年人血液之内,随着衰弱程度的提高,炎性有关的标记物以及炎性细胞都表现出了增高趋势。长此以往,会引起脂蛋白氧化应激反应发生,同时也增加了粥样斑块的不稳定性,加大了患者心血管意外事件的概率[10]。有研究证实从影响衰弱综合征发生的病理机制方面来看,某些肾源激素时改变和老年衰弱综合征发生发展存在关联性。本研究显示Scr和衰弱症之间存在极大关联性。高水平Scr值会对人体机能造成影响。同时不同程度衰弱患者人血白蛋白之间存在统计学意义(P<0.05)。提示营养不良可能会增速衰弱疾病发展[11]。
从衰弱和焦虑抑郁关系来看,有研究表明[12],和以往相比,当前国内人群出现焦虑抑郁的概率明显上升。不同地区、不同群体的焦虑抑郁检出率差别比较大,结合WHO组织针对中华人民共和国老龄化以及健康国家评估报告,预计到2030年,中国的老龄化会引起慢性非传染性疾病负担增加40.00%。本研究结果表明,随着老年人衰弱程度的不断加重,其发生抑郁焦虑的风险变得更高,以上两者呈正相关性。分析原因可能为随着老年患者衰弱程度加重,机体失能,日常生活能力逐渐受限,生活方式和社会角色发生较大变化,患者适应能力减弱,自身感受无法完全表达,对个人能力和自信心造成伤害,从而导致焦虑、抑郁等负面情绪的发生和发展,继而导致更恶劣的临床结局。
心理因素和躯体化症状相互影响。躯体化症状和焦虑抑郁之间有相当高的共患率[13]。当前针对躯体化症状和其他精神障碍疾病共患现象研究较多。躯体性症状和焦虑抑郁存在关联性,可能互为因果关系,患者躯体性症状越严重,其发生焦虑抑郁的危险性越高,而焦虑抑郁程度越严重又可使躯体化症状加重,继而导致病情进展。本项研究结果显示,衰弱组和前期衰弱组SAS评分、SDS评分和PHQ-15评分明显高于非衰弱组,衰弱组SAS评分、SDS评分和PHQ-15评分明显高于前期衰弱组,随着衰弱程度加重,SAS评分、SDS评分和PHQ-15评分呈升高趋势(P<0.05),与上述研究结果一致。因此,在临床治疗工作中,应重视老年衰弱综合征患者的心理健康状况,综合评估患者的病情和心理状况。尽早对病患开展干预可提高其自信心和治疗依从性,提升病患生活质量,使其从心理、生理和社会角度再适应,促使躯体化症状和心理状况达到良性互反馈,从而避免出现不良预后结局。
本研究在校正其余混杂因素之后,针对开展单因素分析有统计学意义的结果实施了多因素logistic分析结果证实,抑郁、焦虑、躯体化症状、冠心病、年龄是导致老年人出现衰弱症的独立性高危因素(P<0.05)。随着老年人年龄的不断增加,老年人多系统、多器官生理和功能下降,机体储备量较低,其出现衰弱的风险明显上升。同时,有研究表明[14],老年衰弱的出现和躯体性症状存在关联性,和非衰弱者相比,老年衰弱者发生躯体性症状的风险高出2.5倍。群体化症状和炎性因子入侵的病理学特点可能为导致这一结果出现的真实原因。另有研究表明[15],老年衰弱症患者出现躯体化症状的同时也会对机体功能产生不良后果,随着患者躯体化症状变得越来越严重,衰弱症状也进一步恶化。
综上所述,老年衰弱综合征与躯体化症状及焦虑抑郁之间存在关联性。医生除了要治疗病患躯体症状外,也应当重视其心理健康水平,做好患者的筛查工作,综合性评估患者的病情和心理状况,提升病患生活质量,促使躯体化症状和心理状况达到良性互反馈,从而避免出现不良预后结局。

