发酵纤维素阴离子衍生物的转化与抗菌应用评价
崔艳丽,李顺尧,张天宇,张敏燕,鲍祥祥,毛旸易
(1.浙江大学 化学系,浙江 杭州 310058;2.郑州财经学院,河南 郑州 450044;3.武汉大学,湖北 武汉 430072)
碳达峰碳中和是一个多维、立体、完整的系统工程。21 世纪已从“石油精炼”依赖向“生物精炼”时代开启。纤维素是地球上最丰富的天然有机物,占植物界碳量的50%以上。纤维素由于具有可持续性、可降解性、生态协调性及多羟基衍生化能力强等特点广受青睐,特别是对功能性纤维素衍生物的研究与开发。提取油脂后的米糠中大约含有50%纤维、20%蛋白质以及10%植酸钙等。常见的纤维素结构修饰有物理修饰、化学修饰(硫酸化、磷酸化、乙酰化等)和生物工程修饰。经生物改造后纤维素分子量和单糖的分布发生变化[1-2]。本文通过对发酵后的米糠纤维素进行化学改造,制备带阴离子的纤维素衍生物,在文物保护、农产品保存、日常防护等中用于抗真菌。全世界有500 多万种真菌,侵袭性霉菌问题日益严重,如文物保存中易受霉菌侵害,农作物在运输、保存中由于受霉菌侵害被大量丢弃等,人类面临变异微生物的劫难。以往用抗真菌剂进行接触性消杀,对人体具有一定的毒性,且会引起微生物变异产生耐药性。PERFECT[3]在抑制真菌途径、靶点和作用机制的基础研究中,对第1~第3 代抗真菌剂进行了总结,指出多糖衍生物是未来的抗菌剂前沿,其具有成膜性,能作为物理屏障阻碍病菌侵入,克服了现有技术的弱点,且对保护对象生态友好,易被接受;带电荷的纤维素可通过其携带的电荷与微生物表面直接作用,由于其独特的抗微生物途径,不惧怕微生物的变异及不同的微生物品种来源,从而具有抑制微生物感染或直接杀伤微生物使其失去感染的能力[3-5]。
现有大多纤维素的衍生物反应条件有待提升,如利用离子液体、不易处理的DMSO 等有机溶剂、无机盐混合物等,成本高、后处理麻烦、转化率低等[6-10]。本文首次将经微生物改造的纤维素作为原料,在水相条件下采用阴离子醚化剂(3-氯-2-羟基丙磺酸钠,CHPASA)通过一锅法进行阴离子化,反应中使用的氢氧化钠溶液既作为反应物,又作为溶剂,还具有催化剂作用;反应条件温和,取代度适中,转化率较高。采用元素分析、核磁共振、傅里叶红外光谱(FTIR)等方法表征纤维素衍生物的组成和结构,并进行了抑真菌生物评估。纤维素阴离子衍生物具有可降解、生态环保、易接受等优点,可用于文保材料如皮革、纸张、石材等的抗菌保护;同时因其具有亲和、低价等特点,可用于农产品的保存;在大范围的防疫抗菌助剂等应用中亦具有潜力。
1 实 验
1.1 主要仪器与试剂
集热式恒温加热磁力搅拌器(DF-101S,上海),冷冻干燥器(FE-1A-50,上海),元素分析仪(vario MICRO cube,德国),红外光谱仪(Nicolet iS 10,美国),核磁共振仪(Bruker Avance Ⅲ 500 MHz,德国)。发酵米糠(酵母发酵7 d,自制),3-氯-2-羟基-三甲基磺酸钠(上海,分析纯),氢氧化钠(上海,分析纯),盐酸(上海,分析纯),去离子水。
1.2 纤维素阴离子衍生物的制备
称取干燥的发酵米糠1 g,置于烧瓶中,加入l4% NaOH 溶液18 mL,搅拌,随后加入3-氯-2-羟基丙磺酸钠。在一定温度(室温,50 ℃,70 ℃,90 ℃)下反应12 h,冷却后用稀盐酸溶液中和,用8 000 Da分子质量的透析袋透析48 h,冷冻干燥,称重,放入干燥器备用。
1.3 元素分析与取代度
采用元素分析仪测试阴离子纤维素衍生物样品中的含硫量(S%),推算阴离子基团取代度(DS)。DS 为纤维素大分子每个失水葡萄糖单元上被取代基团的平均羟基数。S%与DS 的关系为
1.4 红外光谱与取代基团
干燥样品在研钵中与KBr 混合研磨,压片后在400~4 000 cm-1范围进行FTIR 表征分析。
1.5 体外抑真菌活性评价
调整好菌悬液(选用黑曲霉、出芽短梗霉和嗜松青霉)的密度,并均匀涂布于凝结的平板培养基。先对标准滤纸(直径6 mm)灭菌,分别蘸取一定浓度发酵纤维素阴离子衍生物Y1 的水溶液,风干后贴于平板表面,其中1 片为灭菌后的滤纸,用于空白对照,3 片为处理后的滤纸,在平板培养基上25 ℃下培养48 h,测定抑菌圈大小。
2 结果与讨论
2.1 纤维素与CHPASA 反应
纤维素是由D-吡喃葡萄糖单元以β-1,4 苷键脱水而成的均多糖,具有复杂的四级结构。每个葡萄糖残基上有3 个羟基,其中6 位上的属于伯羟基,2,3位上的属于仲羟基。一般情况下伯羟基的反应能力比仲羟基强,且具有空间位阻小的优势;在氢氧化钠作用下,阴离子醚化剂自身发生反应,即3-氯-2-羟基丙磺酸钠的氯与邻位的羟基形成环氧化合物,环氧化合物活性高,在碱性条件下迅速与纤维素发生亲核取代反应,将阴离子基团引至纤维素羟基的氧原子上,获得阴离子纤维素衍生物,具有绿色环保的特点,不需要有机溶剂,与醚化剂共同作用,便可打开纤维素的氢键网络。同时发酵的纤维素,也会破坏一定的分子高级结构,去掉部分基团,从而使纤维素大分子羟基更易反应。
2.2 反应体系的选择
纤维素大分子内部及分子之间存在氢键,难以在常规的溶液或熔融状态下发生反应,因而其应用大受限制。已有报道认为,所有的有机溶剂、无机混合溶剂和离子液体等都是为了破坏其高级结构。进攻纤维素羟基的反应,首要的是破坏其氢键网络。本文采用经酵母发酵7 d 的米糠纤维素,通过脱油、脱水获得易参与反应的粗纤维;为方便后处理且降低成本,将一定浓度NaOH 溶液作为反应体系,在此体系中,NaOH 不仅可以作为溶剂,破坏纤维素的高级结构,而且可作为反应试剂,进攻CHPASA 的氯原子,同时可作为催化剂,去掉纤维素羟基中的氢,改变其环氧结构,使亲核反应更易进行。实验初期,体系为棕色分散液,随着反应的进行,纤维素网络被打开,得到半透明浑浊液,说明纤维素分子已遭其他分子攻击,二级结构被破坏,得到新的纤维素衍生物分子,其形态亦由不透明的棕色固体原料变为浅黄色固体产物。阴离子醚化剂先生成反应活性强的环氧化合物,其实质就是用碱催化烷氧基进攻羟基形成醚。
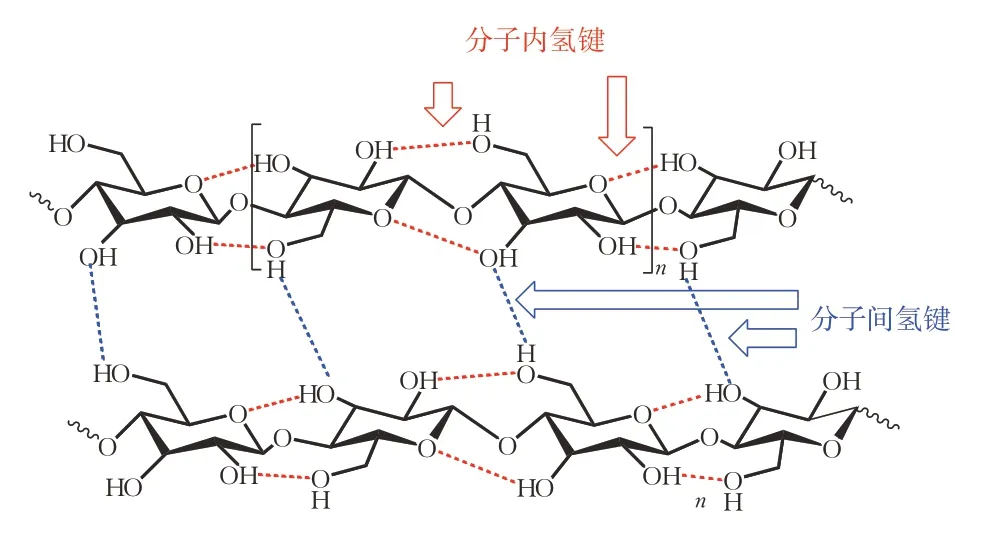
图1 纤维素结构与氢键分布[12]Fig.1 Cellulose structure and its hydrogen bond distribution
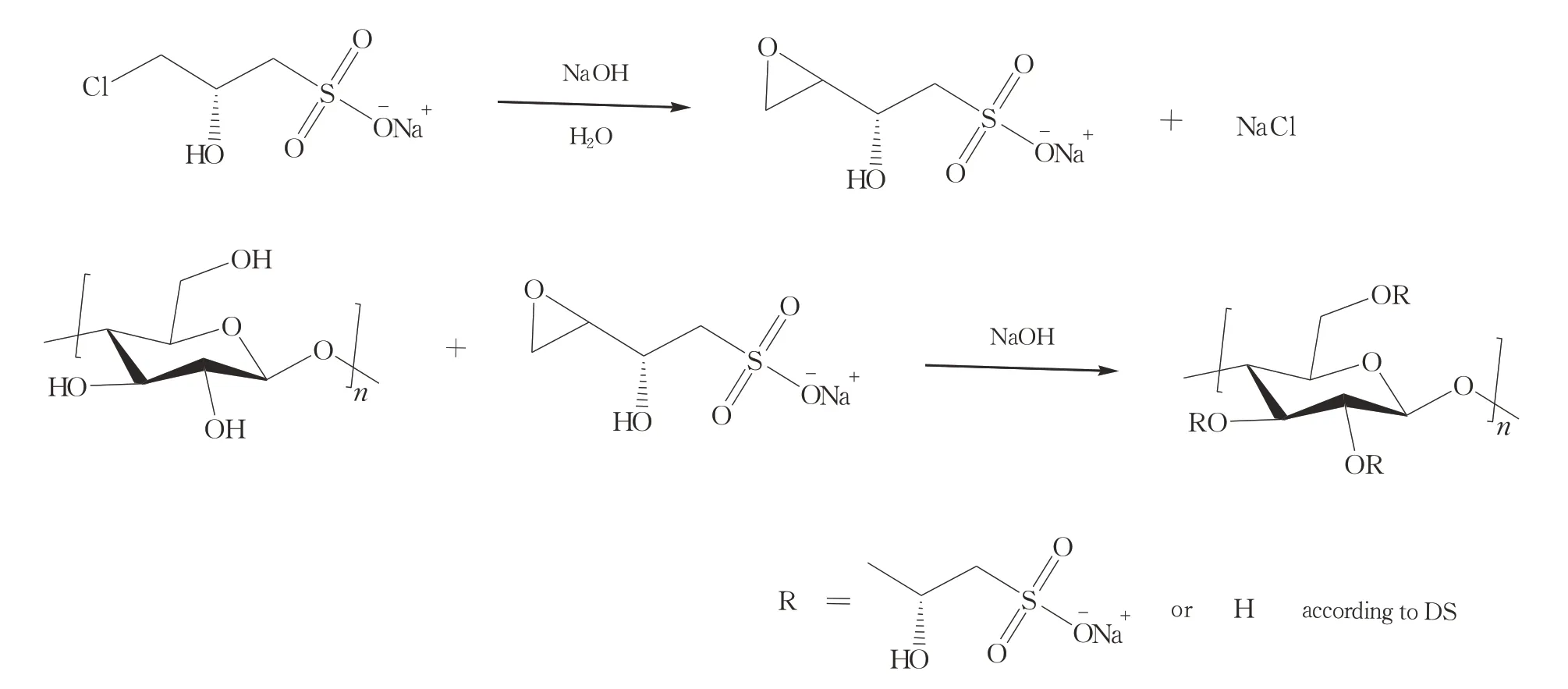
图2 阴离子醚化剂与纤维素的反应Fig.2 Etherification of fermented cellulose with CHPASA
2.3 反应条件对取代度的影响
前期的探索实验表明,反应温度、反应体系的NaOH/CHPASA 物质的量之比、CHPASA/纤维素物质的量之比均可影响产物的反应取代度。反应时间取12 h。
温度对纤维素衍生物取代度的影响结果见表1。由表1 可知,适当升高温度,可加快分子的运动,有利于促进亲核反应,提高取代度,但是温度过高,醚化剂会产生副反应,不利于主反应的发生。
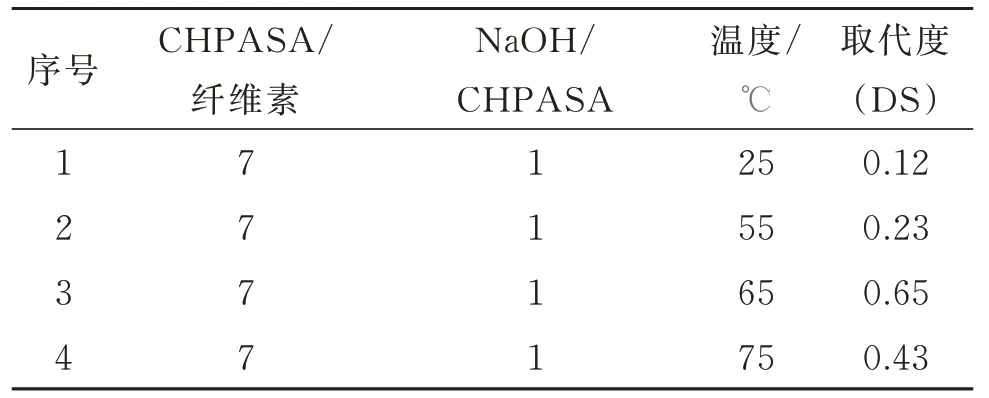
表1 温度对阴离子纤维素取代度的影响Table 1 Effect of temperature on degree of substitution of anionic cellulose
一般情况下醚化剂的投料更多,因为1 个葡萄糖残基有3 个未反应的羟基,CHPASA/纤维素物质的量之比为9,说明针对一个单糖残基的1 个羟基有3 个醚化剂参与进攻反应;由表2 可知,一味增加CHPASA/纤维素物质的量之比,虽能提高取代度,但提高有限甚至有所减小,综合考虑环保与成本,取CHPASA/纤维素物质的量之比为7。
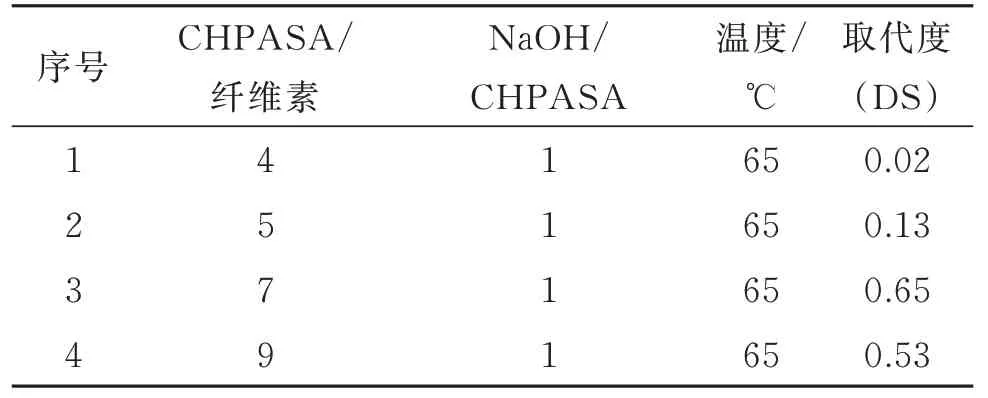
表2 CHPASA/纤维素物质的量之比对阴离子纤维素取代度的影响Table 2 Effect of CHPASA/cellulose molar ratio on degree of substitution of anion cellulose
体系的酸碱度对反应影响很大,当碱性偏强时,醚化剂产生很多副产物,影响主反应。但需保持适当的碱性,以保证环氧的形成和羟基的去质子化。由表3 可知,当NaOH/CHPASA 物质的量之比为1时,取代度最高。
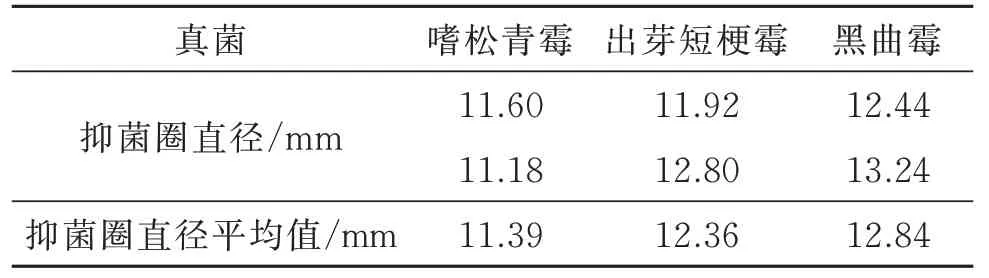
表4 纤维素阴离子衍生物Y1 的抑菌效果Table 4 Antifungal effect of cellulose derivative Y1
综上,优化反应条件为反应温度65 ℃,NaOH/CHPASA 物质的量之比1、CHPASA/纤维素物质的量之比7。
2.4 核磁共振图
图3 为纤维素阴离子衍生物Y1 的1H-13C NMR谱图(溶剂:D2O,温度:25 ℃),横坐标为1H 化学位移,纵坐标为13C 化学位移。
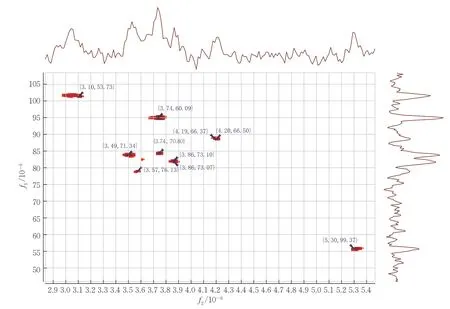
图3 发酵纤维素阴离子衍生物Y1 的二维NMR 谱图Fig.3 2D 1H-13C NMR spectrum of cellulose derivative Y1
从图3 中可看到,Y1 中有9 种碳,与氢谱的化学位移大小对应,并且是单取代;(5.31×10-6,99.33×10-6)处为葡萄糖单体异头碳的化学位移[11];相关点并不杂乱,貌似单糖产物的图谱,说明经过发酵后纤维素更易反应,并且其大分子已展开,无其他基团存在;化学位移(3.10×10-6,53.73×10-6)处为与磺酸基连接的亚基,这充分说明已成功引入了阴离子醚化剂基团;其他7 个点的氢谱化学位移从3.49×10-6至4.20×10-6不等,碳谱化学位移从60.09×10-6至76.13×10-6分别为葡萄糖单元5 个碳与醚基上另外2 个碳的归属。
2.5 傅里叶红外光谱图
图4 为400~4 000 cm-1的发酵纤维素与发酵纤维素阴离子衍生物的FTIR 谱。产物与原料比较,呈现了一些特异吸收峰。由图4 可知,3 415.96 cm-1附近出现的较强吸收峰是由分子O—H 伸缩振动引起的;2 926.81 cm-1处出现的吸收峰由亚甲基伸缩振动引起;1 639.97 cm-1附近的峰为羟基与自由水形成的氢键吸收峰;这3 个吸收峰构成了多糖的特征吸收峰。在1 043.33 cm-1处,由C—O 伸缩振动产生;在615.94 cm-1附近有1 个S—O 特征吸收峰。核磁共振谱图亦证明,纤维素与阴离子醚化剂反应后,带阴离子的基团被成功引入大分子中。
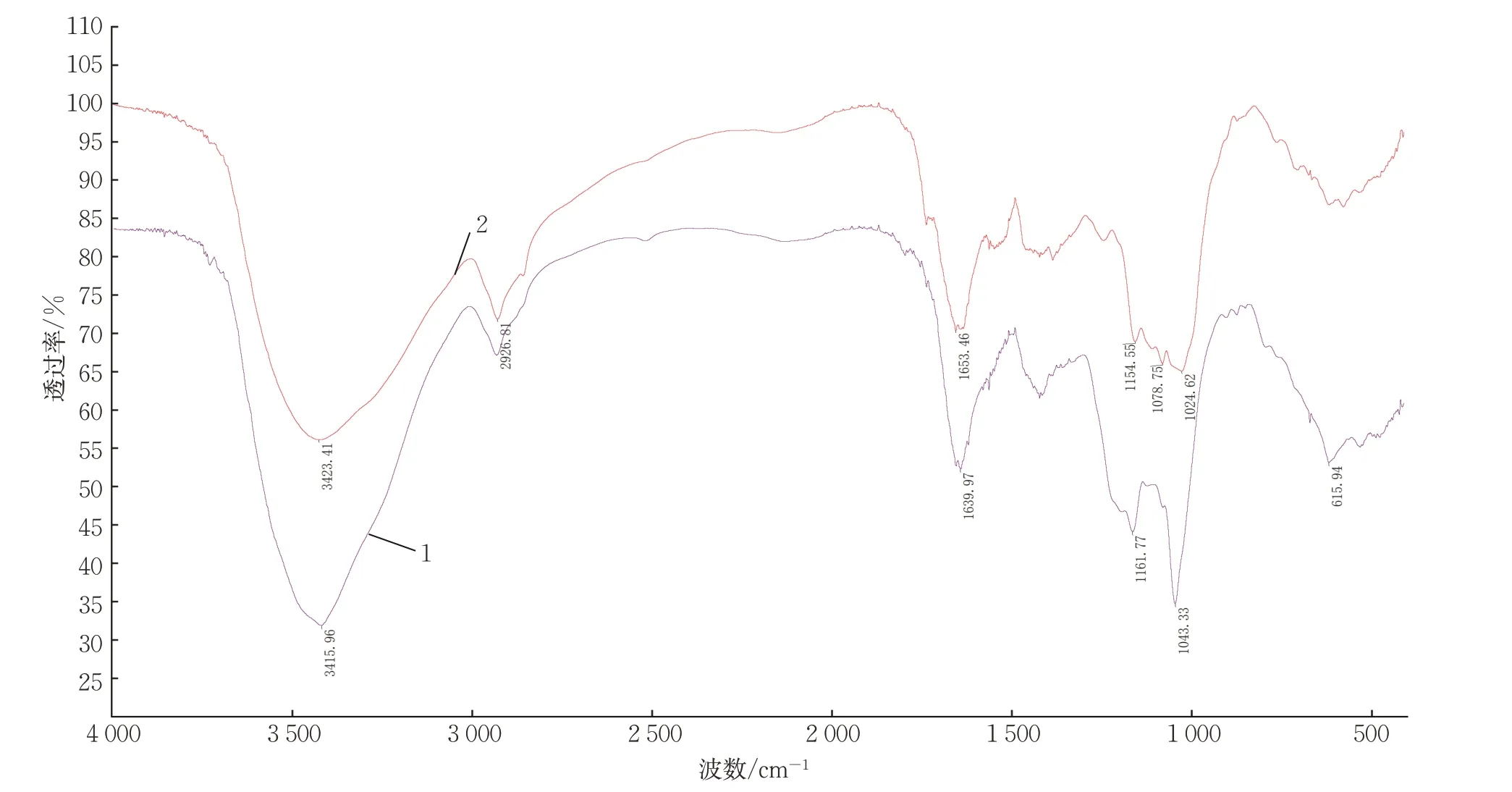
图4 发酵米糠纤维素阴离子衍生物Y1 与发酵米糠纤维素FTIR 谱图Fig.4 Comparison of infrared spectra between cellulose derivative Y1 and fermented cellulose
3 抑制真菌实验
抑制真菌实验选定的含菌量约为1×107~2×107CFU·mL-1,纤维素阴离子衍生物Y1 的浓度为40 mg·mL-1。纤维素阴离子衍生物Y1 对3 种真菌的抑菌效果均表现为中敏,对黑曲霉的抑菌效果相对较强。考虑纤维素阴离子衍生物Y1 具有生态、可降解等优势,在文物保护、农产品储存及长期抗疫防护等方面具有应用潜力。
4 结论
研究了发酵纤维素转化为阴离子衍生物的绿色策略,得到的优化条件为反应温度65 ℃,NaOH/CHPASA 物质的量之比1、CHPASA/纤维素物质的量之比7,获得了取代度为0.65 的纤维素衍生物。通过元素分析、核磁共振、FTIR,表征了纤维素衍生物的结构。

