国家医保谈判新型抗肿瘤药物的发展变化
谢杏梅,高悦(上海市松江区中心医院药剂科,上海 201600)
肿瘤是严重危害人类生命的医学难题,据全球癌症统计数据显示:2020年全球恶性肿瘤新发病例1929万例、死亡病例996万例,其中我国新发病例457万,占世界肿瘤新发比例23.39%;2020年我国肿瘤死亡病例300万例,占世界肿瘤死亡比例30.2%,均位列全球第一[1-2]。随着恶性肿瘤发病率的升高,肿瘤学发展速度加快。近年来,新型抗肿瘤药物逐渐成为肿瘤治疗领域的新手段,相比较传统肿瘤化疗药物,新型抗肿瘤药物具有疗效好、选择性高、患者依从性好等特点,越来越多的新型抗肿瘤药物被纳入国家医保谈判药品目录,然而这些药物临床数据有限、权威用药指南缺失、医师药师用药经验不足,存在临床用药不合理现象[3-5],因此规范抗肿瘤药物合理应用以提高疗效、降低不良反应至关重要。
国家卫生健康委员会为规范新型抗肿瘤药物临床应用,提高肿瘤治疗的合理用药水平,保障医疗质量与医疗安全,维护肿瘤患者健康权益,牵头制定的第一版《新型抗肿瘤药物临床应用指导原则》(简称《指导原则》)[6]于2018年9月21日发布,并于2019年12月16日、2020年12月29日、2021年12月27日对《指导原则》进行更新[7-9]。本研究将对比历年《指导原则》与上一年份或相应年份《国家基本医疗保险、工伤保险和生育保险药品目录》(简称《医保目录》),重点剖析新型抗肿瘤药物数量、系统分布、靶点检测及医保支付限定适应证等方面的发展变化。
1 资料来源和研究方法
1.1 资料来源
2018—2021年版《指导原则》和2017年版、2019年版、2020年版、2021年版的《医保目录》。
《医保目录》分为西药部分、中成药部分、协议期内谈判部分及中药饮片部分,本文仅研究《指导原则》被西药部分和协议期内谈判(或称国家医保谈判)部分收载的新型抗肿瘤药物。
1.2 研究方法
本文采用描述性分析方法,主要比较《指导原则》和上一年或对应年份《医保目录》中新型抗肿瘤药物数量、系统分布、靶点检测及医保支付限定适应证等方面的发展变化。2018年版《指导原则》对应2017年版《医保目录》,2019—2021年版《指导原则》对应相应年份《医保目录》。
2 结果
2.1 《指导原则》及《医保目录》抗肿瘤药物发展变化
2018年版《指导原则》中纳入33个新型抗肿瘤药物,2019、2020、2021年分别增加了13、27、44个。分别以上一年度或相应年度《医保目录》为基准,2018年版《指导原则》中有26个新型抗肿瘤药物品种加入国家医保谈判(简称“国谈”),5个被纳入常规医保目录;2019年版《指导原则》中共有 34 个国谈品种,其中3个被调入常规医保目录;2020年版《指导原则》中共有41个国谈品种,其中2个被调入常规医保目录;2021年版《指导原则》中共51个国谈品种,其中3个被调入常规医保目录(见图1)。国谈工作趋于常态化机制,参与谈判的药品品种数量逐步增加[5],被纳入常规医保目录品种也稳健增加,减轻了参保人的医疗负担。
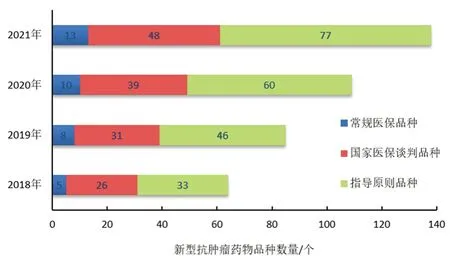
图1 历年《指导原则》药品、常规医保支付药品和国谈药品品种数量的变化Fig 1 Changes in the number of drugs in the Guiding Principles,conventional medical insurance payments and national negotiated drug variety over the years
2.2 《指导原则》各系统抗肿瘤药物分布及数量变化情况
2018年版《指导原则》共涉及7个系统肿瘤用药,2019年版《指导原则》增加了“生殖系统肿瘤用药”。2020年版较前两版《指导原则》稍有不同,将“皮肤与软组织系统用药”拆分为“皮肤系统用药”与“骨与软组织系统用药”。2021年版《指导原则》各系统分类与2020年版《指导原则》一致。与2020年相比,2021年《指导原则》呼吸系统新增药品7个;消化系统新增8个;血液系统新增4个;泌尿系统新增3个,删除1个;头颈部新增5个;生殖系统新增2个;乳腺癌、皮肤系统及骨与软组织数量未发生变化。《指导原则》抗肿瘤药物数量逐年稳步增加,各药物适应证以相应年份药品说明书为准,同一药品适应证可覆盖多个肿瘤系统(见表1)。

表1 新型抗肿瘤药物品种在系统肿瘤中的分布Tab 1 Distribution of novel anti-tumor drug variety in system tumors
与2020年版相比,2021年版《指导原则》共新增17个品种。新增谈判抗肿瘤药物主要分布在消化系统、呼吸系统、头颈部系统及泌尿系统;新增自费抗肿瘤药物集中于呼吸系统、消化系统、血液系统和头颈部系统。其中泌尿系统肿瘤用药新增3个均纳入谈判,删除1个(安罗替尼)。除骨与软组织肿瘤系统用药,各系统均有新增药品(见表2)。

表2 2021年版《指导原则》较2020年版《指导原则》新增品种分布情况Tab 2 Guiding Principles for new variety distribution of 2020 and 2021 edition
2.3 新型抗肿瘤药物靶点检测情况
新型抗肿瘤药物中部分靶向药物须遵循靶点检测后方可使用的原则,不得在未做相关检查的情况下盲目用药[9]。历年《指导原则》中已明确需要检测靶点的药物,可分为小分子靶向药物和大分子单克隆抗体两大类。2018—2021年版《指导原则》中需检测靶点的药物从17个发展为40个,其中2021年《指导原则》中需检测靶点的小分子药物28个,大分子单抗12个。自2018年来,《指导原则》中新型抗肿瘤药物从EGFR、HER2、VEGFR传统靶点发展到作用于PD-L1、BRCA、ALK等新兴靶点[10]。部分药品可能具有多个靶点,不同病种的治疗需检测不同靶点,如帕博利珠单抗治疗食管癌和头颈部鳞状细胞癌需检测PD-L1,治疗结直肠癌时要求KRAS、NARA、BRAF均阴性方可使用(见表3)。

表3 2021年版《指导原则》中明确需靶点检测新型抗肿瘤药物Tab 3 Novel anti-tumor drugs with required in the Guiding Principles 2021 edition
2.4 常规医保目录中新型抗肿瘤药物及其适应证变化
截至2021年,共13个新型抗肿瘤药物陆续纳入常规医保目录,较前一年新增4个新型抗肿瘤药物,包括2个单克隆抗体以及2个蛋白激酶抑制剂,并将埃克替尼从医保常规目录中删除,纳入2021年协议期内谈判目录。常规医保目录新型抗肿瘤药物适应证可覆盖淋巴瘤、肺癌、胃肠间质瘤、肝细胞癌、肾细胞癌、白血病、骨髓瘤等多个瘤种,新纳入4个品种进一步扩大医保常规目录的覆盖适应证,如索拉非尼治疗甲状腺癌;但对于发病率较高的宫颈癌和膀胱癌目前暂无新型抗肿瘤药物被纳入医保支付限定条件中[5]。此外,部分新型抗肿瘤药物的医保支付适应证可覆盖多个瘤种,如贝伐珠单抗可覆盖结直肠癌、肺癌、胶质母细胞瘤、肝细胞癌;沙利度胺无适应证限制。对比《指导原则》适应证,常规医保限定支付适应证的范围扩大(见表4)。主要因为肿瘤药物治疗证据更新快,《指导原则》适应证仅参考药品说明书,存在一定滞后性。

表4 2021年版《指导原则》与常规医保目录中新型抗肿瘤药物适应证比较Tab 4 Indications of novel anti-tumor drugs in the Guiding Principles 2021 edition and the conventional medical insurance catalogues
2.5 协议期内谈判新型抗肿瘤药物及其适应证变化
不仅是常规医保目录中新型抗肿瘤药物临床应用范围不断扩增,对比往年协议期内谈判目录,2021年协议期内谈判目录共有48个新型抗肿瘤药物,相继有药品扩大医保支付适应证,其中包括:① 2020年,医保谈判增加伊布替尼和依维莫司支付适应证范围;② 2021年,医保谈判进一步增加6个药品的适应证,覆盖呼吸、消化道和生殖等系统(见表5)。这些得益于基因组学的进步,以及抗肿瘤药物作用靶点的发现和循证医学证据的不断更新。

表5 协议期内谈判目录新型抗肿瘤药物适应证变化Tab 5 Changes in indications for novel antitumor drugs in the negotiation catalogues
3 讨论
3.1 规范新型抗肿瘤药物的合理使用
为规范新型抗肿瘤药物临床应用,提高肿瘤治疗的合理用药水平,保障医疗质量和医疗安全,维护肿瘤患者健康权益,国家卫生健康委员会特制订了《指导原则》。《指导原则》规定抗肿瘤药物临床应用须遵循药品说明书,不能随意超适应证使用。临床实践中,发现具有高级别循证医学证据的新适应证及新用法用量在说明书中未体现,往往存在滞后情况。因此临床医师通常优先参考权威指南及高级别循证证据,导致现有的《指导原则》不能满足实际需求,增大了其在临床中推行的难度[11-12]。《指导原则》及时更新及开展合理超说明书用药工作尤为重要,一方面国家政策严格把控循证医学证据,另一方面综合分析瘤种治疗现状;另外,借助信息化手段是关键,例如前置审方系统,将该项管理工作真正落地,能从根本上规范临床抗肿瘤药物的超说明书使用,规范抗肿瘤药物使用安全性[13]。2020年版《指导原则》删除《管理办法》,新增“附表”指导发生不良反应时调整治疗方案,进一步规范抗肿瘤药物使用的安全性。
在《指导原则》落实中,要求临床药师要全面掌握其药品说明书外也应结合当前高级别循证医学,从用药合理性、用药安全性、用药教育、医嘱点评等参与新型抗肿瘤药物的合理使用中,为患者提供高质量的药学服务。
3.2 靶点检测纳入医保亟待推广,提升肿瘤治疗经济性
基因突变与抗肿瘤疗效直接相关,不同肿瘤患者对特定药物的敏感性和毒副反应的大小不同,通过检测特定靶点基因可指导肿瘤靶向用药,进而提高肿瘤靶向治疗的有效性和安全性,但另一方面也增加了肿瘤患者的治疗费用。2021年版《指导原则》共收入77个新型抗肿瘤药物,其中明确需基因检测的共计40个,占比51.95%。2021年版《指导原则》中共有61个新型抗肿瘤药物被纳入《医保目录》,其中需基因检测药品共31个,占比50.82%(注:如图1所示,在2021年,《指导原则》中新型抗肿瘤药品有13个纳入常规医保目录+48个纳入国谈目录,所以《医保目录》是61个新型抗肿瘤药物)。由于肿瘤患者的复发检测和耐药较为常见,若在治疗中出现耐药,往往需要多次检测,导致整体肿瘤基因检测总费用高。自2019年6月15日起,北京医耗联动综合改革正式实施,全市执行病理检测医疗保险新政策,首次将肿瘤基因检测纳入医保,报销比例高达90%[14]。目前,我国很多地区未将抗肿瘤靶向药物基因检测纳入医保范围,基因检测作为使用靶向药前的必经之路纳入医保需进一步推进,以减轻肿瘤患者的经济负担。
3.3 医保适应证覆盖范围扩大
《指导原则》中纳入医保目录的药品稳步增加,治疗覆盖范围不断扩大。以2021年版《医保目录》为准,国产君实生物的特瑞普利单抗、信达生物的信迪利单抗、恒瑞医药的卡瑞利珠单抗、百济神州的替雷利珠单抗这四款PD-L 1全部谈判成功纳入医保。这不仅激励我国药品创新,降低我国对进口药品的依赖,还极大减轻了肿瘤患者的经济负担[6]。目前《指导原则》和国谈抗肿瘤药物适应证均主要以肺癌、乳腺癌和淋巴瘤为主,而我国负担较重的甲状腺癌(索拉非尼)、鼻咽癌(特瑞普利单抗)仅有1个抗肿瘤药物被纳入,对于发病率较高的宫颈癌和膀胱癌,当前暂无新型抗肿瘤药物适应证被《指导原则》和《医保目录》收入,提示制订《指导原则》专家组在后续更新中关注缺乏抗肿瘤药物治疗的瘤种;与此同时,卫生行政部门应积极推动肿瘤药物的研发工作,满足不同瘤种的治疗需求[10,13,15]。很多国外指南推荐使用的创新抗肿瘤药物,因价格昂贵、不规范的使用途径以及可及性低,在我国不能及时用于临床治疗。对此,通过医保谈判,提高了抗肿瘤创新药可支付性和可及性,让更多癌症患者享受到了公平可及的医保资源。
3.4 进一步提高国谈新型抗肿瘤药物的可及性
自2017年国家人力资源和社会保障部牵头开展数轮国谈工作,国家陆续将临床疗效确切的新型抗肿瘤药物纳入医保范围或签订协议。截至2021年,《指导原则》共有48个新型抗肿瘤药物进入国谈医保目录,但因国家政策、医疗水平、市场需求,导致部分新型抗肿瘤药物的可及性较低[16]。为提高谈判新型抗肿瘤药物的可及性,需要不同监管部门共同探讨政策的兼容性;医院应及时积极落实、改进相关制度和操作流程(解除对医保谈判药品不配套的政策管制,如医院药占比考核;建立谈判药的审批绿色通道,将新型抗肿瘤药物纳入常规采购目录,保证临床供应,提高药物可及性)[17-18]。
4 总结
《指导原则》中新型抗肿瘤药物不断纳入医保常规目录和协议期谈判目录,不仅提高肿瘤治疗水平、改善抗肿瘤领域的合理用药问题,还大幅提升了医保对癌症患者的保障力度,让更多癌症患者享受公平可及的医保资源。在后续《指导原则》和《医保目录》更新中应关注我国发病率较高但缺乏药物治疗的肿瘤类型,相关研发部门、医疗机构应加强此类瘤种的研发工作以满足肿瘤治疗的需求。

