4899例住院患者注射用洛铂相关血小板减少临床特征及影响因素分析
张博,郭代红,高奥,郭海丽,伏安,李伯妍,王嘉熙,3(. 解放军总医院医疗保障中心药剂科,北京 00853;2. 解放军医学院,北京 00853;3. 重庆医科大学药学院,重庆 40006)
洛铂(lobaplatin)是具有自主知识产权的国家一类抗肿瘤药物,于2005年率先在我国上市,主要用于治疗乳腺癌、小细胞肺癌及慢性粒细胞性白血病;因具有较高的肝癌细胞敏感性,国内也推荐洛铂用于经导管动脉化疗栓塞术(transcatheter arterial chemoembolization,TACE)[1]。血液毒性是洛铂最主要的剂量相关性毒性,以血小板减少最为强烈。这与本团队前期基于药品不良反应(adverse drug reaction,ADR)自发报告数据挖掘得到洛铂在血管/出血及凝血疾病(血小板减少)具有较强风险信号的结果高度一致[2]。目前,国内外洛铂相关血小板减少研究多针对具体疾病或治疗方案开展,鲜有相关大样本真实世界研究(real world study,RWS)结果。
鉴于此,本课题组借助团队自主研发的“医疗机构药物不良事件主动监测与智能评估警示系统(adverse drug event active surveillance and assessment system,ADE-ASAS)”[3-5]开展了相关研究。该系统对接医院信息系统(hospital information system,HIS),自2012年使用以来,经过多年持续完善、拓展、实践,目前已完成涉及百万例次用药人群的自动监测研究。本研究提取2012年至2019年期间住院患者使用注射用洛铂的真实世界数据(real world data,RWD),计算洛铂相关血小板减少的发生率并探究其临床特征及影响因素,以期为临床用药提供参考。
1 资料与方法
1.1 资料来源
利用ADE-ASAS对本院某医学中心使用注射用洛铂(10 mg)的住院患者进行回顾监测研究。考虑到2019年末开始流行的新型冠状病毒感染(coronavirus disease 2019,COVID-19)[6]的影响,结合本院HIS中病例数据的实际情况,监测时间选取为2012年1月1日至2019年12月31日。
1.2 研究方法
纳入目标时间内使用注射用洛铂(10 mg)且年龄在18岁及以上的住院患者,排除相关指标缺失及罹患血液疾病者,得到目标人群4899例,用药10 756例次。参照美国卫生与公众服务部(U.S.department of health and human services,HHS)2017年11月发布的《不良事件通用术语标准》(common terminology criteria for adverse events,CTCAE)5.0版[7]相关内容,将血小板计数<100×109·L-1定义为血小板减少,得到报警病例555例次,以75×109·L-1、50×109·L-1、25×109·L-1为节点将血小板减少程度由轻至重分为1~4级。根据《药品不良反应术语使用指南》中的关联性评价标准,分别由两名临床药师对报警病例进行独立人工甄别,结果不一致者提请相关领域专家评审以确定阳性病例。最终得到评价结果为“肯定”“很可能”“可能”的病例360例,并将其纳入病例组。其余4539例用于对照组病例的选取。
结合文献调研及本院HIS数据实际,收集的变量主要有患者年龄、性别、民族、吸烟史、饮酒史、体质量指数(body mass index,BMI)、入院次数、住院天数、科室、肿瘤类型、肿瘤转移情况、输血史、既往洛铂用药史、洛铂给药剂量、既往病史(病毒性肝炎、高血压、心脏病、糖尿病)、部分风险合并用药(吉西他滨、氟尿嘧啶、丝裂霉素、吡柔比星、表柔比星、羟喜树碱、亚叶酸钙等)、部分实验室检查(血小板、血红蛋白)结果以及病例组ADR发生时间等。其中,罹患肿瘤类型参考美国国家综合癌症网络(national comprehensive cancer network,NCCN)发布的相关肿瘤临床实践指南;以用药前7 d至用药后2 h内最近一次实验室检查结果为基值。
1.3 统计学处理
采用倾向性评分法(propensity score matching,PSM)平衡患者性别、年龄等因素,1∶1匹配选取对照组,匹配容差为0.1。病例组及对照组基线信息录入使用Microsoft Excel 2019,PSM匹配及数据统计分析采用SPSS Statistics 26.0和R软件。符合或近似符合正态分布的计量变量用均数±标准差表示,组间差异性统计分析采用t检验;偏态分布的计量变量用中位数和四分位数范围表示,组间差异性统计分析采用Mann-Whitney U检验。计数变量用率或构成比表示,组间差异性统计分析采用卡方检验。相关影响因素分析采用单因素和多因素Logistic回归模型,将单因素Logistic回归模型分析结果中P<0.1的变量纳入多因素Logistic回归模型,以P<0.05为差异有统计学意义。
2 结果
2.1 用药人群概况
使用注射用洛铂的住院患者共计4899例,用药10 756例次。其中,男性3060例(62.46%),女性1839例(37.54%);患者年龄为(57±10.96)岁,63.11%(3092例)集中在45~64岁;具体分布见表1。患者BMI为(24.08±9.09)kg·m-2,发生肿瘤转移者1570例(32.05%),单次洛铂给药中位剂量为40(20~50)mg。

表1 4899例注射用洛铂用药患者性别、年龄分布Tab 1 Gender and age distribution of 4899 inpatients receiving lobaplatin injection
2.2 病例组与对照组基线特征
科室分布方面,注射用洛铂相关血小板减少病例组患者主要集中在介入放射科(310例,86.11%),对照组患者在放射治疗科(123例,34.17%)、介入放射科(108例,30.00%)等均有分布;其余涉及科室有肿瘤科、介入超声科、妇产科、普通外科、耳鼻咽喉科、消化科、骨科、肝胆外科等。肿瘤类型方面,两组患者均罹患消化系统肿瘤最多,病例组329例(91.39%),其中肝癌301例;对照组209例(58.06%)。其余涉及肿瘤类型有呼吸系统肿瘤、妇科肿瘤、头颈部肿瘤、乳腺癌、体表肿瘤、骨与软组织肉瘤、泌尿生殖系统肿瘤等,具体见表2。
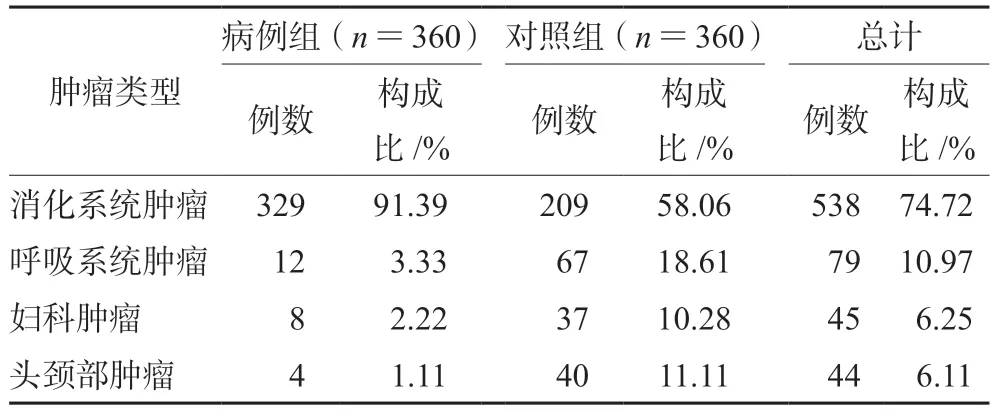
表2 注射用洛铂相关血小板减少病例组与对照组主要肿瘤类型分布Tab 2 Distribution of major tumor types in the case group and the control group of thrombocytopenia associated with lobaplatin injection
病例组中,351例(97.50%)ADR发生于给药7 d内,其中以给药第4日为最多(215例,59.72%)。ADR发生程度方面,血小板减少1级283例(78.61%)、2级74例(20.56%)、3级2例(0.56%)、4级1例(0.27%)。
本研究采用PSM平衡患者年龄、性别等因素,得到病例组与对照组在这两个因素上差异均无统计学意义;而两组患者在入院次数、住院天数、肿瘤转移、既往洛铂用药史、单次洛铂给药剂量≥40 mg、既往病毒性肝炎病史、既往糖尿病史、合并用药、血小板基值、血红蛋白基值等方面差异有统计学意义,具体见表3。
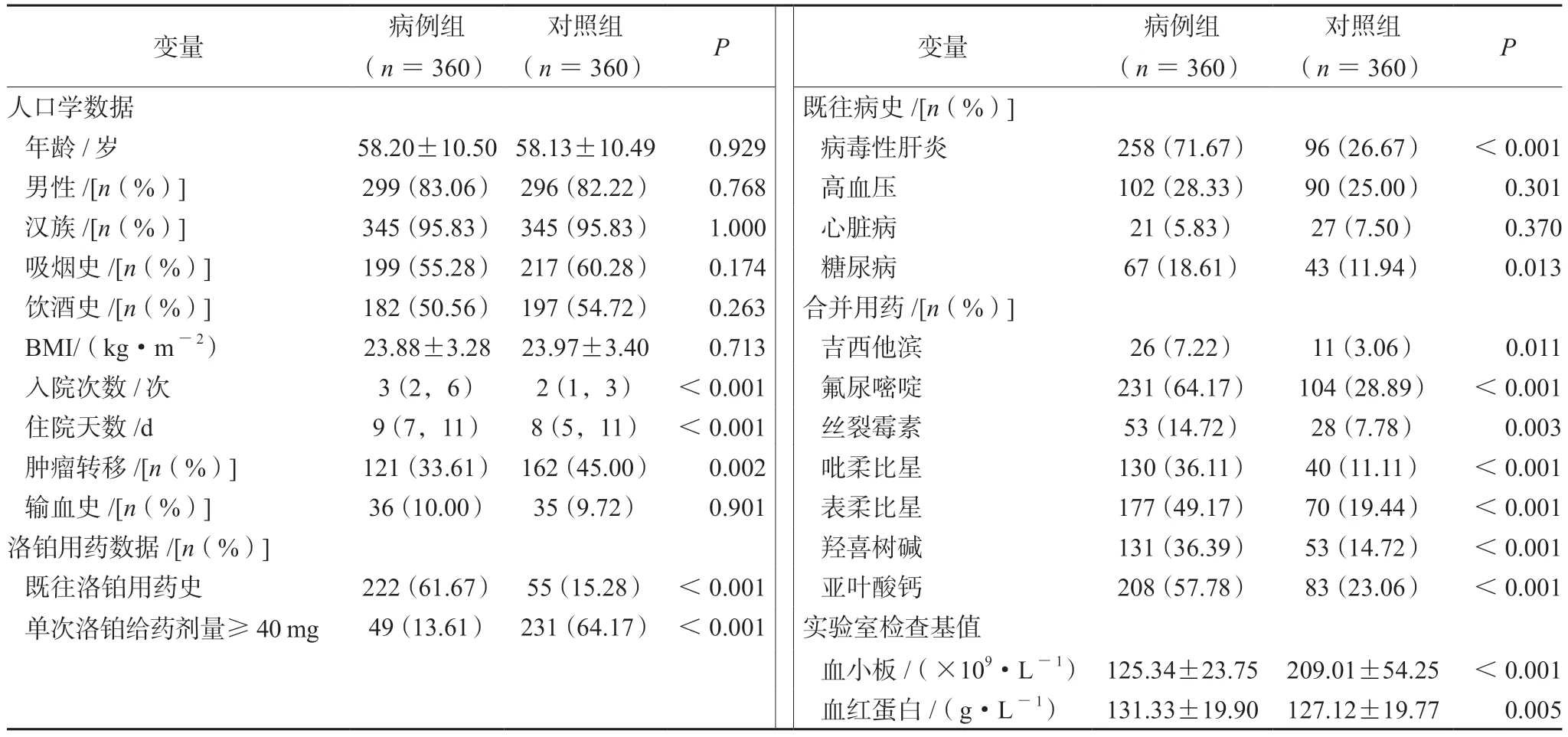
表3 注射用洛铂相关血小板减少病例组与对照组基线特征Tab 3 Baseline characteristics of thrombocytopenia associated with lobaplatin injection case group and control group
2.3 注射用洛铂相关血小板减少影响因素概况
本研究采用Logistic回归模型分析注射用洛铂相关血小板减少的影响因素,其中,单因素Logistic回归模型分析结果显示,相关影响因素包括肿瘤转移、既往洛铂用药史、单次洛铂给药剂量≥40 mg、既往病毒性肝炎病史、既往糖尿病史、合并用药、血小板基值和贫血,具体见表4;将上述因素全部纳入多因素Logistic回归模型,最终得到的影响因素有既往洛铂用药史、合并吡柔比星、血小板基值,具体见表5。
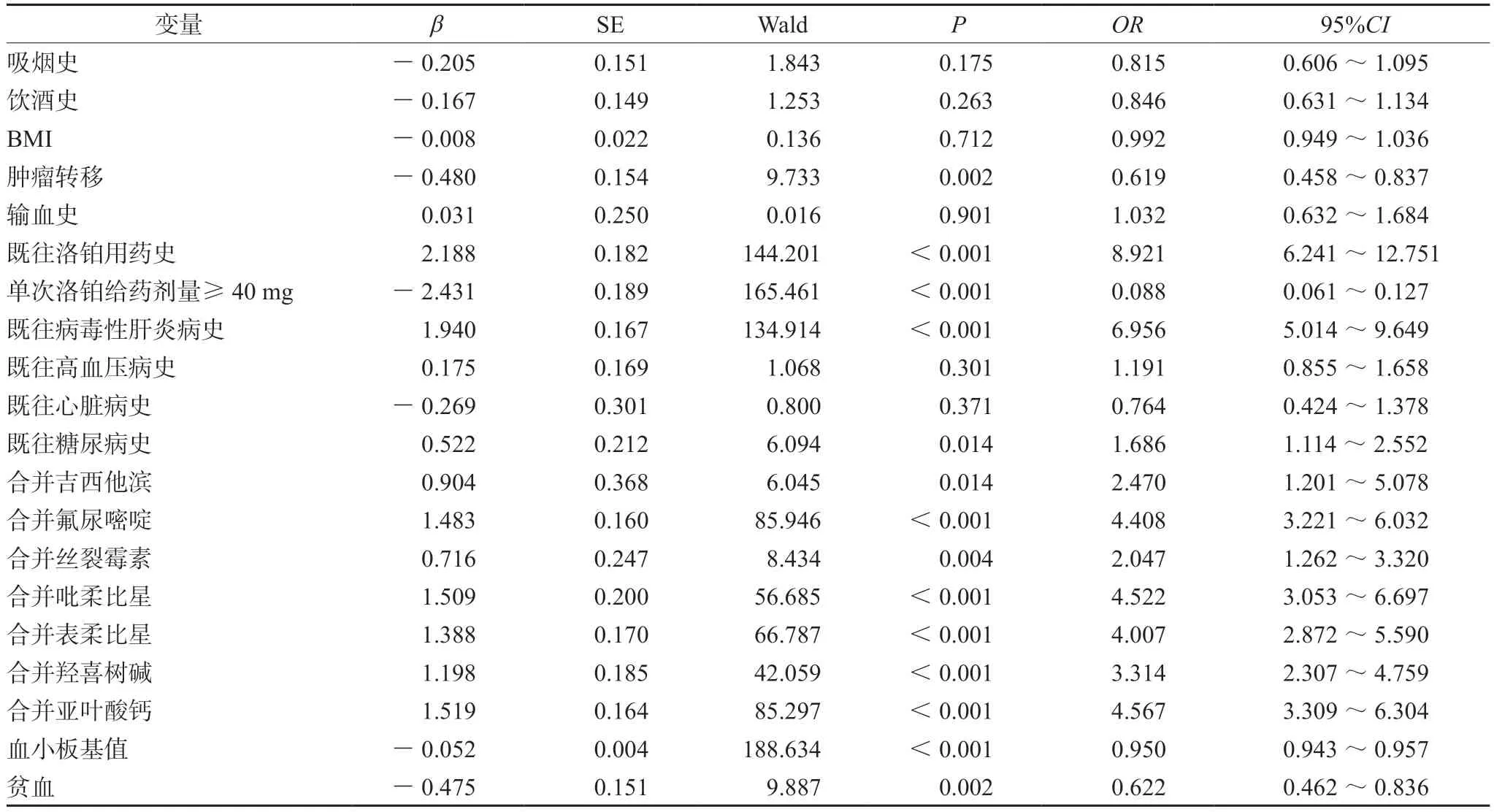
表4 注射用洛铂相关血小板减少单因素Logistic回归模型分析结果Tab 4 Single-way Logistic regression model for thrombocytopenia associated with lobaplatin injection

表5 注射用洛铂相关血小板减少多因素Logistic回归模型分析结果Tab 5 Multivariate Logistic regression model for thrombocytopenia associated with lobaplatin injection
3 讨论
3.1 注射用洛铂相关血小板减少临床特征分析
本研究结果显示,在4899例患者中,360例血小板减少与注射用洛铂的使用存在关联性,发生率为7.35%,属常见的ADR。这一数据低于其说明书记载的26.90%(实体瘤患者,3级以上)和75.00%(大剂量化疗后的卵巢癌患者,未分级),也低于国内相关专家共识[8]中报道的发生率(70.00%)。参照CTCAE 5.0作血小板减少程度分组,得到1~4级的发生率分别为5.78%、1.51%、0.04%、0.02%。一项使用洛铂治疗原发性肝癌的TACE后血小板减少症的回顾性研究结果显示,轻度(对应1级)、中度(对应2级)、重度(对应3~4级)的血小板减少发生率分别为16.50%、10.47%和4.88%[9],与本研究结果存在差异,可能是由于纳入的研究对象不同,本研究纳入了所有注射用洛铂的用药患者而非仅肝癌患者。鉴于本研究中病例组肝癌患者的占比高达83.61%,同时考虑到洛铂在TACE中的应用[1],后续可进一步针对性地开展肝癌人群使用洛铂相关血小板减少的研究。在ADR发生时间方面,说明书报道血小板计数降低常在用药后2周开始,但本研究351例(97.50%)ADR却发生于给药1周内,其中以第4日为最多(215例,59.72%)。一方面,本院对于洛铂用药患者的血小板监测较为密切,能够较早地发现目标ADR;另一方面,病例组患者住院中位时间为9(7,11)d,低于说明书中2周的血小板减少潜伏期,以致患者出院后血小板计数的变化难以被监测,这或许也是本研究得到的ADR发生率较既往报道偏低的原因之一。此外,本研究中病例组血小板基值为(125.34±23.75)×109·L-1,用药后易降至100×109·L-1以下而引发ADE-ASAS报警。多因素Logistic模型分析结果也提示较低的血小板基值与ADR发生增多存在关联关系(OR:0.955;95%CI:0.947~0.962),与既往同类研究[10-11]报道基本一致。
3.2 注射用洛铂相关血小板减少风险因素分析
多因素Logistic回归模型分析结果显示,既往洛铂用药史为血小板减少的风险因素(OR:2.967;95%CI:1.676~5.250)。鉴于其说明书记载用药2周后才发生ADR,因而考虑病例组部分患者血小板减少可能是上一次使用注射用洛铂的结果,这也在一定程度上造成了病例组血小板基值普遍偏低的状况。而患者前一次用药并非都在本院,具体情况较难判定,可能对相关结果产生一定偏倚影响,这也是本研究的局限性之一。因此,临床可对使用过注射用洛铂患者的血小板计数作持续监测,若发现其有降低趋势,再次用药需谨慎,以规避ADR的发生。这也提示开展血小板计数变化趋势研究[12]具有重要意义,后续将在此方向作深入探讨,或可得到更具参考价值的结果。本研究得到的另一风险因素为合并使用吡柔比星(OR:3.634;95%CI:1.355~9.750)。作为蒽环类抗肿瘤抗菌药物的一种,吡柔比星的骨髓抑制ADR较为常见[13]。另有研究表明,与吡柔比星同属抗肿瘤抗菌药物的丝裂霉素是药物诱导的血栓性微血管病(drug-induced thrombotic microangiopathie,DITMA)的可能诱因,而血小板减少正是DITMA的典型临床表现[14]。因此,临床使用注射用洛铂时应警惕联用抗肿瘤、抗菌药物特别是蒽环类药物的潜在风险,密切关注患者血小板计数变化,必要时可输注血小板或预防性应用促血小板生长因子[15],以纠正血小板减少。
综上,本研究基于ADE-ASAS血小板模块,开展了注射用洛铂相关血小板减少的大样本用药人群真实世界研究,高效经济地获取了注射用洛铂相关血小板减少的发生率并分析得到了相关影响因素。研究结果提示临床使用注射用洛铂应重点关注既往有洛铂用药史的患者,加强血小板计数监测;同时应避免抗肿瘤、抗菌药物特别是蒽环类药物如吡柔比星的联用,从而降低血小板减少的发生风险。

