响应曲面法优化蛇纹石负载羟基磷灰石去除矿区地下水氟铁锰研究
李喜林 ,杨雯雯 ,周天然 ,王文菊 ,刘 玲 ,张 龙 ,高佳佳 ,刘思源
(辽宁工程技术大学 土木工程学院, 辽宁 阜新 123000)
0 引 言
矿山开采、人类活动造成地下水污染加剧,这对于以地下水作为主要饮用水源的煤矿区和广大农村地区造成了不小的影响,其中以地下水高氟、高铁锰的问题尤为突出[1]。长期摄入含氟地下水,会导致脑损伤以及甲状腺疾病[2];人体摄入过多的铁和锰会损伤脏器和神经系统,对人体造成不可逆的危害[3]。因此,研究矿区地下水氟、铁和锰同步去除技术具有重要意义。
目前,国内外对单独去除氟、铁、锰离子的研究很多[4-5]。其中,吸附法以效果好、成本低和对环境污染较小等优点,成为近年来除氟去铁锰的首选方法。天然矿物价格低廉、化学稳定性好,在水处理研究中得到了不同程度的应用,如沸石[6]、海泡石[7]、电气石[8]、羟基磷灰石(HAP)[9]、蒙脱石[10]等。HAP是一种天然的磷灰石矿物,20 世纪初,日本学者SUZUKI 等[11]首次将HAP 作为吸附材料处理Cd2+、Zn2+、Ni2+等污染废水,发现HAP 对金属阳离子具有良好的吸附能力。而后有大量学者开展了HAP 对F-、重金属离子吸附去除过程和能力研究[12-13]。但HAP 易团聚,不易与水分离,并且制备需在碱性环境下完成水解反应,需消耗大量的氨水,成本高。蛇纹石(Srp)作为一种有前景的天然吸附剂,对单独除氟,吸附重金属离子有很好的效果,同时Srp 也是良好的载体,但单独使用存在碱度释放,出水pH 较高的问题[14-15]。在此基础上,课题组[16]前期研发了蛇纹石负载羟基磷灰石(Srp/HAP)复合吸附剂,该吸附剂既具备Srp 片状卷曲结构,又解决了HAP 团聚问题,可作为矿区处理含F-、Fe2+、Mn2+地下水的优良吸附剂。
响应优化法(RSM)是一种通过少量试验即可得到试验因子之间最佳组合的一种数学统计分析方法,既包含单个因素,又包含因素之间交互作用对试验结果影响。近年来,许多学者利用RSM 对吸附剂的制备条件以及工艺运行参数等进行了优化研究[17]。但在以往的研究中,大多侧重于研究对单一离子去除条件的优化,而很少有对多种离子同步去除条件的优化研究,将间歇试验和RSM 应用于复合吸附剂处理含F-、Fe2+、Mn2+地下水的吸附影响研究,国内外未见报道。
因此,笔者在课题组前期吸附剂制备基础上,为更进一步探究不同影响因素之间的交互作用对F-、Fe2+、Mn2+的吸附性能的影响,采用响应面设计优化工艺条件,建立了投加量、反应时间、pH 值的预测模型,为Srp/HAP 处理含F-、Fe2+、Mn2+地下水提供参考依据。
1 材料与方法
1.1 试验材料
Srp/HAP 复合颗粒制备:按固液比为20%称取120 目(粒径0.125 mm)的蛇纹石(蛇纹石取自中国辽宁省营口市大石桥后仙峪硼矿区)均匀分散在0.5 mol/L 的Ca(NO3)2溶液中,搅拌6 h 后将1 mol/L 磷酸溶液(控制Ca/P 物质的量之比为1.67)缓慢滴入溶液中形成凝胶。陈化20 h后滴加氨水调节pH 至11,再陈化24 h,抽滤,洗涤后滤饼在烘箱(GZX-9246MBE)中90 ℃烘干72 h 成干凝胶。然后将该凝胶置于马弗炉(SX2-2.5-10A)中,400 ℃煅烧60 min 后,通过120 目筛磨碎,加入2%糊化的醚化淀粉,制成3~5 mm的颗粒,经180 ℃下煅烧90 min后制备成Srp/HAP 复合颗粒吸附剂。
复合水样模拟辽宁地区地下水水质,以氟化钠、硫酸亚铁、硫酸锰进行配制,各离子质量浓度分别为F-为5 mg/L、Fe2+为20 mg/L、Mn2+为5 mg/L,pH控制为6.1。
1.2 试验方法
间歇试验:取150 mL 复合试验水样置于锥形瓶中,分别进行了投加量(50~800 mg)、反应时间(30~210 min)及pH(2~9)为因子的间歇试验,反应后分别测定F-、Fe2+、Mn2+浓度和pH 值。
中心复合设计(CCD)与响应面优化试验:CCD是RSM 常用的优化设计方法之一,是基于5 水平的试验设计方法,可以将因素与结果进行非线性的评估,从而对双向交互作用进行更好的预估[18]。选取投加量、反应时间、pH 值作为响应因素,分别以X1、X2、X3表示。以间歇试验确定的最优条件为基准水平,确定试验因素水平见表1。以复合水样中的F-、Fe2+、Mn2+去除率为响应值,以此构建响应面进行研究。
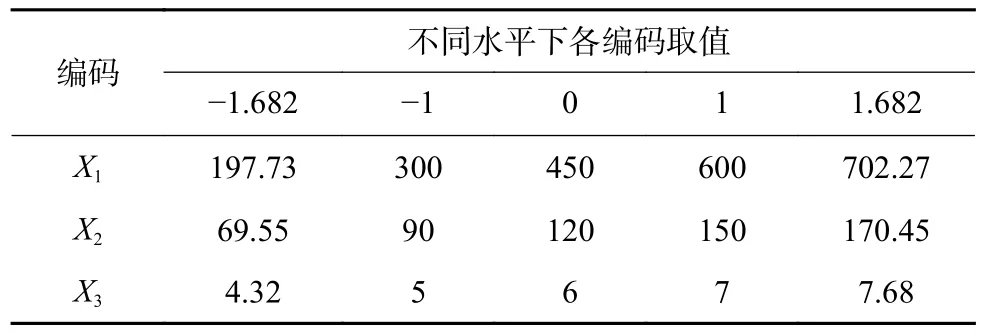
表1 CCD 实验因素水平下编码取值Table 1 Coding value under the level of CCD experimental factor
模型表达式如下:
其中:y为响应值;b0、bi、bii、bij分别为常数、线性参数、二阶参数以及交互参数。
Srp/HAP 解吸再生试验:采用0.1 mol/L Na2CO3和0.1 mol/L HNO3对污染后的Srp/HAP 吸附剂进行再生试验,评价其可重复使用性。首先,采用间歇式试验对已经吸附过F-、Fe2+和Mn2+的Srp/HAP 颗粒进行解吸,将Srp/HAP 颗粒经吸附过滤后从处理介质中分离,用去离子水去除未被吸附的F-,Fe2+和Mn2+。将Srp/HAP 颗粒加入0.1 mol/L Na2CO3溶液中,在35 ℃、150 r/min 的条件下摇匀150 min,进行脱附。随后,用去离子水清洗Srp/HAP 颗粒,除去表面的Na2CO3。将Srp/HAP 颗粒再次加入0.1 mol/L HNO3溶液中,在35 ℃、150 r/min 的条件下搅拌150 min 后,用去离子水清洗,去除表面的HNO3。最后,在110 ℃下干燥2 h,重复吸附-解吸循环试验5 次,测量并记录过程中的F-、Fe2+、Mn2+浓度。
1.3 检测方法
F-:氟离子分光光度法(HJ 488-2009);Fe2+、Mn2+:原子分光光度法;pH:PHS-3C 型精密pH 计测定。
2 结果与讨论
2.1 吸附影响因素
2.1.1 投加量对吸附性能的影响
向150 mL 的复合水样中分别加入不同质量的Srp/HAP,调节pH 为6.5,在120 r/min、25 ℃的恒温振荡摇床中振荡120 min 后分别测定水样pH 值及F-、Fe2+、Mn2+浓度,结果如图1a 所示。
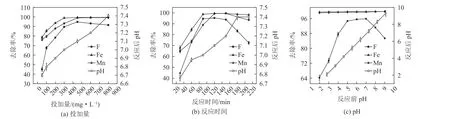
图1 反应条件对Srp/HAP 吸附水中F-、Fe2+、Mn2+的效果影响Fig.1 Effect of reaction conditions on the adsorption of F-、Fe2+ and Mn2+ in water by Srp/HAP
由图1a 可以看出,当投加量从50 mg 增加到450 mg 时,F-的去除率从45.3%增至94.8%,Fe2+的去除率从78.6%增至99.4%,Mn2+的去除率从76.28%增至99.2%,这是因为Srp/HAP 具有片状卷曲的结构,比表面积较大,投加量越多,对F-、Fe2+、Mn2+的吸附能力越强。当投加量继续增加,F-的去除率降低,Fe2+、Mn2+的去除率基本保持稳定。这是由于当Srp/HAP 的投加量继续增大,使得水样中的OH-含量升高,pH 值变大,且OH-与F-由于静电斥力的影响,竞争Srp/HAP 表面的活性位点,对F-的去除效果造成影响,使得F-的去除率呈先上升后下降的趋势,这与卢承龙采用高岭石对氟进行吸附得出的结果一致[19]。由上可知,Srp/HAP 的最佳投加量为450 mg/150 mL 水样(计3 g/L)。
2.1.2 反应时间对吸附性能的影响
向150 mL 的复合水样中加入450 mg 的Srp/HAP复合颗粒,调节pH 为6.5,在120 r/min、25 ℃的恒温振荡摇床中振荡不同时间后分别测定pH 值以及F-、Fe2+、Mn2+浓度,结果如图1b 所示。
如图1b 可知,随着反应时间的延长,pH 值逐渐升高。当反应时间为120 min 时,Srp/HAP 对F-的去除率达到最大为95.3%,随着反应继续进行,F-的去除率逐渐下降;在反应进行到150 min 时,Fe2+、Mn2+的去除率达到最大为99.5%、99.6%,当反应时间超过150 min 后Fe2+、Mn2+的去除率呈缓慢下降的趋势。这是由于在反应初期,Srp/HAP 与溶液中的F-、Fe2+、Mn2+未完全接触,布朗运动不剧烈,导致吸附反应不完全,去除率较低,随着反应时间增大,布朗运动增强,去除率逐渐升高,当吸附剂达到饱和状态时,吸附剂之间产生的碰撞摩擦使得离子脱附,导致去除率有所下降[20]。综合分析,选择最佳反应时间为120 min,此时,Srp/HAP 对水样中F-、Fe2+、Mn2+的去除率分别达到95.3%、99.5%、99.3%。
2.1.3 pH 值对吸附性能的影响
向150 mL 的复合水样中加入450 mg 的Srp/HAP,调节不同pH 值,在120 r/min、25 ℃的恒温振荡摇床中均匀振荡120 min 后分别测定pH 值以及F-、Fe2+、Mn2+浓度,结果如图1c 所示。
如图1c 所示,随着pH 的升高,Fe2+、Mn2+的去除率呈缓慢升高的趋势。pH 为5 到9 时,Fe2+、Mn2+的去除率保持在99.8%左右,水中的OH-会导致Fe2+、Mn2+沉淀,可以促进Srp/HAP 对Fe2+、Mn2+的吸附作用[21];pH 对F-的去除率呈现先升高再下降的趋势,当pH 值在5~7 时,F-的去除率稳定在94.7%~95.9%,当pH 大于7,水中含有大量的OH-,使得F-的去除率呈下降的趋势。综上,确定有效pH值反应区间为5~7,结合研究区域地下水质特性,最终确定最佳反应pH 为6,此时Srp/HAP 对水样中F-、Fe2+、Mn2+的去除率分别达到95.6%、99.7%、99.5%。
2.2 响应曲面优化设计
2.2.1 模型的建立及其显著性检验
在反应温度25 ℃,转速120 r/min 条件下,根据间歇试验结果确定投加量、反应时间和pH 值三因素水平取值范围,优化其对F-、Fe2+、Mn2+去除率的影响,并依据CCD 试验原理,利用Design Expert 软件对试验数据进行拟合,共设计20 组试验,结果见表2。
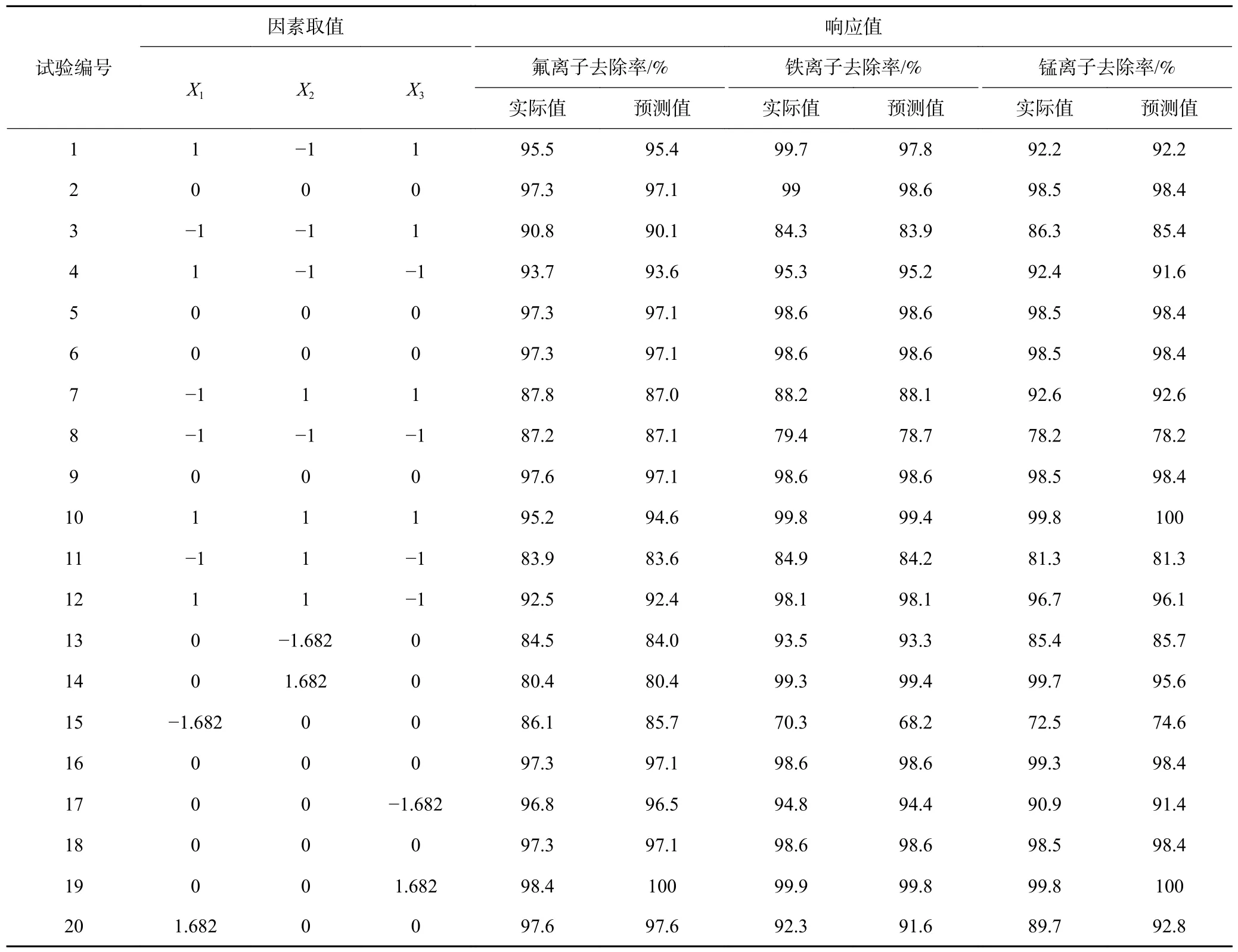
表2 Srp/HAP 响应面试验设计及结果Table 2 Srp/HAP response surface test design and results
依据表2,建立二次多项式回归模型,得到以Srp/HAP 投加量(X1)、反应时间(X2)、pH(X3)为自变量,以Y1:氟离子(F-)去除率、Y2:铁离子(Fe2+)去除率、Y3:锰离子(Mn2+)去除率为响应值的三元二次回归方程。
方差分析结果见表3,模型的相关系数R12=0.992 0、R22=0.998 9、R32=0.990 9,表明响应面拟合较好;校正决定系数R1adj2=0.984 8、R2adj2=0.997 9、R3adj2=0.982 7,表明此模型可分别解释98.48%,99.79%,98.27%的响应值变化。由响应面模型二次多项式的方差分析结果可知,模型的F值分别为137.48、1 007.68、120.65,P值均小于0.000 1,说明该模型可信度高且显著。模型失拟项的F值为64.81、9.44、20.07,P值均小于0.000 1,说明响应面模型的误差小,拟合程度好。
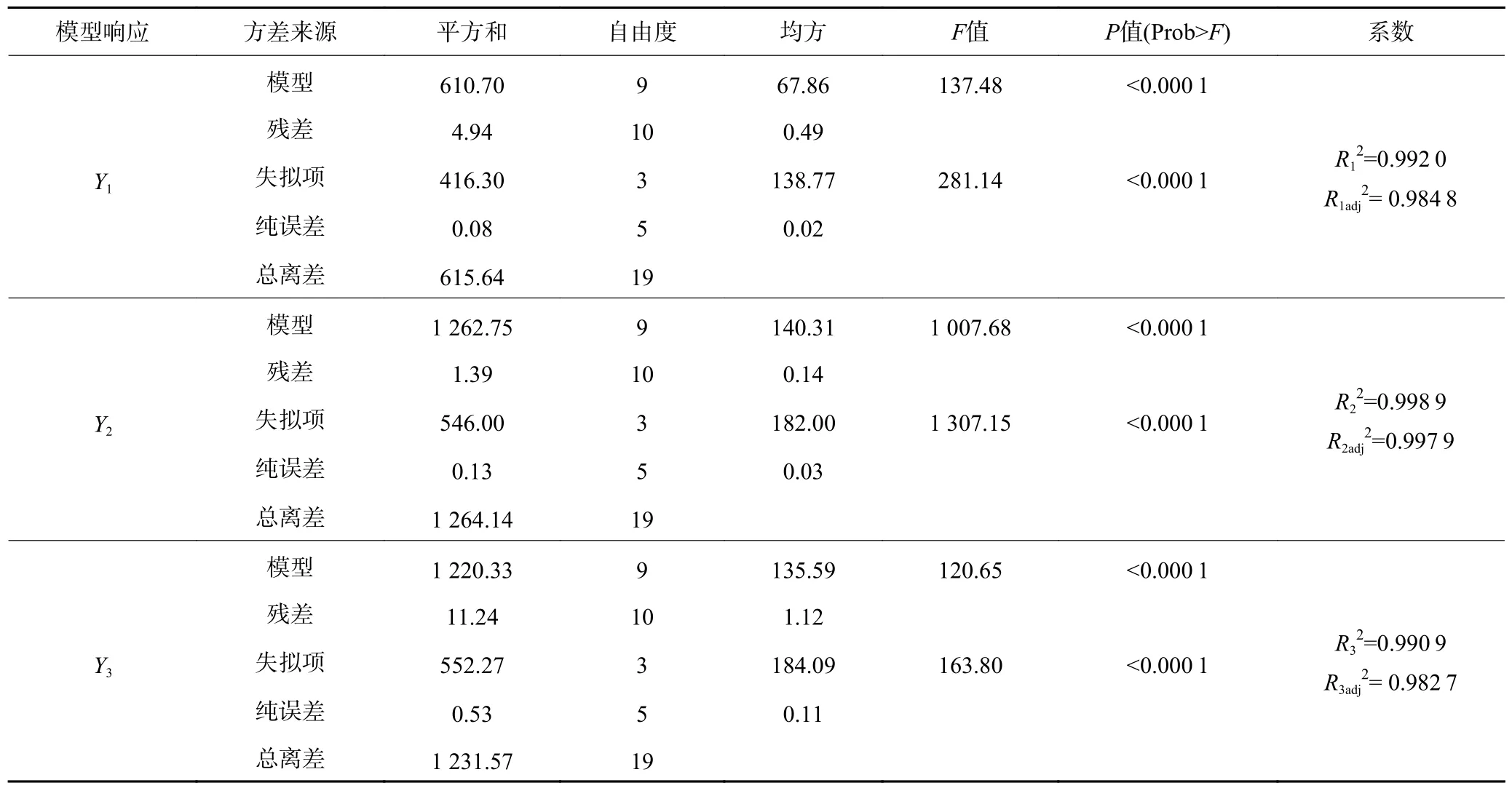
表3 二次多项式的方差分析Table 3 Analysis of variance of quadratic polynomials
2.2.2 响应曲面分析与优化
1)投加量与反应时间的交互作用。图2 显示了pH 值在中心条件下(pH=6),Srp/HAP投加量与反应时间的交互作用对F-、Fe2+、Mn2+去除率的影响。

图2 投加量与反应时间对F-、Fe2+、Mn2+去除率影响的响应结果Fig.2 Response results of the effects of dosage and reaction time on removal rates of F-, Fe2+ and Mn2+
在固定投加量为300~600 mg 内的任意值时,Srp/HAP 对试验水样中F-的去除率随反应时间的延长而呈现出先增大后减小的趋势(图2a);Fe2+的去除率随反应时间的延长而缓慢增大,后趋于稳定(图2b),这是由于Srp/HAP 去除Fe2+的吸附反应是迅速的,当达到吸附饱和时,Fe2+的去除率随反应时间的延长而稳定;图2c 中Mn2+的去除率随反应时间的延长而缓慢增大。当固定反应时间为90~150 min 内的任意值时,F-的去除率随投加量的增加而增大,在反应时间为102~138 min 时去除最为明显;Fe2+、Mn2+的去除率均随投加量的增大而增加。由于图2a,2b,2c 中响应面的曲率均较大,因此Srp/HAP 的投加量与反应时间相互作用对F-、Fe2+、Mn2+去除率影响显著。
2)投加量与pH 值的交互作用。图3 显示了反应时间在中心条件下(反应时间为120 min),Srp/HAP 投加量与pH 值的交互作用对F-、Fe2+、Mn2+去除率的影响。

图3 投加量与pH 值对F-、Fe2+、Mn2+去除率影响的响应结果Fig.3 Response results of dosage and pH on the removal rate of F-, Fe2+ and Mn2+
由图3 可知,在固定投加量为300~600 mg 内的任意值时,Srp/HAP 对试验水样中F-、Fe2+、Mn2+的去除率均随pH 值的升高而缓慢增加,说明在试验条件范围内,Srp/HAP 受地下水pH 值变化影响较小。在固定pH 值为5~7 内的任意值时,增加Srp/HAP的投加量,F-的去除率逐渐提高,Fe2+、Mn2+的去除率先增大后趋于稳定。为达到相同的除氟效果,在pH值较低的条件下,需增加Srp/HAP 的用量。从响应面图的陡峭程度可知,Srp/HAP 投加量与pH 值的相互作用对Fe2+、Mn2+去除率的影响大于对F-去除率的影响。由于图3a 的响应面较平整,图3b、3c 响应面曲率较大,因此两者交互作用对F-去除率影响不显著,对Fe2+、Mn2+去除率影响显著。
3)反应时间与pH 值的交互作用。图4 显示了投加量在中心条件下(投加量为450 mg),反应时间与pH 值的交互作用对F-、Fe2+、Mn2+去除率的影响。
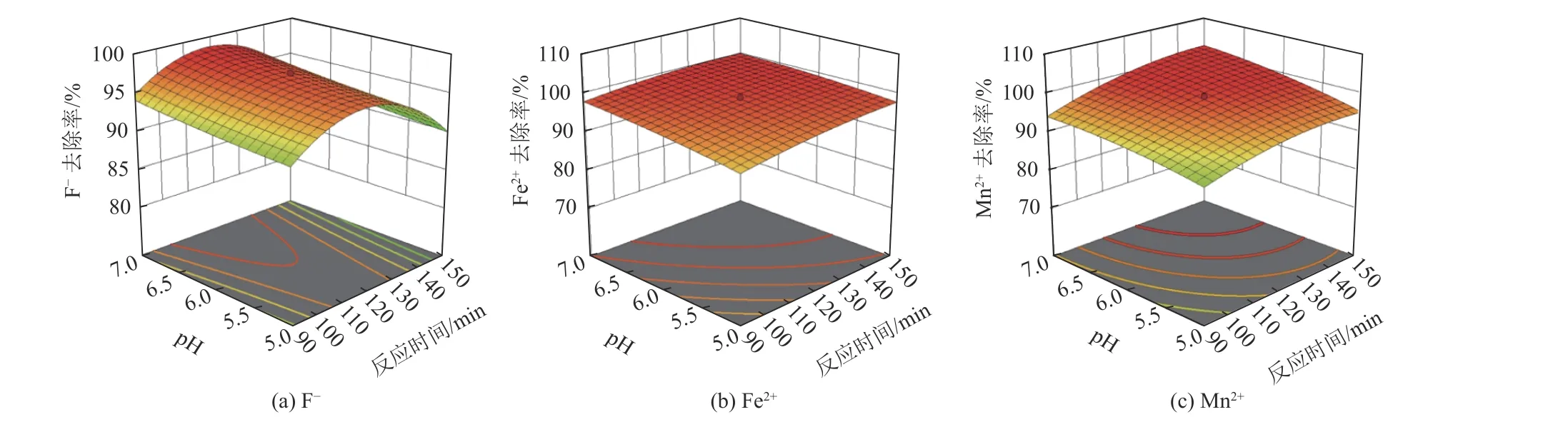
图4 反应时间与pH 值对F-、Fe2+、Mn2+去除率影响的响应结果Fig.4 Response results of reaction time and pH on removal rates of F-, Fe2+ and Mn2+
如图4 所示,在固定pH 值为5~7 内的任意值时,当反应时间逐渐延长,Srp/HAP 对F-的去除率先增加后减小,这是由于随反应时间的增加,当Srp/HAP 对F-的吸附达到饱和后,在恒温振荡条件下发生脱附现象,使其对F-的去除率降低;而Fe2+、Mn2+的去除率则随Srp/HAP 投加量及pH 值的升高而基本保持稳定。在固定反应时间为90~150 min内的任意值时,F-的去除率随pH 值的增大而逐渐下降;Fe2+、Mn2+的去除率随pH 值升高而增大。从响应面图的陡峭程度可知,反应时间与pH 值的相互作用对F-去除率的影响最大,对Mn2+去除率的影响次之,对Fe2+的去除率影响最小。综上,二者交互作用对F-去除率影响显著,对Fe2+、Mn2+去除率影响不显著。
2.2.3 模型验证
在选取的试验因素水平范围内,对响应值最大值进行优化,得到Srp/HAP 处理试验水样的最佳试验条件,即投加量为545.40 mg/150 mL 水样(计3.64 g/L),反应时间为120.47 min,pH 值为6.3,此时F-、Fe2+、Mn2+去除率的预测值分别为99.8%、100%、100%。
为验证结果的可靠性对优化结果进行3 次平行试验,验证结果显示F-、Fe2+、Mn2+平均去除率分别为98.23%、99.9%、99.7%,出水满足《生活饮用水卫生标准》(GB 5749—2006)的要求。预测值与试验值的绝对误差均小于5%,证明试验模型真实且可靠。
2.3 Srp/HAP 的解吸和再生
如图5 所示,随着再生循环次数的增加,Srp/HAP 对F-、Fe2+和Mn2+的去除率逐渐降低。与循环0 相比,5 次再生后F-、Fe2+、Mn2+的去除率分别从98.23%、99.9%、99.7%降为82.1%、89.4%、84.3%(损失率分别为16.13%、10.5%、15.4%,小于20%),表明Srp/HAP 具有良好的再生能力[22]。Srp/HAP 去除效果下降可能与再生过程中吸附剂表面官能团的减少和解吸不完全有关,因为长期洗脱可能会破坏结合位点,或者洗脱不充分可能会在吸附剂中留下吸附离子。结果表明,Srp/HAP 具有良好的可重复使用性,可作为地下水处理的有效吸附材料。
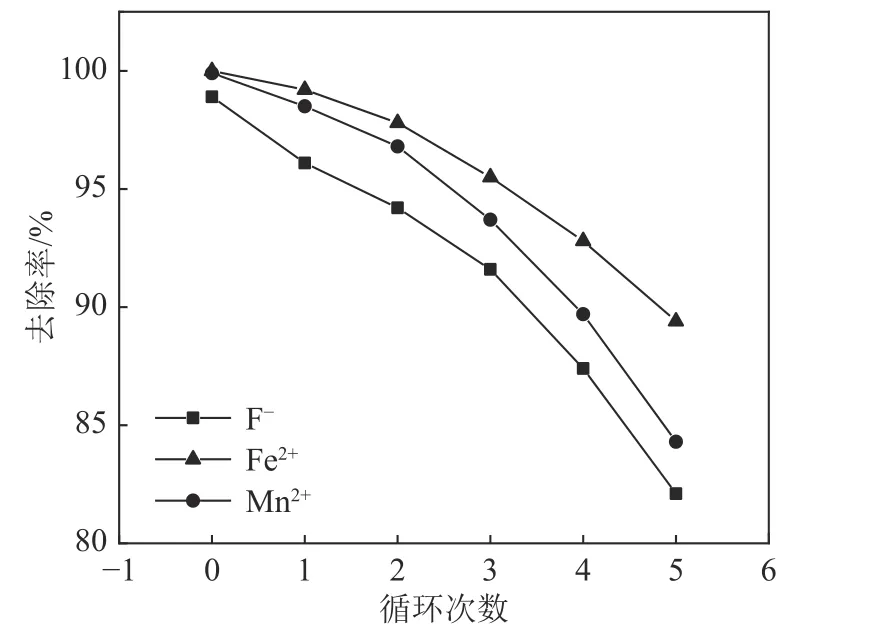
图5 0.1 mol/L Na2CO3 和0.1 mol/L HNO3 对Srp/HAP 的再生Fig.5 Srp /HAP regeneration induced by 0.1 mol/L Na2CO3 and 0.1 mol/L HNO3
3 结 论
1)合成的Srp/HAP 复合吸附剂对F-、Fe2+、Mn2+具有良好的吸附性能,在间歇试验的基础上,建立二阶响应模型并通过试验验证,确定了Srp/HAP去除水样中F-、Fe2+、Mn2+的最优试验条件为:投加量为3.64 g/L,反应时间为120.47 min,pH 值为6.3,此时F-、Fe2+、Mn2+去除率分别为98.23%、99.9%、99.7%,达到《生活饮用水卫生标准》的要求。响应面试验设计较好地拟合了Srp/HAP 对F-、Fe2+和Mn2+的吸附过程,且预测值与试验值的绝对误差均低于5%,证实模型可靠。
2)Srp/HAP 复合颗粒具有较好的再生能力,5 次再生后F-、Fe2+、Mn2+的吸附能力分别降低16.13%、10.5%、15.4%,小于20%,具有良好的可重复使用性,可作为处理含F-、Fe2+、Mn2+矿区地下水的有效吸附材料。

