单剂量舒芬太尼给药在HIV感染者行椎管内麻醉的药代动力学实验①
界中平,张雪松,俞立奇,王 利,李 扬
(1.上海市宝山区吴淞中心医院麻醉科,上海 宝山 200940;2.上海市(复旦大学附属)公共卫生临床中心麻醉科,上海 金山 201540)
舒芬太尼作为芬太尼的衍生物,由于其起效快,镇痛效果作用时间长,清除半衰期较短,对围手术期血压波动较小,并能抑制气管插管刺激,因此较广泛应用于现在外科手术中[1]。HIV(human immunodeficiency virus)感染者是指由机体感染HIV病毒导致其全身免疫功能缺陷,又称获得性免疫缺陷综合征(acquired immunodeficiency syndrome , AIDS)[2],前期动物实验研究表明HIV抗病毒药物利托那韦对舒芬太尼的代谢有较大影响,可延长其清除率及半衰期[3]。此外相关临床研究指出抗HIV病毒药物可以延长芬太尼血药浓度及半衰期,而目前尚未有相关研究表明长期服抗HIV药物的感染者其在接受手术时舒芬太尼血药动力学变化,本研究通过应用液相色谱一质谱法聚焦HIV感染者在行椎管内麻醉时舒芬太尼的血药动力学变化,对临床上针对HIV感染者在接受外科手术治疗时为其舒芬太尼用药的临床麻醉及术后疼痛治疗提供参考依据。
1 资料与方法
1.1 一般资料
2019-02~2020-02本院行腹部外科手术HIV感染者(HIV组)40例,未感染者(正常组)40例。 按照美国麻醉师协会(ASA)分为Ⅰ或Ⅱ级[4],年龄20~48岁的青壮年,未合并心血管、呼吸系统疾病,肝肾功能代偿期以上,未合并其他重大肿瘤。HIV感染者指规律性服用抗HIV药物超过6个月,并排除肥胖、非代偿性甲状腺功能减退和2个月内继续服用成瘾性药物及禁忌使用该药物的患者。所有患者均经复旦大学附属上海公共卫生中心伦理委员会审查和批准并签署知情同意书。
1.2 麻醉与监测方法
患者进入手术室后在基本生命体征监测下,吸氧并建立外周静脉通路后嘱患者行左侧卧位,穿刺间隙选择腰2~3水平,见脑脊液缓慢流出后向头端注入等比重布比卡因12.5mg,注药时间为15~20s,测麻醉平面达到胸8~10水平主诉无明显不适,快速静注舒芬太尼(宜昌人福药业有限公司,批号:1150315,规格50μg/mL)0.3μg/kg, 麻醉手术期间监测无创动脉血压、心率、心电图、脉搏氧饱和度、开放上肢静脉输注乳酸钠林格液。
1.2.1 舒芬太尼给药方法与血样采集
将3μg舒芬太尼注射液以10mL的生理盐水进行稀释,在椎管内麻醉后以0.3μg·kg-1剂量单次静脉给药,以秒表计时保证5秒内注射完毕。静脉注射后分别以1,3,5,10,20,30,60,120,240,360min,从桡动脉采血5mL放置于含有肝素化试管中,1200r/min离心10min后,移液器抽取1mL血浆放置无菌EP管中,-80℃深低温冰箱保存。
1.2.2 血药浓度测定方法与血浆标本的处理
本次实验中血浆舒芬太尼测定采用液相色谱一质谱联法,现简述如下:收集血浆1mL,4℃溶解后取血浆200μL,移置EP管中加入内标10μL混匀,再加入乙腈400μL,将其涡旋混匀静置5min,以12000r/min离心10min,取上清液200μL置于样品瓶,上样量为50μL。
1.3 方法学考察与评价
方法回收率为(101.70±1.20)%,线性范围为0.1~50ng/mL,最低检测限为0.1ng/mL, 日间与日内精密度分别为2.21%和2.03%。精确度为32.7%,摆动度为29.8%,室温稳定性及冻融稳定性良好。上述研究结果表明该方法可满足临床药代动力学。
根据不同时间点的血浆舒芬太尼浓度,以血浆白蛋白浓度计算血液稀释度并对血药浓度进行校正后,用3P97药理学程序计算药代动力学参数。
1.4 统计学方法
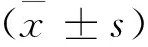
2 结果
2.1 一般情况
两组患者性别构成比、年龄、体质量、手术时间、出血量的比较,差异均无统计学意义(P>0.05),见表1。
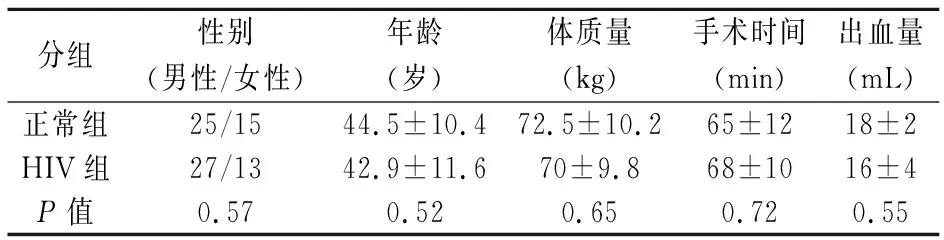
表1 正常者与HIV感染者临床情况的比较
2.2 血药浓度与时间曲线
两组受试者在注射舒芬太尼1min后,血药浓度均达峰值。血药浓度-时间衰减曲线符合三指数函数方程:正常组(Control组)为Cp(t)=10.84925e(-0.0191t)+1.8e(-0.0028t)+0.28e(-0.0031t),HIV组为Cp(t)=14.59672e(-0.0141t)+3.8e(-0.0048t)+3.25e(-0.0021t)。用药后60 min,在正常组和HIV组患者的血药浓度,分别由14和16μg·L-1下降至0.28和0.35μg·L-1,约有98%的舒芬太尼在血浆中已经清除。HIV组患者,血浆舒芬太尼浓度在给药后至60min的血药浓度,两组间差异有统计学意义(**P<0.01或*P<0.05),见图1。
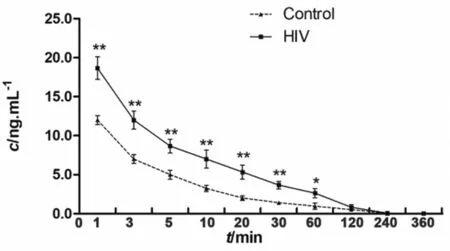
图1 芬太尼单次静脉注射后血药浓度一时间曲线
2.3 药代动力学参数
两组患者的主要药代动力学参数舒芬太尼缓慢分布半衰期(T1/2a),排除半衰期(T1/2β),药物从中央室消除(K10),药物从中央室到周边室(K12)以及周边室到中央室(K21)的转运时间,药物在中心室分布面积均无明显差异性(P>0.05)显著性。而两组患者之间的药物浓度-时间曲线下面积(AUC)以及药物清除率(CL)均有明显差异性(P<0.01)。

表2 两组舒芬太尼的体内代谢情况比较
3 讨论
本研究表明,舒芬太尼在HIV感染者中药代动力学特征符合三室开放模型。给予单次同等剂量的舒芬太尼后,HIV感染者的血药浓度高于正常者(P<0.05);给药60 min后,两组间无显著性差异。而两者相比较而言,AUC及CL有明显统计学差异(P<0.05),提示HIV组清除率显著下降,这可能与HIV感染者长期服用抗逆转录药物有关。此外本研究为了消除混杂因素导致舒芬太尼药代学评价失误,统一采用单一的椎管内麻醉技术,相对于全身麻醉,对心血管循环系统影响较小,能较好反应舒芬太尼在长时间服用抗HIV药物患者体内的代谢情况。
由于蛋白酶抑制剂类作为HIV抗病毒药物其毒副作用小及不易产生耐药,临床上针对HIV感染者目前常规口服蛋白酶抑制剂类药物[5]。其作用机制为抵抗HVI-1蛋白酶作用下的功能蛋白生成,避免病毒成熟,将病毒迅速从体内消除出去[6],临床上常用蛋白酶药物为那韦类[7],在我们收集的40例HIV感染者病例当中,均口服那韦类药物并且常规超过6个月。以往的研究表明那韦类药物主要经过一类存在人体肝脏及肠道细胞内质网中的单加氧酶即细胞色素P450超家族(cytochrome P450 proteins,CYP)所代谢[8]。近期研究表明在代谢过程中,那韦类药物在同样经过相同的 CYP 酶代谢、或者对 CYP 酶产生抑制或诱导作用,因此可导致相同代谢途径消除的药物发生药物相互作用[9]。HIV感染者的抗病毒治疗是一个长期服药的过程,在此过程中感染者由于获得其他疾病或者自身并发症等,使得在临床上与不同的药物同时应用的现象很普遍[10]。本院作为上海市定点HIV感染者的收治医院,其麻醉科承载了大量HIV感染者的手术治疗,其接受手术治疗者均需要静脉注射舒芬太尼缓解其术中及术后疼痛。而国内外关于 HIV 感染者的舒芬太尼药代动力学研究报道较少,服用抗HIV病毒药物组芬太尼的18h的血药浓度和未服用组的输入芬太尼后4h的血药浓度基本持平,抗HIV药物增加了67%的血浆浓度,把芬太尼的半衰期从(9.4±4.6)h增加到(20.1±8.4)h[11]。而麻醉医师对于 HIV 感染者使用舒芬太尼的用量知之甚少,只能经验性给药。我们之前的动物实验研究表明抗HIV蛋白酶抑制剂药物利托那韦可提升舒芬太尼在家兔体内的分布,延长舒芬太尼滞留时间。本研究发现相对于正常组,HIV组中中心分布面积(Vc)及清除率(CL)显著降低,药物浓度-时间曲线下面积(AUC)显著增高,提示口服HIV药物可以延长体内舒芬太尼的降解,导致部分其降解受到抑制。因此,针对HIV感染者,单次舒芬太尼给药浓度较常规正常者用药剂量较少。
由此,本研究得出临床上应该特别注意HIV感染者临床麻醉要考虑到合理用药问题,尤其是镇痛药舒芬太尼与抗蛋白酶抑制剂那韦类联合用药问题,结合HIV感染者的生理状况如血压、心率以及服药时间、剂量等设计联合用药方案,提高围手术期治疗安全。有条件者可以进行血药浓度监测,以期获得更为理想的联合用药方案。

