生脉散对2 型糖尿病模型大鼠糖脂代谢和肠道菌群的影响
丘文龙,彭瑜威,杨心怡,谭晓君,张雪杨,赵文昌,吴都督,卢洪梅,刘小柳,阮永队*,陈稚*(.广东医科大学药学院,广东东莞 5808;.广东医科大学附属东莞第一医院,广东东莞 570;.中国深圳市深圳罗湖人民医院医学实验室,广东深圳 5800)
2 型糖尿病(T2DM)是危害人类健康的重大疾病,其病死率在肿瘤、心血管之后居第三位,是目前备受全球关注的公众卫生问题。在我国T2DM 的患病率高达11.6%,T2DM 的防治已成为研究热点[1-2]。目前T2DM 的发病机制较为复杂,但普遍认为胰岛素抵抗是T2DM 的主要发病机制。而肠道菌群与糖尿病的发生、发展密切相关,肠道菌群在胰岛素抵抗的发生、发展过程中发挥了至关重要的作用[3-6]。因此,靶向调控肠道菌群及其代谢产物,调节肠道菌群的稳态,被认为是治疗T2DM 的有效手段。
另外,在中医理论中,糖尿病属于“消渴病”范畴,是以气阴虚弱为本,燥热炽盛为标的一种慢性发展性疾病。不少研究表明,生脉散能有效改善胰岛素抵抗,明显改善T2DM 患者的临床症状和体征[7-9]。目前生脉散改善胰岛素抵抗的作用机制并未明了,本研究将从肠道微生态的角度探讨生脉散调节糖脂代谢治疗 T2DM 的可能作用机制,旨在为其临床应用提供理论和实验依据。
1 材料和方法
1.1 材料
1.1.1 动物 选择SD 大鼠70 只,雄性,SPF 级,身体质量(100.0±10.0)g,由广东医科大学院动物实验中心提供,许可证号码SCXK(粤)2013-0008。所有动物均在无病原体的环境中饲养并随意喂食。照顾和使用动物的程序得到广东医科大学动物中心伦理委员会的批准,并遵守了有关动物道德使用的所有适用的机构和政府法规。
1.1.2 药物与试剂 受试药物:生脉散,药物组成按照普通高等教育中医药类规划教材 《方剂学 》第五版所载 : 人参、麦冬、五味子按3∶3∶2 比例组成,本实验中取人参9 g、麦冬9 g、五味子6 g,以上药物麦冬和五味子以10 倍量水煎煮1.5 h 后,人参10 倍水另煎1.5 h 后滤出药液和其余药物药液混合、过滤,浓缩至0.5 g/mL。用药剂量依据2015 年版《中华人民共和国药典》,根据人和动物体表面积折算的等效剂量比率表计算,用药总量为200 mg/kg,将该剂量设为中剂量,低、中、高剂量分别为50.0、200.0、400.0 mg/kg。对照药物:(1)盐酸二甲双胍,250 mg/片,河北天成药业有限公司,国药准字H20031134,按照临床常用剂量换算后给动物灌服,剂量为4.0 mg/kg;(2)辛伐他汀,20 mg/片,浙江京新药业股份有限公司,国药准字H20000009,按照临床常用剂量换算后给动物灌服,剂量为0.32 mg/kg。采用葡萄糖氧化酶测定试剂盒、胰岛素放免试剂盒、大鼠胰岛素试剂盒、DNA 提取试剂盒(美国Cayman 试剂公司)、链脲佐菌素(STZ,美国Sigma 公司)。
1.1.3 主要仪器 AUW120D 电子分析天平,Shimadzu 公司,日本;DYCP-24DN 电泳仪,北京六一仪器厂,中国;TQ8040 气相色谱-质谱仪,日本岛津公司;MiSeq PE300 高通量测序平台,美国Illumina 公司。ABI 9700 逆转录PCR 仪,ABI 公司,美国;PikoReal荧光定量PCR 仪,Thermo Scientific 公司,美国;iMark 酶标仪:美国Bio-Rad 公司。
1.2 造模与分组
大鼠饲养于广东医科大学院动物实验中心,室内温度(25±2)℃,湿度50%~70%,采用12 h∶12 h 昼夜间断照明,每天给予换水1 次,定量添加饲料1 次,并及时更换垫料次,动物自由饮水进食,维持饲料由广东医科大学动物实验中心提供,进行适应性喂养1 周后,按随机区组法分为正常组10 只,造模组60 只。造模组用高糖高脂饲料(猪油∶蔗糖∶奶粉∶鸡蛋∶常规饲料=10∶20∶4∶3∶63)持续喂养8 周并结合腹腔注射30 mg/kg 链脲佐菌素诱导大鼠制备成糖尿病模型,正常组动物腹腔注射等剂量的生理盐水作为对照。
1.3 干预方法
选取造模成功的实验性糖尿病大鼠随机分组,共分为正常组、模型组、二甲双胍组(4.0 mg/kg)、辛伐他汀组(0.32 mg/kg)、生脉散低剂量组(50.0 mg/kg,L-SMS)、生脉散中剂量组(200.0 mg/kg,M-SMS)和生脉散高剂量组(400.0 mg/kg,H-SMS),每组10 只。给药组每日上午定时灌胃给药,模型组和正常组用等剂量(1 mL/100 g)的生理盐水灌胃,连续6 周,期间配合普通饲料喂养。
1.4 检测指标与方法
1.4.1 血清FBG、FINS、HbAlc 的检测 所有动物在取标本前均禁食并自由饮水,禁食12 h 后,采用剪尾法从尾静脉末梢取血0.2 mL 收集于干燥试管中,3 000 r/ min 离心15 min 后,取血清用于检测。检测药物干预后的空腹血糖(FBG)、空腹胰岛素(FINS)及糖化血红蛋白(HbAlc)的水平,其中FBG 使用葡萄糖氧化酶试剂盒检测,FINS 采用胰岛素放免试剂盒检测,血清中HbAlc 使用相关试剂盒进行检测。
1.4.2 血脂水平的检测 测量完小鼠空腹血糖后,从小鼠眼球部取血,取血后采用颈椎脱臼方法处死小鼠。全血室温静置3 h,以3 000 r/min 离心15 min,缓慢轻柔吸取上层血清样品,利用试剂盒及酶标仪分析血清中总胆固醇(TC)、甘油三酯(TG)、高密度脂蛋白胆固醇(HDL-C)、低密度脂蛋白胆固醇(LDL-C)的水平。
1.4.3 DNA 提取和测序 采用DNA 提取试剂盒提取各组小鼠结肠及盲肠内容物中的微生物总DNA。对样品进行 PCR 扩增、产物纯化、文库制备与库检及 Miseq 上机测序。利用 overlap 将双端数据进行拼接,并进行质控、嵌合体过滤,获得高质量的有效数据。由于序列数量庞大,本试验对最终获得的有效数据进行 97% 的相似度聚类,为降低假阳性率,会过滤 singleton 序列,获得最终的 OTU 丰度及代表序列,进一步进行多样性分析、主坐标分析分析(principal coordinates analysis,PCoA)及微生物菌属组成差异分析等。
1.4.4 短链脂肪酸含量的测定 从收集的粪便中取0.1 g 置于2 mL 离心管中,加500 μL 的饱和氯化钠溶液,在冰浴条件下用打碎机打碎均匀,再加20 μL 10% H2SO4溶液,混合器振荡混匀,到通风橱中加 500 μL 无水乙醚,混合器振荡混匀,14 000 r/min 离心15 min,取上清液置于装有0.25 g 无水硫酸钠的2 mL离心管中,再以同样的条件离心,取上清液置于气相瓶中待测。
1.5 统计学处理
应用SPSS 26.0 软件进行统计学处理,计量资料以均数± 标准差表示,采用单因素方差分析及LSD-t检验。P<0.05 为差异有统计学意义。
2 结果
2.1 生脉散对大鼠血糖的影响
与正常组比较,模型组大鼠的FBG、FINS、HbAlc水平显著升高(P<0.01);与模型组比较,生脉散不同剂量组的FBG、FINS、HbAlc 水平均降低(P<0.01 或0.05),且其降糖作用随剂量增加而增加,尤其是生脉散高剂量组,其效果与二甲双胍组接近,提示生脉散可降低胰岛素抵抗大鼠的血糖水平。见表1。
表1 生脉散对大鼠血糖的影响(,n=10)

表1 生脉散对大鼠血糖的影响(,n=10)
与正常组比较:aP<0.01;与模型组比较:bP<0.01,cP<0.05;与二甲双胍组比较:dP<0.01;与生脉散低剂量组比较:eP<0.01,fP<0.05
2.2 生脉散对大鼠血脂水平的影响
与正常组相比,模型组大鼠的模型组TC、TG、LDL-C 水平升高(P<0.01),HDL-C 水平降低(P<0.01);与模型组比较,辛伐他汀组和生脉散不同剂量组的TC、TG、LDL-C 水平降低,HDL-C 水平升高(P<0.01或0.05);尤其是生脉散高剂量组,其降脂效果与辛伐他汀组基本一致,提示生脉散能够改善高脂饮食诱导的小鼠血脂紊乱的现象。见表2。
表2 生脉散对大鼠血脂的影响(,n=10)

表2 生脉散对大鼠血脂的影响(,n=10)
与正常组比较:aP<0.01;与模型组比较:bP<0.01,cP<0.05;与辛伐他汀组比较:dP<0.01,eP<0.05;与生脉散低剂量组比较:fP<0.01,gP<0.05
2.3 生脉散对大鼠肠道菌群多样性及组成的影响
正常组、模型组、生脉散低剂量组和生脉散高剂量组分别观测到1 034、755、894 和971 个特有OTU数。与正常组比较,模型组的OTUs 数下降;而在大鼠接受不同剂量的生脉散后,OUTs 数目较模型组有一定程度提高。这表明生脉散有利于肠道菌群的恢复,丰富肠道菌群数。见图1。

图1 大鼠肠道菌群OTUs 分布的Venn 图
Alpha 多样性主要与种类数目和多样性相关,即丰富度和均匀性。菌群丰富度主要包括 Chao1 指数,而菌群均匀性主要包括Shannon 和Simpson 指数。与正常组相比,模型组的 Shannon 以及 Chao1 指数均降低(P<0.01),而生脉散组与模型组相比,能有效升高Chao1、Shannon 与Simpson 指数(P<0.01)。上述结果表明,生脉散可以有效防止糖尿病大鼠的肠道微生物群丰富度及多样性的降低。见表3。
表3 生脉散对大鼠肠道菌群Alpha 多样性的-影响(,n=10)

表3 生脉散对大鼠肠道菌群Alpha 多样性的-影响(,n=10)
与正常组比较:aP<0.01;与模型组比较:bP<0.01
为比较微生物群落之间的差异,计算了β 多样性并进行主成分分析(principal co-ordinates analysis,PCoA),其结果如图2 所示。从图2 可见,横坐标和纵坐标成分的贡献率分别是45.39%和13.28%,提示分组关系较好。而各组(正常组、模型组、生脉散低剂量组和生脉散高剂量组)样本点区别明显,其中生脉散低剂量组和生脉散高剂量组与正常组样本点距离小于模型组和正常组间的距离,说明生脉散干预后的菌群结构有向正常组的菌群结构模式调节的趋势。

图2 大鼠肠道菌群β 多样性的PCoA 图
为进一步评估肠道微生物群的组成变化,进行了门水平的分类学分析。在门水平上,与正常组比较,模型组肠道菌群中放线菌门和变形菌门丰度升高,厚壁菌门和拟杆菌门丰度降低(P<0.01)。而与模型组相比,生脉散组使厚壁菌门、拟杆菌门和疣微菌门丰度升高,放线菌门和变形菌门丰度降低(P<0.01 或0.05)。这表明生脉散可在一定程度上改善糖尿病大鼠体内肠道菌群紊乱的状态,诱导其肠道微生物组成恢复成正常大鼠状态。见表4。
表4 生脉散对大鼠肠道菌群基于门水平的物种构成影响(,n=10,%)

表4 生脉散对大鼠肠道菌群基于门水平的物种构成影响(,n=10,%)
与正常组比较:aP<0.01;与模型组比较:bP<0.01,cP<0.05
2.4 生脉散对大鼠粪便中短链脂肪酸含量的影响
采用高效液相色谱法,考察了生脉散对大鼠粪便中SCFAs 含量的影响。结果发现,经灌胃高剂量生脉散后,大鼠粪便中的水分含量高于正常组,表明生脉散可能具有一定的润肠通便的功能;另外,大鼠粪便中SCFAs 的含量较正常组和模型组均有增加,表明生脉散能有效促进大鼠肠道内产SCFAs 细菌的增殖,增加SCFAs 的产生量。见表5。
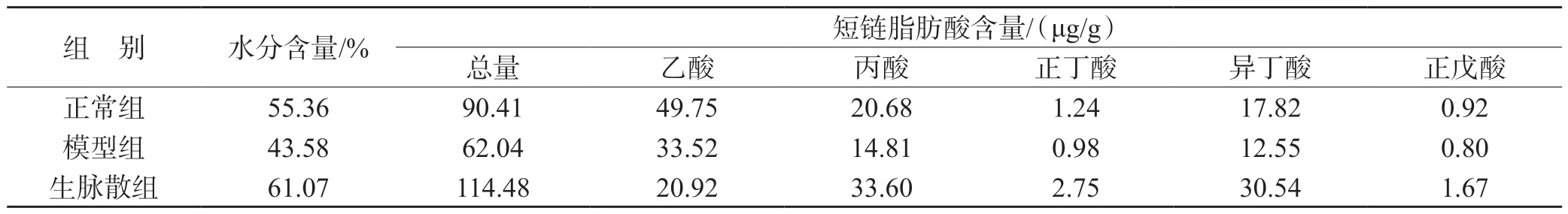
表5 生脉散对大鼠粪便中SCFAs 含量的影响
3 讨论
随着人们生活方式尤其是饮食习惯的变化,使得诸如冠心病和糖尿病之类的慢性代谢性疾病发病率增加[10]。糖尿病是由于体内胰岛素分泌缺陷而引发的以高血糖为特征的代谢性疾病,其中90%以上患者为T2DM。而胰岛素抵抗被认为是造成T2DM 的主要病理基础和发病机制。近年来,中药复方因具有多成分、多靶点、毒性低、价格低、整体调节糖代谢、改善胰岛素抵抗的作用而成为了研究热点[11-13]。且临床研究已证明,生脉散对糖尿病及其并发症有良好的防治作用[14]。本研究以传统的中药为切入口,使用生脉散对T2DM模型大鼠进行治疗,从肠道微生态的角度探讨生脉散调节糖脂代谢治疗 T2DM 的可能作用机制。
本实验结果显示,生脉散可以降低T2DM 模型大鼠的血糖以及HbAlc 水平,也可以调节血脂水平。同时通过16SrDNA 高通量测序法研究肠道微生物,大鼠肠道菌群的OTUs 分布结果显示,与正常组比较,模型组肠道菌群Chao1、Shannon、Simpson 指数均降低,表明模型组的肠道菌群丰度、多样性均有降低;而生脉散低剂量与高剂量组中,Chao1、Shannon、Simpson指数明显回调,提示生脉散对肠道菌群结构的多样性有显著改善且效果良好。此外,β 多样性的PCoA 图显示,生脉散低剂量和高剂量组之间相互聚拢,表明生脉散低、高剂量这两组在相应的维度上菌群群落组成相似;而且生脉散低、高剂量两组有向正常组靠近的趋势,提示大鼠肠道菌群的结构组成,在生脉散的干预下可以在一定程度上往正常大鼠菌群的结构组成回调。
此外,据文献报道在T2DM 患者肠道内,厚壁菌门与拟杆菌门的比值与血糖水平呈正相关,而且这两门菌群也是影响能量代谢平衡的主要群落[15-18]。因此我们在门水平上评估了肠道微生物的群落变化,结果显示,与正常组比较,模型组的肠道菌群中放线菌门和变形菌门丰度明显增加,拟杆菌门降低。作为肠道微生态失调的潜在生物标志物,变形菌门相对丰度增加与体内代谢紊乱有关联,这一结果证实了模型组大鼠体内出现了肠道菌群失调[19]。经生脉散干预后,厚壁菌门、拟杆菌门和疣微菌门丰度升高,变形菌门丰度降低,说明生脉散对T2DM 大鼠肠道菌群有一定改善作用。最后,本实验还考察了大鼠粪便中SCFAs 含量。SCFAs 主要包括乙酸、丙酸和丁酸,丙酸是拟杆菌门发酵的主要产物,可抑制胆固醇合成,丁酸是厚壁菌门发酵的主产物,可维持肠道内环境稳定[20]。本研究结果显示,模型组大鼠的SCFAs 含量较正常组少,而生脉散组SCFAs 含量显著回调且高于正常组,表明生脉散可使产SCFAs 的菌群丰度增加。
综上,生脉散能显著调节T2DM 模型大鼠的血糖、HbAlc 和血脂水平,且能增加肠道厚壁菌门、拟杆菌门和疣微菌门的丰度,降低变形菌门的丰度,生脉散改善糖脂代谢的机制可能与调节体内肠道菌群的结构密切相关。

