核心素养导向下的高考化学试题特点及教学启示
赖增荣 林红梁|福建省上杭县第一中学
一、核心素养导向下的高考化学试题特点分析
核心素养导向是《中国高考评价体系》提倡的重要理念,高考中的学科核心素养包括学习掌握、思维方法和实践探索3 个一级指标。其中,思维方法是高考化学试题核心素养考查的关键内容之一。《中国高考评价体系》将思维方法划分为3 个二级指标,包括科学思维、人文思维和创新思维[1]。而高考化学试题中所考查的化学思维方法,则包括宏观辨识与微观探析、变化观念与平衡思想、证据推理与模型认知三个方面[2]。下面,笔者以2022年全国理综乙卷第26题第(1)小题为例,说明基于思维方法考查的试题特点。
【真题】废旧铅蓄电池的铅膏中主要含有PbSO4、PbO2、PbO和Pb。还有少量Ba、Fe、Al的盐或氧化物等。为了保护环境、充分利用铅资源,通过下(右)图流程实现铅的回收。(注:试题给出了难溶电解质PbSO4、PbCO3、BaSO4、BaCO3的溶度积常数,此处略)
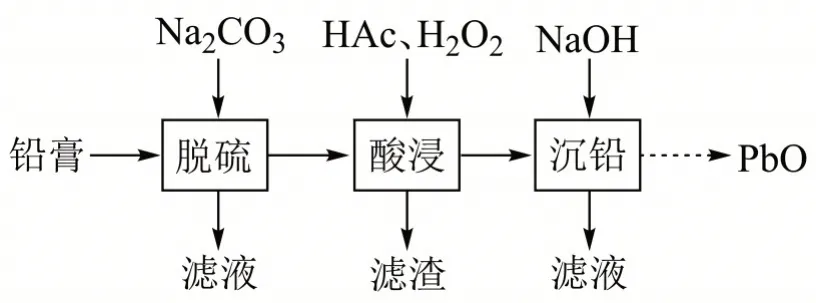
(1)在“脱硫”中PbSO4转化反应的离子方程式为________,用沉淀溶解平衡原理解释选择Na2CO3的原因________。
该题具有如下典型特点。
情境陌生。试题情境一般源于生产生活的实践应用,彰显化学学科价值。试题情境的陌生主要表现为物质陌生、概念陌生、化学式陌生、符号陌生、表征方式陌生、化学方程式陌生、仪器装置陌生、设问陌生等,高考化学试题要求考生能够在真实且陌生的情境中分析问题、解决问题并表达思维结果。该题中,铅膏的组成与性质、硫酸铅脱硫方程式、工艺名称、生产流程等,对学生来说均属于陌生知识。
情境复杂。这主要体现在以下几个方面。第一,试题涉及的物质体系复杂。试题往往包含了各类物质的反应或转化,甚至还隐含了部分化学反应。该题就考查了中学化学中常见的各类别物质(单质、氧化物、酸、碱、盐、常见氧化剂等)的性质及其应用,流程中的“酸浸”“沉铅”等也是物质的转化。第二,认识角度宽广。试题内容或问题设置涉及学科域、自然域、社会域等多角度,以全面检测学生的迁移创新能力。该题中“废旧铅蓄电池的铅膏”来源于工农业、生产生活等社会域,将其进行回收利用可以保护环境、充分利用铅资源,又涉及自然域,而试题设问则主要回归到学科域。第三,认识程度深。该题要求学生既要从定性、宏观、静态、文字等角度认识问题,又要从定量、微观、动态、符号等角度分析、解决问题。
融合多种思维方法。试题一般全面考查多种化学思维方法及其指标,学生需要综合多种思维方法的各个维度才能分析解决某一个问题。如该题中的大多数任务就需要学生综合应用上述三种化学思维方法,方能顺利完成。
该小题第1 问,要求考生写出“脱硫”中PbSO4转化反应的离子方程式,其思维过程如下。
首先,分析各种物质在溶液中的各自行为(电离、水解、沉淀溶解平衡等)。PbSO4属于难溶物,在水中存在溶解平衡;Na2CO3溶于水发生完全电离。
其次,确定离子之间的反应结果。依据题给Ksp可知,PbCO3属于难溶物,且溶解度比PbSO4低,因此当上述两种物质在溶液中相遇时,Pb2+与CO32-结合形成更加难溶的PbCO3,导致c(Pb2+)减小,从而引起PbSO4溶解平衡向右移动,最终转化为PbCO3和SO42-,据此可以写出离子方程式:PbSO4+CO32-=PbCO3+SO42-。
该小题第2问思维过程如下。
依据题意,要解释选用Na2CO3的原因,这隐含着从定性与定量两个维度进行回答的要求,即选用Na2CO3能否实现转化以及能否完全转化?
首 先,由 题 给Ksp(PbCO3)=7.4×10-14和Ksp(PbSO4)=2.5×10-8可知,前者小于后者且两种难溶物的组成形式相同(AB 型),依据沉淀转化原理可判断,选用Na2CO3能实现沉淀转化。
其次,需从定量视角(如反应平衡常数K)论证沉淀能否完全转化。依据已学知识,若K>1×10-5,则可认为反应完全。该反应的平衡常数K≈3.4×105>105,说明可以转化得比较彻底,且转化后生成的PbCO3可由酸浸进入溶液中,这能减少铅的损失。
上述分析过程,涉及对宏观辨识与微观探析、变化观念与平衡思想、证据推理与模型认知等多种思维方法的考查。
二、培养化学思维方法的策略
培养化学思维方法,可从教师和学生两个层面展开,以下分别阐述。
(一)教师层面
1.精准定位教学目标
教学目标直接影响教学设计以及教学行为,因此教师在制订教学目标时应将思维方法的培养列入关键内容。例如鲁科版普通高中教科书《化学》(以下简称“鲁科版《化学》”)必修第一册第1 章第2 节《研究物质性质的方法和程序》中的“氯气的性质”,除了介绍氯气性质的知识外,更承载了研究物质性质的程序建构与体验功能。学生既要学习氯气、次氯酸、次氯酸盐的性质,更要通过有关氯气性质的探究过程,学会研究物质性质的程序和方法,并在研究过程中培养化学思维方法。如果只是强化氯气及其化合物的性质与应用,并不断进行练习巩固,却只字不提对氯气性质的研究程序与方法以及思维方法的培养,就严重脱离了课标要求和教材设计意图。
要准确定位教学目标,教师首先应认真研读《普通高中化学课程标准(2017年版2020年修订)》(以下简称“《课程标准》”)。《课程标准》规定了高中化学课程学习应该达到的国家标准,包括学业要求、学业质量标准、化学学科核心素养等。学业要求主要基于某一主题中具体内容学习后应达到的要求,学业质量标准与学科核心素养则主要基于高中课程学习后的总体要求。教师应在整体把握《课程标准》的基础上,落实好各阶段教学目标以及课时教学目标。其次,高考评价体系、化学命题标准是针对选考化学的学生的考试要求,在针对此类学生的教学尤其是复习教学中,教师应特别关注这二者的要求,并将之贯穿到教学中。再次,历年高考试题是对高考评价体系及命题要求的诠释,通过研究历年高考试题的内容与要求,教师能更加清晰地了解高考评价体系的理念与要求,从而指导高考复习教学。最后,高考评价报告主要阐述当年考生对高考试题的答题情况及应答水平,能很好地反映当年考生的整体水平及其在知识、能力、素养等方面存在的主要问题,这为不断提升教学成效提供了极具针对性的导向。
根据以上分析,笔者明确了制订高考化学复习教学目标的基本流程(详见图1)。
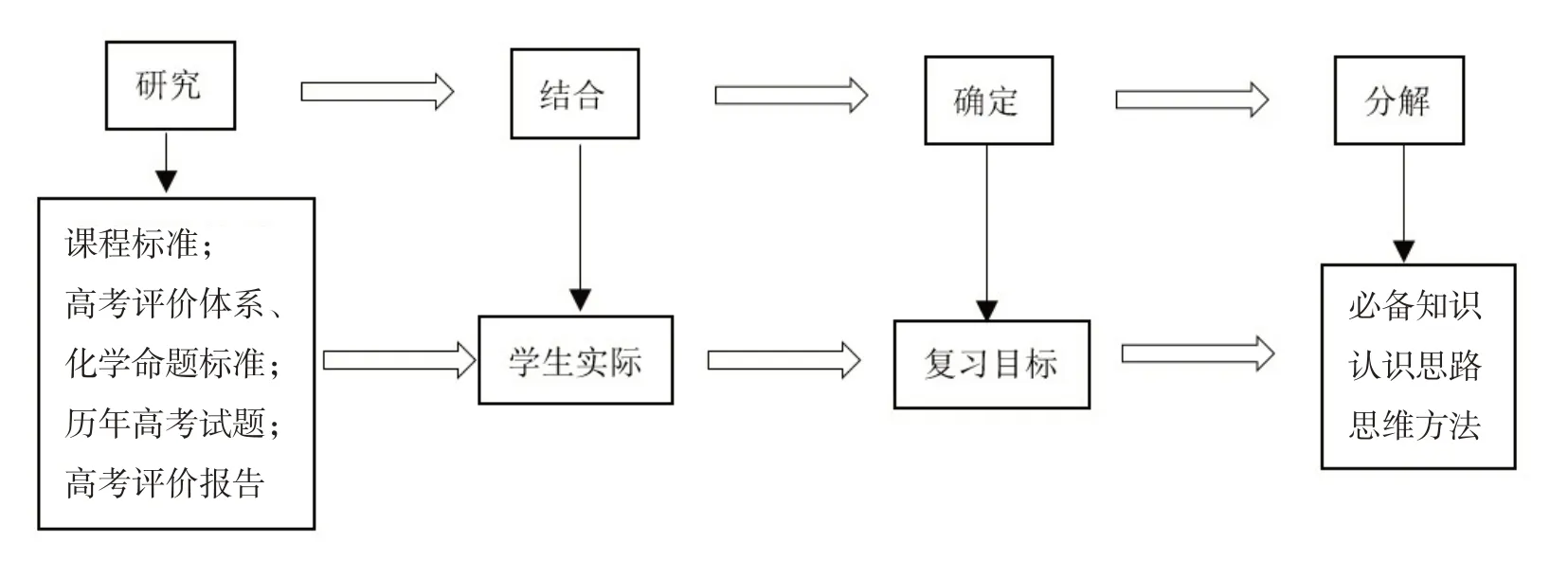
图1 制订高考化学复习教学目标的基本流程
2.基于情境开展教学
化学思维方法不是陈述性知识,而是程序性知识(或元认知知识),因此通过讲授或机械记忆无法形成思维方法,更不能提升应用思维方法的水平。在特定情境中解决问题、完成任务的能力和品质的素养,并不能脱离情境而习得[3]。它必须在面对真实具体问题情境时,通过分析问题、解决问题的过程才能形成和发展。因此在教学中,教师应具有不断创设真实且富有价值的情境,并从不同视角提出问题的能力。这可以有效引导学生分析并解决问题,使学生形成思维方法,进而达到程序化、自动化的水平。
依据问题的来源,情境可以分为日常生活情境、生产环保情境、学术探索环境、实验探究情境和化学史料情境[4];而依据情境的复杂程度不同,则可以将情境划分为简单情境、综合情境、应用性情境和开放性情境[5]。下面,笔者以鲁科版《化学》必修第二册第1章“微项目”板块中的“碘的提取”内容为例,对不同复杂程度的情境及思维方法的要求作分析(详见表1)。
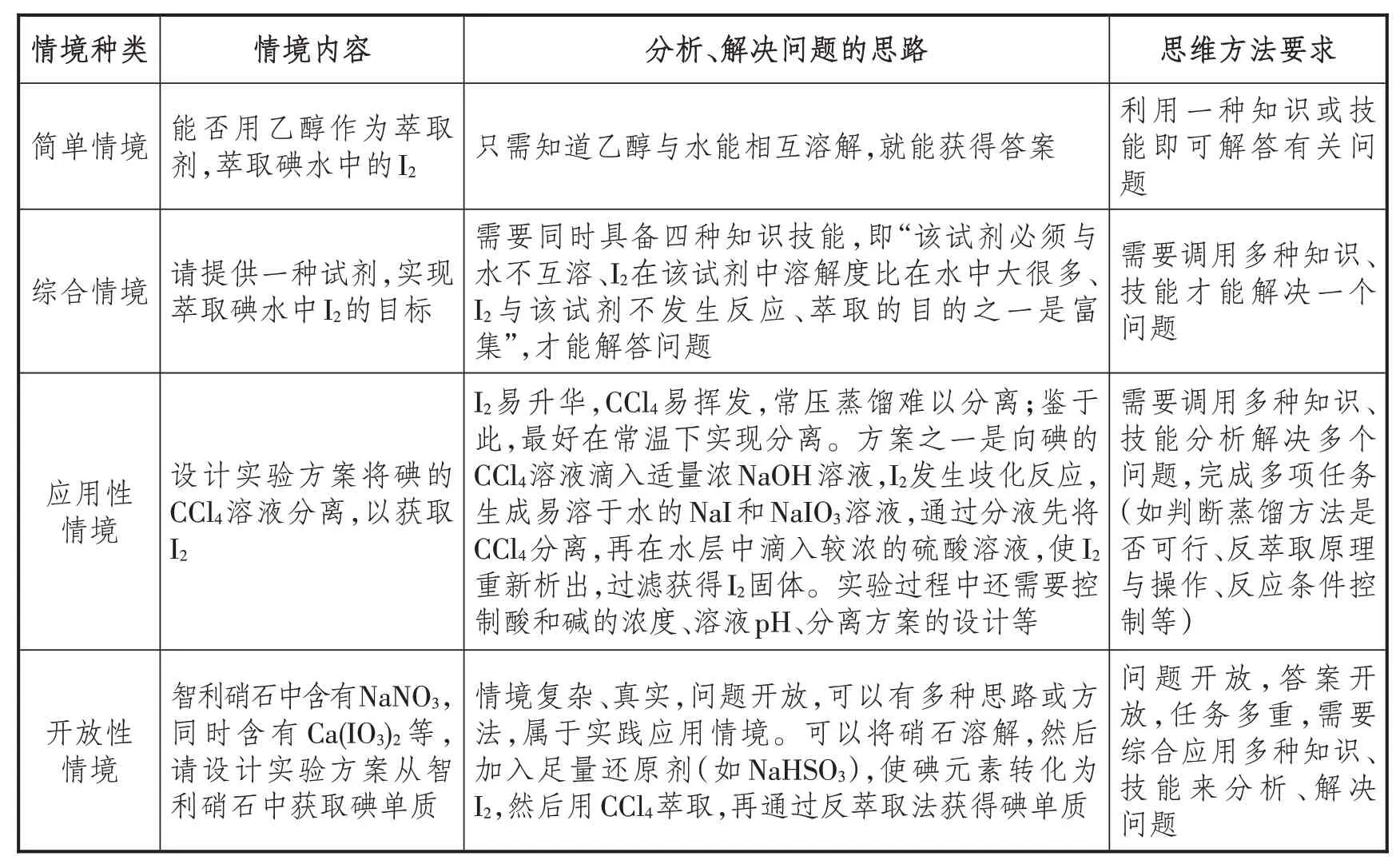
表1 不同复杂程度的情境及思维方法要求分析
在设计教学时,教师应依据教学目标的不同,来选择不同复杂程度的情境,以达到提升相应思维水平的实效。
3.提升自身的“题能力”
“题能力”指教师把握试题或习题的能力,包括做题、选题、讲题、改题、命题和评题等多个方面。习题教学是中学化学教学必不可少的环节,教师应该不断提升“题能力”,选择有价值的习题让学生独立思考,发挥讲评效益,提升习题教学质量。同时,教师应善于改编或命制试题,这一方面可以提升自身的专业能力,另一方面可以为学生提供有针对性的、使学习效率更高的习题。这样,既能减轻学生的课业负担,又能提升学生的学习效率,从而实现“减负增效”。
(二)学生层面
1.掌握必备知识
知识学习的最高层次是将知识转化为思维方法,而必备知识是形成关键能力、思维方法的基础。因此,融会贯通中学化学的必备知识,可以为思维方法的培养提供保障。学生在知识掌握的过程中需要跨越学科逻辑与心理逻辑之间的鸿沟,将科学家或教师的间接经验转化为自身经验[6]。必备知识的掌握程度可以从知识的内化与外化两个维度来表征或评价。
(1)知识内化
知识内化指对所学的相关知识能否达到结构化、语言化、方法化(知识学习的最高层次)的状态。下面,笔者以鲁科版《化学》选择性必修1第3章第2节中的“盐类水解”内容为例说明。
①知识结构化。知识结构化指与某一核心概念或原理相关联的知识,按照一定逻辑形成一个认识体系。新课学习时,学生对相关知识往往是进行零碎的、进阶式的学习。因此在教学过程中,教师必须随着学段的上升,使这些知识逐步结构化、系统化,从而将不同单元、不同模块的知识贯通起来。如盐类水解相关知识达到结构化的特征过程可以这样表述。
盐类溶于水,电离什么离子→哪些离子能水解→离子水解的结果→水解程度的定性、定量描述方式→水解平衡移动方向及移动结果→预测盐溶液可能有的性质→有何应用(分析问题、解决问题)。
②知识语言化。知识语言化指能用正确的化学语言表述核心概念的内涵。如盐类水解离子方程式、盐溶液中存在的定量关系表述(水解常数、电荷守恒、元素守恒、水解百分率等)、盐类水解的速率、限度、平衡移动,以及难溶盐溶解平衡(溶度积常数、沉淀溶解、沉淀形成条件)有关表征及应用等。
③知识方法化。知识学习理解的最高层次就是将知识转化为思维方法。比如盐类水解知识体系最终达成的思维方法就是,能正确判断或预测盐溶液的性质,解释盐溶液中发生的反应及其所表现的宏观现象。
(2)知识外化
如果能将所学知识、技能从熟悉情境迁移到陌生情境,将简单情境迁移到复杂情境,将封闭情境迁移到开放情境,并能对问题进行分析和解决,那么知识就达到了外化的要求。
例如:依据CH3COONa 的水解分析思路,能分析任意一种弱酸强碱盐的水解,说明学生能从熟悉情境迁移到陌生情境;从会分析单一盐类水解,到能分析多种盐水解(醋酸钠、碳酸钠混合溶液中的水解情况分析,氯化铵与醋酸钠混合溶液中的水解情况分析),说明能从简单情境迁移到复杂情境;从会分析热纯碱溶液可以去油污的原理,到能利用盐类水解原理设计方案除去MgCl2溶液中存在的少量FeCl3,说明学生能从封闭情境迁移到开放情境。
教学中,教师应依据知识内化与外化的具体体现,有意识地设计问题,诊断并发展学生的知识内化与外化水平,帮助学生养成良好的思维习惯和思维方法。
2.建构认识思路
认识思路指面对陌生情境,如何调用已有知识分析和解决真实的问题。它主要包括认识角度、认识程序(方向)、认识深度三个方面,我们也可以将其简单理解为“从什么角度想”“怎样想”“想到什么程度”三个方面,这也是解决问题的基本思维方法。在平时的教学过程中,学生不但要掌握必备知识,更重要的是要通过知识的学习及其产生过程,提炼认识问题的基本思路,不断提升思维水平。
例如对“CO2通入CaCl2溶液中,能否产生沉淀”这一问题,可以有如下认识思路。
【认识角度】
对实际问题进行分析,抽出问题涉及的知识归属,找出解决问题的角度。该例属于难溶电解质溶解平衡问题,应该通过沉淀形成的条件进行分析。
【认识程序】
分析电解质在水溶液中行为的基本程序如下。
(1)分别分析单一电解质在溶液中可能存在的行为(电离、水解、平衡)。
①CO2溶于水产生碳酸,碳酸发生电离:H2CO3⇌HCO3-+H+HCO3-⇌CO32-+H+。
②CaCl2溶液中存在电离平衡:CaCl2⇌Ca2++2Cl-。
③水的电离平衡:H2O⇌H++OH-。
因此溶液中存在的阳离子为Ca2+、H+;阴离子为Cl-、HCO3-、CO32-、OH-。
(2)将多种电解质溶液混合后,哪些离子之间能发生作用?判据是什么?离子浓度的影响因素有哪些?作用结果如何?
依据上述溶液中的离子情况,Ca2+与CO32-有可能发生作用形成沉淀,但必须依据离子浓度积Q(CaCO3)与Ksp(CaCO3)的相对大小进行判断。溶液中Ca2+、CO32-的浓度与溶液浓度有关,为了说明不会产生沉淀,必须寻找它们的最大值。室温下,我们可由饱和H2CO3溶液的pH=3.7,算出c(CO32-)=1×10-10.33,由CaCl2的溶解度为74.5g,算出饱和溶液中c(Ca2+)=6.05mol·L-1,进而算出离子浓度积Q(CaCO3)=6.05×1×10-10.33 【认识深度】 分析问题、解决问题需要具有一定的深刻性。教师要引导学生从宏观到微观、从定性到定量、从静态到动态、从孤立到联系地进行思考,使其认识问题的深度不断增加、解决问题的能力与水平逐渐上升,最终得出更加可靠的结论。这一案例涉及微观、定量、动态、联系等各方面的思想方法,具有较强的代表性。 3.体验思维方法的应用 教学中,教师应引导学生分析典型试题,挖掘隐含的思维方法,使其通过深度剖析,明确化学思维方法在试题中的具体要求,进而提升应用思维方法的水平。下面,笔者以2022年全国高考理综乙卷第36 题(节选)为例,展示学生对证据推理与模型认知这一思维方法在试题中考查要求的分析。 a.含有一个苯环和三个甲基; b.与饱和碳酸氢钠溶液反应产生二氧化碳; c.能发生银镜反应,不能发生水解反应。 该题主要考查证据推理与模型认知思维方法的应用水平。在教师的指导下,学生经充分讨论,一致认为分析指定条件的同分异构体数目,其基本思维过程为:分析分子→推测碎片→重组分子(详见表2)。 表2 分析指定条件的同分异构体数目的基本思维过程 剖析高考试题的另一个意义是,学生可以体验化学思维方法在试题中的体现方式,进而能够理解思维方法的意义、价值。这有利于学生找到学科知识与思维方法的结合点,从而拓宽思维方法的培养路径。 综上,在化学教学中,教师应全面领悟《课程标准》和评价体系的内涵,对照高考试题的具体内容,体会核心素养的考查要求与考查形式,并在核心素养发展目标的基础上,选择真实复杂的情境,设置学科高级思维活动,帮助学生在学习知识的过程中,提炼解决问题的通识通法,将已有知识迁移应用到新的情境中,从而实现提质增效的目标,有效发展学生的核心素养。□◢

