基于“四重表征”模式 培养学生学科素养
——以“探究盐酸与碳酸钠、碳酸氢钠反应”的教学为例
李健荣
(东莞松山湖未来学校 广东东莞 523112)
一、问题的提出
学科核心素养是学科育人价值的集中体现,是学生通过学科学习而逐步形成的正确价值观念、必备品格和关键能力。《普通高中化学课程标准(2017 年版2020年修订)》提出,化学学科核心素养包括“宏观辨识与微观探析”“变化观念与平衡思想”“证据推理与模型认知”“科学探究与创新意识”“科学态度与社会责任”5个方面。[1]如何理解化学学科核心素养的内涵和概念?如何在课堂教学中培养学生的化学学科核心素养?这些都是化学教育工作者面临的重要问题。课堂教学是培养学生化学核心素养的主要途径,教师需要选择合理的教学内容,挖掘教学内容中蕴含的学科核心价值,采用合适的教学模式和教学策略,从而达到培养学生学科核心素养的目的。
碳酸钠、碳酸氢钠是钠的重要化合物,也是高中学习元素化合物的重要内容。人教版教材的内容中,就二者的外观、溶于水的热量变化、热稳定性及溶液碱性进行了探究,对两者和稀盐酸的反应仅要求写出反应的离子方程式。但教材对如何组织“碳酸钠、碳酸氢钠与稀盐酸的反应探究”并未提出建议。在实际的教学中,教师进行演示实验,一般是向等物质的量的碳酸钠、碳酸氢钠溶液中加入等浓度等体积的稀盐酸,然后根据气泡产生的快慢进行粗糙的对比,再从微观角度解释反应快慢的原因。笔者认为,该教学过程缺乏严谨的证据支撑。
本文挖掘“碳酸钠、碳酸氢钠与盐酸反应”背后所蕴含的化学学科核心价值,以“四重表征”教学模式为基础,创设真实且富有价值的问题情境,通过3个“递进式实验”,逐步使学生理解碳酸钠、碳酸氢钠与盐酸反应的机理,从而培养学生的化学学科核心素养。
二、教学设计
1.教学思想
钱扬义主编的《化学概念与化学“学科关键词”的学习与认知》一书中,对化学“四重表征”教学模式进行了具体的介绍,即宏观表征、微观表征、符号表征和曲线表征。[2]在定性和定量的实验探究过程中,都会涉及到实验现象记录等宏观表征,解释实验现象等微观表征,书写化学方程式等符号表征,在连续性的定量测量实验中会生成与反应过程相匹配的曲线图像等曲线表征。因此,科学探究的过程与“四重表征”有着紧密的联系。[3]
“探究盐酸与碳酸钠、碳酸氢钠反应”一课以“四重表征”教学模式进行设计(见图1)。通过碳酸钠、碳酸氢钠与盐酸反应并使气球膨胀的实验,发现碳酸钠与盐酸反应的速率较慢(宏观表征);引导学生从微观的角度猜测碳酸钠与盐酸反应的机理(微观表征);用pH传感器绘出反应过程中溶液的pH变化曲线,验证微观猜想(曲线表征);促使学生建立微粒观,从而写出碳酸钠、碳酸氢钠与盐酸反应的离子方程式(符号表征)。

图1 本节课中“四重表征”的教学思想
2.“四重表征”教学模式与化学学科核心素养的联系
培养学生化学学科素养是化学教学的重要目标,宏观辨识与微观探析是“四重表征”中的两个表征方式,曲线表征能将宏观现象与微观本质通过曲线的形式抽象地表示。变化的曲线有利于学生理解化学变化的动态过程,培养学生的变化观念与平衡思想。数字化技术实验能将传统化学实验中无法直接观察到的现象和变化,通过反应曲线呈现出来,使其变得可视化,为实验证据的收集提供了新的途径,有利于培养学生证据推理的素养。“四重表征”教学模式促使学生从多个维度认识研究对象的性质、特征及其相互转换,能建立起有效的化学学科认知模型。因此,“四重表征”教学模式为在课堂中培养学生化学学科核心素养提供了有效途径。
本节课的“四重表征”与化学学科核心素养的关系见图2。

图2 本节课的“四重表征”与化学学科核心素养的关联
3.教学目标
本节课的教学目标如表1所示。

表1 基于化学学科核心素养确定的教学目标
三、教学过程
1.新课导入——自制泡沫灭火器,模拟灭火过程
【引入】发生火灾时,我们常会用泡沫灭火器进行灭火。同学是否思考过泡沫灭火器的工作原理是什么?
【教师】展示泡沫灭火器的说明书,请学生结合说明书提供的信息分析泡沫灭火器的工作原理。
【学生】阅读说明书后知道,泡沫灭火器中有两个容器,分别盛放碳酸氢钠溶液和酸性液体。当使用泡沫灭火器时,将灭火器倒转使两种液体充分混合产生二氧化碳,从而灭火。
【趣味实验】向装有100 mL 饱和碳酸氢钠溶液和5 mL洗涤剂的塑料瓶(塑料瓶的瓶口连接一根橡胶导管)中放置一支装有20 mL 6 mol/L 盐酸溶液的试管。倒转塑料瓶并将橡胶导管对准火焰根部,观察到火焰熄灭(见图3)。

图3 用自制泡沫灭火器模拟灭火过程
2.实验初探——碳酸钠溶液、碳酸氢钠溶液与盐酸的定量实验
【提问】NaHCO3和Na2CO3都能与酸反应放出CO2。为什么泡沫灭火器使用的是NaHCO3而不是Na2CO3?
【学生】提出猜想:碳酸氢钠与酸反应的速率可能更快。因为放出同等体积的二氧化碳,碳酸氢钠消耗的盐酸要比碳酸钠消耗的盐酸的量少。
【追问】如何验证同学们的猜想?
【学生活动】用“实验装置拼图”,设计碳酸氢钠、碳酸钠与盐酸反应实验的方案。各小组展示设计方案,由其他小组成员进行点评,最终选出最优方案(见图4)。

图4 使用自主研发的“实验装置拼图”设计实验方案
【定量实验】实验装置如图5 所示。在滴定管夹两侧夹两根硬质玻璃管,用带有针筒的橡胶塞塞紧玻璃管的下端。向两硬质玻璃管中分别倒入10 mL 0.1 mol/L 碳酸钠溶液和10 mL 0.1mol/L 碳酸氢钠溶液,用气球套紧玻璃管的上端。用针管向两支硬质玻璃管中注入10 mL 0.1mol/L 盐酸溶液,观察到装有碳酸钠溶液玻璃管的上方的气球无明显变化,而装有碳酸氢钠溶液玻璃管上方的气球迅速变大。随后将针筒中剩余的10 mL 0.1 mol/L 盐酸溶液全部注入到玻璃管中,观察到两只气球都膨胀变大。

图5 碳酸钠溶液、碳酸氢钠溶液与盐酸反应的定量实验
【教师】根据上述实验的现象,同学们可以得出什么结论?
【学生】套在装有碳酸氢钠溶液玻璃管上方的气球先膨胀变大,所以碳酸氢钠溶液与盐酸反应的速率更快。
3.实验再探——验证碳酸钠与盐酸反应的微观机理
【提问】在碳酸钠、碳酸氢钠与盐酸反应的定量实验中,为什么第一次注入10 mL盐酸时盛碳酸钠溶液的玻璃管中没有气体产生?第二次注入剩余的10 mL盐酸时却有气体产生?
【学生】提出猜想:从化学方程式中可以观察到,NaHCO3与盐酸反应只需要一个H+,而Na2CO3与盐酸反应需要两个H+,所以Na2CO3获取第一个H+变成NaHCO3,然后NaHCO3再获取一个H+变成H2CO3,最终放出CO2。在刚刚的定量实验中,盐酸是分两次注入到硬质玻璃管中的,也从侧面说明Na2CO3与盐酸反应放出CO2时分两步进行。
【提问】同学们提出Na2CO3与盐酸反应可能是分两步进行的,我们如何验证这个猜想?
【数字化实验】实验装置如图6所示。用0.1 mol/L盐酸滴定25 mL 0.1 mol/L 碳酸钠溶液,测量溶液中的pH 变化,并通过电脑记录并显示滴定过程中溶液的pH 随时间变化的曲线(见图6、图7、图8)。观察到曲线中有两个突变点,说明Na2CO3与盐酸反应是分步进行的。其中第一个突变点的pH值为8.20,与0.05 mol/L NaHCO3溶液的pH(8.39)基本相同,这就证明Na2CO3与盐酸反应时先转变为NaHCO3,再转变为碳酸,最终放出CO2。

图6 用盐酸滴定碳酸钠溶液并测定溶液pH的实验装置

图7 用pH计测量0.05 mol/L碳酸氢钠溶液的pH
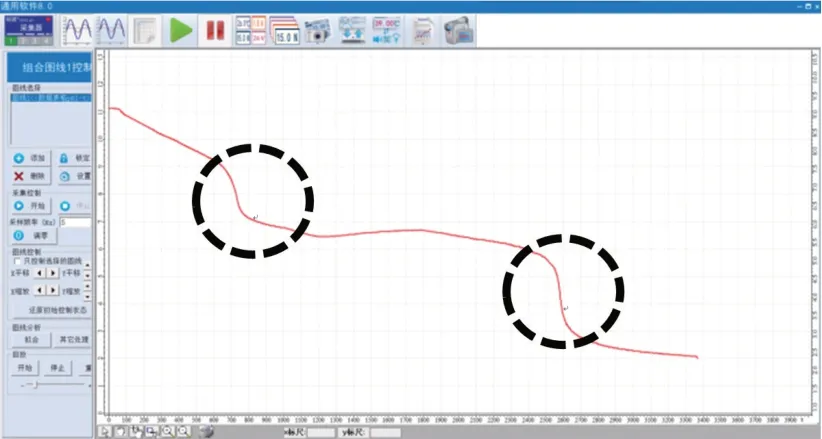
图8 用盐酸滴定碳酸钠溶液时pH变化曲线
【教师】根据上述实验现象,同学们可以得出什么结论?
4.联系生活——碳酸钠、碳酸氢钠在生产、生活中的价值
【总结】本节课我们一起研究了碳酸钠、碳酸氢钠溶液与盐酸反应的实质。通过定量实验和数字化实验,我们理解了与H+反应的微观机理。更为重要的是,我们初步建立了探究物质性质、反应及其相互转换的思维模式。
【教师】碳酸钠、碳酸氢钠在生产、生活中有重要的应用。例如:我们经常服用的维生素C泡腾片是利用碳酸氢钠与有机酸的反应实现药片的自动崩解。纯碱是一种重要的化工原材料,在19世纪中期,欧美各国将纯碱的制造方法垄断起来,中国工业所需要的纯碱完全依赖进口。为了打破欧美各国的垄断局面,我国著名的化工开拓者侯德榜先生经过上千次的尝试终于探索出制碱的新工艺,降低了成本,这种制碱法被命名为“侯氏制碱法”。
四、教学评价与成效分析
1.问题研究方法
教学完成后,采用学生问卷调查法,从教学目标和化学学科核心素养的方面调查学生对本节课的反馈与评价,从而获得定量的数据。定量数据采用SPSS 23.0进行分析。
本次调查选取了东莞市某高中127名学生作为测试对象,测试对象的综合成绩和化学单科成绩较好。
本次调查问卷采用李克特5 点量表计分法,共有24题,选项包括十分同意、同意、一般、不同意、非常不同意,分值分别计为5、4、3、2、1 分。发放了127 张问卷,回收问卷127张,回收率为100%。
2.调查结果与分析
该问卷的Alpha 为0.821,信度较好,问卷的统计数据具有较高的可靠性(见表2)。
由表2 的问卷调查反馈可知,学生通过本节课的学习,化学学科核心素养落实情况较好,平均分均在4.5以上。

表2 问卷统计和数据分析
第8、9题的得分均在4.5以上,说明在课堂中使用数字化实验得到学生的认同,有助于学生认知化学反应的机理和本质,为学生观察实验现象和收集实验数据提供了新的途径,对于培养“证据推理”的核心素养起到很好的促进作用。第5、6 题的平均得分为4.659,说明学生对于通过动态曲线分析化学反应十分感兴趣。同时,动态曲线可以直观地呈现过程,有利于学生动态地分析化学变化,促使“变化观念”的建立。根据上述问卷数据的分析,说明“四重表征”中的曲线表征对于培养学生化学学科核心素养具有更大的价值。
为保证问卷数据的有效性和科学性,问卷的第4、7、13、20、21题为反向题,平均得分都在1.7以下,其中第4 题的平均得分为1.658,分值相对其他反向题较高。造成该现象的主要原因是本节课知识性层面的内容学生在之前的学习中已经掌握(离子方程式的书写和碳酸钠、碳酸氢钠的部分性质),学生在课堂中收获的知识性内容并不多,从而造成第4题(反向题)得分相对偏高的情况。第22 题的得分为4.771,得分较高,说明学生在知识层面虽然收获较少,但认为本节课验证猜想的方法十分严谨,学生的科学探究的思维得到了一定的提升。
五、教学反思
根据研究结果可以发现,“四重表征”教学模式对培养学生化学学科核心素养有较好的效果,为培养学生的学科素养提供了有效途径。
结合本节课的教学思想、教学模式、教学内容和教学效果,在课堂上落实学生化学学科核心素养的培养需要做好以下3个方面:
1.创设真实且富有价值的问题情境
真实、具体的问题情境是学生化学学科核心素养形成和发展的重要平台,为培养学生化学学科核心素养提供了真实的表现机会。因此,教师在教学中应重视创设真实且富有价值的情境。本节课用泡沫灭火器创设情境,层层设问深挖“为什么灭火器使用的是碳酸氢钠而不是碳酸钠?”充分发挥真实情境的价值。
2.制订科学的教学目标
学生化学学科核心素养的发展是持续进步的过程,合理的教学目标是在课堂教学中落实核心素养的保障,同时也是对教学效果评价的重要标准。在制定教学目标时,应当着重分析化学学科核心素养的内涵与教学内容、学情的联系,将学科核心素养的要求转变为教学目标,从而将素养的培养落实到教学活动中。
3.发挥化学实验的独特价值
在本节课中,如何帮助学生认识碳酸钠与盐酸反应的机理?如何使学生“看到”溶液中离子是如何反应的?数字化实验有着不可替代的作用。本节课通过三个递进式实验:“模拟灭火器”“碳酸钠、碳酸氢钠与盐酸反应的定量实验”和“数字化实验测定溶液的pH 变化”,增进学生对科学探究的理解,使化学知识的学习、科学探究能力的形成与化学学科核心素养的发展有机地结合。

