细菌溶解产物胶囊联合布地奈德福莫特罗粉吸入剂对稳定期慢性阻塞性肺疾病患者的应用效果
曹利静,秦海玲,李荟苹,任红敏,刘方方,徐娜,王潇,秦文婧
(河南大学第一附属医院 呼吸内科,河南 开封 475000)
慢性阻塞性肺疾病(chronic obstructive pulmonary disease,COPD)简称慢阻肺,是一种以慢性呼吸道症状、肺功能持续恶化为特征的临床综合征,具有高患病率、高病死率、高疾病负担等特点[1]。已有研究指出,长效β2-受体激动剂(long term effect β2-receptor agonist,LABA)/吸入糖皮质激素(inhaled glucocorticoid,ICS)可明显改善COPD患者症状,提升运动耐量,提高生活质量[2]。布地奈德福莫特罗粉吸入剂为LABA/ICS复合制剂,可有效减轻炎症反应,缓解临床症状。此外,细菌感染是导致COPD急性发作的主要诱因,而COPD患者免疫应答紊乱会加剧细菌感染风险[3]。细菌溶解产物胶囊可通过激活免疫系统特异性及非特异性免疫,增强机体对细菌感染免疫力[4]。但细菌溶解产物胶囊联合布地奈德福莫特罗粉吸入剂在稳定期COPD治疗方面的疗效报道较少,鉴于此,本研究首次在布地奈德福莫特罗粉吸入剂基础上加用细菌溶解产物胶囊,并从肺功能、免疫功能及生活质量方面探究其临床效果。
1 资料和方法
1.1 选例与分组河南大学第一附属医院伦理委员会已批准本研究,选取河南大学第一附属医院2020年7月至2022年3月门诊就诊的稳定期120例COPD患者作为研究对象进行前瞻性研究。纳入标准:符合COPD诊断标准[5],晨间常有咳嗽,夜间阵咳排痰,且多为白痰;肺功能分级Ⅱ~Ⅲ级;近1个月内未服用糖皮质激素、抗生素;既往无肺部手术史;患者自愿签署知情同意书。排除标准:其他因素所致气流受限;造血、肾、肝功能严重异常;急性加重期;长期服用激素类药物;治疗依从性较差,未完成治疗。根据上述纳入标准研究共纳入120例。按照随机数字表法分为联合组(n=60)、常规组(n=60)。
1.2 一般资料两组患者性别、年龄、体重指数(body mass index,BMI)、肺功能分级等一般资料见表1,经统计分析,两组资料具有均衡性(P>0.05),可进行对照研究。

表1 两组资料均衡性分析
1.3 治疗方法两组均接受预防和维持治疗,包括抗感染、祛痰、平喘、减少危险因素暴露、营养均衡摄入、肺康复训练等基础治疗。在此基础上常规组接受布地奈德福莫特罗粉吸入剂(Astra Zeneca AB,H20140457,规格:60吸/支,每吸含布地奈德320 μg和福莫特罗9 μg)治疗,每天2次,每次1吸,连续吸入3个月。联合组给予细菌溶解产物胶囊(瑞士欧姆制药有限公司,S20150042,规格:每粒7 mg)联合布地奈德福莫特罗粉吸入剂(给药方法同常规组)治疗,每日清晨口服1粒细菌溶解产物胶囊,连服10 d,停20 d,以此类推,连续治疗3个月。
1.4 观察指标
1.4.1临床疗效 参照《慢性阻塞性肺疾病诊治指南(2007年修订版)》[5]评价治疗效果,分为显效(临床症状消失,X线片显示肺部病变显著改善)、好转(临床症状明显减轻,X线片显示肺部病变有所好转)、无效(未达上述标准)。显效及好转计入总有效。
1.4.2运动耐力、呼吸困难程度 比较两组治疗前、治疗3个月后6分钟步行试验(6-minute walk test,6MWT)、改良的医学研究委员会呼吸困难量表(modified Medical Research Council dyspnea scale,mMRC)[6]。6MWT:统计患者6 min内行走距离,距离越长则运动耐力情况恢复越理想。mMRC总分0~4分,分值与呼吸困难程度成正比。
1.4.3肺功能 比较两组治疗前、治疗3个月后第1秒用力呼气容积(forced expiratory volume in one second,FEV1)占预计值百分比(FEV1%)、用力肺活量(forced vital capacity,FVC)、FEV1/FVC、残气量(residual volume,RV)、肺总量(total lung capacity,TLC)、RV/TLC,采用肺功能仪(德国康讯CareFusion公司,型号:Master-Screen)检测。
1.4.4免疫功能 比较两组治疗前、治疗3个月后CD4+、CD8+、免疫球蛋白G(IgG)、IgA,采用流式细胞仪[艾森生物(杭州)有限公司,型号:NovoCyte D1040]检测CD4+、CD8+;全自动生化分析仪(德国西门子公司,型号:ADVI-A2400)检测IgG、IgA。
1.4.5安全性 比较两组治疗期间呛咳、恶心、咽部不适、口干等不良反应发生情况。
2 结果
2.1 临床疗效联合组总有效率高于常规组(P<0.05)。见表2。
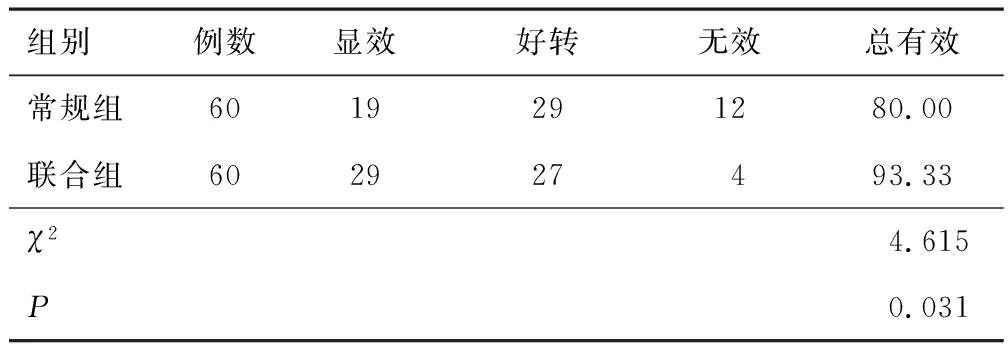
表2 两组临床疗效比较(n,%)
2.2 运动耐力、呼吸困难程度组内比较:治疗3个月后,两组6MWT距离长于治疗前,mMRC评分低于治疗前(P<0.05)。组间比较:与常规组相比,联合组治疗3个月后6MWT距离增加,mMRC评分下降(P<0.05)。见表3。
表3 两组6MWT及mMRC评分比较
2.3 肺功能组内比较:治疗3个月后,两组FEV1%、FEV1/FVC高于治疗前,RV/TLC低于治疗前(P<0.05)。组间比较:治疗3个月后,联合组FEV1%、FEV1/FVC、RV/TLC改善幅度大于常规组(P<0.05)。见表4。
表4 两组肺功能比较
2.4 免疫功能组内比较:治疗3个月后,两组CD4+、IgA、IgG高于治疗前,CD8+低于治疗前(P<0.05)。组间比较:与常规组相比,联合组治疗3个月后CD4+、IgA、IgG升高,CD8+下降(P<0.05)。见表5。
表5 两组免疫功能比较
2.5 安全性治疗期间,联合组出现3例恶心,2例咽部不适,1例呛咳;常规组2例恶心,1例咽部不适,1例呛咳。联合组不良反应发生率为10.00%(6/60),常规组不良反应发生率为6.67%(4/60),两组比较,差异无统计学意义(χ2=0.436,P=0.508)。
3 讨论
调查显示,我国40岁以上人群COPD患病率约为13.7%,总人数近1亿,已经成为与糖尿病、高血压“等量齐观”的重大慢性疾病,造成了巨大疾病负担[7]。COPD发生主要同患者吸入有害气体至气道后引发的异常炎症反应有关,气道慢性炎症通过刺激气道平滑肌使其收缩,导致气道壁受损以及修复期间反复性出现,引起不完全可逆气流受限状况[8-9]。故而预防其反复发作对提高稳定期COPD治疗效果意义重大。
布地奈德福莫特罗粉吸入剂由LABA、ICS相混合而成,其中前者通过与气道中β2受体相结合,兴奋气道平滑肌及肥大细胞表面β2受体,起到扩张平滑肌、减少炎症递质释放作用;后者可增强β2受体敏感性,有效避免气道重塑,二者结合具有互补、协同效应,但仍不能阻止肺功能慢性下降趋势[10-11]。刘迪等[12]报道,COPD发生细菌感染与机体免疫应答功能减弱有关,增强免疫应答被认为是治疗COPD有效方式。临床研究证实,COPD患者普遍存在免疫应答紊乱,表现为CD4+、CD8+的比例失调。而机体免疫应答紊乱不仅会增加COPD患者感染风险,还可诱发多种炎症递质释放,加剧气道重塑、气道炎症,进一步损害肺功能[13]。此外,免疫活性分子IgA、IgG也参与细菌清除过程,IgA能够抵御细菌、病毒在呼吸上皮附着,其水平下降会增加感染风险;IgG是血清免疫球蛋白主要成分,具有调节免疫功能和抗感染作用。细菌溶解产物胶囊由金黄色葡萄球菌、肺炎双球菌、化脓性链球菌等细菌提取物组成,具有特异和非特异性免疫刺激作用,通过不断刺激单核细胞及巨噬细胞的活性促进T淋巴细胞成熟,同时提升T淋巴细胞反应性及抗病毒干扰素活性,调节免疫应答,并能预防病原菌再次侵袭[14-15]。同时还能提高呼吸道黏膜对免疫球蛋白的分泌,加快T淋巴细胞在体内的循环,提升唾液黏膜相关上皮趋化因子的分泌,具有显著的调节机体免疫功能的作用[16-17]。本研究发现,经治疗后联合组CD4+、CD8+、IgA、IgG改善程度均优于常规组。推测原因:布地奈德福莫特罗粉吸入剂通过改善COPD患者免疫功能,抑制炎症因子释放,为加快临床症状改善创造有利条件,结合细菌溶解产物胶囊,对T、B淋巴细胞、巨噬细胞的刺激作用,提高机体对感染免疫力,并可增强呼吸道黏膜免疫球蛋白分泌,协同发挥作用,减轻炎症因子对气道损伤作用,促进机体免疫应答恢复。
COPD 急性发作可表现为肺功能迅速下降,继而并发呼吸衰竭,机体对缺氧的耐受性下降,因此改善肺功能对患者的预后有至关重要[18-19]。本文中采用FEV1%、FEV1/FVC、 RV/TCL评价患者肺功能,采用6MWT、mMRC评估患者运动耐量。本研究发现,采用布地奈德福莫特罗粉吸入剂联合细菌溶解产物胶囊治疗稳定期COPD患者,能提高治疗效果,进一步降低mMRC评分,增加6MWT距离,改善肺功能,与曾敦煌等[20]研究结果相符。分析认为:布地奈德福莫特罗粉吸入剂具有抗炎症细胞聚集、黏附及保护呼吸道黏膜等功能,细菌溶解产物胶囊通过刺激黏膜淋巴组织而激活免疫系统[21],二者联合可从增强免疫力、调控总抗氧化能力、改善肺功能等不同机制、多环节治疗稳定期COPD,充分发挥各自功能,从而强化疗效,促进临床症状、肺功能改善,提高患者运动耐量。此外,本研究还发现,两组不良反应发生率差异无统计学意义,可见两者联合不增加药物不良反应,具有一定安全性。
综上可知,布地奈德福莫特罗粉吸入剂治疗稳定期COPD能改善免疫功能,促进肺功能恢复,有效缓解病情,增强疗效,提高生活质量,安全可靠。

