铜纳米簇探针-荧光分光光度法测定矿泉水和饮料中日落黄的含量
陈中兰,李思灵,胡 月
(西华师范大学 化学化工学院 四川省化学合成与污染控制重点实验室,南充 637009)
随着生活水平的提高,人们对食品的要求不仅仅局限于其营养丰富,而且还要求其色香味俱全,因此厂家通常会在食品中添加不同种类人工合成或天然的色素来改善食品的色泽。而人工合成色素日落黄因具有毒性低、色泽亮丽、成本低等优点,成为最常用的人工合成食品色素之一。国家标准GB 2760-2014《食品安全国家标准 食品添加剂使用标准》中规定日落黄在食品中的质量分数应不大于0.1 g·kg-1。因此,准确测定食品中日落黄的含量对食品安全控制具有重要意义。目前,日落黄的测定方法有高效液相色谱法[1]、电化学法[2-3]、近红外光谱法[4]、共振瑞利散射光谱法[5]、紫外-可见光谱法[6]等,而这些方法存在仪器昂贵、样品前处理复杂、测试成本高等缺点,导致其在实际应用中受到限制。
金属纳米簇,如金纳米簇(Au NCs)、银纳米簇(Ag NCs)、铂纳米簇(Pt NCs)、铜纳米簇(Cu NCs)等具有尺寸小、毒性低、荧光强度高、光稳定性好、生物相容性佳等优点,在生物成像、医疗诊断、化学传感、纳米制药等领域广泛应用[7]。与Au NCs、Ag NCs、Pt NCs相比,Cu NCs不仅具有高的量子产率和好的生物相容性,而且制备成本低[8]。文献[9]开发了一种以双链DNA(dsDNA)模板制备的Cu NCs作为荧光探针来检测三磷酸腺苷(ATP)的方法,该方法可用于测定人血清和人宫颈癌海拉(Hela)细胞中ATP的含量,回收率为104%~108%;文献[10]探讨了DNA 的G 碱基增强合金纳米簇DNA-Cu/Ag NCs荧光的原理,并且将其用于检测Cu2+,检出限为5.0 nmol·L-1。鉴于此,本工作采用一步湿化学法制备Cu NCs,以Cu NCs为荧光探针,采用荧光分光光度法测定矿泉水和饮料中日落黄的含量,并探讨了Cu NCs的荧光猝灭机理。
1 试验部分
1.1 仪器与试剂
JEM-2100型透射电子显微镜(TEM);Nicolet-6700型傅里叶变换红外光谱仪(FTIR);ESCALAB 250Xi型X 射线光电子能谱仪(XPS);Cary eclipse型荧光分光光度计;UV-2550 型紫外-可见分光光度计。
日落黄标准储备溶液:1.0×10-3mol·L-1,移取适量的日落黄标准品,用水溶解、稀释,配制成1.0×10-3mol·L-1日落黄标准储备溶液。使用时,用水稀释至所需浓度。
日落黄标准品的纯度为95%;所用试剂均为分析纯;试验用水为超纯水。
1.2 试验方法
1.2.1 Cu NCs的制备
参考文献[11],将水15.0 mL、0.01 mol·L-1L-半胱氨酸溶液4.0 mL和0.1 mol·L-1硝酸铜溶液0.2 mL 依次加入30 mL 带盖反应瓶中,立即将反应瓶放入15 ℃水浴中搅拌5 min,溶液由无色变为乳白色;然后缓慢滴加1.0 mol·L-1氢氧化钠溶液1.00 mL,此时溶液由乳白色逐渐变为黑色,继续在15 ℃水浴中搅拌反应2.5 h,得到L-半胱氨酸保护的Cu NCs,此时溶液呈浅蓝色;接着将浅蓝色溶液用透析膜(截留分子量为500 Da)透析72 h,得到纯净的Cu NCs溶液,于4 ℃保存备用。将纯净的Cu NCs溶液放入60 ℃真空干燥箱中干燥72 h,得到Cu NCs固体。取适量的Cu NCs固体,用水配制成不同质量浓度的Cu NCs溶液。
1.2.2 标准曲线的建立
将不同浓度的日落黄标准溶液分别与0.33 g·L-1Cu NCs溶液0.5 mL混合,然后用pH 8.0的伯瑞坦-罗宾森(B-R)缓冲溶液稀释至3.0 mL,室温下反应60 s。设置荧光分光光度计的激发波长为370 nm,激发和发射的狭缝宽度分别为5,10 nm,记录加入日落黄前后体系在490 nm 处的荧光强度F0、F。以日落黄浓度为横坐标,体系的荧光强度比值(F/F0)为纵坐标绘制标准曲线。
1.2.3 样品分析
矿泉水和饮料经0.22μm 微孔滤膜过滤,收集澄清滤液并于4 ℃保存备用。各分取50μL,分别与0.33 g·L-1Cu NCs溶液0.5 mL 混合,然后用pH 8.0 的B-R 缓冲溶 液稀释 至3.0 mL,按 照1.2.2节所述的仪器工作条件进行测定。
2 结果与讨论
2.1 CuNCs制备条件的优化
为了使Cu NCs有好的发光性能,对其制备条件进行优化。试验首先考察了1.0 mol·L-1氢氧化钠溶液用量分别为0.50,0.75,1.00,1.25,1.50 mL时对Cu NCs荧光强度的影响,结果见图1(a)。
由图1(a)可知,加入氢氧化钠溶液1.00 mL时,Cu NCs荧光强度较大,继续增大氢氧化钠溶液用量,Cu NCs荧光强度逐渐减小。可能是由于过多的氢氧化钠与部分Cu2+反应生成Cu(OH)2,导致生成的Cu NCs减少,进而使Cu NCs荧光强度显著降低。因此,试验选择的氢氧化钠溶液用量为1.00 mL。
接着考察了合成温度分别为10,15,25,35,45,55 ℃对Cu NCs荧光强度的影响,结果见图1(b)。
由图1(b)可知:合成温度由10 ℃升高至25 ℃时,Cu NCs荧光强度变化不大;继续升高温度,Cu NCs荧光强度显著降低,可能是由于温度较高不利于Cu NCs的生成。从节省能耗角度考虑,试验选择的合成温度为15 ℃。
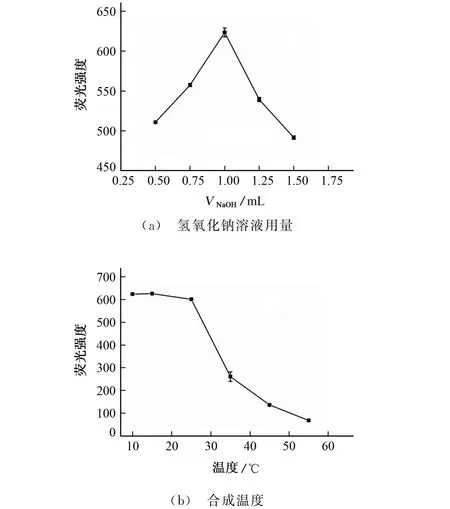
图1 氢氧化钠溶液用量和合成温度对Cu NCs荧光强度的影响Fig.1 Effects of amount of sodium hydroxide solution and synthesis temperature on the fluorescence intensity of Cu NCs
2.2 CuNCs表征
Cu NCs的TEM 图及其粒径分布图见图2。
由图2可知,制备的Cu NCs分散性较好,平均粒径为1.54 nm。
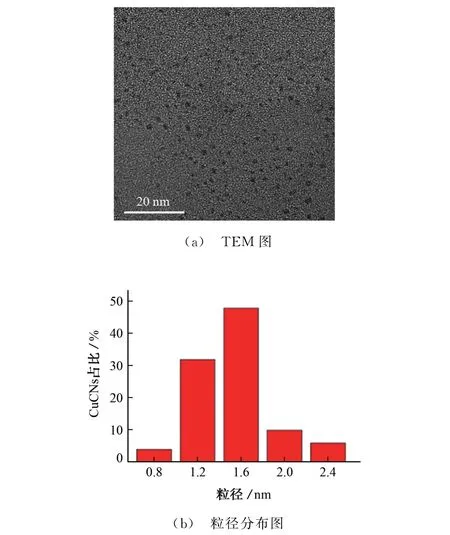
图2 Cu NCs的TEM 图和粒径分布图Fig.2 TEM and particle size distribution of Cu NCs
为进一步探讨Cu NCs表面官能团及其组成,对其XPS能谱图和FTIR 图进行分析,结果见图3。
由Cu NCs全谱图[图3(a)]可知,Cu NCs含铜、硫、碳、氮、氧等元素;Cu 2p的高分辨谱图[图3(b)]在932.8,952.6 eV 处的两个拟合峰分别对应Cu(0)的2p3/2和2p1/2[12],表明Cu NCs核中存在Cu(0);从Cu NCs的FTIR 图[图3(c)]可看到,L-半胱氨酸中2 551 cm-1处S-H 键的拉伸振动在Cu NCs中消失,表明铜与L-半胱氨酸中硫相互作用形成Cu-S键。以上结果表明Cu NCs已生成。

图3 Cu NCs的XPS能谱图和FTIR 图Fig.3 XPS energy spectra and FTIR spectra of Cu NCs
2.3 选择性和干扰试验
按照1.2.2节试验方法,考察了常见金属离子(K+、Na+、Zn2+、Ca2+、Mg2+、Mn2+)、氨基酸[L-赖氨酸(L-Lys)、L-异亮氨酸(L-Iso)、L-缬氨酸(LVal)、L-苯丙氨 酸(L-Phe)]、维 生素[维生素B3(VB3)、维生素B6(VB6)]、食品添加剂[安赛蜜(AP)、苯甲酸(BA)、柠檬酸(CA)、烟酰胺(NC)、山梨酸钾(PS)、二乙酸钠(SD)、六偏磷酸钠(SH)、肌糖、糖胶、蔗糖、葡萄糖]对F/F0的影响(各物质浓度均为60.00μmol·L-1),结果见图4。
由图4可知,除日落黄外,加入其他物质后,F/F0均接近1.0,表明Cu NCs对日落黄选择性好。

图4 Cu NCs对不同物质的选择性Fig.4 Selectivity of Cu NCs to different materials
接着在Cu NCs和日落黄混合溶液中分别加入上述物质(Cu NCs质量浓度为0.33 g·L-1,日落黄浓度为60.00μmol·L-1,其他干扰物浓度均为600.00μmol·L-1)。结果显示,加入干扰物后,F/F0基本保持不变,表明Cu NCs检测日落黄的抗干扰能力较强。
2.4 荧光猝灭机理
Cu NCs的激发、发射光谱(λex、λem)与日落黄的紫外-可见吸收光谱展现部分重叠[图5(a)],表明日落黄对Cu NCs的荧光猝灭可能由内滤效应(IFE)和/或Förster共振能量转移(FRET)引起的[13]。
若日落黄对Cu NCs的荧光猝灭是由IFE引起的,IFE抑制效率由下式估算:
式中:CF为校正因子;Aex和Aem分别为加入日落黄后体系在370 nm 和490 nm 处的吸光度;d、g、s分别为1.00,0.40,0.10 cm[12];Fobsd为加入日落黄后实测的体系荧光强度;Fcor为加入日落黄后校正的体系荧光强度;Fobsd,0为不加入日落黄时实测的体系荧光强度;Fcor,0为不加入日落黄时校正的体系荧光强度;Eobsd和Ecor分别为实测和校正的体系荧光强度比值。
加入不同浓度日落黄标准溶液后,Eobsd和Ecor见图5(b)。

图5 紫外-可见吸收光谱,激发、发射光谱和日落黄对Cu NCs的抑制效率Fig.5 UV-Vis absorption spectra,excitation and emission spectra,and suppressed efficiency of sunset yellow to Cu NCs
结果表明,日落黄对Cu NCs的IFE 抑制效率高达总抑制效率的90%,表明日落黄对Cu NCs的荧光猝灭机理主要来自IFE。
2.5 标准曲线和检出限
按照1.2.2节方法进行试验,加入0,2.00,3.33,6.67,10.00,13.33,16.67,20.00,23.33,26.67,30.00,33.33,36.67,40.00,43.33,46.67,50.00,53.33,56.67,60.00,63.33μmol·L-1日落黄标准溶液后的荧光光谱图见图6。
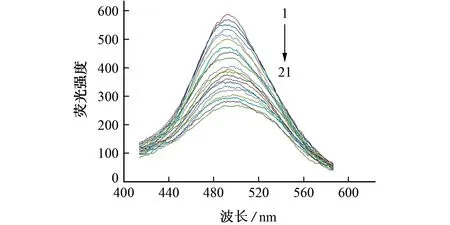
图6 加入不同浓度日落黄标准溶液后荧光光谱图Fig.6 Fluorescence spectra after adding different concentrations of sunset yellow standard solutions
结果显示,体系在490 nm 处的荧光强度随日落黄浓度的增大逐渐减小,且最大发射峰位置基本不变。日落黄浓度在2.00~60.00μmol·L-1内与F/F0呈线性关系,线性回归方程为F/F0=-0.007 889c+0.947 3,相关系数为0.996 7。
连续测定11次不加入日落黄时体系在490 nm处的荧光强度,以3倍标准偏差(s)与线性回归方程斜率(k)的比值计算方法检出限(3s/k),结果为1.31μmol·L-1。
2.6 样品分析和回收试验
按照试验方法对矿泉水和饮料进行分析,并对其进行回收试验,计算回收率和测定值的相对标准偏差(RSD),结果见表1。
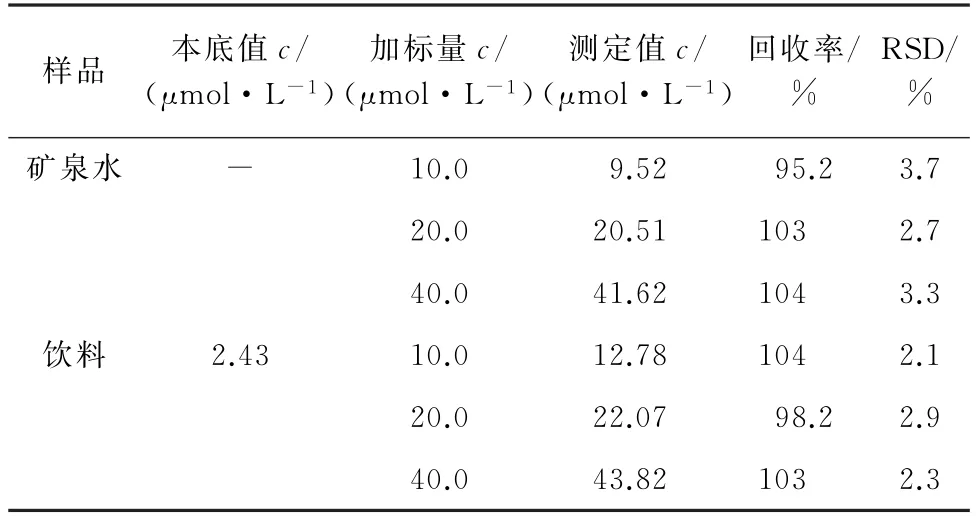
表1 样品分析和回收试验结果(n=5)Tab.1 Results of the sample analysis and test for recovery(n=5)
结果显示,矿泉水中未检出日落黄,两个样品中日落黄的回收率为95.2%~104%,测定值的RSD为2.1%~3.7%,表明本方法能准确检测样品中的日落黄。
本工作采用简单的一步法合成Cu NCs,将其作为荧光探针,采用荧光分光光度法测定矿泉水和饮料中日落黄的含量,同时讨论了日落黄对Cu NCs的荧光猝灭机理。该方法具有较好的选择性、较低的检出限和较高的精密度,并且操作简单、制备成本低,可用于矿泉水和饮料中日落黄的检测。

