‘锦斛1号’铁皮石斛对干旱胁迫的生理响应
杨秋悦 ,罗影子 ,杨 洋 ,文大成 ,阮宝丽 ,王大昌 ,杨 渊 ,黄明进 *
(1.贵州大学 农学院,贵州 贵阳 550025; 2.贵州大学 石斛研究院,贵州 贵阳 550025;3.贵州省药用植物繁育与种植重点实验室,贵州 贵阳 550025)
铁皮石斛为兰科植物铁皮石斛(Dendrobium officinaleKimura et Migo)的干燥茎[1]。在《神农本草经》、《名医别录》、《本草纲目》等古代中药典籍中均有收录,具有养胃生津,滋阴清热等功效,为九大仙草之首,药界有“北有人参,南有石斛”之说[2]。干旱胁迫下,植物在形态结构和生理生化特征方面对干旱的响应主要包括生长发育、形态适应特征、光合作用、抗氧化酶活性、渗透调节物质、内源激素含量变化以及干旱诱导蛋白等[3]。轻度的干旱有利于根系的延伸生长[4],严重干旱条件下,植物根系活力降低,根系的数目和水压传导能力被抑制,从而进一步影响整个植物的生长[5],并且随着干旱胁迫程度的加剧,植物会因为根系活力不足以维持生命而受到不可逆转的伤害,甚至彻底死亡[6]。在干旱或盐胁迫等逆境条件下,植物受到渗透胁迫,通常会合成一类小分子质量、高度可溶的物质,如甜菜碱、多胺、脯氨酸、海藻糖和甘露糖等物质能维持细胞正常渗透压水平、保护细胞蛋白质活性和细胞膜结构[3,7]。轻度干旱下,脯氨酸(Proline,Pro)含量的积累有利于渗透调节,但随着干旱胁迫程度加深,Pro含量的多少可能是胁迫伤害程度大小的指标[8]。一般来说,干旱胁迫下植物体内的超氧化物歧化酶(Superoxide dismutase,SOD)活性与抗氧化能力呈正相关[9];过氧化氢酶(Catalase,CAT)与SOD协同作用可清除体内具有潜在危害的O2和过氧化氢(H2O2);过氧化物酶(Peroxidase,POD)在逆境初期清除H2O2,表现为保护效应[3]。前人研究发现在干旱胁迫下,铁皮石斛组培苗的游离脯氨酸增多、丙二醛增加、叶片SOD、POD、CAT酶活性均呈现先增加后下降的趋势,且胁迫处理高于正常水分对照[10]。本试验对‘锦斛1号’品种受水分胁迫的生理生化变化进行探究。‘锦斛1号’是从浙江雁荡山产区种群中选出并于2020年认定的品种,其特征性稳定性一致,一年生植株每丛具13 ~ 22条茎秆,向光面紫红色,茎有灰白色叶鞘包被,茎节8 ~ 15个,茎长13 ~ 20 cm,茎粗0.58 cm左右,每条茎秆上具10 ~ 15朵花。本研究探究基质不同水分含量对‘锦斛1号’生长、渗透调节物质含量、丙二醛含量及抗氧化酶活性的变化的影响,探讨‘锦斛1号’对干旱胁迫的耐受性,以期为铁皮石斛抗旱育种提供理论依据,且为‘锦斛1号’栽培及水分管理措施提供实验和理论依据。
1 材料与方法
1.1 材料与试验设计
石斛材料来自于中国浙江省乐清,选育培育于中国贵州省锦屏县的铁皮石斛‘锦斛1号’,经贵州大学黄明进副教授鉴定为兰科植物铁皮石斛。
该干旱胁迫试验于2021年8 ~ 9月在贵州大学石斛研究院进行,试验设计参照裴忠孝[11]、巫晓璐[12]的方法:依据基质含水量的不同设置4个梯度:(1)重度干旱胁迫(L):25% ~ 30%;(2)中度干旱胁迫(M):40% ~ 45%;(3)轻度干旱胁迫(H):55% ~60%;(4)湿润水分处理(B):70% ~ 75%,每个处理20个重复,挑选长势一致的一年生石斛苗,整丛移栽于深17 cm、内径22 cm的白色塑料花盆中,所用基质为树皮、木屑,材料均一。盆栽于电子秤上称重浇水,先浇至饱和含水量再逐步控制其达到所设定的水分条件,每天于下午17:00对各花盆进行称重,并补充水分使达到所设定的水分范围(所浇的水为沉淀后的清水)。当不同的水分处理达到设定条件后,于10、20、30 d对植株进行采样,每个处理采3丛,测定生理生化指标。
饱和含水量以栽培基质含水量达到饱和状态为准,基质含水量=× 100%
1.2 测定内容与方法
1.2.1 株高的测定
每丛用直尺测定3株长势均一的单株其根部至顶叶基部的长度,精准到小数点后一位,单位为厘米(cm)。
1.2.2 茎粗的测定
每丛用游标卡尺测定3株石斛中部茎秆最粗的部位,精准到小数点后两位,单位为毫米(mm)。
1.2.3 叶片含水量的测定
叶片含水量采取植物的由上至下的第4片叶片测定。采集石斛的叶片,并迅速放至密封袋中避免其水分散失。用电子天平记录叶片鲜重,然后将其放置105℃的烘箱内,杀青10 min,然后调节温度至65℃,烘干直至叶片重量不变,记录其干重[12]。
1.2.4 根系活力的测定
用氯化三苯基四氮唑(TTC)法测定根系活力,用分光光度计在485 nm下比色,以空白试验调零,测定吸光值,查标准曲线,求出四氮唑的还原量[13]。
1.2.5 叶绿体色素的测定
用96%乙醇研磨法测定,以96%乙醇为空白,在波长665、649和470 nm下测定吸光度,按下列公式计算叶绿素a、叶绿素b、类胡萝卜素的的浓度[13]。
1.2.6 抗氧化酶活性的测定
‘锦斛1号’叶片的CAT活性用紫外吸收法测定(以每克组织每分钟催化1 μmol H2O2降解定义为一个酶活力单位),SOD活性用氮蓝四唑法测定(以每克组织在每毫升体系中SOD抑制率达50%时所对应的SOD量为一个酶活单位),POD活性用愈创木酚法测定(以每克组织在每毫升体系中每分钟A470变化0.01为一个酶活力单位),称取0.1 g新鲜叶片,利用试剂盒进行测定,试剂盒购自北京盒子生工科技有限公司。
1.2.7 渗透调节物质的测定
‘锦斛1号’叶片的丙二醛(Methylene dioxyamphetamine,MDA)含量采用硫代巴比妥酸显色法测定,脯氨酸(Pro)的含量采用酸性茚三酮比色法利用试剂盒进行测定,试剂盒购自北京盒子生工科技有限公司。可溶性蛋白含量采用考马斯亮蓝G-250法[14]、可溶性糖含量采用蒽酮-硫酸法[15]。
1.3 统计分析
采用Excel 2010整理数据,SPSS 26.0对数据进行方差分析、多重比较,Prism 9.3.1进行绘图。
2 结果与分析
2.1 不同水分处理在不同时期对‘锦斛1号’株高、茎粗、叶片含水量及根系活力的影响
对不同水分处理下不同时期‘锦斛1号’的株高、茎粗、叶片含水量及根系活力进行分析见表1。可知各水分处理下不同时期的‘锦斛1号’株高、茎粗无显著差异,水分胁迫组与对照组相比叶片含水量的差异不明显;对于不同水分处理下的根系活力干旱胁迫10 d时,L、M、H组分别比B组增强12.34%、降低17.95%、增强2.47%;干旱胁迫20 d时,L、M、H组分别比B组降低29.49%、16.84%、12.08%;干旱胁迫30 d时,L、M、H组分别比B组增强了40.95%、24.83%、2.23%,其中水分含量为55%~60%时10 d与20 d、30 d的根系活力间存在显著差异,其存在大幅度下降。
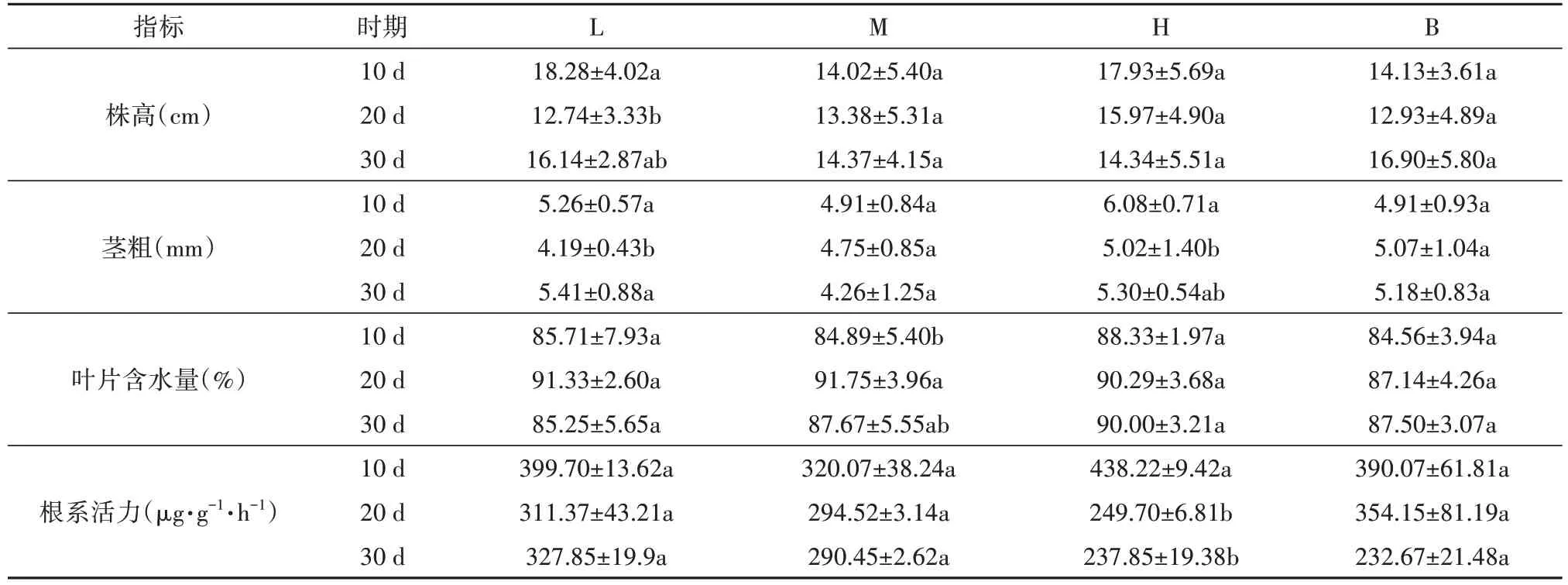
表1 不同水分处理对‘锦斛1号’株高、茎粗、叶片含水量及根系活力的影响Tab.1 Effects of different water treatments in different periods on plant height, stem diameter, leaf water content and root activity of‘Jinhu NO.1’
2.2 不同水分处理在不同时期对‘锦斛1号’叶绿体色素的影响
对不同水分处理下不同时期‘锦斛1号’的叶绿体色素含量进行分析见表2。可知在不同水分处理下,随着水分的增多叶绿体色素也增多,叶绿素a、叶绿素b、类胡萝卜素及色素总量具有一致的变化趋势,随时间延长,L、H、B组叶绿素总量呈上升趋势,M组呈下降趋势。其中叶绿素a在H 30 d和B 20 d时达到峰值,叶绿素b在H 30 d时达到峰值,类胡萝卜素在B 20 d时达到峰值,叶绿体色素总量在H 30 d、B 20 d时达到峰值,可知水分对叶绿体色素含量的影响较大,随着水分的减少,叶绿体色素也减少。

表2 不同时期不同水分处理对‘锦斛1号’叶绿体色素的影响Tab.2 Effects of different water treatments in different periods on chloroplast pigments of ‘Jinhu No.1’
2.3 不同水分处理在不同时期对‘锦斛1号’抗氧化酶活的影响
对不同水分处理下不同时期‘锦斛1号’抗氧化酶活进行分析,如图1所示。对于CAT酶活,随着水分减少,CAT酶活先增强后下降,当达到重度干旱处理后,CAT酶活明显下降,但随着处理时间的延长,CAT酶活性增强,L 30 d比L 10 d增强了58.54%,M 30 d比M 10 d增强68.51%,H 30 d比H 10 d增强30.71%,B 30 d比B 10 d增强71.83%。在10 d时,H组的CAT酶活显著高于其他组。对于POD酶活,随着水分的减少其先降低后升高,当达到重度干旱后,POD酶活增强来抵御干旱,在30 d时,B组间与其他组间的POD酶活存在显著差异。对于SOD酶活,随着处理时间的延长,SOD酶活呈总体上升趋势,干旱胁迫10 d时,L、M、H组分别比B组增加5.07%、2.55%,降低23.9%;干旱胁迫20 d时,L、M、H组分别比B组增强9.35%、14.75%、38.42%;干旱胁迫10 d时,L、M、H组分别比B组增强12.94%、降低29.84%、增强3.43%。

图1 不同水分处理对‘锦斛1号’抗氧化酶活性的影响Fig.1 Effects of different water treatments on antioxidant enzyme activity of ‘Jinhu No.1’
2.4 不同水分处理在不同时期对‘锦斛1号’渗透调节物质及丙二醛含量的影响
对不同水分处理下不同时期‘锦斛1号’渗透调节物质含量进行分析,如图2所示。随着水分的减少,丙二醛含量呈下降趋势,随着处理时间的延长,其含量呈先增多后减少趋势,证明水分充足时其丙二醛含量较高;随着水分的减少,脯氨酸含量先是增多,但当超过限度后,即水分≤ 40%~45%,脯氨酸含量转而下降,且随着处理时间的延长,脯氨酸含量呈下降趋势;对于可溶性蛋白含量而言,在水分胁迫初期,随着水分的减少,可溶性蛋白增多,但随着处理时间延长,到30 d时,水分的减少使可溶性蛋白含量大幅降低,B组与其他组间存在显著差异;对于可溶性糖含量而言,随着水分含量的减少,其含量逐渐增加,随着处理时间的延长,其含量呈先下降后上升趋势。

图2 不同水分处理对‘锦斛1号’渗透调节物质的影响Fig.2 Effects of different water treatments on Osmoregulation Substances of ‘Jinhu No.1’
2.5 不同水分处理下不同时期‘锦斛1号’生理生化指标的相关性
对不同水分处理下‘锦斛1号’的根系活力、叶绿素含量、CAT活性、SOD活性、POD活性、MDA含量、Pro含量、可溶性糖含量、可溶性蛋白含量9个指标进行相关性分析如表3所示。可知根系活力与CAT活性呈极显著负相关,与脯氨酸和可溶性蛋白含量呈显著正相关;CAT活性与POD活性呈极显著负相关;丙二醛含量与可溶性糖含量呈显著负相关。

表3 不同时期不同水分处理下‘锦斛1号’生理生化指标相关性分析Tab.3 Correlation analysis of physiological and biochemical indexes of ‘Jinhu No.1’ under different water treatment in different periods
3 结论与讨论
叶片相对含水量关系着叶片的生理功能,是植物在遭受逆境胁迫下保水能力的一个重要指标[16]。在阔叶树种幼苗对干旱胁迫的研究中证明,当达到重度胁迫时叶片的相对含水量仍能维持在较高的水平,表示抗旱能力较强[17]。对水稻进行研究发现,不同叶位叶片含水量受到水分胁迫时,拔节期叶片含水量呈第一叶<第二叶<第三叶<第四叶,随胁迫时间的推移,灌浆期不同水分处理间叶片含水率变化规律出现差异[18]。本研究选取第4叶进行测定,达到重度干旱后叶片含水量也并未大幅下降,或许是由于不同叶位的叶片含水量存在差异,故可能因此受干旱胁迫影响小,从叶片含水量变化幅度可反映出‘锦斛1号’的抗旱能力较强,受水分胁迫影响小。前人研究发现随着干旱胁迫程度的加重,植物根系活力显著增强[19],本研究反映出随着水分的减少,‘锦斛1号’的根系活力显著增加,随着时间的延长,根系活力减弱,这或许与裸果木幼苗研究结果相同,通过降低代谢强度来抵御和适应干旱胁迫[20]。叶绿素是植物进行光合作用的主要色素,植物叶片内叶绿素含量的高低在一定程度上可以衡量植物抗逆性强弱[21]。本研究中,随着干旱胁迫的加重,叶绿体色素减少,但在轻度干旱下,叶绿体色素略有增加,说明轻度干旱对光合能力的影响不大,但在中度及重度干旱下,或许是因为叶片的叶绿素合成速度小于降解速度,其含量会明显下降。
干旱条件下的植物体内会产生大量的活性氧,使细胞膜被破坏,同时加速细胞的衰老和解体[17]。POD在逆境或衰老的后期,参与活性氧的生成、叶绿素的降解,并能引发膜脂过氧化作用,表现为伤害效应,是植物体衰老到一定阶段的产物,甚至可作为衰老指标[22]。本研究中,SOD活性受水分胁迫影响在初期及后期均呈上升趋势,随着胁迫强度的增大,CAT活性呈现先上升后下降的趋势,POD活性是先下降后上升,可能是由于到了胁迫中后期,抗氧化酶系统被破坏,代谢失调[23]。MDA含量可反映植物组织内脂质过氧化的程度,间接反映细胞膜损伤程度,其含量越高说明细胞膜受损越严重,抗逆境胁迫能力越弱[24-25]。本研究显示,随着干旱胁迫的加重,POD活性和MDA含量都呈下降趋势,说明‘锦斛1号’抵御干旱的能力较强,在重度胁迫下仍具有自我调整能力。前人研究证明随着干旱胁迫或淹水程度的加深[26],MDA含量增加,本研究在20 d处理时呈现这一趋势,但其余时期呈下降趋势。
脯氨酸和可溶性蛋白作为植物体内主要的渗透调节物质,可以有效清除植物体内的活性氧自由基,提高其抗氧化能力,从而提高植物抗逆性[27]。植物体内可溶性糖是渗透调节物质,及细胞内重要有机溶质,可调节谷子对不利环境(如干旱胁迫)的适应能力[28],也可以增大细胞原生质浓度,进而增强植物的抗旱性[29]。本研究中脯氨酸随着胁迫程度的加重呈下降趋势,可溶性糖呈上升趋势,可溶性蛋白在胁迫初期呈上升趋势,但各组间差异不显著与前人在豹皮樟扦插苗中研究结果相同[30]。综合各指标可知在胁迫后期植株的POD酶活下降,CAT、SOD酶活上升,MDA、脯氨酸、可溶性蛋白呈下降趋势,可溶性糖呈上升趋势,证明植株保水能力降低。
综合各指标可知,‘锦斛1号’在中度干旱胁迫时,即基质水分含量40% ~ 45%时所受影响并不大,因此,在生产中可以将基质水分含量控制在这一范围内,减少浇灌的水分,减少生产成本,且通过对‘锦斛1号’在干旱胁迫下生理生化指标的分析,证明铁皮石斛具有一定的抗旱性,可在今后的研究中更深入的挖掘其抗旱机理,进行抗旱品种的选育,增加其适生性。本试验仅对干旱胁迫下‘锦斛1号’的生理生化指标进行了测定,未来还应进一步对其品质指标(如多糖、黄酮等)进行测定,以期为‘锦斛1号’的栽培管理措施提供更全面的理论依据。

