淮北市HCV感染者基因亚型分布特征及1b型天然耐药突变分析
木朝宇,张晓梅,范德胜,2,刘培明,姚慧琳
慢性丙型病毒性肝炎(chronic viral hepatitis C,CHC) 是一种由丙型肝炎病毒(hepatitis C virus,HCV)感染引起的病毒性肝炎,可导致肝脏慢性炎症坏死和纤维化,部分病人可发展为肝硬化甚至肝细胞癌,已成为严重的社会和公共卫生的问题[1-2]。我国HCV的感染约有1 000万例[3]。HCV基因易变异,在已报道的HCV 7个基因型中,中国发现的有1、2、3和6型[4]。HCV基因型及亚型的检测是直接抗病毒药物(direct antiviral agent,DAA) 治疗方案的基础,即不同HCV基因型病人所采用的DAAs治疗方案以及疗程不相同[3]。因此,HCV基因型及亚型的检测在直接抗病毒治疗方案中具有重要意义。随着DAAs药物的广泛应用,尤其是单药应用时,部分病人出现耐药相关突变(ristance-associated substitutions,RASs),而且未经过任何抗病毒治疗的丙型肝炎病人体内也存在DAAs耐药突变株,即天然耐药突变[5]。本研究旨在分析安徽省淮北地区HCV感染者基因亚型的分布情况,同时检测主要流行亚型NS3/4A、NS5A和NS5B的DAAs靶点RASs,以了解该地区HCV基因亚型的流行特征及主要亚型的天然耐药情况,为本地区HCV感染防控和临床个体化抗病毒治疗提供理论依据。
1 资料与方法
1.1 一般资料 选取2019-2022年就诊于淮北矿工总医院住院的HCV-RNA阳性HCV感染者(未经任何DAAs治疗)血清130例。其中男82例,女48例,年龄25~88岁。以上所有CHC诊断符合我国《丙型肝炎防治指南(2019版)》[3]。排除合并感染HIV或其他病毒性肝炎、酒精性肝病、自身免疫性疾病等病人。血清标本-70 ℃保存备用。
1.2 方法
1.2.1 HCV-RNA抽提 采用中山大学达安基因股份有限公司提供的核酸柱提取试剂盒,操作步骤参照试剂盒说明书。
1.2.2 RT-PCR 采用Thermo Fisher Scientific公司生产的RevertAid First Strand cDNA Synthesis Kit(货号:K1622)进行逆转录,步骤参照试剂盒说明书。
1.2.3 HCV基因分型、RASs检测 采用巢式PCR进行HCV基因分型、RASs检测。PCR引物见表1,扩增条件均参考文献[4,7-8],其中NS5B区PCR条件:94 ℃ 5 min,94 ℃ 30 s、58 ℃ 30 s、72 ℃ 1 min、35个循环,72 ℃ 5 min;第二轮与第一轮PCR条件相同;NS3/4A区PCR条件:第一轮94 ℃ 5 min,94 ℃ 1 min、55 ℃ 60 s、72 ℃ 70 s、35个循环,72 ℃ 10 min,第二轮94 ℃ 5 min,94 ℃ 1 min、52 ℃ 60 s、72 ℃ 70 s、35个循环,72 ℃ 10 min;NS5A区PCR条件:第一轮94 ℃ 5 min,94 ℃ 30 s、58 ℃ 30 s、72 ℃ 2 min、35个循环,72 ℃ 10 min,第二轮94 ℃ 5 min,94 ℃ 30 s、65 ℃ 30 s、72 ℃ 1.5 min、35个循环,72 ℃ 10 min。PCR产物在2.5%的琼脂糖凝胶进行电泳后测序。PCR引物合成及产物测序均由上海生工生物工程股份有限公司完成。
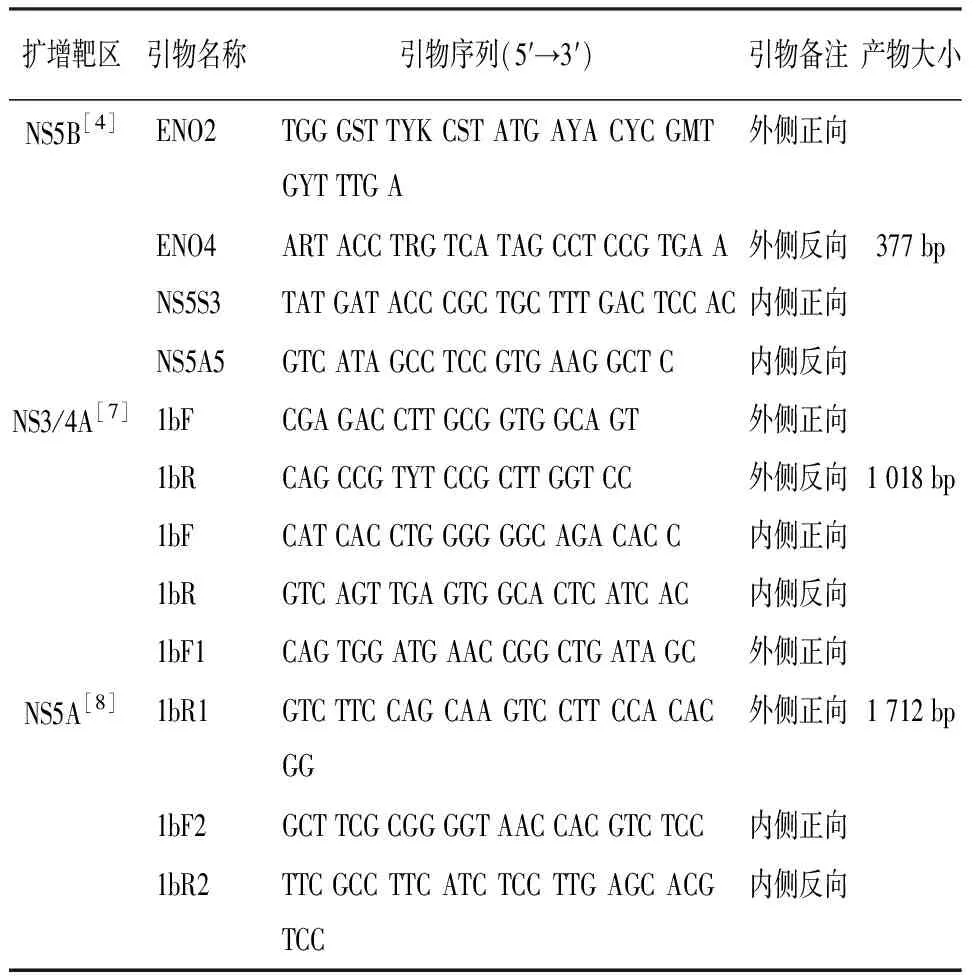
表1 HCV基因各亚型引物名称及序列
1.2.4 序列比对与分析 从GenBank下载HCV 1b型标准序列株(AJ238799.1),采用Mega.11软件进行NS5B、NS5A及NS3/4A区的序列比对分析。
1.3 统计学方法 采用χ2检验。
2 结果
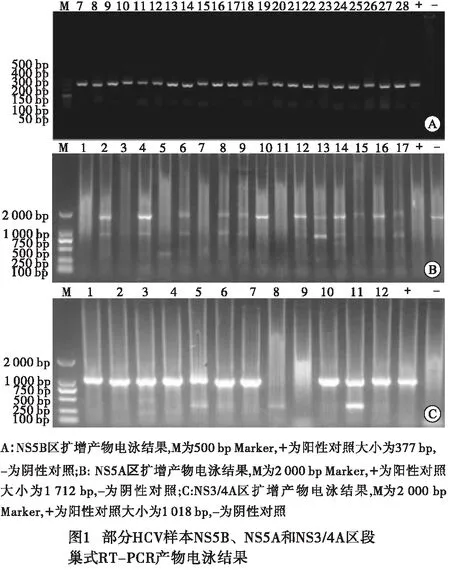
2.1 HCV基因亚型分布特征 130例HCV感染者中有102例样本NS5B区扩增成功,扩增成功率为78.46%,NS5B区段扩增PCR产物片段大小377 bp,电泳结果见图1A。PCR产物经测序分析后,其中1b型70例(68.63%),2a型30例(29.41%),3a型2例(1.96%),其他型别未检出。1b型为HCV流行的优势亚型,2a型次之;HCV 1b、2a型男女感染分布差异无统计学意义(P>0.05)(见表2)。
2.2 HCV基因亚型分布与年龄的关系 本研究中HCV感染者按年龄分为<55岁和≥55岁组,HCV基因型在2个年龄组中的分布差异无统计学意义(P>0.05)。HCV 1b型的CHC病人多见于≥55岁年龄组中。HCV 1b型与非1b型在2个年龄组中分布差异无统计学意义(P>0.05)(见表3)。
2.3 HCV 1b型NS5B、NS5A及NS3/4A区RASs发生情况 70例1b亚型样本中,NS5B区全部扩增成功(见图1A),扩增成功率100.00%,70例均检出NS5B相关耐药位点突变,突变率100%;NS5A区扩增成功42例(产物大小1 712 bp,见图1B),占60.00%,其中28例检出NS5A相关耐药位点突变,突变率66.67%;NS3/4A区扩增成功68例(产物大小1 018 bp,见图1C),扩增成功率97.14%,64例检出NS3/4A相关耐药位点突变,突变率94.12%。NS5B区主要RASs类型:C316N(70例,100.00%);NS5A区主要RASs类型:Q54H(17例,40.47%)、Y93H(8例,19.05%);NS3/4A区RASs类型:Q86P(21例,30.88%)、I71V+Q86P(13例,19.12%)、V170I+Q86P(10例,14.71%)及T72I/A+Q86P(9例,13.24%)(见表4、5)。其中NS3/4A区突变频率较高的RASs依次为:Q86P(53.78%)、I71V/S(15.97%)、V170I(10.92%)及T72I/A(10.08%);NS5A区突变频率较高的RASs依次为:Q54H(60.00%)、Y93H(33.33%);NS5B区突变频率较高的为C316N(100.00%)。
表2 102例HCV感染者基因亚型分布[n;百分率(%)]

表3 HCV基因亚型在年龄中的分布情况[n;百分率(%)]
3 讨论
本研究明确了淮北市HCV亚型流行特征:以1b型为主,2a型次之,此外首次检出3a型(2例,1.96%)。这与国内HCV亚型的流行情况基本相符[3]。HCV亚型的分布在性别、年龄上无明显差异(P>0.05),与国内的报道[9]不尽相同,其中HCV 1b型的HCV感染者多见于≥55岁年龄组中,2a型在2个年龄组中均常见。2例3a型的病人均分布在<55岁年龄组。
目前NS5A、NS5B及NS3/4A区域是DAAs治疗的主要靶点。随着DAAs广泛应用,有部分丙肝病人体内存在针对NS5A、NS5B及NS3/4A抑制剂的天然耐药位点突变,会影响抗病毒治疗的疗效[6-8,10-11]。NS5A抑制剂主要有Daclatasvir、Ledipasvir、Qmbitasvir、Elbasvir及Velpatasvir等,主要RASs包括L31M和Y93H突变,其中L31M主要是对Ledipasvir耐药,对Daclatasvir可能耐药,而Y93H对Daclatasvir、Ledipasvir和Qmbitasvir均明显耐药。H58P和P58S主要针对Daclatasvir耐药,Q54H主要是Daclatasvir和ABT-267的耐药[8];本研究中HCV1b型NS5A相关耐药位点突变率66.67%,远高于伍菲菲等[8,12]报道的46.0%、22.4%,推测以上结果可能是HCV基因型分布的地域差异性导致。NS5A区主要突变为Q54H(40.47%)、Y93H(19.05%),其中Y93H突变率远高于SUN等[12]报道的6.6%、15.5%的结果。此外,不同的是,本研究未检测出L31M突变,检出的联合突变为Q54H+Y93H、P58S+Y93H。这些联合突变是否会增加抗病毒药物疗效的影响,还有待于进一步研究。
NS5B抑制剂主要包括核苷类聚合酶抑制剂Sofosbuvir和非核苷类聚合酶抑制剂Dasabuvir,RASs主要包括S282T、C316N等;其中S282T是索磷布韦的重要耐药位点,C316N被认为是引起病人未达到持续病毒学应答的原因之一[6]。本研究中HCV 1b亚型NS5B区域C316N为100.00%,均未发现S282T,这与国内的相关报道[6]一致。而HCV C316N出现选择性变异与HCV-796治疗的病人后迅速出现病毒反弹有关[11],提示日后应用该药时易出现耐药,也提示联合药物治疗的必要性。
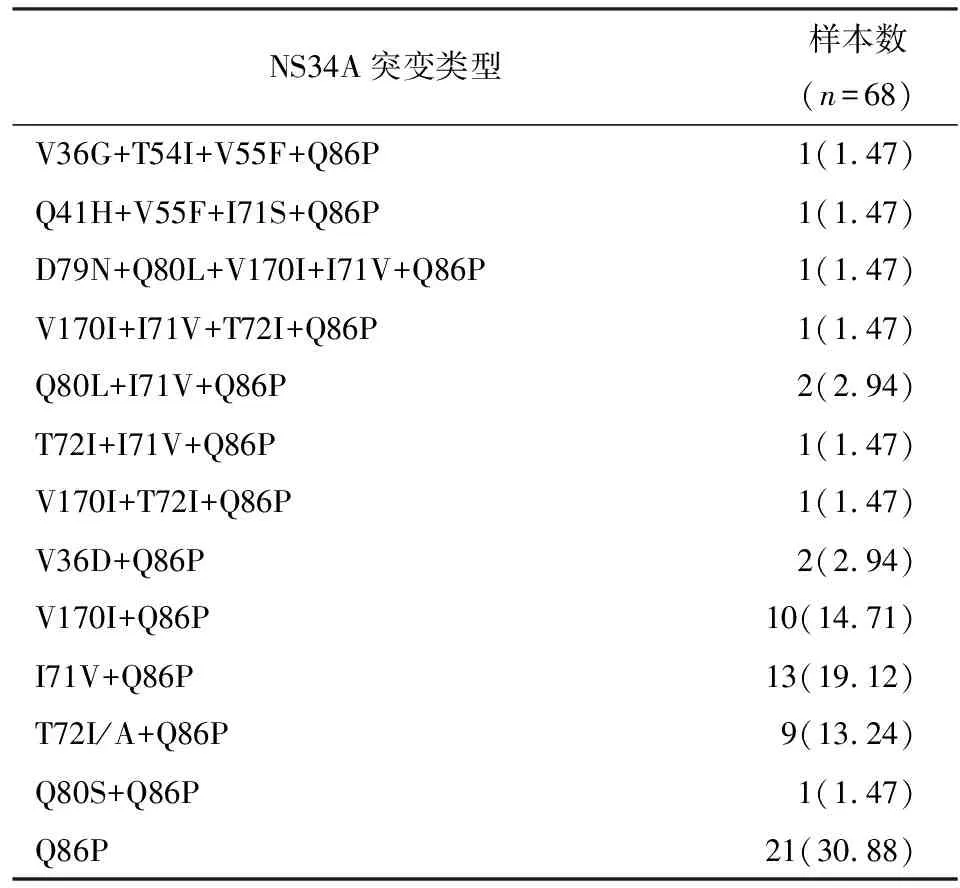
表4 68例HCV感染者NS3/4A耐药相关突变情况[n;百分率(%)]

表5 42例HCV感染者NS5A耐药相关突变情况[n;百分率(%)]
NS3/4A抑制剂主要有Telaprevir、Roceprevir、ITMN191、SCH900518及TMC435等,主要RASs包括V36G、V55F、I71V/L、T72I/A/L、Q80N、Q86P、V170A/T及M175L等,其中V36、V55F及V170A/T与Telaprevir、Roceprevir耐药相关,M175L与Boceprevir耐药相关,Q80N与TMC435耐药相关等[7,10]。
本研究中HCV lb型NS3/4A耐药相关位点突变率为94.12%,远高于国内李展翼等[10]报道的38.33%。68例HCV型样本中NS3/4A区以联合突变为主,最多可达五重突变,均存在Q86P变异。NS3/4A区RASs主要为低-中度耐药的变异,如V36L、T54S、Q80P、Vl70I等,未检出致高度耐药的主要变异Al56S及Rl55Q[7,10],多位点耐药联合突变的现象是否会增加对抗病毒药物的影响还需进一步研究。此外,本研究还提示淮北市HCV 1b型突变频率较高的天然耐药突变位点依次为:C316N(100.00%)、Q54H(60.00%)、Q86P(53.78%)、Y93H(33.33%)及I71V/S(15.97%)。这提示该地区感染HCV 1b型病人DAAs替换治疗时候应对以上位点耐药相关的药物引起注意,避免和减少耐药的发生。
综上所述,淮北市未经过抗病毒治疗HCV感染病人以1b型为主,2a型次之,3a型较少。其主要流行的1b型存在天然耐药位点突变。DAAs抗病毒治疗时,需要先进行基因型和RASs的检测,再制定适合的治疗方案。

