食品中菌落总数检测能力验证的结果分析与质量控制
李文绮,谷天雨,李自芹
(1.石河子质量与计量检测所,新疆 石河子 832000;2.新疆生产建设兵团质量技术评价中心,新疆 乌鲁木齐 830000;3.新疆农垦科学院农产品加工研究所,新疆 石河子 832000)
能力验证是考核实验室检测能力的有效手段,通常预先制定好相应的计划和实施方案,利用试验室间比对或者测量审核,以评价各参加者的能力[1-2]。
菌落总数(Aerobic plate count),是指待检样品经过一定的处理(通常是采用无菌磷酸盐缓冲液或无菌生理盐水进行10倍梯度稀释),在特定的环境条件中进行培养后,1 g或1 mL样品中形成的细菌菌落总数量[3],是一个统称,包含各种各样的细菌。当食品中的细菌超标,就会危害人体的健康,因此在食品检验中,菌落总数通常是非常重要的微生物指标,其准确测定和计数对把控食品安全质量具有重要的意义。于2020年和2021年参加由中国检验检疫科学研究院测试评价中心组织的食品中菌落总数的检测能力验证,现将连续2年的试验操作和结果及由此获得的经验总结分享如下。
1 材料与方法
1.1 测试样品
能力验证测试样品见表1。
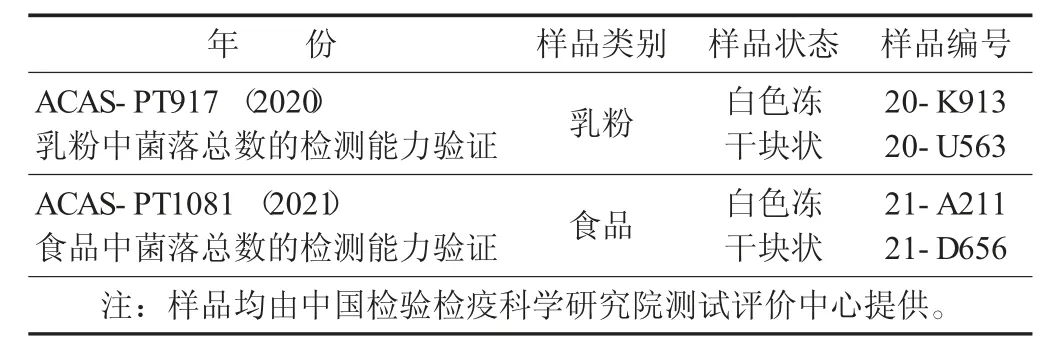
表1 能力验证测试样品
1.2 仪器与试剂
JE3002型电子天平(0.01 g),上海浦春计量仪器有限公司产品;YXQ-LS-50SⅡ型和YXQ-LS-70A型立式压力蒸汽灭菌器2台、BSC-1300ⅡA-B3型生物安全柜、BSP-150型生化培养箱,上海博迅实业有限公司医疗设备厂产品;DZKW-D-6型电热恒温水浴锅,北京市永光明医疗仪器有限公司产品;Talboys型旋涡混合器,美国公司产品;PHS-3C型酸度计,上海仪电科学仪器股份有限公司产品。
0.85%的无菌生理盐水(氯化钠AR),天津市致远化学试剂有限公司提供;平板计数琼脂(BR),北京奥博星生物技术有限责任公司提供。
1.3 检验方法
依据GB 4789.2—2016《食品安全国家标准食品微生物学检验菌落总数测定》[3]和测试样附带的参试指导书(ACAS-PT917(2020)乳粉中菌落总数的检测能力验证参试指导书、ACAS-PT1081(2021)食品中菌落总数的检测能力验证参试指导书)的要求进行检测。
1.4 检验步骤
1.4.1 样品接受与制备
(1)样品接受。实验室应随时关注能力验证样品寄送情况,及时接受。接到样品后,建议立即进行检验。如不能立即检测,应严格按照参试指导书的要求先行保存(2020年乳粉样品要求的保存温度2~6℃,2021年食品样品要求的保存温度2~8℃),防止样品中原有微生物的状况发生变化[4]。
(2)样品制备。能力验证的样品一般包装于真空西林瓶内,应小心开启。开启后,立即加入5 mL稀释液(0.85%的无菌生理盐水)进行再水化,待冻干样品充分溶解后,用无菌移液管吸出放入无菌瓶中,再反复多次用稀释液清洗西林瓶内壁和瓶盖,稀释液一并转入无菌瓶中,确保瓶内待测样品尽可能被全部转入参试指导书指定体积的稀释液中(文中2次能力验证均为60 mL)。最终的混合液即为待测样品原液,将该样品原液置于旋涡混合器上充分混匀待用(从冰箱中取出的样品应先恢复至室温再进行上述操作)。
1.4.2 样品稀释
用灭菌的移液管吸取上述样品原液25 mL置于0.85%灭菌生理盐水225 mL中,旋涡混匀,制成10-1的样品匀液,再吸取10-1的样品匀液1 mL,加入到9 mL灭菌生理盐水中(移液管切勿触碰稀释液面),旋涡混匀。重复上述操作,逐级稀释成10倍系列梯度的样品匀液(每递增稀释1次,都要更换无菌移液管)。考虑到能力验证样品的复杂性,2次试验均设置9个梯度,即原液、10-1~10-8。
1.4.3 样品取样及培养
各稀释梯度(包括样品原液)各取1 mL样液加入到90 mm无菌平皿内,每个稀释度至少接2个平皿,操作时间允许的话可接4个平皿。同时,做3组空白对照(无菌室环境监测、生理盐水空白对照、平板计数琼脂空白对照)各2个平皿。加好样液后,及时将置于46℃(温度过高会影响细菌生长,过低琼脂易凝固)恒温水浴锅的琼脂培养基取18~20 mL倾注到90 mm的平皿中[5],并顺时针、逆时针转动平皿,使样液和培养基充分混匀,待琼脂凝固后再覆盖一层约4 mL培养基(防止菌落蔓延、造成计数不准)。待完全凝固后,将培养皿倒置于36±1℃生化培养箱中培养48 h。
1.4.4 菌落计数
当平板上菌落大量生长时即可进行观察,选择典型的菌落计数。菌落数小于300 CFU的平板均应记录具体的数量,大于300 CFU的可不记详细的数量,以多不可计表示。每个稀释度的菌落在计数时,综合考虑其他稀释梯度的菌落数,菌落生长的个数应与稀释度大小呈反比,理论上每个稀释度的菌落数应接近10倍的关系,若不符合上述规律,且差异比较大,在计算时,应剔除异常的平板,采用其他稀释度的2个平板平均计数。详细的计数规则参见GB 4789.2的要求[3]。
2 结果与分析
2.1 样品检测结果分析
2020年的乳粉样品,2个测试样可计数的稀释梯度为10-1,10-2,10-3,只有稀释梯度10-1,10-2的平皿,菌落数在30~300 CFU,故选择这2个稀释度的平皿菌落数进行计算。
2021年的食品样品,21-A211样可计数的稀释梯度为10-2,10-3,10-4;21-D656样可计数的稀释梯度为10-3,10-4。同样,选取菌落数在30~300 CFU的平板计数,则21-A211样以稀释梯度10-2的平皿,21-D656样以稀释梯度10-3的平皿菌落数进行计算。
连续2年的样品菌落总数检测结果见表2。

表2 连续2年的样品菌落总数检测结果
2.2 能力验证结果分析
能力验证的结果通常采用Z值(由能力验证的指定值和能力评定标准差计算实验室偏倚的标准化度量[6)]进行评价。当时,表示检测结果满意;时,表示检测结果可疑;时,表示检测结果不满意。
菌落总数的检测能力评价结果见表3。
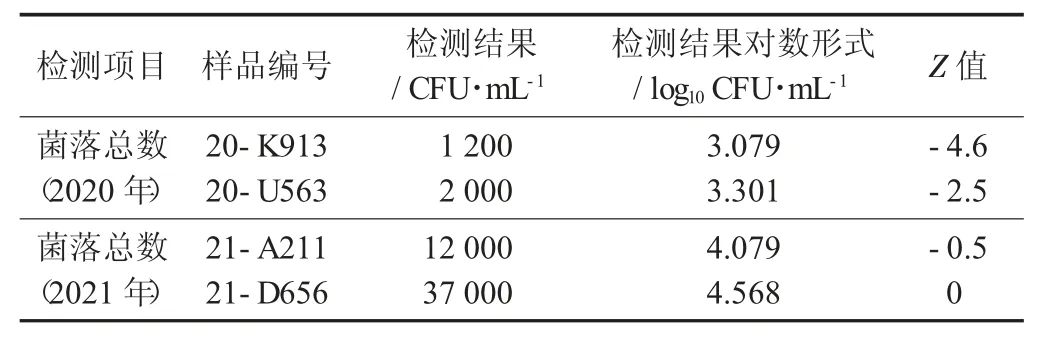
表3 菌落总数的检测能力评价结果
2.3 菌落总数检测的影响因素和质量控制分析
2020年的2个样品的检测结果均偏小,经过分析,主要存在以下几个方面的原因:①倒平板时未进行覆盖,菌落生长过程中出现蔓延,计数时存在较大的误差。②计数时对蔓延的菌落计数不规范,造成数值偏小。③对标准理解不透。虽然选取了菌落数在30~300 CFU范围的平板,但是疏忽了一个重要的附加条件——无蔓延菌落生长,导致计算公式选用错误,结果偏低。在对能力验证不满意结果认真分析之后,再次申报了2021年该项目的能力验证,并取得了满意的结果。
微生物能力验证一般不指定方法,要求各实验室优先选择常用的检测方法。
测试样品不同于平时的检验样品,具有复杂性。因此在具体的操作过程中每一个环节都要考虑到,尤其是微生物能力验证样品,其微生物多样的特性决定了很难进行多次重复试验,基本都是一次试验报送结果,这就要求从检验准备到试验结束的每一个环节都不能疏忽。严格按照国标方法及能力验证参试指导书的要求操作至关重要,同时要对试验过程每个可能存在的风险因素进行把控。
2.3.1 人员的控制
能力验证的操作人员一定是实验室检测该项目的人员,要求具备相应的微生物学知识,具有一定的操作能力,熟练掌握授权范围内的各类检测项目和参数,能独立完成下达的能力验证项目。不能请其他机构该方面的专家或者是实验室该工作岗位以外的人员承担此项工作,即使能力验证最终的结果为满意,对检测式验的外部质量控制没有任何意义,更不能体现出实验室真实的检测能力。
2.3.2 环境的控制
报名参加能力验证计划后,要随时关注能力验证组织者寄发测试样品的动态,提前对微生物实验室、生物安全柜进行空气洁净度监测,主要是沉降菌、浮游菌、悬浮粒子等参数,确保微生物实验室符合万级要求,生物安全柜符合百级要求,方可开展检测工作。无菌室的推荐温度为20℃,相对湿度为40%~60%[8]。
2.3.3 检测方法的控制
微生物能力验证一般要求各实验室优先选择常用的检测方法。通常检验人员对相关的检测方法都能熟练操作,但是有一个常被忽视的点就是能力验证参试指导书,其对样品的处理有详细的规定,是检测方法至关重要的一部分。接到能力验证样品的第一时间,一定要认真阅读参试指导书,按照相关要求处理样品,同时充分理解标准规定的检测方法,才能确保后续试验顺利进行。
2.3.4 仪器设备及试剂的控制
(1)仪器设备。试验涉及的仪器设备均应有效溯源(检定或者校准),同时相关的检验人员对所用设备进行计量确认、确保仪器的各项参数满足试验的要求。
(2)耗材及试剂。所用的耗材及试剂均应按要求进行灭菌处理(同时监测灭菌效果),确保无菌状态。最重要是培养基的制备,平板计数琼脂(PCA培养基)一般要求的pH值在7.0±0.2,一定要对pH值进行监测,配置时先煮沸溶解,调pH值到指定的范围内,分装试管或锥形瓶,于121℃下高压灭菌15 min后备用。
2.3.5 试验操作环节的控制
无菌操作:严格按照无菌操作要求进行试验,试验开始前,应对微生物实验室、生物安全柜紫外灭菌30 min换气后,试验人员穿戴好衣、帽、口罩、手套、鞋套,方可进入实验室。能力验证样品中含有活的微生物(可能含有致病菌),整个试验操作应在生物安全柜中进行。试验过程中,取用东西后,随时用75%乙醇喷洒双手,以免污染样品。
详细的检测步骤在1.4中已提及注意事项:①样品处理中若遇到难以溶解的情况,应提前将稀释液保温到与培养基接近的温度(一般为46±1℃),有利于冻干粉样品更好溶解。②样品转移过程应尽可能完全,60 mL的稀释液可分多次清洗西林瓶内壁及瓶盖。③能力验证的样品无法预估样品污染的状况,故不能依据标准只选2~3个适宜的稀释梯度,应多制备几个梯度,不要少于6个,每个稀释度均做2个平皿。一是避免菌落数过多,稀释越小难以计数,二是多个梯度的菌落生长状况有利于发现规律(稀释度越大,菌落数越少,反之亦然),选择更适宜的梯度平板进行计数。④每个稀释梯度,均应准确移取样液和稀释液,此为试验操作的关键一步。⑤实验室可根据情况,选择0.85%生理盐水或者磷酸盐缓冲液(PBS)作为稀释液,两者都是为了给微生物细胞提供一个相对稳定的渗透压,防止细胞因渗透压改变而破裂或脱水死亡。在选择稀释液时还有一个原则,就是尽量与样品处理的60 mL溶液保持一致。⑥试验中为防止稀释液体积因高压灭菌蒸发减小,应先灭菌,再进行分装。⑦从制备样品匀液至样品接种完毕,全过程应控制在15 min内[9](在理想的温湿度和营养条件下,细菌20 min进行一次增殖)。
2.3.6 结果观察与试验数据的控制
(1)生长过快或过慢。菌落经过36℃培养后,一般在46~50 h进行观察,但是在实际操作过程中,培养24 h以后,菌落已能明显计数,针对这种情况,应隔一段时间观察菌落的生长情况,并做好记录,防止过早计数,漏掉生长缓慢的菌落;也要防止过晚计数,以免菌落过度生长,相互覆盖,影响计数结果。另一方面,也存在菌落缓慢生长的情况,最长的培养时间不应超过50 h,防止培养基缺水裂开造成计数不准。无论是菌落生长过多或是个体太小,在肉眼观察的同时,借用放大镜来辅助计数。
(2)蔓延生长。倾倒培养基时再覆盖4 mL,能有效防止菌落蔓延。但有时覆盖后仍会出现蔓延的情况,这个时候还是要采用上面的方法,在菌落已能明显计数的时候,多观察,多记录。对不同时间段的菌落数进行记录,选取相对稳定的计数结果,避免后期菌落蔓延生长造成计数不准。
对于较大片状和链状的菌落,GB 4789.2已有详细的计数处理。每个稀释梯度的平皿只有计数准确了,才能选择最适的计算方法,根据不同的情况选择GB 4789.2—2016条款7.1中的6种方法进行计算,并报送结果。
3 结论
通过比较连续2年能力验证的结果,分析不满意、可疑结果的原因,并采取有效措施,通过再次的能力验证并获得满意结果。文中各环节的质量控制点和注意事项均为多次试验中积累,对于检测机构开展同类试验具有一定的指导意义。微生物检测不同于其他的理化检验,日常检验中的样品中很少有阳性菌,对于试验操作人员来说,很多微生物检验,尤其是涉及致病菌的检验,往往进行到分离培养环节就结束,很少进行到鉴定环节。所以很多检测机构都存在微生物检验人员虽然熟悉完整流程,却很少能操作下来的问题。而解决这一问题,最有效的手段就是参加能力验证。能力验证大部分都是阳性样品,能够锻炼和提升检验人员的技术水平;同时,能力验证的结果可以作为体现实验室检测能力的有效证明,既可以为监管机构评价和认可有能力的实验室提供依据,又可以为客户和其他利益共同体选择合适的检测机构提供参考。鼓励各检测机构积极参加能力验证,通过能力验证,可及时发现实验室在各个环节存在的问题,是确保实验室质量体系持续有效的重要手段[10]。

