羧基共价有机骨架材料对Cd(Ⅱ)的吸附性能及其机理研究
贾昊,姜红新,李明堂,刘潇威*
(1.吉林农业大学资源与环境学院,长春 130000;2.农业农村部农产品质量安全环境因子控制重点实验室/农业农村部环境保护科研监测所,天津 300191)
随着工农业的快速发展,重金属污染带来的环境问题越来越严重[1]。生产生活中排放的废水、废气、废渣含有大量的Cd(Ⅱ),可导致土壤、地下水及地表水污染[2-4],Cd(Ⅱ)进入到植物体内,进而通过食物链循环进入到人体内[5-6]。Cd(Ⅱ)具有累积性、不可降解性和极强的毒性[7],长期摄入Cd(Ⅱ)会严重危害人体健康[8-11]。目前去除水中Cd(Ⅱ)的主要方法有离子交换[12]、膜过滤[13]、化学沉淀[14]、吸附[15]、电解[16]、高级氧化[17]等。其中吸附法由于具有原材料广泛易得、成本低、操作简单、净化高效和环境友好等优势而被广泛使用[18-19]。因此开发吸附容量大且吸附快速的材料成为当前国内外学者研究的热点。
共价有机骨架(Covalent Organic Frameworks,COFs)是一种由轻元素(H、B、C、N、O)组成的有机单体通过化学共价键连接而形成的新型多孔结晶材料[20-21]。COFs 根据空间结构主要分为二维(2D)结构和三维(3D)结构,合成方法主要有溶剂热法、微波合成法、离子热合成法和机械合成法等,其具有结晶度高、比表面积大、孔隙率高、水热稳定性好、孔径均匀可调、易于功能化、对环境友好等优势[22-23]。COFs 键的连接方式也是区分COFs 的一种方式,目前包括:(1)硼酸和醇/酚酯化得到的硼酸酯键;(2)醛基和氨基通过席夫碱反应得到的亚胺键类;(3)醛基和酰肼/肼通过可逆共聚缩合得到的腙键和吖嗪键类;(4)通过可逆席夫碱反应及不可逆的烯酮异构化反应得到的酮胺类;(5)通过单体交换或氧化亚胺键得到的酰胺类;(6)通过羟醛缩合反应得到的烯烃/双键类;(7)邻二氟苯和邻苯二酚类单体通过亲核取代反应得到的聚芳醚类;(8)缩醛胺键类;(9)酯键类。每种类型的COFs都有其独特的优点和局限性[24]。
COFs 在污染物吸附去除方面具有广阔的应用前景。近年来,已有相关研究报道了COFs 材料在Cd(Ⅱ)去除方面的应用。Ghazi等[25]以一种基于三嗪的共价骨架(CTF-1)作为有效吸附剂去除水溶液中的Cd(Ⅱ),pH 为7 时,50 min 达到吸附平衡,最大吸附量为29.26 mg·g-1。Wang 等[26]利用1,3,5-三甲基间苯三酚和脒基硫脲合成的TpAt— COF 对水溶液中的Cd(Ⅱ)进行吸附,结果显示其在180 min 内对Cd(Ⅱ)达到最大吸附量100.76 mg·g-1。Liu 等[27]设计合成了四苯乙烯骨架与邻苯二酚相结合的异孔COFs材料,在25 ℃,中性条件下,其对Cd(Ⅱ)的吸附在60 min后达到吸附平衡,饱和吸附量为116 mg·g-1。虽然以上报道的COFs材料在Cd(Ⅱ)去除方面展现了良好的性能,具有较高的吸附容量,但吸附速度依然较慢,常需要30 min 以上才能达到吸附平衡。因此开发新的COFs材料,通过合理的设计,修饰功能基团,使其携带能与Cd(Ⅱ)作用的丰富位点,实现高容量快速吸附仍然具有重要的意义,但有关此方面的研究目前仍鲜有报道。
本研究以1,3,5-三醛基间苯三酚(TP)和联苯胺(BD)为单体,采用水热法制备TpBD COF,并通过4,4-二氨基联苯-2,2-二羧酸(DAA)对其进行修饰,引入--COOH 官能团,制备了TpBD--COOH COF 材料,该合成方法简单高效、绿色安全。同时利用扫描电镜、傅里叶红外光谱、X 射线衍射等表征手段对材料的结构进行分析,探究了TpBD--COOH COF 材料吸附Cd(Ⅱ)的影响因素及吸附机理,为水体中Cd(Ⅱ)的去除提供理论及数据支撑,同时推进COFs 材料在水体污染治理中的应用。
1 材料与方法
1.1 仪器、试剂与材料
仪器:电感耦合等离子体质谱仪(ICP-MS 2030,日本,岛津公司);扫描电子显微镜(SEM,TESCAN MIRA LMS,捷克,泰思肯公司);傅里叶红外变换光谱仪(FT-IR,TENSOR II,德国,布鲁克公司);X 射线衍射仪(XRD,Smartlab 9 kW,日本,理学公司);热重分析仪(TG,STA 2500,德国,耐驰公司);X 射线光电子能谱仪(XPS,Thermo Scientific K-Alpha,美国,赛默飞世尔科技公司);纳米粒度电位仪(Zetasizer Nano ZS90,英国,马尔文仪器有限公司);能谱分析仪(EDS,Xplore 30,捷克,泰思肯公司);全自动四站比表面积及孔径分析仪BET(ASAP 2460,美国,麦克公司);十万分之一电子天平(SQP,普多利斯科学仪器公司);pH 计(TDZ 5M,中国,上海森信实验仪器有限公司);高速离心机(3-30K,德国,Sigma);超声波清洗机(JP-030S,中国,深圳市洁盟清洗设备有限公司)。
试剂与材料:乙二醇、1,3,5-三甲苯、1,4-二氧六环和N,N-二甲基乙酰胺(DMF)购自天津市康科德科技有限公司(中国天津);浓硝酸(HNO3)和氢氧化钠(NaOH)购自天津风船化学试剂科技有限公司(中国天津);硝酸镉[Cd(NO3)2·4H2O]购自天津市津科精密化工研究所(中国天津);TP购自吉林中科研申科技有限公司(中国吉林);BD购自阿尔法化工有限公司(中国郑州);DAA 购自上海阿拉丁生化科技股份有限公司(中国上海);1 000 mg·mL-1的Cd(Ⅱ)、Na(Ⅰ)、Mg(Ⅱ)、Ca(Ⅱ)、K(Ⅰ)、Cu(Ⅱ)、Zn(Ⅱ)标准储备液从国家有色金属和电子材料分析测试中心购买(中国北京)。所有试剂均为分析纯,实验中使用的水均为超纯水。
1.2 COFs材料的合成
合成TpBD COF 材料:依据参考文献[28],采用溶剂热法合成TpBD COF 材料。称取63.0 mg TP 和82.9 mg BD 于10 mL 离心管中,再加入8.5 mL 1,3,5-三甲苯/1,4-二氧六环(V∶V=1∶1)作为反应溶剂,超声至完全溶解,向其缓慢滴加0.5 mL 9 mol·L-1的醋酸作为催化剂,然后将反应混合液超声5 min混匀,所得混合液倒入反应釜,在120 ℃烘箱中反应3 d。离心分离所得的黄色沉淀物用1,4-二氧六环与DMF 交替洗涤,去除未反应的单体与杂质,最后获得的COFs 材料在70 ℃下真空干燥10 h,产率约为54.2%,获得的棕黄色粉末即为TpBD COF。
TpBD-COOH COF 材料的合成路径如图1 所示:a.称取63.0 mg TP溶解在3 mL的混溶剂(1,3,5-三甲苯与1,4-二氧六环体积比=1∶1)中;b.称取20.4 mg DAA 和69.1 mg BD 溶解在3 mL 的混溶剂中;c.将0.5 mL浓度为9 mol·L-1的醋酸与2.5 mL的混溶剂混合均匀。将a、b 混合均匀,在超声条件下,缓慢加入c 溶液,最后将其转移至反应釜中,在120 ℃烘箱中反应3 d。离心所得的沉淀物用1,4-二氧六环与DMF 交替洗涤,去除未反应的单体与杂质,将干净的COFs材料在70 ℃下真空干燥10 h,产率约为69.7%,获得的粉末即为TpBD—COOH COF。
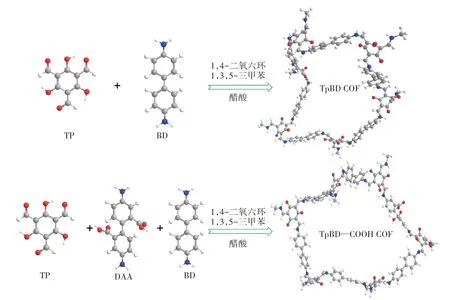
图1 COFs材料的合成路径图Figure 1 Synthetic scheme of COFs materials
1.3 COFs材料的性能表征
本研究使用SEM 在0.9 nm@15kV(二次电子图像)和2.0 nm@30 kV(背散射电子图像)条件下对COFs 的微观结构和表面形貌进行观察。使用FT-IR对COFs 材料表面官能团以及化学键类型进行表征,其扫描波数范围为4 000~400 cm-1,扫描次数32 次,分辨率4 cm-1。使用XRD 分析COFs 样品的晶体结构,扫描范围2θ为1.5°~30°,扫描速度2 s·步-1,连续扫描。使用全自动四站比表面积及孔径分析仪对COFs 材料的比表面积进行测定,测试前先将COFs 材料在120 ℃下用氮气脱气12 h,然后在液氮温度下获得COFs 样品的N2吸附-脱附等温线,再用Brunauer-Emmett-Teller(BET)法计算样品的比表面积。采用EDS分析样品表面的元素组成,能谱分析工作距离为15 nm。XPS全谱扫描:通能为1 350 eV,步长1 eV;窄谱扫描:通能为200 eV,步长0.1 eV。Zeta 电位分析:BeNano 90 Zeta 测量范围为0.3 nm~15 μm,分辨率为2.5~3.0倍粒径微米。使用TG 分析了COFs 样品的热稳定性,测试条件为氮气气氛,升温范围为室温至800 ℃,升温速率为10 K·min-1。
1.4 吸附实验
1.4.1 储备液的配制
将1 000 mg·L-1Cd(Ⅱ)标准储备液用5% HNO3稀释成浓度为0.1、0.2、0.5、1、2、5、10、20、50、100、200、400 μg·L-1的溶液,绘制标准曲线(附图1)。
用1 000 mg·L-1标准储备液配制1 mg·L-1的Cd(Ⅱ)储备液,并使用NaOH溶液和5%HNO3溶液调节pH 为4、5、6、7、8、9,4 ℃储存待用,用于考察pH 对Cd(Ⅱ)吸附的影响。
配制单个浓度为1 mg·L-1和50 mg·L-1、pH=8 的Cd(Ⅱ)、Na(Ⅰ)、Mg(Ⅱ)、Ca(Ⅱ)、K(Ⅰ)、Cu(Ⅱ)、Zn(Ⅱ)混标溶液用于测定共存离子对Cd(Ⅱ)吸附的影响。
1.4.2 吸附实验的影响因素
通过吸附实验考察pH、吸附剂用量和共存离子对TpBD--COOH COF吸附Cd(Ⅱ)性能的影响。
溶液pH 对Cd(Ⅱ)吸附的影响:将6 mg COFs材料吸附剂分散在1 mL,1 mg·L-1,pH 为4、5、6、7、8、9的Cd(Ⅱ)溶液中,常温超声条件下充分接触吸附10 min;吸附剂用量对Cd(Ⅱ)吸附的影响:将2、3、4、5、6 mg的COFs材料吸附剂分散到1 mL、1 mg·L-1,pH为8 的Cd(Ⅱ)溶液中,常温超声条件下充分接触吸附10 min;共存离子对Cd(Ⅱ)吸附的影响:称取多份4 mg TpBD-COOH COF 材料吸附剂,分别分散在1 mL,pH=8 的各离子浓度为1 mg·L-1和50 mg·L-1的Cd(Ⅱ)、Na(Ⅰ)、Mg(Ⅱ)、Ca(Ⅱ)、K(Ⅰ)、Cu(Ⅱ)、Zn(Ⅱ)混标溶液中,超声吸附10 min。
1.4.3 动力学吸附
称取多份4 mg TpBD--COOH COF 材料吸附剂,分别加入到多个含有1 mL,1 mg·L-1,pH为8的Cd(Ⅱ)溶液的离心管中,提前开启超声波,将离心管放入超声,同时计时,分别在1、2、3、4、5、6 s时取出。
1.4.4 等温吸附
使用硝酸镉配制pH=8,浓度为200、400、600、800、1 000、1 200、1 400 mg·L-1的Cd(Ⅱ)溶液,考虑碱性条件下沉淀情况,对以上Cd(Ⅱ)溶液取上清液测定最终Cd(Ⅱ)浓度(C0)(附表1),参与饱和吸附量计算。称取多份4 mg TpBD--COOH COF材料吸附剂分别加入到各浓度1 mL Cd(Ⅱ)溶液中,常温超声条件下充分吸附6 s。
1.4.2 至1.4.4部分超声后的样品,取出在5 000 r·min-1下离心3 min 将COFs 材料与上清液分离。使用5% HNO3溶液稀释至ICP-MS 检测范围内,过0.22 μm 滤膜,在ICP-MS 上分析测定吸附前后溶液离子浓度。
1.5 实际水体研究实验
选用纯水、自来水、地表水(津河)作为实际水体实验的研究对象。实际水体中包含悬浮颗粒物,不利于仪器分析的检测,因此,将其经过0.45 μm 的滤膜过滤后再用于配制0.01、0.1、1.0、10.0 mg·L-1,pH=8的Cd(Ⅱ)溶液。将4 mg COFs 材料吸附剂分散在40 mL 用不同实际水体配制的Cd(Ⅱ)溶液中,常温超声条件下充分接触吸附6 s。然后将样品在5 000 r·min-1下离心3 min,将COFs 材料与上清液分离,使用5%HNO3溶液稀释至ICP-MS检测范围内,过0.22 μm滤膜,在ICP-MS 上分析测定吸附前后溶液Cd(Ⅱ)的浓度。
1.6 检测方法
采用ICP-MS 测定Cd(Ⅱ)浓度。等离子体条件:高频功率1.2 kW,采样深度5.5 mm,等离子体气9.0 L·min-1,辅助气1.10 L·min-1,载气0.70 L·min-1。池条件:池气体5.5 mL·min-1,池电压-21.0 V,能量过滤器7.0 V。积分条件:积分时间分割次数20 次,雾室温度5 ℃。
1.7 数据处理与分析
1.7.1 表征数据分析
XRD 是通过MS Jade(Materials Studio Jade)数据处理并结合Origin 软件绘图;XPS 谱图通过Thermo Avantage 数据处理软件并结合Origin 软件绘图;N2吸附-解吸等温线图、FT-IR、TG、Zeta 电位等数据均使用Origin软件制图。
1.7.2 Cd(Ⅱ)吸附量和吸附率的计算
Cd(Ⅱ)溶液的吸附量(q,mg·g-1)和吸附率(R,%)分别通过下列公式计算。
式中:W代表材料的质量,g;V代表吸附溶液的体积,L;C0和Ce分别为Cd(Ⅱ)的初始浓度和达到吸附平衡时的浓度,mg·L-1。
1.7.3 动力学吸附模型
式中:qe和qt分别表示平衡时及时间t时吸附Cd(Ⅱ)的量,mg·g-1;k1表示准一级动力学方程反应速率常数,s-1;k2表示准二级动力学方程反应速率常数,g·mg-1·s-1;t表示吸附时间,s。
1.7.4 等温吸附模型
式中:qe表示TpBD-COOH COF 材料对Cd(Ⅱ)的吸附容量,mg·g-1;qmax表示最大吸附量,mg·g-1;KL为Langmuir 常数,L·mg-1;KF和n分别代表Freundlich 的吸附能力和吸附强度常数。
2 结果与讨论
2.1 COFs材料的性能表征
2.1.1 扫描电镜(SEM)分析
图2a 和图2b 分别是TpBD COF 和TpBD--COOH COF 材料的SEM 图。通过外观形貌分析可知,羧基官能团修饰TpBD 前后,COFs材料的形貌结构变化较小。从图2a和图2b对比可以看出,TpBD COF表面更为粗糙、呈不规则层状堆积,TpBD--COOH COF 表面也呈现层状堆积,但层状结构的规整度有所增加,呈现规则的花瓣状。另外,两种COFs 材料表面均有很多大直径的孔道,同时结构内部层与层之间有明显的孔隙结构。

图2 COFs材料的扫描电镜图Figure 2 SEM image of COFs material
2.1.2 红外光谱(FT-IR)分析
为了验证TpBD COF 和TpBD--COOH COF 的官能团构成,使用FT-IR 对样品进行了表征。从TpBD COF 材料的FT-IR 光谱可知(图3a),3 325 cm-1处的(BD)N--H 和2 893、1 642 cm-1处的(Tp)的吸收峰 消失[29],另外1 283 cm-1处C--N 峰和1 580 cm-1处峰的出现说明形成了胺键连接的高度聚合的材料。相比于TpBD COF,从TpBD--COOH COF吸收峰中可以观察到,在3 422 cm-1处出现很明显的--OH振动峰,同时在1 719 cm-1出现新的峰,表明TpBD--COOH COF中具有羧基结构[29-31],这些键的出现都为羧基官能团的成功修饰提供了证据,表明TpBD-COOH COF材料的成功合成。
2.1.3 X射线衍射(XRD)分析
通过XRD 对TpBD COF 和TpBD--COOH COF 材料的晶型结构进行表征。由XRD 谱图可见(图3b),TpBD COF 和TpBD--COOH COF 均在低角度范围处观察到一个强峰出现,TpBD COF 在3.35°处的信号最强,TpBD--COOH COF在3.48°处的信号最强,它们都对应于(100)晶面,这与之前报道的许多六边形结构的COFs 的结晶度一致[29-30]。以上结果表明羧基官能团修饰并未影响COFs材料的结晶度,两种COFs材料都具有很好的结晶性。
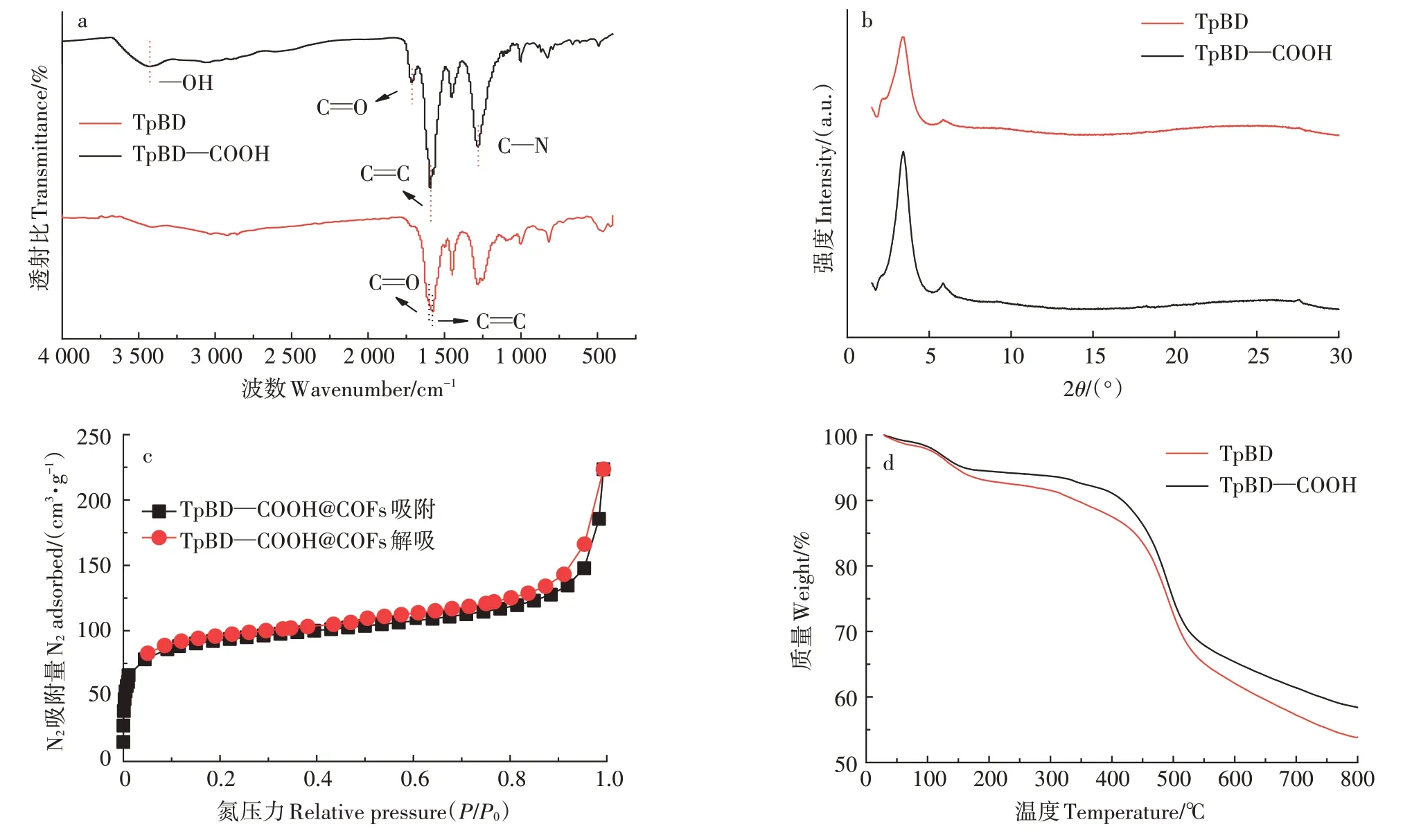
图3 COFs材料的FT-IR图(a)、X射线衍射图(b)、氮气吸附-解吸等温线(c)和热重曲线(d)Figure 3 FT-IR spectra(a)of COFs material,X-ray diffraction pattern(b),N2-adsorption-desorption isotherms(c)and thermogravimetric curves(d)
2.1.4 比表面积(BET)分析
使用N2吸附-脱附等温线获得了TpBD——COOH COF材料的比表面积。如图3c所示,根据IUPAC的吸附等温线及迟滞回线类型可知,TpBD--COOH COF材料的N2吸附-脱附等温线属于Ⅱ型,证明存在微孔结构。在P/P0=0.05~0.35 的范围内使用Brunauer-Emmett-Teller 理论模型计算出的TpBD--COOH COF 材料的比表面积为339 m2·g-1。与TpBD COF 材料相比[28],修饰官能团后形成的TpBD--COOH COF材料比表面积有所降低,这可能是由于更多的孔隙空间被修饰基团(--COOH)占用的原因[32-33]。
2.1.5 热重(TG)分析
使用TG分析验证了两种COFs材料的热稳定性。如图3d 所示,在TpBD COF 和TpBD--COOH COF 材料的TG 曲线中发生了3 次明显的失重。第一次失重发生在30~100 ℃,TpBD COF 和TpBD--COOH COF的质量损失约为5%,主要是由于水分的蒸发。第二次失重发生在100~400 ℃,TpBD COF和TpBD--COOH COF的质量损失接近10%,主要是由于一些反应单体物质的挥发[34]。第三次失重发生在400~500 ℃,TpBD COF 和TpBD——COOH COF 的质量损失接近15%,主要是由于COFs 的分解和燃烧。测试结果表明,两种材料的热稳定性相似,羧基基团的引入并未影响COFs 材料的热稳定性,在450 ℃以下两种COFs材料均表现出良好的热稳定性。
2.1.6 吸附前后COFs中O和Cd(Ⅱ)元素的能谱分析
使用EDS 分析更直观地验证了TpBD--COOH COF 的形成,以及TpBD--COOH COF 对Cd(Ⅱ)的吸附。从图4a 和图4c 中可以看出,与TpBD COF 相比,TpBD--COOH COF 中O 元素增加0.2%(附表2),表明羧基官能团修饰TpBD COF 成功。从图4b 和图4d 可以看出,与TpBD COF 吸附的Cd(Ⅱ)元素相比,TpBD--COOH COF 吸附Cd(Ⅱ)元素的量明显更多(增加0.48%),这也直观地证明了TpBD--COOH COF对Cd(Ⅱ)吸附性能的提升。
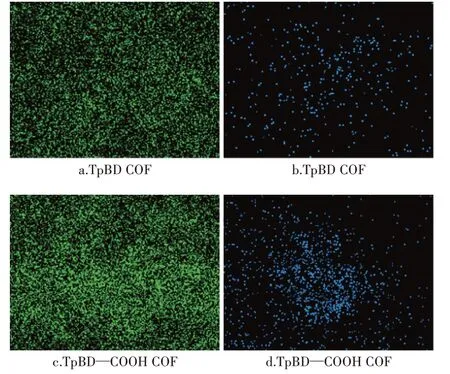
图4 COFs材料的元素映射图像Figure 4 Elemental mapping image of COFs material
2.2 吸附实验影响因素
采用单一变量法,对吸附溶液的pH、吸附剂用量、共存离子等影响吸附性能的条件进行了考察。
2.2.1 溶液pH 对Cd(Ⅱ)吸附的影响
如图5a 所示,随着Cd(Ⅱ)溶液pH 由4 升高到8,TpBD--COOH COF材料对Cd(Ⅱ)的吸附率明显优于TpBD COF,当Cd(Ⅱ)溶液从pH=8 继续升高到pH=9时,吸附率基本保持不变。这是由于酸性条件下,COFs 材料上的羧基会质子化,从而减弱了与Cd(Ⅱ)的静电作用,而溶液从酸性到碱性,是去质子化的过程,TpBD--COOH COF 材料在pH=6~9 时带负电荷(图5b),其会与Cd(Ⅱ)产生静电作用,从而提高了吸附率。同时如图5b 所示,TpBD COF 的Zeta 电势呈现出与TpBD--COOH COF 相同的变化趋势,这可能是由于亚氨键发生了去质子化,导致TpBD COF 带少量负电荷而与Cd(Ⅱ)产生静电作用。根据以上实验数据,选择pH=8的Cd(Ⅱ)溶液进行后续实验。
2.2.2 吸附剂用量对Cd(Ⅱ)吸附的影响
如图5c 所示,随着吸附剂用量的增加,TpBD--COOH COF 对Cd(Ⅱ)的吸附率变化较小,吸附率均在95%以上,综合吸附效果和节约成本两方面考虑,选择4 mg 用量进行后续实验。由以上两个实验可知,相比于TpBD--COOH COF,TpBD COF 对Cd(Ⅱ)的吸附性能很弱,因此后续只对TpBD--COOH COF吸附Cd(Ⅱ)的性能进行了研究。
2.2.3 共存离子对Cd(Ⅱ)吸附的影响
共存离子是影响TpBD--COOH COF 材料在水溶液中吸附Cd(Ⅱ)的关键因素。如图5d 所示,TpBD—COOH COF对K(Ⅰ)、Na(Ⅰ)基本不吸附,而对Ca(Ⅱ)、Mg(Ⅱ)、Cu(Ⅱ)、Zn(Ⅱ)同样具有较好的吸附效果,缺乏对Cd(Ⅱ)的吸附选择性。这是因为K(Ⅰ)、Na(Ⅰ)是典型的碱金属,属于路易斯硬酸,半径较小,而且没有可用的空轨道,与TpBD——COOH COF 很难发生配位作用,因此基本没有被吸附。而Ca(Ⅱ)、Mg(Ⅱ)、Cu(Ⅱ)、Zn(Ⅱ)具有和Cd(Ⅱ)相近的原子轨道和电荷密度,都具有空的电子轨道,属于路易斯软酸,可以与TpBD--COOH COF上的羧基官能团产生很强的配位作用,因此TpBD COOH COF 对这些离子具有相同的吸附能力。同时TpBD--COOH COF 与金属离子也存在一定的静电作用。但由于TpBD--COOH COF吸附能力较强,在此6种离子共存的条件下,仍能对Cd(Ⅱ)有很好的吸附作用,吸附率可达90%。
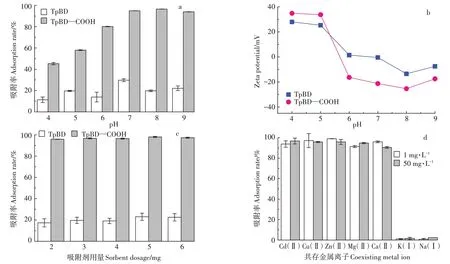
图5 溶液pH、COFs材料用量、共存金属离子对Cd(Ⅱ)吸附的影响及不同pH条件下COF材料的Zeta电位值Figure 5 Effects of pH,sorbent dosage and coexisting metal ions on the adsorption efficiency of Cd(Ⅱ),and the relationship between Zeta and pH in aqueous solutions
2.3 TpBD--COOH COF 材料对Cd(Ⅱ)的动力学吸附研究
两种COFs 材料对Cd(Ⅱ)吸附量随时间变化的动力学曲线如图6 所示。随着时间的延长,TpBD--COOH COF 对Cd(Ⅱ)的吸附量快速上升,最终在6 s时基本达到吸附平衡。为了深入了解TpBD--COOH COF 材料对Cd(Ⅱ)吸附的动力学过程,采用准一级动力学和准二级动力学模型对此数据进行拟合,其拟合结果如图6 所示,拟合参数列于表1。通过拟合结果得知,由准二级动力学拟合所得的R2值(0.940)高于准一级动力学拟合所得的R2值(0.860)。同时TpBD--COOH COF材料对Cd(Ⅱ)呈现出了较高的吸附速率,其速率常数K2达到0.035 g·mg-1·s-1。
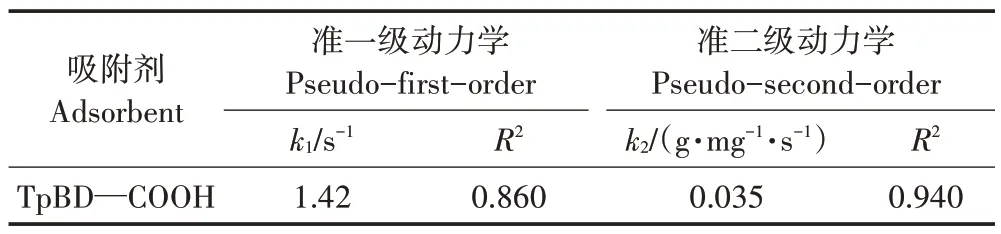
表1 TpBD--COOH对Cd(Ⅱ)吸附的动力学模型拟合参数Table 1 Fitting parameters of the kinetic model of TpBD--COOH
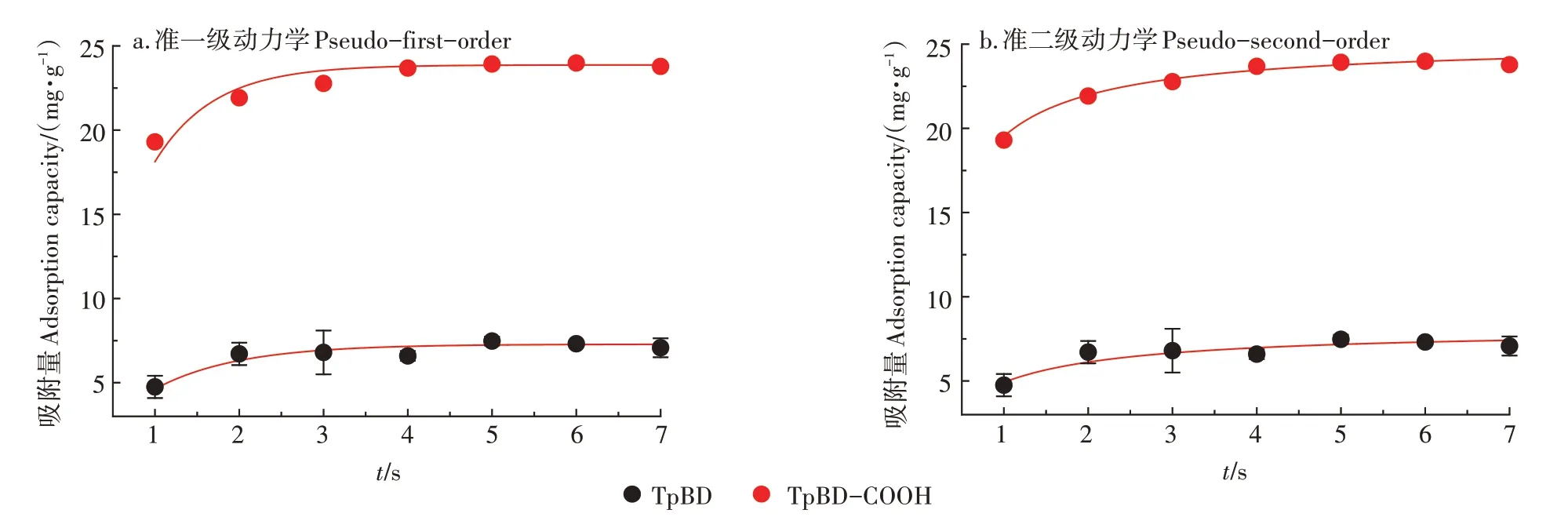
图6 TpBD—COOH COF吸附Cd(Ⅱ)的准一级动力学和准二级动力学拟合曲线Figure 6 Pseudo-first-order kinetic and pseudo-second-order kinetic of TpBD--COOH COF adsorption of Cd(Ⅱ)
2.4 TpBD--COOH COF材料对Cd(Ⅱ)的等温吸附研究
两种COFs 材料对Cd(Ⅱ)的吸附量随着平衡浓度的变化曲线见图7,随着Cd(Ⅱ)浓度的增大,TpBD COF 和TpBD--COOH COF 的吸附量逐渐增加,当吸附量不再增加时吸附达到饱和。TpBD COF 和TpBD—COOH COF 对Cd(Ⅱ)的饱和吸附量分别为29.6 mg·g-1和142.0 mg·g-1,与TpBD COF 相比,TpBD--COOH COF 对Cd(Ⅱ)的吸附量提高了3 倍多。由此可见,羧基官能团修饰有效提高了COF 材料对Cd(Ⅱ)的吸附能力,这可能是因为引入羧基官能团会一定程度增强COFs 材料与Cd(Ⅱ)的静电作用和配位作用。
采用Langmuir 和Freundlich 模型拟合Cd(Ⅱ)在TpBD—COOH COF 上的吸附等温线,结果如图7 所示,拟合参数列于表2。从图7和表2可以看出,Langmuir 和Freundlich 模型均能较好地拟合Cd(Ⅱ)在TpBD--COOH COF 上的吸附等温线,其中Langmuir模型拟合效果更好,R2=0.977,表明该吸附为单分子层吸附过程[35]。此外,由表2 可知,通过拟合得到TpBD--COOH COF材料对Cd(Ⅱ)的理论最大吸附量(qmax)为150 mg·g-1,而实验中所得TpBD--COOH COF材料对Cd(Ⅱ)的吸附量为142 mg·g-1,两者差距可能来自于实验中的误差[36],且与其他吸附材料相比(附表3),该吸附量有所提升。

表2 TpBD--COOH COF等温吸附拟合参数Table 2 Fitting parameters of TpBD--COOH COF isotherm adsorption
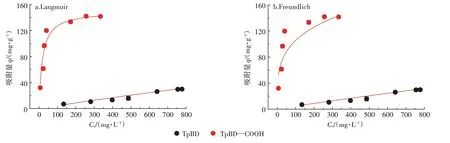
图7 Langmuir和Freundlich模型拟合的TpBD--COOH COF对Cd(Ⅱ)吸附等温线Figure 7 Cd(Ⅱ)adsorption isotherms of TpBD--COOH COFs fitted by Langmuir and Freundlich models
2.5 TpBD--COOH COFs对Cd(Ⅱ)吸附的机理
FT-IR 和XPS 被用来研究TpBD--COOH COF 对Cd(Ⅱ)吸附的机理,对比最优条件下TpBD--COOH COF 材料对Cd(Ⅱ)吸附前后的FT-IR 图发现(附图2):含氧官能团的峰发生明显变化,其中峰从1 719 cm-1到1 714 cm-1发生明显位移且峰强有所降低,——OH 峰从3 422 cm-1移至3 407 cm-1,波峰明显变宽,说明在吸附过程中,Cd(Ⅱ)与TpBD--COOH COF材料表面的羧基发生了一定的化学作用。结合XPS表征研究了TpBD--COOH COF 对Cd(Ⅱ)的吸附机理。如图8a 所示,通过比较TpBD--COOH COF 材料吸附Cd(Ⅱ)前后的XPS 光谱发现,TpBD--COOH COF 吸附Cd(Ⅱ)后的全谱图中410 eV 附近有信号峰出现,证明Cd(Ⅱ)成功吸附在了TpBD--COOH COF材料上。TpBD--COOH-Cd 峰对应的Cd(Ⅱ)3d轨道XPS高分辨光谱图(图8b)显示,两个信号峰分别位于412.19 eV 和405.36 eV 处,对应于Cd(Ⅱ)3d 轨道的3/2 和5/2 处,表明Cd(Ⅱ)成功存在于TpBD--COOH COF 材料表面。如图8c 所示,TpBD--COOH COF 的O1s 峰的XPS 高分辨光谱图在531.94 eV 和530.48 eV处显示两个峰,分别配位于Cd--O 和--COOCd,吸附Cd(Ⅱ)后两个峰发生了0.62 eV 和0.52 eV 的电子正移(图8d),证明TpBD—COOH COF 的电子通过配位键向Cd(Ⅱ)转移。此外,与Cd(Ⅱ)配位后,在404.88 eV 处出现一个新的N1s 峰(附图3),其可能是来自Cd(NO3)2·4H2O 中硝酸盐配体。综上所述,TpBD--COOH COF材料对Cd(Ⅱ)吸附是配位作用,且配位吸附主要作用于TpBD--COOH COF 材料上羧基基团。同时根据图5b Zeta电位分析结果可知,TpBD--COOH COF材料对Cd(Ⅱ)吸附也存在一定的静电作用。
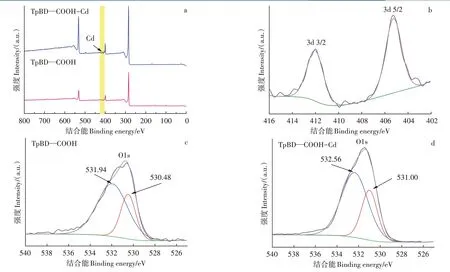
图8 TpBD-COOH COF吸附Cd(Ⅱ)的XPS测量全谱图(a),Cd的高分辨光谱图(b),吸附Cd(Ⅱ)前(c)和吸附Cd(Ⅱ)后(d)的O1s高分辨光谱图Figure 8 XPS measurement full spectrum of Cd(Ⅱ)adsorption on TpBD-COOH COF(a),high-resolution spectrum of Cd(b),O1s high-resolution spectrum before(c)and after adsorption of Cd(Ⅱ)(d)
2.6 实际水体应用
由于实际水样基质比纯水更加复杂,如包括各种离子等,这些因素不可避免地会对吸附产生竞争性的影响,导致吸附能力下降,因此研究了TpBD--COOH COF 材料在实际水体中对Cd(Ⅱ)的去除能力。本研究选用矿泉水、自来水、天津市地表水3 种水体作为实际水体,首先考察了3 种水体中所含金属离子的种类和浓度(附表4),及以上金属离子背景值对TpBD--COOH COF 吸附Cd(Ⅱ)的影响(图5d)。结果表明,虽然TpBD--COOH COF 材料对二价金属离子有一定的吸附作用,但是较低的含量水平并未对TpBD--COOH COF吸附Cd(Ⅱ)的性能有显著影响。
其次用以上3 种水体分别作为溶剂配制了0.01、0.1、1.0、10 mg·L-1的Cd(Ⅱ)溶液,研究了TpBD--COOH COF 材料在这3 种实际水样中对Cd(Ⅱ)的去除能力。结果如表3所示,在3种实际水样中,TpBD--COOH COF 材料对Cd(Ⅱ)的吸附能力差异较小,即使在自来水和地表水中,TpBD--COOH COF 材料对Cd(Ⅱ)的吸附量仍能达到在实验室纯水条件下的90%以上,3 种水体中的去除率均能达到95%(附表5),说明TpBD--COOH COF 材料具备很好的抗干扰能力。且依据《生活饮用水卫生标准》(GB 5749—2022)、《地表水环境质量标准》(GB 3838—2002),吸附过后水质中残留Cd(Ⅱ)含量均可达标。这些结果都表明,TpBD--COOH COF 材料在去除实际水体中的Cd(Ⅱ)方面有很大应用潜力。
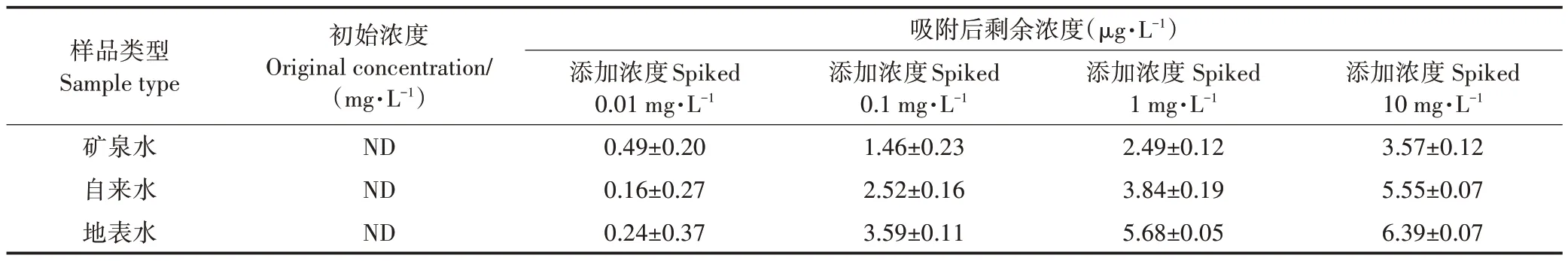
表3 实际水体样品中Cd(Ⅱ)的测定(平均值±标准偏差,n=5)Table 3 Determination of Cd(Ⅱ)in actual water samples(mean±s,n=5)
3 结论
(1)扫描电镜、红外光谱、X 射线衍射等多种表征结果表明,两种共价有机骨架(COFs)均具有很高的结晶度、较大的比表面积、优异的热稳定性。而且羧基官能团修饰TpBD COF后并未影响材料的结构和热稳定性。
(2)相比于TpBDCOF,TpBD--COOHCOF对Cd(Ⅱ)的吸附能力明显增强,饱和吸附量提高了3 倍多。TpBD--COOH COF对Cd(Ⅱ)的吸附仅需6 s。TpBD--COOH COF 对Cd(Ⅱ)的吸附符合准二级动力学和Langmuir 等温吸附模型。通过Zeta 电位和X 射线光电子能谱证明了TpBD--COOH COF 对Cd(Ⅱ)的吸附机理主要是静电作用和配位作用。
(3)在实际水体样品(矿泉水、自来水、地表水)中,TpBD--COOH COF 对Cd(Ⅱ)的吸附性能并未受到明显影响,说明其具有很好的环境适应性,对吸附去除水环境中的Cd(Ⅱ)具有很好的应用前景。
(本文附图和附表1 见补充材料,可扫描首页OSID码,点击“本文开放的科学数据与内容”查看)

