胸壁侵袭性纤维瘤病1例*
王文培 刘 兴 周 湘 刘红光
1.深圳市第二人民医院甲乳外科 (广东 深圳 518035)
2.南华大学衡阳医学院深圳市第二人民医院研究生协作培养基地(湖南 衡阳 421001)
1 临床资料
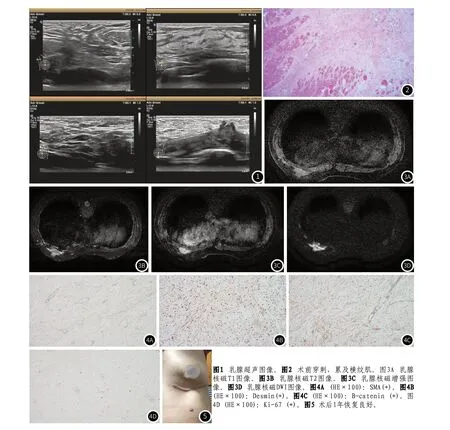
患者,女,27岁。发现左乳肿物4月余,4年前于我院行左乳纤维瘤切除术,入院查体见左乳5-7点连接胸壁可扪及一大小约8x3cm肿物,质中,边界欠佳,无触痛。检验指标无明显异常。B超示左乳5-7点方向低回声区,上近乳晕区,下超出乳房范围,浅层紧邻皮肤层,边界至胸壁肌层,局部肌肉纹理紊乱消失,范围约88x30x17mm(图1)。术前穿刺活检诊断梭形细胞肿瘤(图2)。核磁结果为左乳片状的不规则低回声,左区皮下脂肪层模糊,T1等信号,T2高信号,内部强化均匀,TIC曲线平台型,ADC值混杂高信号,DWI信号高(图3)。术中探查见左胸壁肿物与左胸壁筋膜、胸大肌、肋间肌融为一体,用电刀锐性游离,肌纤维为核心完整切除肿物,术后病理:1.左乳病变组织符合纤维瘤病,2.左胸壁病变组织考虑为侵袭性纤维瘤病,免疫组化结果:SMA(+),S100(-),CD34(-),Desmin(+),B-catenin(细胞浆及细胞核+),AE1/AE3(-),P63(-),Ki- 67(3%+)(图4-1至4-4)。术后随访至今1年,患者恢复良好,复查核磁未见复发及明显异常。
2 讨 论
A F 也叫做肌肉腱膜纤维瘤病、韧带样型纤维瘤病。Farlances医生在1832年首先描述了该疾病,该病发生率在所有软组织肿瘤中占比小于3%,局部复发率在25%~77%[1]。本病胸壁类型少见,它的发病原因尚不清楚,或许和创伤、遗传或激素等有关[2]。临床表现为深在、界限不明的质硬无痛肿物。
术前由于胸壁AF影像学及临床表现无特异性,在年轻女性患者中多发,患者多因乳腺肿物就诊于甲乳外科,在术前临床易误诊为乳腺来源的纤维瘤,侵及胸肌或胸壁;显微镜下,其边界不清且具有浸润性,由致密的胶原基质和长束带、均匀的成纤维细胞组成,细胞密度低[3],无多形性和坏死,有丝分裂很少见[4](每10个高倍视野最多5个)。在肿瘤的外围,有可能会导致萎缩的横纹肌残留物,因此放射科医生也可能将其误认为是恶性疾病的证据。本病例术前考虑为复发性乳腺纤维瘤,术前穿刺病理考虑梭形细胞瘤,未能明确诊断,有资料显示在AF初始检查中误诊病例约为 30~40%[5,6],穿刺活检在间质细胞来源肿瘤的诊断,存在固有的取材不足问题。
受术前诊断信息不充分,术中手术医生常按乳腺来源的肿瘤标准来切除肿物,导致肿瘤非腺体部分纤维缘切除不完整,术中残余高概率发生,此外,如果肿物侵犯超过乳腺组织且在纤维轴延伸,即使冰冻回报恶性,术者扩大切除范围仍按环形切除,而非延纤维轴扩大,切缘仍可能阳性。在没有认识到AF多来源胸壁肌肉时,乳腺来源累及肌肉或肌肉来源肿瘤累及乳腺,术后肿瘤基底部的肿瘤残余率会有差异。手术切缘阴性的最佳切除应该是手术的主要目标,从而获得最佳的肿瘤学预后[7-9]。
另一些研究报告[10-11],手术切缘阳性与阴性患者的 5 年无进展生存率没有显着差异。尽管文献报告对切缘阳性扩大切除和保守治疗间选择对比,常出现相互矛盾的结果,但我们对于手术切缘阳性可手术患者仍推荐扩大切除。考虑到该患者既往乳腺纤维瘤手术史,此次肿块深层累及胸壁肌层,便采用以肌纤维为核心广泛切除病灶,术后完整病理的免疫组化提示胸壁AF。文献报道[12-13]AF灶里细胞波纹蛋白染色呈强阳性,B-catenin蛋白与平滑肌肌动蛋白(SMA)也呈不一样的阳性程度(图4A、4C),但通常不表达CD-34和S-100蛋白,本病例病理学表现与文献报道相符。
此外,女性病人对乳房的美容要求较高,顾及到术后乳房的完整性及美观性,手术医生在切除范围权衡时,侧重点偏向了外形,这一点也是术后复发的重要因素。我们建议采取根治性手术,辅以整形修复技术,以最大的可能争取切缘阴性,避免再次手术及早期复发。
综上所述,胸壁AF目前的临床及影像学表现均无特异性,术前易误诊,术中易残留,整块切除术后病理诊断仍是“金标准”。目前手术仍是一线的治疗手段,初始切除一定要彻底,再次手术以纤维轴广泛切除,对于复发的乳腺纤维瘤病及性质未明的浸润胸肌的肿物,在日常工作中要求临床、放射科及病理科医师考虑到此病的可能性,避免漏诊或误诊。