急性缺血性脑卒中病人医院感染与卒中复发风险研究
胡富勇,芈 静,潘宇芹,郭华陵,杨 静,吴君仓,刘秋皖,吴竹青,群 森
脑卒中目前是我国成年人致死、致残的首位病因[1]。更为严重的是,随着人口老龄化、城市化进程的加快、不良生活方式以及卒中年轻化的影响[2],我国脑卒中发病呈逐年上升的趋势,疾病负担有爆发增长的态势,防治形势将日益严峻[3]。脑卒中以其高发病率、高复发率、高致残率、高死亡率及逐年递增的防治费用给社会造成巨大的经济负担,已成为严重影响国计民生的重要公共卫生问题[4]。
脑卒中幸存者有较高的复发风险,复发性缺血性脑卒中占所有脑卒中的近三分之一,且复发性卒中的发病率和死亡率明显高于首次卒中[5],预防卒中复发在缺血性脑卒防治中尤为关键。研究[6-7]证据表明,炎症在缺血性脑卒中的发生,发展和预后中起着关键作用。感染是脑卒中病人最常见的并发症[8-9],缺血性脑卒中急性期,免疫炎症的激活造成继发性脑损害,随后免疫炎症被下调以避免进一步的脑损伤,但以卒中后免疫抑制为代价,增加继发感染的风险,尤其是卒中相关性肺炎[10]。本研究通过对急性缺血性脑卒中(acute ischemic stroke,AIS)病人进行随访,研究医院感染与脑卒中复发之间的相关性。现作报道。
1 对象与方法
1.1 研究对象 收集2015年1月至2017年5月在合肥市第二人民医院神经内科收治的AIS病人作为研究对象,纳入标准:卒中症状发作后3 d内入院、通过磁共振成像扩散加权图像序列确诊为AIS并签订知情同意书的病人(2020KY伦审第116号),排除标准:6个月内的脑卒中史、严重脑部疾病、严重的全身性疾病(如急/慢性肾功能不全)、内分泌疾病(糖尿病除外)、癌症、创伤、传染病和血液病。
1.2 方法 AIS病人过夜禁食,其血液样本在入院后第2天的早晨(6:00-7:00)收集,收集后立即将所有样品送去测试。用颗粒增强的比浊免疫测定法测量血清β2微球蛋白(β2microglobulin,B2M),用免疫透射浊度法测定C反应蛋白(C reaction protein,CRP),用酶法测量其他生化参数,包括同型半胱氨酸(homocysteine,Hcy)、肌酐(creatinine,Crea)、尿素氮(blood urea nitrogen,BUN)、尿酸(uric acid,UA)、低密度脂蛋白(low-density lipoprotein cholesterol,LDL)、三酰甘油(triglyceride,TG)、总胆固醇(total cholesterol,TC)、高密度脂蛋白(high-density lipoprotein cholesterol,HDL)、极低密度脂蛋白(very low-density lipoprotein cholesterol,VLDL)和胱抑素C(cystatin C,CysC)。以上检测均采用自动生化分析仪(HITACHI Automatic Analyzer 7600-020,Japan)测定所有血清生化参数。
收集所有参与者的年龄、性别、高血压、糖尿病、卒中史、冠心病、吸烟和饮酒个人史资料,以及美国国立卫生院卒中评分(National Institute of Health Stroke Scale,NIHSS)和Essen卒中风险评分(Essen Stroke Risk Score,ESRS)资料。高血压的判定以诊断为高血压或先前使用抗高血压药物,未使用任何抗高血压药物且收缩压(systolic blood pressure,SBP)≥140 mmHg或舒张压(diastolic blood pressure,DBP)≥90 mmHg。糖尿病的判定为未使用任何降糖药物且空腹血糖≥7.0 mmol/L或口服糖耐量试验2 h血糖≥11.1 mmol/L,或已诊断为糖尿病。冠心病的判定根据病人有心绞痛症状或心肌梗死病史或冠脉CT、冠脉造影证实。病人在住院期间患有肺炎或尿路感染等,依据中华人民共和国卫生部2001年颁布的《医院感染诊断标准(试行)》的诊断标准界定为医院感染。上述资料经纸质病例填写后输入电子数据库,通过电话随访的方式了解病人出院后的健康状况。病人出院日期记为队列起始时间,病人出院后随访期内再次被诊断为脑卒中记为终点事件,随访截止时间为2019年5月。
1.3 统计学方法 采用Shapiro-Wilk检验、t检验、秩和检验、χ2检验及Cox回归分析、二元logistic回归。
2 结果
2.1 基本情况 本研究共纳入121例AIS病人,其中男72例(62.0%),年龄37~94岁;有24例(19.8%)住院期间出现医院感染,95%CI:0.127~0.269,卒中复发32例(26.4%),95%CI:0.185~0.343。未感染组在性别、高血压、2型糖尿病、卒中史、冠心病、吸烟、饮酒、DBP、Hcy、血糖、Crea、BUN、UA、LDL、TG、TC、HDL、VLDL、CysC、CRP和NIHSS评分上与感染组差异均无统计学意义(P>0.05),而在年龄、SBP、B2M、ESRS评分和卒中复发上与感染组差异均有统计学意义(P<0.05~P<0.01)(见表1)。
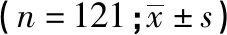
表1 AIS病人中医院感染与未感染者的基本资料比较
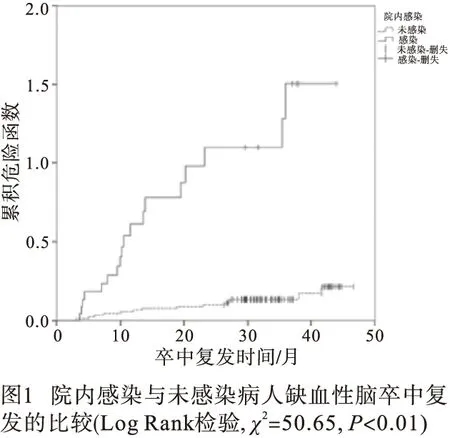
2.2 医院感染与卒中复发的Cox回归分析 经Cox回归分析,模型1中医院感染变量,模型2中医院感染及B2M,模型3中医院感染B2M、冠心病、吸烟和CRP与卒中复发的HR差异均有统计学意义(P<0.05~P<0.01),其余变量均无统计学意义(见表2、图1)。
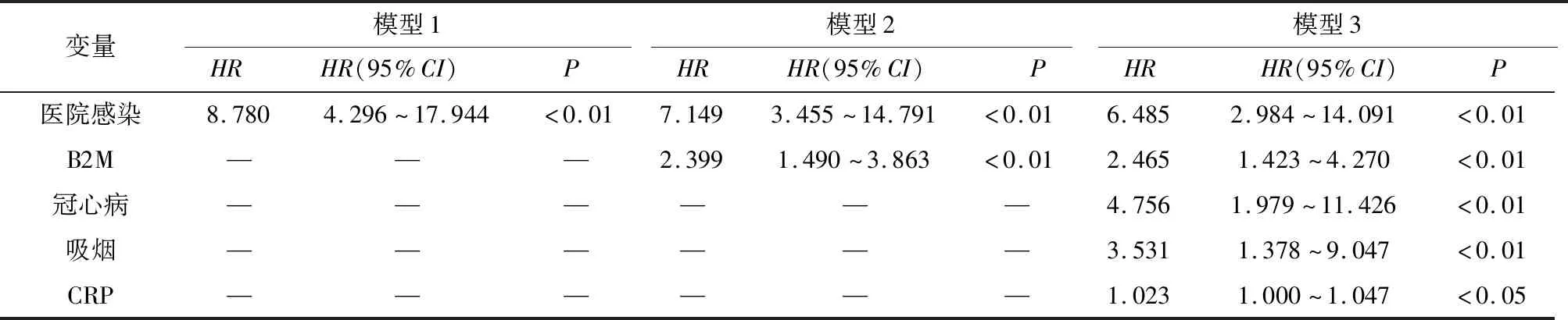
表2 121例卒中病人出院后卒中复发Cox回归分析结果
2.3 影响医院感染发生的二元logistic回归分析 二元logistic回归分析显示,B2M、SBP、NIHSS是AIS病人医院感染的危险因素(P<0.05~P<0.01)(见表3)。

表3 AIS病人医院感染的二元logistic回归分析
3 讨论
本研究对121例AIS病人进行了随访,最短随访时间为3个月,最长随访时间为47个月,期间无失访病例,脑卒中复发率为26.4%。在所有脑卒中的患病人群中,复发型缺血性脑卒中病人的比例高达三分之一[5]。虽然目前仍缺乏有效的预防措施,但通过积极开展可控的风险因素如高血压、血脂水平、吸烟等管理,可以有效预防卒中,尤其是复发型缺血性脑卒中。随着我国脑卒中防治体系的不断完善,动脉再通如静脉溶栓和介入治疗以恢复血液供应和减轻脑损伤技术的完善和推广[11-12],我国脑卒中病人的死亡率近年呈平稳下降趋势,但发病率和患病率仍呈上升趋势[3],因此有必要研究脑卒中复发相关的危险因素。
感染是脑卒中病人最常见的并发症[8-9],AIS病人医院感染可能是卒中复发的一个独立风险因素[13]。本次研究中,近20%的病人在住院期间继发医院感染,经Cox回归分析发现,医院感染是卒中复发的一个独立风险因素(HR=6.485,95%CI:2.984~14.091)。在缺血性脑卒中的发病过程中,因脑组织缺血缺氧,造成缺血核心区脑组织不可逆损伤及坏死,促发卒中后炎症反应,诱导合成和释放炎症相关细胞因子,梗死区域促炎和抗炎细胞因子之间的动态平衡对卒中的发展及预后产生决定性影响[6],而早期脑梗死部位炎症反应的高表达[14-15],则诱发免疫抑制综合征,导致淋巴细胞谱的长期改变和细胞因子产生的紊乱[16],增加了AIS病人医院感染的概率。缺血性卒中有23%的是再发性卒中,缺血性卒中再发的机制复杂,既往研究发现,不同亚型缺血性脑卒中的复发率不同[17],按照TOAST分型,心源性、大动脉硬化性和小动脉梗死型占卒中的主要部分[18]。心源性卒中的再发以房颤为主要原因,部分隐源性卒中病因也是阵发性房颤[19],而大动脉硬化再发性卒中与颈动脉、颅内大动脉的斑块稳定性有关[20],机体的炎症状态与大动脉斑块的稳定性密切相关[21]。最近的研究[22]报道炎症与房颤直接相关,且房颤可能是炎症的直接结果。AIS病人感染后的炎症反应,对大动脉硬化斑块及房颤的影响可能是卒中复发关键因素。当然,炎症与缺血性卒中关系复杂,针对卒中后感染与缺血性卒中的亚型的相关性分析,将可能有助于进一步阐明其中机制。
本研究二元logistic回归分析显示,入院时B2M、NIHSS评分是住院感染的风险因素,而SBP则作用相反。B2M是细胞表面人白细胞抗原(HLA)的β链(轻链)部分,作为一种与炎症相关的生物学标志物,在心血管疾病、肿瘤和淀粉样病变等多个领域被广泛研究,并被建议作为心血管疾病的新兴生物标志物[23-24],用于评估机体免疫及炎症状态[25-26]。NIHSS评分表明病人病情的严重程度[27],高NIHSS评分与卒中相关性感染正相关,提示重症病人卒中相关性感染风险增加。同时研究中发现SBP与卒中相关性感染呈负相关,相关研究发现血压变异度与缺血性卒中预后复发呈正相关,亦是目前研究热点[28],SBP与卒中相关性感染及卒中复发关系研究较少,有待进一步了解其机制。本研究中另外一个炎症相关指标CRP与卒中复发相关,但与医院感染无关联,提示急性缺血性脑卒中损伤与修复过程中,相关炎症指标表达时的时间依赖性。
综上所述,本研究显示AIS病人医院感染可能是卒中复发的一个独立风险因素,通过积极防治医院感染,有利于降低卒中复发的风险。同时急性期病情的改善,有效控制血压对预防卒中复发有重要意义。但本次研究样本量较小,且未对医院感染进行分类,需在后期的研究中补充论证。

