基于标准汤剂的鲜地黄配方颗粒质量标准研究
张志鹏,徐 杰,刘佩仪,黄梦婷,钟志奎,程学仁
基于标准汤剂的鲜地黄配方颗粒质量标准研究
张志鹏1,徐 杰1,刘佩仪1,黄梦婷1,钟志奎1,程学仁2*
1. 广东一方制药有限公司,广东省中药配方颗粒企业重点实验室,广东 佛山 528244 2. 中国中药控股有限公司,广东 佛山 528300
建立基于标准汤剂的鲜地黄配方颗粒质量标准,为鲜地黄配方颗粒质量控制提供参考。根据《中药配方颗粒质量控制与标准制定技术要求》,制备25批鲜地黄标准汤剂,测定各批次标准汤剂的出膏率、指标成分梓醇和地黄苷D的含量,构建能全面表征鲜地黄环烯醚萜苷类成分和苯乙醇苷类成分的UPLC特征图谱;基于标准汤剂出膏率、指标成分含量、特征图谱的一致性,制备3批鲜地黄配方颗粒,验证制定标准的合理性。鲜地黄标准汤剂出膏率实测范围为13.93%~20.09%;梓醇和地黄苷D的质量分数分别为36.14~73.37、2.96~5.33 mg/g;环烯醚萜苷类成分特征图谱共标定了10个共有峰,指认峰3、4、6分别为梓醇、地黄苷D、益母草苷;苯乙醇苷类成分特征图谱共标定了8个共有峰,指认峰1、4、5、6分别为洋地黄叶苷C、毛蕊花糖苷、焦地黄苯乙醇苷B1、异毛蕊花糖苷;3批鲜地黄配方颗粒出膏率、指标成分含量、特征图谱均与同批次药材制备的标准汤剂接近,且均在质量标准规定范围内。该研究建立的基于标准汤剂的鲜地黄配方颗粒质量标准科学合理、稳定可行,可为鲜地黄配方颗粒的质量控制提供参考。
鲜地黄;标准汤剂;配方颗粒;质量标准;梓醇;地黄苷D;益母草苷;洋地黄叶苷C;毛蕊花糖苷;焦地黄苯乙醇苷B1;异毛蕊花糖苷
鲜地黄为玄参科植物地黄Libosch.的新鲜块根,鲜用,具有清热生津、凉血、止血的功效,主治热病伤阴、舌绛烦渴、温毒发斑、吐血、衄血、咽喉肿痛等症[1]。鲜地黄始载于《神农本草经》,列为上品,用于治疗高热急证和血热妄行、吐血衄血[2]。近代,鲜地黄的应用仍较为广泛,在《中国药典》1963~2020年版中均有收载[3]。研究表明,鲜地黄主要含有环烯醚萜苷类和苯乙醇苷类成分,包括梓醇、地黄苷D、桃叶珊瑚苷、益母草苷、京尼平苷、焦地黄苯乙醇苷A1、毛蕊花糖苷、焦地黄苯乙醇苷B1、异毛蕊花糖苷等[4-6]。相比于生地黄,鲜地黄在消炎抗菌、凉血止血以及免疫作用等方面表现出更为显著的疗效[7-9]。
中药饮片标准汤剂是以中医理论为指导、临床应用为基础,参考现代提取方法,经标准化工艺制备而成的单味中药饮片水煎剂,用于规范和标化临床用药[10]。《中药配方颗粒质量控制与标准制定技术要求》规定,中药配方颗粒所有药学研究,包括工艺参数确定、质控方法和指标选择、限度制定等,均应与标准汤剂进行对比研究。2021年2月,国家药监局等4部门联合发布了《关于结束中药配方颗粒试点工作的公告》,规定自2021年11月1日起,所有不具有国家药品标准或省级药品监督管理部门制定标准的中药配方颗粒均不得上市销售。因此,为保证鲜地黄配方颗粒的市场供应,建立鲜地黄配方颗粒质量标准已迫在眉睫。本研究根据《中药配方颗粒质量控制与标准制定技术要求》,采集了25批不同产地的鲜地黄药材,制备标准汤剂,并以与标准汤剂出膏率、指标成分含量、特征图谱3大指标的一致性为表征,建立了鲜地黄配方颗粒质量标准,以期为鲜地黄配方颗粒及其他新型饮片的质量评价与控制提供参考。
1 仪器与材料
1.1 仪器
Waters Acquity型超高效液相色谱系统,包括真空脱气机、二元梯度泵、自动进样器、柱温箱、TUV检测器、Empower数据处理系统,美国Waters公司;ME203E型万分之一分析天平、XP26型百万分之一天平,美国Mettler Toledo公司;TRL-0.5型真空冷冻干燥机,大连双瑞科技有限公司;DN1000型多功能提取罐、NS200型单效浓缩器,江苏华泰重工装备有限公司;SODA-45型喷雾干燥机,上海大川原干燥设备有限公司;LGS20型干法制粒机,南京迦南制药设备有限公司;MiliQ Direct 8型超纯水机,德国默克密理博公司。
1.2 材料
对照品梓醇(批号110808-201711,质量分数99.6%)、毛蕊花糖苷(批号111530-201914,质量分数95.2%),中国食品药品检定研究院;对照品地黄苷D(批号ST11190120,质量分数98.0%),上海诗丹德标准技术服务有限公司;对照品益母草苷(批号17122601,质量分数99.62%),成都普菲德生物技术有限公司;对照品洋地黄叶苷C(批号DST201109-057,质量分数98.0%)、焦地黄苯乙醇苷B1(批号DST201203-071,质量分数98.0%),成都乐美天医药科技有限公司;对照品异毛蕊花糖苷(批号PS0003-0020,质量分数98.0%),成都普思生物科技股份有限公司。麦芽糊精(批号FH1905002),中粮生化能源(公主岭)有限公司;色谱级甲醇、乙腈,德国默克股份两合公司;色谱纯磷酸,天津市科密欧化学试剂有限公司;水为超纯水,其余试剂均为分析纯。
25批鲜地黄药材(Y1~Y25)均经广东一方制药有限公司孙冬梅主任中药师鉴定,为玄参科地黄属植物地黄Libosch.的新鲜块根,来源信息见表1。
2 方法与结果
2.1 标准汤剂与配方颗粒的制备
2.1.1 标准汤剂 根据《中药配方颗粒质量控制与标准制定技术要求》,称取鲜地黄饮片100 g,置电陶瓷壶中,加水煎煮2次;第1次加9倍量水,浸泡30 min,武火煮沸后,改文火保持微沸,继续煎煮30 min,滤过;第2次加7倍量水,武火煮沸后,改文火保持微沸,继续煎煮25 min,滤过;合并2次滤液,低温减压浓缩至投料量(清膏-投料量1∶1),在磁力搅拌下,分装至10 mL西林瓶中,每瓶分装约2 mL,分装完毕后转移至真空冷冻干燥机中冻干,即得标准汤剂。
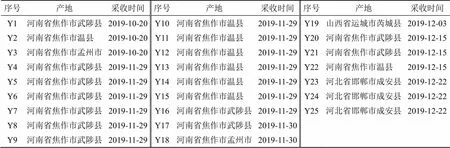
表1 25批鲜地黄药材来源信息
2.1.2 配方颗粒 取鲜地黄饮片5000 g,加水煎煮2次;第1次加9倍量水,浸泡30 min,武火煮沸后,改文火保持微沸,继续煎煮30 min,滤过;第2次加7倍量水,武火煮沸后,改文火保持微沸,继续煎煮25 min,滤过;合并2次并滤液,滤液减压浓缩成相对密度为1.04~1.08 g/cm3(80 ℃)的清膏,加麦芽糊精适量,混匀,喷雾干燥(进风温度175~185 ℃,出风温度85~95 ℃),得干浸膏粉;再加麦芽糊精适量,混匀,干法制粒(压辊压力15~20 MPa,输料转速为20~45 r/min,压轮转速3.5~5.5 r/min),制成1000 g,即得配方颗粒。
2.2 出膏率测定
标准汤剂出膏率以冻干粉量/饮片量计;配方颗粒出膏率以干浸膏粉量(扣除辅料)/投料量计。结果(表2)显示,25批鲜地黄标准汤剂(S1~S25)的出膏率为13.93%~20.09%,平均值为(17.23±1.68)%;3批配方颗粒(C20~C22)的出膏率分别为18.03%、18.15%、19.07%,平均值为(18.42±0.57)%。根据25批鲜地黄标准汤剂出膏率的浮动范围以及3批配方颗粒出膏率的实际情况,鲜地黄配方颗粒制成量(制成的配方颗粒总量/投料量)拟定为20.0%,即每1 g配方颗粒相当于饮片5.0 g。
2.3 梓醇定量测定
2.3.1 供试品溶液的制备 取鲜地黄标准汤剂/配方颗粒适量,研细,取约0.1 g,精密称定,置具塞锥形瓶中,精密加入60%甲醇25 mL,密塞,称定质量,超声处理(功率250 W、频率40 kHz)30 min,放冷,再称定质量,用60%甲醇补足减失的质量,摇匀,滤过,精密量取续滤液10 mL,浓缩至近干,残渣用流动相溶解,转移至10 mL量瓶中,加流动相至刻度,摇匀,滤过,取续滤液即得供试品溶液。

表2 25批标准汤剂及3批配方颗粒出膏率
S1~S25为25批药材(Y1~Y25)制备的标准汤剂,C20~C22为S20~S22同批次药材(Y20~Y22)制备的配方颗粒,S20~S22下称随行标准汤剂
S1—S25 are standard decoction prepared from 25 batches of medicinal materials (Y1—Y25), C20—C22 are formula particles prepared from the same batch of medicinal materials (Y20—Y22) in S20—S22, and S20—S22 are hereinafter referred to as accompanying standard decoction
2.3.2 对照品储备液的制备 精密称取梓醇对照品5.285 mg,加流动相溶解,并定容至5 mL,制成质量浓度为1 052.772 µg/mL的对照品储备液,摇匀,备用。
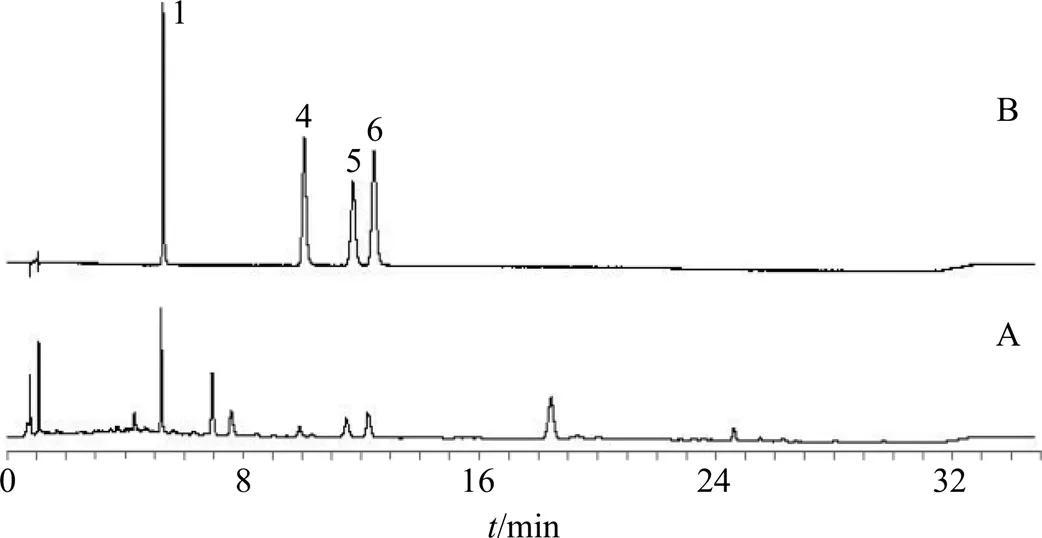
2.3.3 色谱条件 采用Waters Acquity HSS T3(100 mm×2.1 mm,1.8 mm)色谱柱;流动相为甲醇-0.1%磷酸水溶液(1∶99);检测波长为210 nm;体积流量0.3 mL/min;柱温30 ℃;进样量2 μL。梓醇对照品溶液以及鲜地黄标准汤剂供试品溶液色谱图如图1所示。
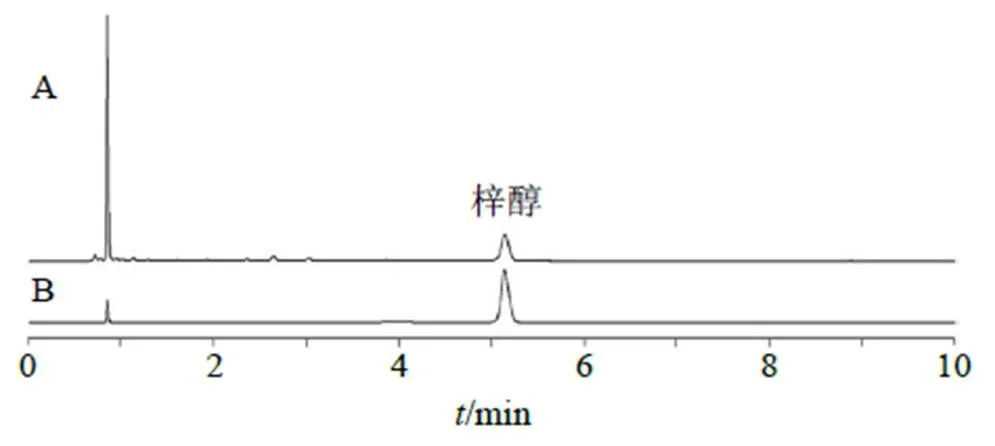
图1 鲜地黄标准汤剂(A)和梓醇对照品(B)的UPLC图
2.3.4 线性关系考察 分别精密吸取梓醇对照品储备液0.10、0.25、0.50、1.00、2.50 mL,置于5 mL量瓶中,加流动相定容至刻度,摇匀,制成含梓醇21.055、52.639、105.277、210.554、526.386 µg/mL的对照品溶液。精密吸取各质量浓度的对照品溶液,按“2.3.3”项下色谱条件分别进样测定,记录峰面积。以梓醇对照品质量浓度为横坐标(),峰面积为纵坐标(),绘制标准曲线,得回归方程= 1 573.3-7 311.9,2=0.999 4,结果表明梓醇在21.055~526.386 μg/mL与峰面积线性关系良好。
2.3.5 精密度考察 取鲜地黄标准汤剂(S3)供试品溶液,按“2.3.3”项下色谱条件连续进样6次,计算得到梓醇峰面积的RSD为0.70%,表明仪器精密度良好。
2.3.6 稳定性考察 取鲜地黄标准汤剂(S3)供试品溶液,按“2.3.3”项下色谱条件,分别在制备后0、2、4、8、16、24 h进样测定,计算得到梓醇峰面积的RSD为1.21%,表明供试品溶液在24 h内稳定性良好。
2.3.7 重复性考察 分别取鲜地黄标准汤剂(S3)供试品6份,按“2.3.1”项下方法制备供试品溶液,按“2.3.3”项下色谱条件进样测定,计算得到梓醇质量分数的RSD为2.17%,表明该方法重复性良好。
2.3.8 加样回收率考察 取鲜地黄标准汤剂(S3)样品9份,每份0.05 g,精密称定,置于锥形瓶中,平均分为3组。分别向3组锥形瓶中精密加入梓醇对照品(梓醇对照品加入量与所取样品中梓醇成分含量之比控制在0.5∶1、1∶1、1.5∶1),按“2.3.1”项下方法制备供试品溶液,按“2.3.3”项下色谱条件进样测定,计算梓醇得平均加样回收率为101.95%,RSD为2.55%,表明该方法的准确度良好。
2.3.9 梓醇定量测定 取25批鲜地黄标准汤剂样品,分别按“2.3.1”项下方法制备供试品溶液,按“2.3.3”项下色谱条件进样测定,结果见表3。可见,25批鲜地黄标准汤剂中梓醇的质量分数为36.14~73.37 mg/g,平均值为(52.83±8.79)mg/g;3批配方颗粒中梓醇的质量分数分别为42.65、39.79、38.66 mg/g,稍低于3批随行标准汤剂按制成量20.0%折算后的质量分数。

表3 25批标准汤剂指标成分含量测定结果
2.4 地黄苷D定量测定
2.4.1 供试品溶液的制备 除残渣用“2.4.3”项下流动相溶解并定容外,其他操作同“2.3.1”项方法。
2.4.2 对照品储备液的制备 精密称取地黄苷D对照品1.444 mg,加流动相溶解并定容至5 mL,制成质量浓度为283.024 µg/mL的对照品储备液,摇匀,备用。
2.4.3 色谱条件 采用Waters Acquity HSS T3(100 mm×2.1 mm,1.8 mm)色谱柱;流动相为乙腈-0.1%磷酸水溶液(5∶95),检测波长为203 nm;体积流量0.3 mL/min;柱温30 ℃;进样量2 μL。地黄苷D对照品溶液以及鲜地黄标准汤剂供试品溶液色谱图如图2所示。

图2 鲜地黄标准汤剂(A)和地黄苷D对照品(B)的UPLC图
2.4.4 线性关系考察 分别精密吸取地黄苷D对照品储备液0.10、0.25、0.50、1.00、2.50 mL,置于5 mL量瓶中,加流动相定容至刻度,摇匀,制成含地黄苷D 5.660、14.151、28.302、56.605、141.512 µg/mL的对照品溶液。精密吸取各质量浓度的对照品溶液,按“2.4.3”项下色谱条件分别进样测定,记录峰面积。以地黄苷D对照品质量浓度为横坐标(),峰面积为纵坐标(),绘制标准曲线,求得回归方程=2 811.3-3 560.3,2=0.999 4,结果表明,地黄苷D在5.661~141.512 μg/mL与峰面积线性关系良好。
2.4.5 精密度考察 取鲜地黄标准汤剂(S3)供试品溶液,按“2.4.3”项下色谱条件连续进样6次,计算得到地黄苷D峰面积的RSD为0.43%,表明仪器精密度良好。
2.4.6 稳定性考察 取鲜地黄标准汤剂(S3)供试品溶液,按“2.4.3”项下色谱条件,分别在制备后0、2、4、8、16、24 h进样测定,计算得到地黄苷D峰面积的RSD为0.83%,表明供试品溶液在24 h内稳定性良好。
2.4.7 重复性考察 分别取鲜地黄标准汤剂(S3)供试品6份,按“2.4.1”项下方法制备供试品溶液,按“2.4.3”项下色谱条件进样测定,计算得到地黄苷D质量分数的RSD为1.39%,表明该方法重复性良好。
2.4.8 加样回收率考察 取鲜地黄标准汤剂(S3)供试品9份,每份0.05 g,精密称定,置于锥形瓶中,平均分为3组。分别向3组锥形瓶中精密加入地黄苷D对照品(地黄苷D对照品加入量与所取供试品中地黄苷D成分含量之比控制在0.5∶1、1∶1、1.5∶1),按“2.4.1”项下方法制备供试品溶液,按“2.4.3”项下色谱条件进样测定,计算得地黄苷D的平均加样回收率为101.92%,RSD为2.55%,表明该方法的准确度良好。
2.4.9 地黄苷D定量测定 取25批鲜地黄标准汤剂样品,分别按“2.4.1”项下方法制备供试品溶液,按“2.4.3”项下色谱条件进样测定,结果见表3。25批鲜地黄标准汤剂中地黄苷D质量分数为2.96~5.33 mg/g,平均值为(3.73±0.57)mg/g;3批配方颗粒中地黄苷D质量分数分别为3.15、3.26、3.16 mg/g,与3批随行标准汤剂按制成量20.0%折算后的质量分数基本一致。
2.5 环烯醚萜苷类成分特征图谱建立
2.5.1 供试品溶液的制备 取鲜地黄标准汤剂/配方颗粒适量,研细,取约0.2 g,精密称定,置具塞锥形瓶中,精密加入60%甲醇25 mL,称定质量,超声处理(功率250 W、频率45 kHz)60 min,放冷,再称定质量,用60%甲醇补足减失的质量,摇匀,滤过,精密量取续滤液10 mL,浓缩至近干,残渣加0.1%磷酸水溶液溶解,转移至10 mL量瓶中,加0.1%磷酸水溶液至刻度,摇匀,滤过,取续滤液,即得。
2.5.2 对照品溶液的制备 精密称取梓醇、地黄苷D、益母草苷对照品适量,精密称定,加0.1%磷酸水溶液溶解并定容,制成混合对照品溶液。
2.5.3 色谱条件 采用Waters Acquity HSS T3(100 mm×2.1 mm,1.8 mm)色谱柱;以乙腈-0.1%磷酸水溶液为流动相,梯度洗脱:0~5 min,100% 0.1%磷酸水溶液;5~7 min,0~5%乙腈;7~10 min,5%乙腈;10~16 min,5%~11%乙腈;16~18 min,11%~16%乙腈;18~35 min,16%~30%乙腈;柱温30 ℃;检测波长203 nm;体积流量0.3 mL/min;进样量2 μL。
2.5.4 精密度考察 取鲜地黄标准汤剂(S3)供试品溶液,按“2.5.3”项下色谱条件,连续进样6次,以4号地黄苷D色谱峰为参照峰(S,相比于梓醇和益母草苷,4号峰指认为地黄苷D,保留时间和峰面积居中,且作为环烯醚萜三糖苷,在量值传递过程中较为稳定[11-12],故作为参照峰),计算得各特征峰与S峰的相对保留时间与相对峰面积的RSD均小于4%,表明仪器的精密度良好。
2.5.5 稳定性考察 取鲜地黄标准汤剂(S3)供试品溶液,按“2.5.3”项下色谱条件,分别在样品制备后的0、2、4、8、16、24 h进样检测,计算得各特征峰与S峰的相对保留时间与相对峰面积的RSD均小于3%,表明供试品溶液在24 h内稳定性良好。
2.5.6 重复性考察 取鲜地黄标准汤剂(S3)适量,按“2.5.1”项下方法制备供试品溶液,平行6份,按“2.5.3”项下色谱条件进样测定,计算得各特征峰与S峰的相对保留时间与相对峰面积的RSD均小于4%,表明该方法重复性良好。
2.5.7 特征图谱的建立及共有峰的确定 取25批鲜地黄标准汤剂(S1~S25),按照“2.5.1”项下方法制备供试品溶液,按照“2.5.3”项下色谱条件进样检测,记录各特征峰相对保留时间和相对峰面积,计算平均值,结果见表4。
将各批次标准汤剂特征图谱数据导入“中药色谱指纹图谱相似度评价系统(2012版)”软件进行处理,建立鲜地黄标准汤剂的对照特征图谱(R),结果如图3所示。计算相似度,25批鲜地黄标准汤剂(S1~S25)与R的相似度分别为0.999、0.999、0.999、0.999、0.999、0.999、0.999、0.998、1.000、0.999、0.997、0.999、0.995、0.998、1.000、0.998、0.999、0.994、1.000、1.000、0.999、0.999、0.998、0.998、0.993,均大于0.99,表明建立的特征图谱检测方法适应性良好,符合标准汤剂的要求。建立的特征图谱共标定了10个共有峰,通过对照品比对,对峰3(梓醇)、4(地黄苷D)、6(益母草苷)进行了指认,结果如图4所示。
取3批鲜地黄配方颗粒(C20~C22),按照“2.5.1”项下方法制备供试品溶液,按照“2.5.3”项下色谱条件进样检测,结果见图5。记录各特征峰相对保留时间和相对峰面积,结果见表5、6。结果表明,3批配方颗粒特征图谱均呈现与R相同的10个特征峰,且各特征峰的相对保留时间和相对峰面积与随行标准汤剂基本一致。

表4 共有峰相对保留时间与相对峰面积均值(环烯醚萜苷类)

图3 25批鲜地黄标准汤剂UPLC特征图谱(环烯醚萜苷类)
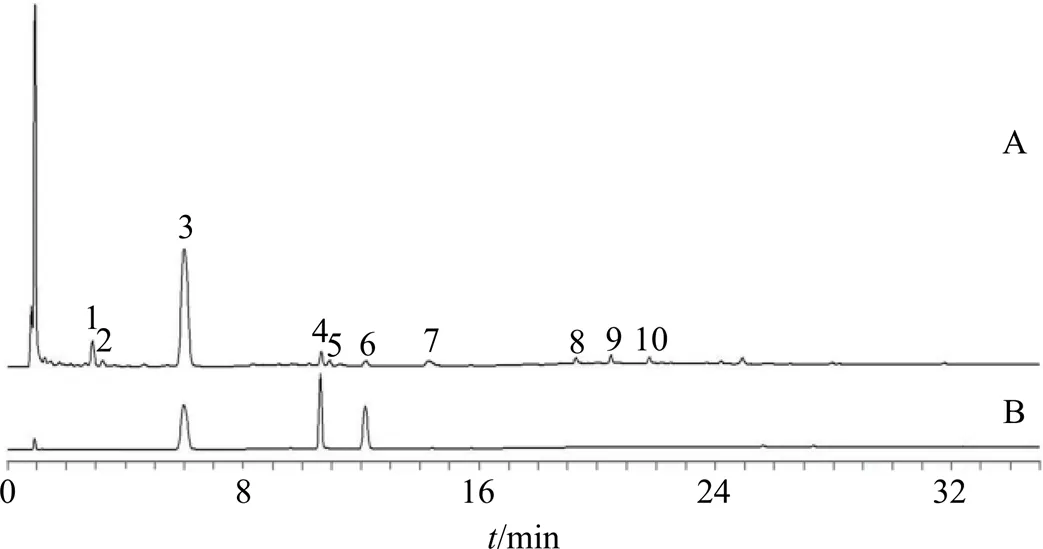
3-梓醇 4-地黄苷D 6-益母草苷
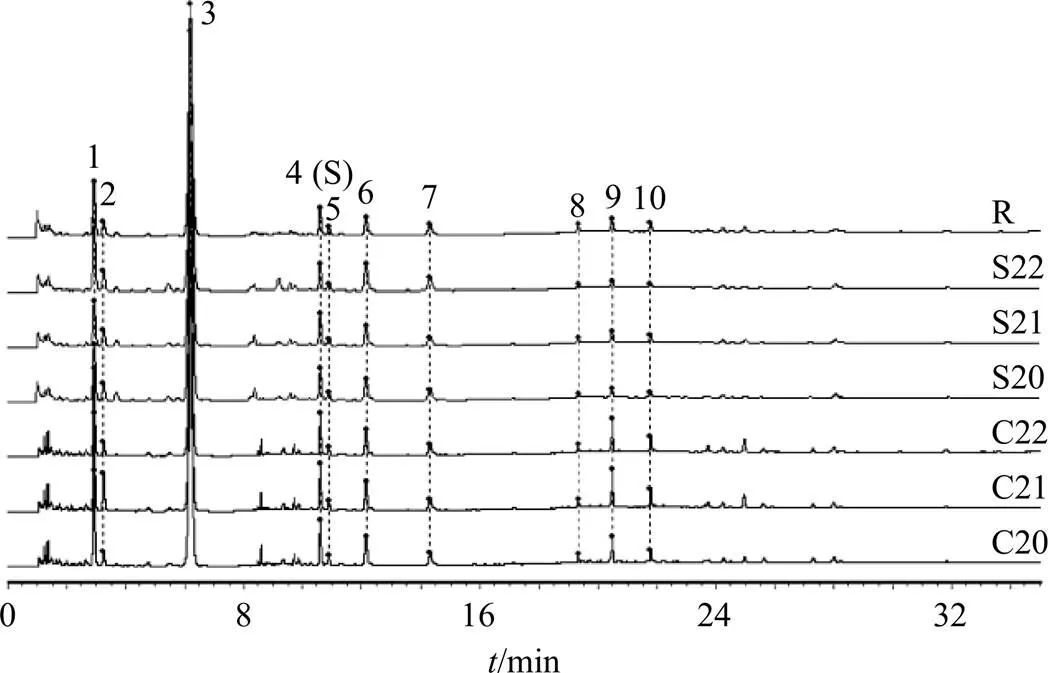
图5 3批鲜地黄配方颗粒与随行标准汤剂的UPLC特征图谱及对照特征图谱(R) (环烯醚萜苷类)
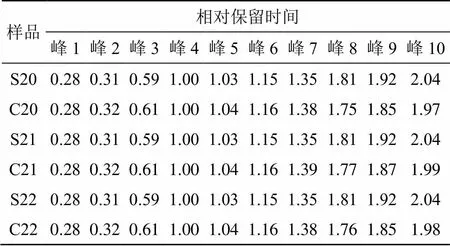
表5 3批鲜地黄配方颗粒与随行标准汤剂特征图谱相对保留时间比较(环烯醚萜苷类)

表6 3批鲜地黄配方颗粒与随行标准汤剂特征图谱相对峰面积比较(环烯醚萜苷类)
2.6 苯乙醇苷类成分特征图谱建立
2.6.1 供试品溶液制备 取标准汤剂/配方颗粒适量,研细,取约0.2 g,精密称定,置具塞锥形瓶中,精密加入30%甲醇20 mL,密塞,称定质量,超声处理(功率250 W、频率40 kHz)20 min,放冷,再称定质量,用30%甲醇补足减失的质量,摇匀,滤过,取续滤液,即得供试品溶液。
2.6.2 对照品溶液的制备 精密称取洋地黄叶苷C、毛蕊花糖苷、焦地黄苯乙醇苷B1、异毛蕊花糖苷对照品适量,精密称定,加甲醇溶解并定容,制成混合对照品溶液。
2.6.3 色谱条件 采用Waters Acquity HSS T3(100 mm×2.1 mm,1.8 mm)色谱柱;以乙腈-0.1%磷酸水溶液为流动相,梯度洗脱:0~3 min,0~16%乙腈;3~10 min,16%~17.5%乙腈;10~20 min,17.5%~21%乙腈;20~22 min,21%~26%乙腈;22~27 min,26%~30%乙腈;27~30 min,30%乙腈;柱温35 ℃;检测波长330 nm;体积流量0.3 mL/min;进样量4 μL。
2.6.4 精密度考察 取鲜地黄标准汤剂(S3)供试品溶液,按“2.6.3”项下色谱条件,连续进样6次,以5号焦地黄苯乙醇苷B1色谱峰为参照峰[S,指认的4个特征峰均为苯乙醇苷类成分,洋地黄叶苷C出峰时间较早,与峰8相距较远,不宜作为参照峰;峰4和峰6为毛蕊花糖苷和异毛蕊花糖苷,受热会相互转化,是热敏性成分[13-14],不宜作为参照峰;峰5(焦地黄苯乙醇苷B1)保留时间居中,性质相对稳定,故选择为参照峰],计算得各特征峰与S峰的相对保留时间与相对峰面积的RSD值均小于4%,表明仪器的精密度良好。
2.6.5 稳定性考察 取鲜地黄标准汤剂(S3)供试品溶液,按“2.6.3”项下色谱条件,分别在样品制备后的0、2、4、8、16、24 h进样检测,计算得各特征峰与S峰的相对保留时间与相对峰面积的RSD均小于4%,表明供试品溶液在24 h内稳定性良好。
2.6.6 重复性考察 取鲜地黄标准汤剂(S3)适量,按“2.6.1”项下方法制备供试品溶液,平行6份,按“2.6.3”项下色谱条件进样测定,计算得各特征峰与S峰的相对保留时间与相对峰面积的RSD均小于4%,表明该方法重复性良好。
2.6.7 特征图谱的建立及共有峰的确定 取25批鲜地黄标准汤剂(S1~S25),按照“2.6.1”项下方法制备供试品溶液,按照“2.6.3”项下色谱条件进样检测,记录各特征峰相对保留时间和相对峰面积,计算平均值,结果见表7。
将各批次标准汤剂特征图谱数据导入“中药色谱指纹图谱相似度评价系统(2012版)”软件进行处理,建立鲜地黄标准汤剂R,结果如图6所示。计算相似度,25批鲜地黄标准汤剂(S1~S25)与R的相似度分别为0.975、0.978、0.978、0.994、0.976、0.937、0.943、0.887、0.873、0.890、0.948、0.958、0.985、0.969、0.974、0.933、0.954、0.934、0.895、0.894、0.975、0.852、0.837、0.901、0.847,均大于0.83,表明建立的特征图谱检测方法适应性良好,符合标准汤剂的要求。
建立的特征图谱共标定了8个共有峰,通过对照品比对,对峰1(洋地黄叶苷C)、4(毛蕊花糖苷)、5(焦地黄苯乙醇苷B1)、6(异毛蕊花糖苷)进行了指认,结果如图7所示。

表7 共有峰相对保留时间与相对峰面积均值(苯乙醇苷类)

图6 25批鲜地黄标准汤剂UPLC特征图谱(苯乙醇苷类)
取3批鲜地黄配方颗粒(C20~C22),按照“2.6.1”项下方法制备供试品溶液,按照“2.6.3”项下色谱条件进样检测,结果见图8。记录各特征峰相对保留时间和相对峰面积,见表8、9。结果表明,3批配方颗粒特征图谱均呈现与对照特征图谱相同的8个特征峰,且各特征峰的相对保留时间和相对峰面积与随行标准汤剂基本一致。
1-洋地黄叶苷C 4-毛蕊花糖苷 5-焦地黄苯乙醇苷B1 6-异毛蕊花糖苷
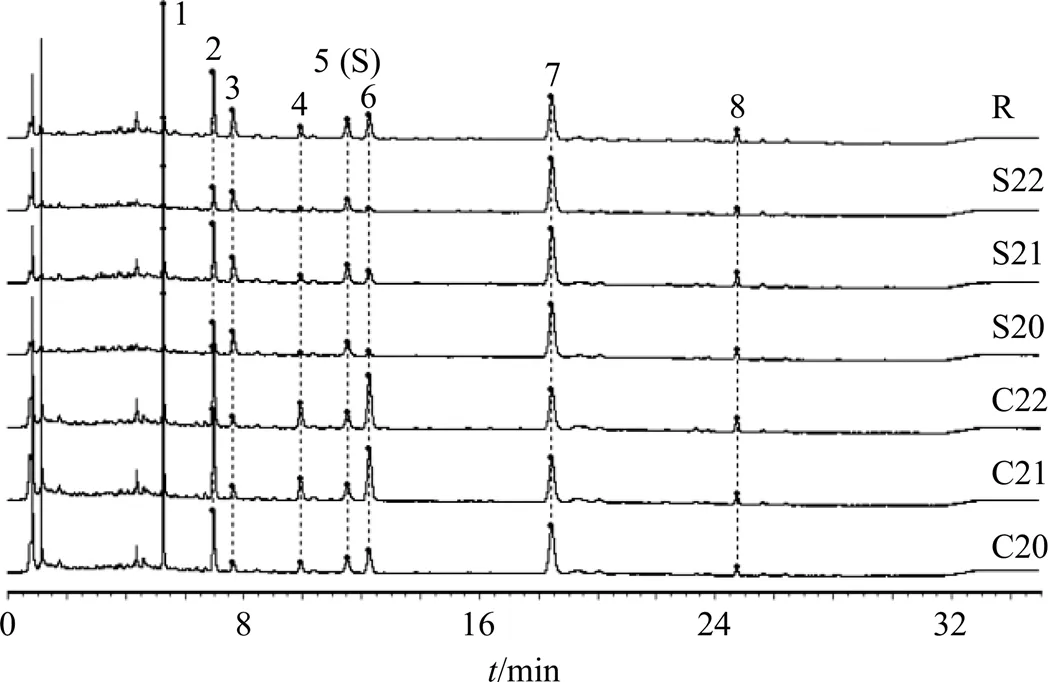
图8 3批鲜地黄配方颗粒与随行标准汤剂的UPLC特征图谱及对照特征图谱(R) (苯乙醇苷类)

表8 3批鲜地黄配方颗粒与随行标准汤剂特征图谱相对保留时间比较(苯乙醇苷类)
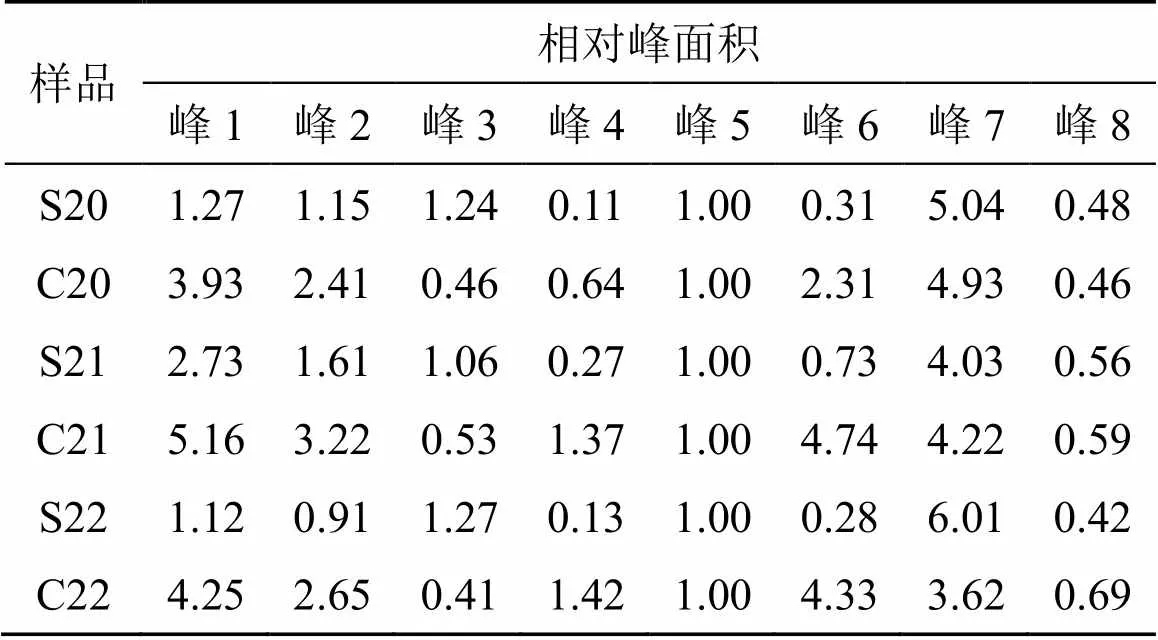
表9 3批鲜地黄配方颗粒与随行标准汤剂特征图谱相对峰面积比较(苯乙醇苷类)
3 讨论
3.1 出膏率范围的确定
《中药配方颗粒质量控制与标准制定技术要求》标准汤剂的表征与应用项下建议,以干膏粉计算浸膏得率及标准偏差,以均值加减3倍SD(或均值的70%~130%)为出膏率的允许范围。25批鲜地黄标准汤剂出膏率平均值为(17.19±1.57)%。若鲜地黄标准汤剂出膏率取均值±3倍SD范围或取均值的70%~130%,即12.49%~21.88%或12.03%~22.34%,二者范围较为接近;为严格控制大生产中的鲜地黄配方颗粒的出膏率,保证鲜地黄配方颗粒的质量均一和稳定,结合25批鲜地黄标准汤剂出膏率的浮动范围以及3批配方颗粒出膏率的实际情况,由鲜地黄配方颗粒制成量确定为20.0%,故建议鲜地黄配方颗粒干浸膏出膏率应取均值的70%~制成量20%,即控制在12.03%~20.0%为宜,修约为12.0%~20.0%。
3.2 指标成分选择及含量范围的确定
研究表明,梓醇为地黄环烯醚萜苷类成分发挥降血糖生物活性的主要药效物质基础[15],其可以调节脂肪细胞的糖脂代谢,通过活化位于肾上腺髓质的肾上腺受体,促进β-内啡肽释放,提高葡萄糖运转蛋白-4(glucose transporter 4,GLUT-4)的表达,从而提高葡萄糖转运率,增加葡萄糖利用,抑制糖异生,降低链尿佐菌素诱导的糖尿病大鼠血糖[16-17]。张莉等[18]发现地黄苷D可能是地黄发挥抗抑郁作用的重要物质基础之一,地黄苷D可有效缓解由高浓度皮质酮诱导的PC-12细胞损伤,其作用机制可能为提高BDNF表达,并通过BDNF-TrkB通路发挥抗凋亡作用,最终保护神经细胞,从而发挥抗抑郁作用[19]。说明梓醇和地黄苷D均为地黄的活性成分,且《中国药典》2020年版一部地黄含量测定项下的指标成分亦为梓醇和地黄苷D,故本研究以梓醇和地黄苷D作为鲜地黄配方颗粒质量控制的指标成分。本研究分别考察了提取溶剂、提取方式、溶剂用量以及提取时间,对鲜地黄标准汤剂/配方颗粒梓醇和地黄苷D含量的影响。结果表明,加入60%甲醇25 mL,超声提取30 min,效率高、效果好、溶剂用量少。
《中药配方颗粒质量控制与标准制定技术要求》标准汤剂的表征与应用项下建议,根据含量测定得到的指标成分的含量,以均值加减3倍SD(或均值的70%~130%)为含量测定的允许范围。25批鲜地黄标准汤剂中梓醇质量分数均值为52.83 mg/g,SD为8.79 mg/g。含量范围若取均值加减3倍SD的范围为26.46~79.21 mg/g,25批标准汤剂梓醇含量均在范围内,范围过宽,不利于产品的质量控制;若取均值70%~130%的范围为36.98~68.68 mg/g,25批鲜地黄标准汤剂中有2批不在范围内,为S13(36.14 mg/g)和S17(73.37 mg/g),所占比例较小,利于鲜地黄配方颗粒的质量稳定和大生产质量的控制,故认为鲜地黄标准汤剂梓醇含量范围取均值的70%~130%较为合理,即控制在36.98~68.68 mg/g为宜。相应的鲜地黄配方颗粒梓醇的含量范围取标准汤剂按制成量20.0%折算后均值的70%~130%,即31.91~59.26 mg/g,3批鲜地黄配方颗粒梓醇含量均在此范围内。
25批鲜地黄标准汤剂中地黄苷D质量分数均值为3.73 mg/g,SD为0.57 mg/g。质量分数范围若取均值加减3倍SD的范围,即2.01~5.46 mg/g,25批标准汤剂地黄苷D含量均在范围内,范围过宽,不利于产品的质量控制;若取均值70%~130%的范围为2.61~4.85 mg/g,25批鲜地黄标准汤剂中有1批不在范围内,为S11(5.33 mg/g),所占比例较小,利于鲜地黄配方颗粒的质量稳定和大生产质量的控制,认为鲜地黄标准汤剂地黄苷D的含量范围取均值的70%~130%较为合理,即控制在2.61~4.85 mg/g为宜。相应的鲜地黄配方颗粒地黄苷D的含量范围取标准汤剂按制成量20.0%折算后均值的70%~130%,即2.24~4.16 mg/g,3批鲜地黄配方颗粒地黄苷D含量均在此范围内。
3.3 特征图谱相对保留时间与相对峰面积范围的确定
鲜地黄主要含有环烯醚萜苷类和苯乙醇苷类成分,环烯醚萜苷类成分极性强,具有较好的水溶性,且在203 nm的波长处有较强的吸收;苯乙醇苷类成分极性较弱,在330 nm的波长处有较强的吸收,由于鲜地黄中环烯醚萜苷成分梓醇的含量较高,苯乙醇苷类成分含量均较低,难以将环烯醚萜苷类和苯乙醇苷类成分呈现在同一色谱图上,为了保证各特征峰的有效分离以及基线平稳,降低杂质峰的干扰,本研究分别建立了表征环烯醚萜苷类成分和苯乙醇苷类成分的特征图谱。此外,研究表明,鲜地黄在加工成生地黄和熟地黄的过程中,环烯醚萜苷类成分会发生降解反应,脱去糖基,生成非苷类环烯醚萜成分,降解程度与连接糖基的数目有关[11]。本课题组对比了鲜地黄、生地黄和熟地黄配方颗粒环烯醚萜苷类成分特征图谱,发现生地黄和熟地黄配方颗粒中缺失峰8,且熟地黄配方颗粒中几乎无法检出峰3(梓醇),故建立的环烯醚萜苷类成分特征图谱,可用于鲜地黄配方颗粒专属性鉴别。
此外,地黄中的苯乙醇苷类成分具有显著的抗氧化活性[20],建立苯乙醇苷类成分特征图谱亦对鲜地黄配方颗粒质量控制具有重要意义。本研究分别考察了不同提取溶剂、提取方式、溶剂用量以及提取时间对鲜地黄标准汤剂/配方颗粒特征图谱的影响。结果表明,加入60%甲醇25 mL,超声提取60 min,环烯醚萜苷类成分各特征峰响应值较高,溶剂用量少;加30%甲醇20 mL,超声提取20 min,苯乙醇苷类成分各特征峰响应值较高、溶剂用量少、效率高。
环烯醚萜苷类成分:以峰4地黄苷D峰为参照峰S,25批鲜地黄标准汤剂各特征峰与S峰的相对保留时间的RSD在0.21%~2.23%;说明各特征峰的相对保留时间较稳定,因此,可以利用相对保留时间均值对特征峰进行定位。根据25批鲜地黄标准汤剂的对照特征图谱信息,鲜地黄标准汤剂供试品色谱中应呈现10个特征峰,与地黄苷D参照物峰相对应的峰为S峰,计算各特征峰与S峰的相对保留时间,其相对保留时间应该在规定值的±10%之内,规定值为0.27(峰1)、0.31(峰2)、0.58(峰3)、1.03(峰5)、1.15(峰6)、1.34(峰7)、1.81(峰8)、1.91(峰9)、2.03(峰10)。各特征峰与S峰的相对峰面积的RSD在24.57%~59.62%,说明不同批次的样品相对峰面积相差较大,表明不同批次鲜地黄标准汤剂各特征峰所代表的化学成分的比例存在较大的差异,不建议对特征峰的相对峰面积作出规定。
苯乙醇苷类成分:以峰5焦地黄苯乙醇苷B1峰为参照峰S,25批鲜地黄标准汤剂各特征峰与S峰的相对保留时间的RSD在0~0.83%;说明各特征峰的相对保留时间较稳定,因此,可以利用相对保留时间均值对特征峰进行定位。根据25批鲜地黄标准汤剂的对照特征图谱信息,鲜地黄标准汤剂供试品色谱中应呈现8个特征峰,与焦地黄苯乙醇苷B1参照物峰相对应的峰为S峰,计算各特征峰与S峰的相对保留时间,其相对保留时间应该在规定值的±10%之内,规定值为0.46(峰1)、0.61(峰2)、0.66(峰3)、0.86(峰4)、1.06(峰6)、1.60(峰7)、2.14(峰8)。各特征峰与S峰的相对峰面积的RSD在27.59%~109.65%,说明不同批次的样品相对峰面积相差较大,表明不同批次鲜地黄标准汤剂各特征峰所代表的化学成分的比例存在较大的差异,不建议对特征峰的相对峰面积作出规定。
本研究基于与鲜地黄标准汤剂的一致性,进行配方颗粒的制备工艺研究,确定了鲜地黄配方颗粒生产工艺,制备的配方颗粒各指标均在标准汤剂规定范围内。同时,本课题组开展了鲜地黄和生地黄配方颗粒的药效学对比研究,发现鲜地黄配方颗粒对脂多糖致大鼠体温上升的抑制率明显强于生地黄配方颗粒。由此可见,本研究建立的鲜地黄配方颗粒质量标准科学合理,配方颗粒的制备工艺基本可行,可为鲜地黄配方颗粒国家标准的制定提供指导。
利益冲突 所有作者均声明不存在利益冲突
[1] 中国药典[S]. 一部. 2020: 129-130.
[2] 张昭, 李志亮, 肖培根. 浅议鲜用植物药的研究现状及发展方向 [J]. 中草药, 1998(11): 781-783.
[3] 徐杰, 张志鹏, 陈丹燕, 等. 中药鲜药的现代应用与研究进展 [J]. 中国现代中药, 2022, 24(1): 160-168.
[4] 张波泳, 江振作, 王跃飞, 等. UPLC/ESI-Q-TOF MS法分析鲜地黄、生地黄、熟地黄的化学成分 [J]. 中成药, 2016, 38(5): 1104-1108.
[5] 崔微, 郑琇梅, 李虹霞, 等. 鲜地黄的化学成分研究 [J]. 中药材, 2022, 45(10): 2369-2375.
[6] 刘卫欣. 鲜地黄有效部位提取分离、含量测定方法及降糖活性研究 [D]. 北京: 中国人民解放军军事医学科学院, 2009.
[7] 贾秀梅, 张振凌, 吴瑞环. 鲜地黄及保鲜加工品对血热出血模型大鼠凉血止血药效比较 [J]. 中国实验方剂学杂志, 2014, 20(6): 127-132.
[8] 梁爱华, 薛宝云, 王金华, 等. 鲜地黄与干地黄止血和免疫作用比较研究 [J]. 中国中药杂志, 1999, 24(11): 663-666.
[9] 张芳芳. 地黄不同炮制品对阴虚动物的影响研究 [D]. 济南: 山东大学, 2018.
[10] 陈士林, 刘安, 李琦, 等. 中药饮片标准汤剂研究策略 [J]. 中国中药杂志, 2016, 41(8): 1367-1375.
[11] 刘彦飞, 赵宇, 武卫红, 等. 地黄的化学成分及其在加工炮制过程中的变化 [J]. 国外医药: 植物药分册, 2007(3): 102-108.
[12] 李更生, 刘明, 王慧森, 等. 地黄药材炮制过程中环烯醚萜苷类成分动态变化的研究 [J]. 中国中医药科技, 2008, 15(6): 440-442.
[13] 于文娜, 张振凌, 张颖, 等. 地黄炮制过程中异毛蕊花糖苷含量的动态变化 [J]. 中国实验方剂学杂志, 2017, 23(18): 22-26.
[14] 张超, 华悦, 廉婧, 等. 肉苁蓉炮制过程中苯乙醇苷类成分含量变化规律研究 [J]. 中国中医药信息杂志, 2022, 29(04): 92-97.
[15] 张月月, 王君明, 巫晓慧. 基于以梓醇为主要成分的地黄环烯醚萜苷生物活性研究 [J]. 中华中医药学刊, 2022, 40(12): 75-77.
[16] Lindor K D, Gershwin M E, Poupon R,. Primary biliary cirrhosis [J]., 2009, 50(1): 291-308.
[17] European Association for the Study of the Liver. EASL clinical practice guidelines: Management of cholestatic liver diseases [J]., 2009, 51(2): 237-267.
[18] 张莉, 卢仁睿, 王慧慧, 等. 地黄苷D对皮质酮诱导的PC-12细胞损伤的保护作用及机制研究 [J]. 中草药, 2022, 53(11): 3385-3393.
[19] 王慧慧, 卢仁睿, 张莉, 等. 地黄中地黄苷D通过调控小胶质细胞M1/M2极化抑制神经炎症 [J]. 中药材, 2021, 44(11): 2683-2687.
[20] 沈华旦, 方江济, 郭鹏程, 等. 基于HPLC-UV-DPPH法的地黄和熟地黄药材抗氧化活性成分比较研究 [J]. 中草药, 2018, 49(3): 582-588.
Study on quality standard of freshformula granules based on standard decoction
ZHANG Zhi-peng1, XU Jie1, LIU Pei-yi1, HUANG Meng-ting1, ZHONG Zhi-kui1, CHENG Xue-ren2
1. Guangdong Provincial Key Laboratory of Traditional Chinese Medicine Formula Granule, Guangdong Yifang Pharmaceutical Co., Ltd., Foshan 528244, China 2. China Traditional Chinese Medicine Holdings Co., Ltd., Foshan 528300, China
The quality standard of freshformula granules based on standard decoction was established to provide reference for the quality control of freshformula granules.According to, 25 batches of freshstandard decoction were prepared, the extraction rate and the contents of catalpol and rehmannioside D were determined in each batch of standard decoction, and the UPLC characteristic chromatogram that can fully characterize the iridoid glycosides and phenylethanolic glycosides of freshwas constructed; Three batches of freshformula granules were prepared based on the consistency with the extraction rate, index component content and characteristic chromatogram of the standard decoction to verify the rationality of the standard formulation.The measured range of the extraction rate of freshstandard decoction was 13.93%—20.09%; The measured contents of catalpol and rehmannioside D were 36.14—73.37 mg/g and 2.96—5.33 mg/g; Ten common peaks were identified in the characteristic chromatogram of iridoid glycosides. The identified peaks 3, 4 and 6 were catalpol, rehmannioside D and leonuride; Eight common peaks were calibrated in the characteristic chromatogram of phenylethanolic glycosides, and peaks 1, 4, 5 and 6 were identified as purpureaside C, verbascoside, jionosideB1 and isoacteoside; The extract rate, index component content and characteristic chromatogram of the three batches of freshformula granules were close to the standard decoction prepared from the same batch of medicinal materials, and were within the scope of the quality standard.The quality standard of freshformula granules based on standard decoction established in this study is scientific, reasonable, stable and feasible, and can provide a reference for the quality control of freshformula granules.
fresh; standard decoction; formulation granules; quality standard; catalpol, rehmannioside D; leonuride; purpureaside C; verbascoside; jionosideB1; isoacteoside
R283.6
A
0253 - 2670(2023)04 - 1127 - 11
10.7501/j.issn.0253-2670.2023.04.012
2022-09-26
广东省科技计划项目(2018B030323004);广东特支计划科技创业领军人才项目(2017TY04R197)
张志鹏,硕士,主要从事中药配方颗粒质量标准研究。E-mail: zhangzp0909@163.com
程学仁,硕士,主任中药师,主要从事中药饮片与配方颗粒质量标准研究。Tel: (0757)85128604 E-mail: chengxr@126.com
[责任编辑 郑礼胜]

