多层螺旋CT结合MRI对胃肠道间质瘤病理危险度分级的诊断价值
王德娟
山东省临清市人民医院CT室 (山东 聊城 252600)
胃肠道间质瘤 (gastrointestinal stromal tumor,GIST) 起源于具有多向分化性潜能的原始间质干细胞,是消化系统最常见的间叶来源肿瘤[1],约占全部胃肠道恶性肿瘤的 1%~3%[2]。 由于其具有潜在的恶性生物学行为,故在对胃肠道间质瘤进行治疗之前,了解其可能的恶性程度,并做出准确而清晰的判断,对选择GIST治疗方案并判断预后、降低复发转移的风险等有着异常显著的意义。多层螺CT(multislice spiral CT,MSCT) 和高场MRI能够清晰显示病灶的形态、大小、密度和信号、部位等特征,是GISTs诊断的重要手段。本研究旨在探讨MRI征象与其病理危险度的分级与GIST多种CT之间的相关关系。
1 资料与方法
1.1 临床资料
对2010年1月至2021年1月经过手术病理而证实的胃肠道间质瘤病例27例进行回顾,其中男性15例,女性12例,年龄12~75岁,平均年龄45岁,主要以腹部不适、腹痛就诊。27例患者术前均行CT平扫和增强扫描及MRI平扫和动态增强扫描。所有病例均在术后1~6个月进行了随访。
1.2 检查方法
1.2.1 CT检查 对全部患者采用GE 64排螺旋CT机进行全腹部平扫及增强扫描,其扫描范围自膈肌顶至耻骨联合,管电压120kV,电流300mAs,层厚0.625mm。在进行增强扫描时,在静脉处注碘海醇90mL~100mL,注射速率约为3.5mL/s,注射时使用高压注射器,在注射后30秒、60秒、180秒分别进行动脉期、门静脉期及延迟期扫描。将原始数据传送至pacs工作站进行分析。所有患者检查前12小时禁食,扫描前2小时、0.5小时、15分钟分别口服500mL温水充盈小肠,开始扫描前温水(1000mL)灌肠充盈结肠及直肠。
1.2.2 MRI检查 24例患者行病变部位MRI平扫和动态增强扫描,所有患者检查均在GE Signa HDxt1.5T磁共振扫描仪上进行扫描,扫描序列含有:(1)单次激发平面回波成像(SE-EPI)序列DWI;(2)快速扰相梯度回波(FSPGR)序列T1WI同反相位;(3)脂肪抑制快速自旋回波(FS-FSE)序列T2WI; (4)多期动态增强扫描序列,扫描时先对蒙片进行扫描,注射对比剂后2分别于0 s、50s、90s行动脉期、静脉期、平衡期的轴位动态增强扫描以及冠状位、矢状位平衡期增强扫描和300s轴位进行延迟扫描。所有患者检查前6h禁水禁食,检查前20分钟注射山莨菪碱20mL。以上我们设置(2)中DWI的扩散敏感因子为800s/mm2和0s/mm2,在(4)中采用高压注射器,通过手背静脉注入对比剂钆喷酸葡胺(Gd-DT-PA)或钆特酸葡胺,剂量为0.2mmol/kg,速率为2.5mL/s。
1.3 影像学分析
1.3.1 CT图像分析 由2名高年资主治及以上CT诊断医师独立阅片,先判断图像质量是否符合诊断要求,并分别记录所有病例肿瘤的MSCT征象,包括发病部位、直径(以长径及短径的平均值为肿瘤的直径)、形状(类圆形、团块状、不规则形)、边界及与周围结构的关系(清楚、模糊、侵及周围结构)、生长方式(粘膜下、浆膜下、跨壁型、胃肠道外)、肿瘤与胃肠道壁关系(窄基底、宽基底)、肿瘤密度(均匀实性、不均匀实性、囊实性)、有无溃疡、强化程度(轻度、中度)、强化方式(渐进性、非渐进性),将所有病例的影像学征象与病理危险程度分级进行对照。
1.3.2 MRI图像分析 24例患者所有图像均传送至工作站GE ADW 4.6,使用软件Functool,对其进行数据的测量及图像的处理。由2名高年资主治以上MRI诊断医师独立阅片,首先判断图像质量是否符合诊断要求,然后分别对病变部位、大小、形态、边界、信号均匀性、表观扩散系数(ADC)等做出分析。对我们所感兴趣区域(ROI)的选择应尽量避开出血区、囊变区和坏死区, 对ADC值进行3次测量并取平均,并对低、中、高危病灶的ADC 值做对比分析。
1.4 统计学分析
利用 SPSS 20.0 统计软件对肿瘤的MSCT征象与肿瘤病理危险分级进行单因素χ2分析,以P<0.05 为差异有统计学意义。
2 结 果
2.1 手术及病理结果
40例GIST 发生于胃部18 例,小肠9 例(其中1例小肠可见3处),结肠5例,网膜及肠系膜5例,直肠2例,食1例。所有病例按照病理危险程度分级分为极低度危险5例,低度危险16例,中度危险12例,高度危险7例,术后复发3例,术后腹腔种植转移3例,肝脏转移2例。
2.2 CT影像学表现与肿瘤病理危险度分级的关系
所有病例CT征象统计见表1。肿瘤发病的部位、形态、大小、其边界及与周围结构的关系(模糊、清楚、侵及周围结构)、肿瘤密度、有无溃疡与病理危险程度分级有统计学差异。肿瘤生长方式、强化、强化程度与肿瘤的危险分级无统计学意义。
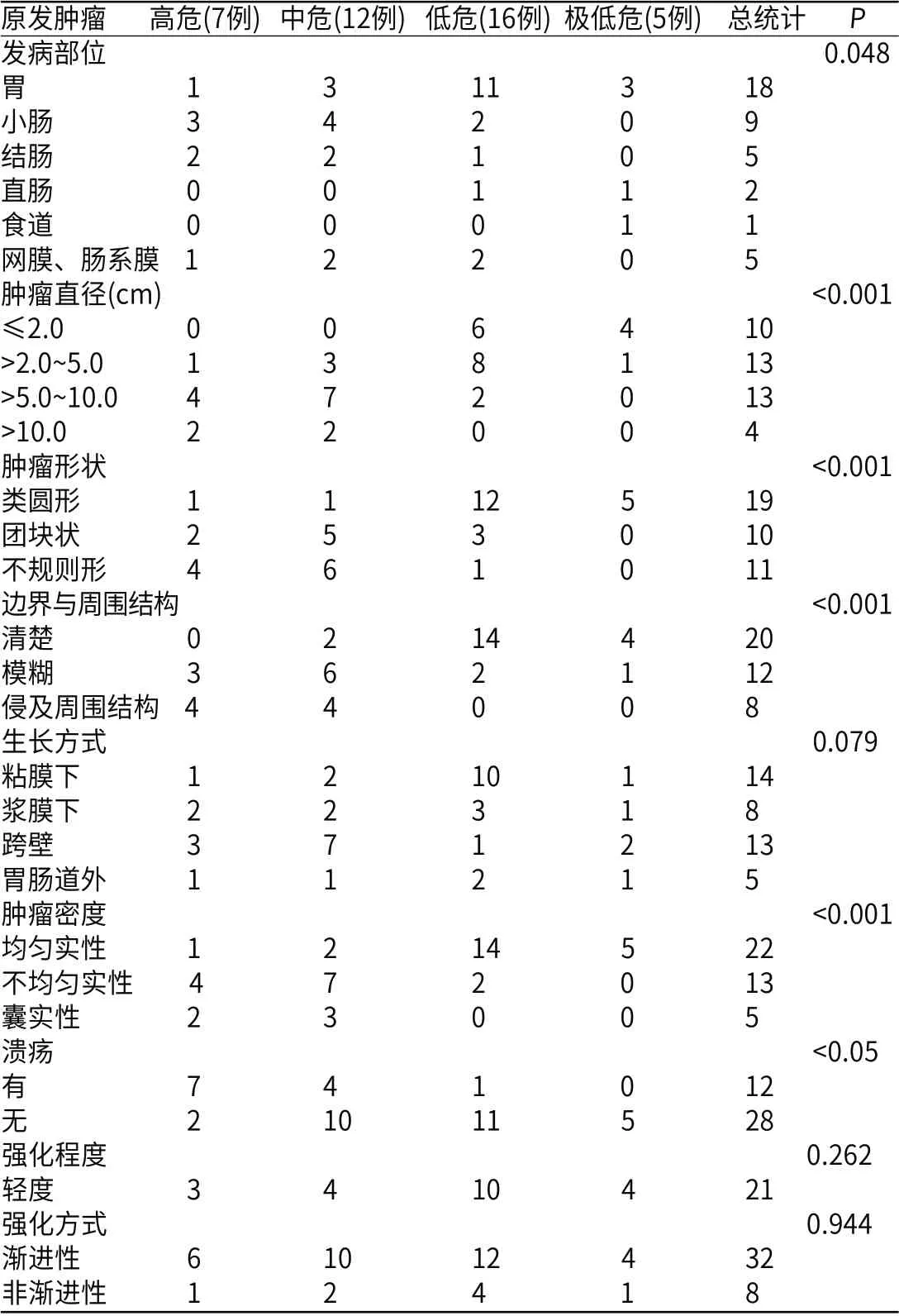
表1 GIST的CT征象与病理分级的关系
2.3 MRI影像学表现与肿瘤病理危险度分级的关系
24 例GIST发生于胃部17 例,小肠2 例,结肠3例,直肠2例;其中形态不规则14例,规则10 例;直径>5cm 者13例,直径<5cm 者11例;边界模糊9例,边界清晰15例;信号均匀8例,信号不均匀16例;所有病例均弥散受限,DWI呈高、稍高信号,ADC值高、低不等;统计结果显示肿瘤大小、部位、形态、边界、信号均匀性及ADC值与病理危险程度分级有统计学意义(P<0.05,见表2)。
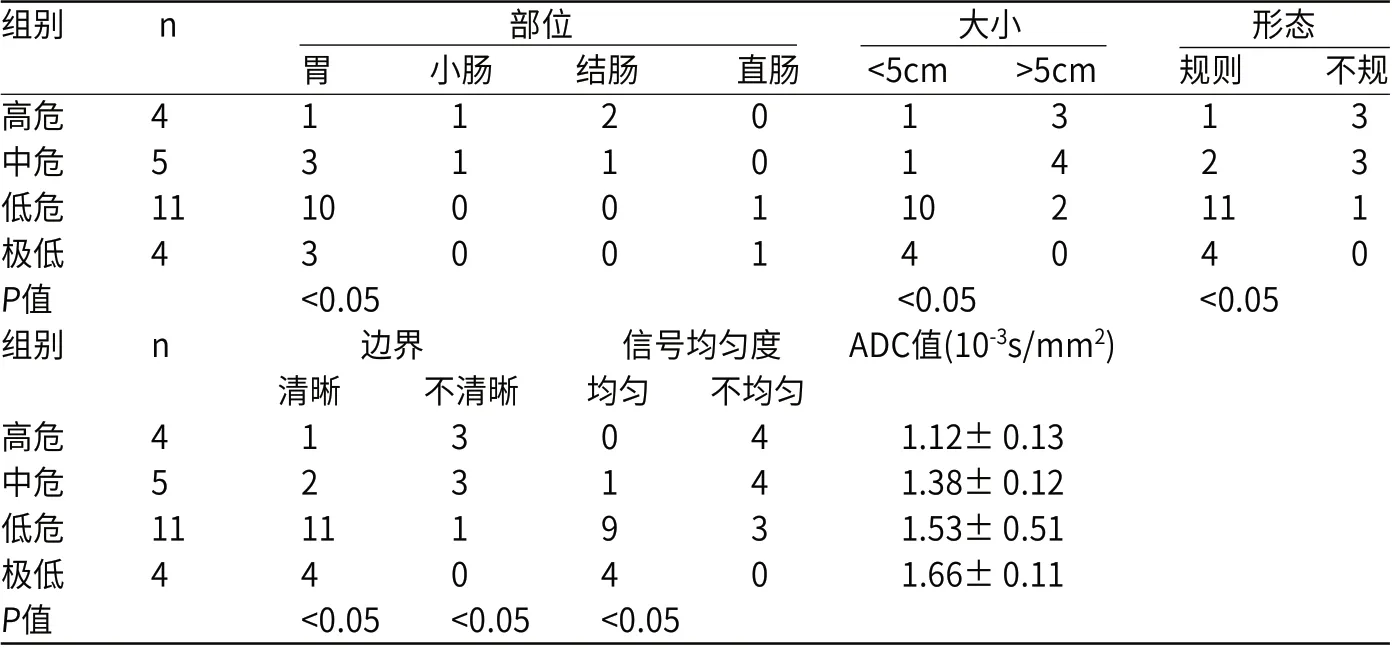
表2 MRI 表现、ADC 值与病理危险度分级相关性
3 讨 论
现已知 GIST 是是消化道中常见的间叶组织肿瘤,是胃肠道Cajal 间质细胞来源的非上皮肿瘤[3]。其临床表现无特异性,大部分症状以腹胀、腹痛为主,其次为消化道出血。根据间质瘤的大小、发病部位及肿瘤是否破裂等可以将其分为极低、低、中及高危险度四级,不同的危险度对应不同的临床治疗方案。GIST由于其血供丰富, 常出现坏死、出血等继发性改变[3],如若进行穿刺活检,有可能性造成肿瘤的破溃、出血,同时也会增加肿瘤播散的危险性,因而对于经过术前评估,确认可以较为完整切除肿瘤的患者,可以直接行手术切除,并不推荐采用术前穿刺活检的方案[4]。从上述可知,术前对肿瘤的危险程度的评估极其重要。
目前临床上对于检查GIST 常见影像学方法主要是CT检查,CT扫描时间快,操作简单,可以大范围成像,可以清晰的显示病变的部位、形态、大小、密度及其和附近组织关系,在GIST 诊断中得到广泛的应用,给临床诊断、判断不同危险度等级以及选择治疗方案等可以提供极为有力的影像学资料。MRI可以多平面、多参数成像,具有较短的成像时间,很高的软组织分辨率,如若使用DWI等功能成像法,便可以很好表现肿瘤的内在特征,在肿瘤的检出及诊断方面具有较高优势。
影像学表现 GIST 多表现为圆形或类圆形、分叶状或不规则形的软组织肿块,边界多较清晰,随着恶性程度的增加,肿瘤的危险程度等级越高,越容易表现为侵袭性生长,其形态越发不规则,更容易向周围浸润使得其轮廓较为模糊,肿瘤密度低于或与肌肉呈等密度,随着肿瘤体积增大,导致肿瘤血供不足,导致肿瘤密度不均匀。本组病例显示肿瘤可为轻度或中度均匀或不均匀强化,与石磊等[5]报道一致。
本研究亦通过对MSCT及MRI影像的分析表明肿瘤大小、部位、形态、边界、密度、生长方式、强化方式、MRI信号均匀性及ADC值与病理危险程度分级进行统计。对于肿瘤的大小、部位、形态、边界、生长方式的显示和分析,CT和MRI具有高度的一致性,说明二者在以上方面对间质瘤的诊断和病理危险程度分级方面价值相当。MRI多序列及多参数成像的特点,且软组织具有较高的分辨率,对病变的均匀性显示更加清晰,对于出血的显示,MRI比CT具有更高的敏感性,另外MRI能较好的显示壁间较小肿瘤,因此,对于较小壁间肿瘤的显示,MRI具有更大的优势。
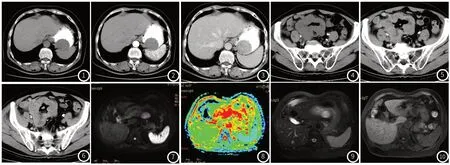
图1~图3 为同一病例,胃间质瘤,肿瘤直径约5cm,位于胃腔内粘膜下,内生性生长,圆形,边界清晰光滑,密度均匀,增强扫描呈渐近性均匀强化。病理核分裂像2/50,低度危险。图4~图6 为同一病例,病理小肠中度危险间质瘤。肿瘤直径约9cm,肿瘤外生性,形态不规整,可见分叶,其内密度不均匀,见穿通性溃疡及气体,与小肠腔相通,增强扫描中度不均匀强化。术中见肿瘤与小肠、系膜、卵巢广泛粘连。图7~图10 为同一病例,肿瘤直径约2mm,位于胃小弯侧浆膜下,外生性生长,病理为极低风险,呈长T1长T2信号,DWI(b=800)呈高信号,ADCmin=1.89×10-3mm2/s。
同时,对于不同危险程度等级的GIST 肿瘤,其生长方式及实性部分强化程度差异的P值均大于0.05,故而二者无统计学意义。本研究所纳入的 27例患者CT和MRI表现发生于小肠及结肠间质瘤的危险度明显高于发生于胃的间质瘤(P<0.05),食道及直肠各1例,无统计学意义。本研究显示肿瘤直径>5cm时危险度明显增高,肿瘤恶性程度会随时间的推移及肿瘤体积的增大而增加。
本研究显示极低-低危组病变 GIST 多为类圆形,边界清晰,CT为等或低密度,MRI表现为T1WI等信号,T2WI等或稍高信号,内部密度(信号)均匀;中-高危病变多为不规则形,边界模糊,密度及信号不均匀,与国内学者报道一致[6],肿瘤形态不规则、边缘模糊、周围浸润、密度和信号不均匀、有溃疡的危险程度明显高于呈近似圆形、具有光滑的边缘、密度均匀的肿瘤的危险程度,由于P<0.05,故而在对其生物学危险程度差异的评价中具有较高的统计学意义。研究表明GIST 随着恶性程度的增加越容易向周围浸润从而导致其轮廓模糊,肿瘤形态越发不规则。随着肿瘤的体积逐渐增大、肿瘤的生长速度远超新生血管的生长速度,此种情况将会使得肿瘤无法供血充足,致使部分肿瘤细胞死亡形成溃疡或者坏死,其最终结果使肿瘤表现为密度和信号的不均匀。当囊变坏死与胃肠道相通时肿瘤内可以观察到气- 液平面影(Torri-celli-Bernoulli 征)时,有较高可能性为高危险度的间质瘤[7]。研究还表明,具有术后复发3例,术后腹腔种植转移3例,肝脏转移2例,小肠多发1例,全部隶属于高度危险组,其差异具有高度的统计学意义(P<0.05)。可见,此种情况出现复发、转移提示GIST恶性的风险等级较高。
通过对比MRI和CT对病变均匀度的显示,发现在高危组和中危组中,MRI大部显示病变信号不均匀,高于CT显示病变不均匀例数,差异具有统计学意义(P<0.05);低危组和极低危组中,大部信号均匀,显示不均匀例数略高于和CT,差异没有统计学意义。MRI具有良好的组织分辨率,对病变的均匀性显示更加清晰,GIST MRI表现为软组织信号,一般呈等、长T1WI稍长T2WI信号,FS-T2WI呈高信号。对于出血的显示,MRI比CT具有更高的敏感性,因此,对于病变均匀度的显示,MRI具有更大的优势。通过以上分析和对比,我们认为,在对高危和中危病变均匀度的显示和判断上,MRI有一定的优势;但是低危组和极低危组病变的均匀的判断上,二者价值相当。
DWI近年来在间质瘤肿的诊断、预后中得到越来越多的应用。有结果显明,ADC值可用于术前评估间质瘤侵袭性[8]。有文章中使用DWI方法,对十二指肠间质瘤做出一些相应分析,他们发现,间质瘤全部具有高信号的表现[9],低ADC值伴随着高的恶行度。恶性肿瘤具有细胞数目多,复制快,密度大等的特征,此类特征与细胞生物膜的阻碍及其他可能原因的影响,会对分子扩散进行限制,随着DWI 信号的增高,ADC 值呈现下降趋势[8]。文中ADC的值如表3,如若选取任意两组进行对比,可发现P<0.05,具有统计学价值。肿瘤的危险等级越高,ADC 值越高,这提示我们ADC 值同样可以作为手术前肿瘤的危险程度评定的标识。

表3 低危组、中危组、高危组的ADC值比较
在MRI检查的病例中,有3例存在运动伪影,其中1例伪影较重,对病变的显示造成了一定的影响,因此患者的配合程度和检查前准备会在一定程度上影响MRI检查的图像质量。而CT检查速度快,可以大范围扫描,能对以上问题进行避免。
综上所述,CT 和MRI是 GIST 的诊断、治疗及预后判断的重要检查方法,可以对胃肠道间质瘤的危险度分级进行初步判断。对于肿瘤的大小、部位、形态、边界、生长方式的显示和分析,CT和MRI具有高度的一致性。但是对于病变均匀度的显示,MRI相对于CT具有一定的优势,尤其是结合功能成像,病变的ADC值对胃肠道间质瘤的危险度分级具有一定价值,相对于CT检查,MRI对胃肠道间质瘤的诊断和危险度分级价值更高。但是,MRI图像的显示有时会受到患者的影响,因此,充分利用CT的速度快、高空间分辨率、大范围扫描结合MRI的多方位、多序列成像、高组织分辨率和功能成像可以更好的对胃肠道间质瘤的危险度分级进行判断,对于术前判断肿瘤的危险度分级有重要的参考价值,有利于临床手术和治疗方案的制定。

