白藜芦醇的生物活性及其运载体系研究进展
田艳杰,石爱民,刘红芝,*,代 蕾,刘 哲,王 强,*
(1.中国农业科学院农产品加工研究所,农业农村部农产品加工综合性重点实验室,北京 100193;2.青岛农业大学食品科学与工程学院,山东 青岛 266109)
白藜芦醇(C14H12O3)又称芪三酚,是一种天然的有益于健康的非黄酮类多酚化合物,早期从毛叶藜芦的根部分离提取分离[1],随后研究人员在葡萄、花生、蓝莓等100多种植物中均检出了白藜芦醇[2-4]。白藜芦醇有顺式和反式两种异构体,自然界中主要以反式构型为主,在紫外线的照射下,反式白藜芦醇异构化生成顺式白藜芦醇[5]。白藜芦醇的异构化现象和水溶性差限制了其开发与利用,目前,食品、药物领域已经开展了许多将白藜芦醇包埋于递送系统的研究,这些运载体系包括纳米颗粒、乳液(纳米乳液、多重乳液、Pickering乳液)、脂质体、水凝胶、环糊精(cyclodextrin,CD)包合物等[6]。本文综述近年来有关白藜芦醇的生物活性及运载体系,并总结现有运载体系存在的问题,以期为白藜芦醇运载体系相关研究提供参考。
1 白藜芦醇理化性质
白藜芦醇化学名称为3,5,4’-三羟基苯二烯,熔点256~258 ℃,为无味、白色的针状结晶,易溶于有机溶剂,难溶于水,化学性质不稳定性,需在低温避光的条件下保存,可与三氯化铁-铁氰化钾、氨水发生显色反应。白藜芦醇的存在形式主要有4 种:顺、反式白藜芦醇和顺、反式白藜芦醇苷,其中反式白藜芦醇具有芳香环、酚羟基及双键等官能团[7],且具有相对较高的稳定性。近年来白藜芦醇的多种生物活性被广泛研究,因此在食品、药品及化妆品行业的需求不断增加,但其在植物中的含量相对较少,因此,相关研究着重于提高植物中白藜芦醇含量或人工合成白藜芦醇。研究表明可通过物理方法,如超声处理[8]、紫外线处理[9]等增加植物中白藜芦醇的含量,此外,一些化学合成法及生物合成法也被用来合成白藜芦醇。目前的化学合成法有Perkin缩合反应法、Witting合成法、Heck合成法、Witting-Horner合成法[10],生物合成法主要集中在细胞、酶、基因方面,可以通过植物细胞培养技术法[11]、芪合酶转基因技术法[12]、微生物工程技术法[13]合成。
2 白藜芦醇生物活性
白藜芦醇作为一种植物抗毒素,在植物中发挥保护作用,具有抵御紫外线辐射、预防真菌感染的作用[14]。由于这些作用的存在,白藜芦醇在促进人体营养健康中也发挥了优异的功能活性,主要包括抗氧化、抗菌、抗炎、抗心血管、抗肿瘤等作用。
2.1 抗氧化作用
正常细胞代谢会通过谷胱甘肽、超氧化物歧化酶和过氧化氢酶等通过解毒产生过氧化氢、羟自由基等氧化中间体。正常生理条件下代谢是处在一种动态平衡中,但是若发生氧化中间体的异常积累,会导致体内氧化与抗氧化失衡,加速生物体的老化。活性氧(reactive oxygen species,ROS)在细胞信号传导控制体内氧化/抗氧化中具有重要意义。白藜芦醇具有抗氧化性,可清除自由基,抑制ROS的生成。Santos等[15]研究白藜芦醇在不同年龄供体人单核细胞氧化应激环境中的抗氧化作用,结果表明,白藜芦醇通过调节信号通路能够降低中年组和老年组的ROS水平,对比发现在中年组的抗氧化效果更好。此外,将白藜芦醇添加至饲料中,可以增强肉鸡肌肉的抗氧化能力同时刺激线粒体生物发生,从而改善鸡肉的品质[16];可以增加谷胱甘肽过氧化酶活性并上调肌球蛋白重链基因表达,减少蛋白质羰基和丙二醛含量,提高抗氧化能力与氧化纤维成分,从而提高猪肉品质[17]。因此,白藜芦醇可通过信号调节途径或者增加机体谷胱甘肽过氧化物酶等活力,抑制ROS的产生,提高抗氧化能力。
2.2 抗炎作用
白藜芦醇抗菌抗炎作用可在受真菌感染的葡萄植株中发现[14]。炎症是机体在损伤刺激下产生的一种生理应激反应,如果不能有效控制,就会引起慢性疾病或对机体造成更大的损伤。研究表明,白藜芦醇可抑制促炎细胞因子的表达,减少炎症的发生,同时促进抗炎细胞因子的表达[18]。Ma Chunfang等[19]探究了白藜芦醇对脂多糖诱导的炎症反应及其在RAW264.7鼠巨噬细胞中的潜在分子作用机制,结果表明白藜芦醇可下调诱导型一氧化氮合酶和白细胞介素(interleukin,IL)-6的表达,从而抑制脂多糖刺激RAW264.7细胞中一氧化氮的产生和IL-6的分泌。
2.3 抗菌作用
相比于白藜芦醇的抗氧化及抗炎作用,白藜芦醇的抗菌作用研究较少,但也是近年来的研究热点。白藜芦醇能够抑制细菌和真菌生长,改变毒性因子的表达,减少生物膜的形成,降低其运动性并影响细菌对各种常规抗生素的敏感性[20]。痤疮是常见的皮肤病,由皮质堵塞、金黄色葡萄球菌感染等多种因素引起,研究发现白藜芦醇比抗菌药物过氧化苯甲酰具有更好的抗痤疮作用[21]。同时,白藜芦醇可用于治疗皮肤癣菌病[22]。李峰等[23]发现质量浓度15 μg/mL白藜芦醇溶液能够显著抑制核桃细菌性黑斑病菌生物膜的形成。白藜芦醇抗菌作用主要通过干扰细菌细胞壁的合成,干扰细菌的信号传导,从而影响其正常生长[24]。
2.4 抗心血管疾病作用
据统计,每年有1700多万人口死于心血管疾病,占全球人类的死因首位,死亡率约占总死亡人口的30%[25],其中动脉粥样硬化是造成心血管疾病的主要原因[26]。研究表明,白藜芦醇可预防高水平的总胆固醇、甘油三酯、低密度脂蛋白胆固醇和高密度脂蛋白胆固醇,并减少高脂肪饮食和脂多糖诱导的动脉粥样硬化病变,说明其具有降脂和抗动脉粥样硬化的潜力[27]。白藜芦醇可改善全心肌缺血和再灌注后的心脏功能,并减少单次和齐射心律失常、室性心动过速、心室颤动等情况[28]。另外,白藜芦醇还能提高一氧化氮的生物利用度,促进与血管舒张相关的信号调节与转导,影响离体人肺内小动脉血管的张力[29]。以上研究表明,白藜芦醇可以舒张血管并改善动脉粥样硬化,具有广泛的心血管保护作用,是一种很有潜力的生物活性成分。
2.5 抗肿瘤作用
在白藜芦醇的多种生物活性中,以其抗肿瘤作用展开的研究相对较多。癌细胞的扩散和转移是恶性肿瘤的重要标志,癌细胞会通过血液系统和淋巴系统扩散到全身,从而形成新的肿瘤。研究表明,白藜芦醇可通过多种机制和靶点抑制肺癌、肝癌、胰腺癌、结肠癌等肿瘤细胞增殖,促进癌细胞凋亡。在抑制肿瘤细胞增殖方面,白藜芦醇可以调控癌细胞的生长周期,通过阻滞癌细胞增殖的S期抑制癌细胞DNA合成[30]。在体外和完整细胞中可抑制血清/糖皮质激素调节激酶-1,抑制人肝癌细胞的增殖和存活[31]。近年来,越来越多的研究表明,白藜芦醇可以通过调节各种癌症中的上皮-间充质转变来调节肿瘤细胞迁移和侵袭,例如结肠癌[32]、胰腺癌[33]、肺癌[34]等。另外,在促进肿瘤细胞凋亡方面,白藜芦醇可通过激活胱天蛋白酶3、胱天蛋白酶9、磷脂酰肌醇3激酶等多条通路来促进肿瘤细胞凋亡[35]。还有研究证明,白藜芦醇可通过下调Notch1/人第10号染色体缺失的磷酸酶及张力蛋白同源的基因、蛋白激酶B等信号传导诱导人卵巢癌细胞凋亡[36],可以使基础细胞外信号调节激酶失活,诱导宫颈癌细胞凋亡[37]。以上研究表明,白藜芦醇的抗肿瘤作用主要是通过调节内/外途径、调控相关分子靶点抑制肿瘤侵袭转移和阻滞细胞周期诱导癌细胞凋亡。
3 白藜芦醇的食品运载体系
白藜芦醇具有多种生物活性,可作为功能成分应用于食品及保健品中,但在相关产品制备过程中通常需要进行加工(温度、压力)与贮存(光照)。由于白藜芦醇水溶性差、稳定差以及见光易发生异构化,其生物利用度较低,且食品加工工艺可能进一步降低其生物利用度,从而限制了白藜芦醇的应用。通过纳米颗粒、乳液、脂质体、水凝胶、CD等运载体系(图1)将白藜芦醇进行包埋可以显著改善其稳定性及水溶性,从而提高白藜芦醇的缓释功效并增加其生物利用度。不同白藜芦醇运载体系的特性如表1所示。
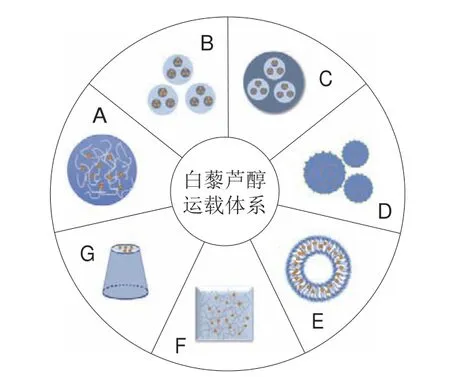
图1 白藜芦醇运载体系Fig.1 Delivery systems for resveratrol

表1 不同白藜芦醇运载体系的特性Table 1 Characteristics of different resveratrol delivery systems
3.1 纳米颗粒
纳米颗粒通过氢键和疏水相互作用包埋白藜芦醇,增加其溶解度,减少其在胃肠道中的破坏,从而达到缓释的目的。纳米颗粒载体主要有蛋白质纳米颗粒、多糖纳米颗粒和蛋白质-多糖复合颗粒等[38-39]。此外,根据不同的造粒工艺,颗粒分为挤出颗粒和干燥颗粒。纳米颗粒具有体积小、稳定性高、负载率高等特点,可减少活性成分在食品加工和贮藏中的损失[40]。
Huang Xulin等[41]通过抗溶剂沉淀和静电沉积制备成负载白藜芦醇的纳米颗粒,该颗粒以玉米醇溶蛋白纳米颗粒为核,果胶涂层形成壳,制备成玉米醇溶蛋白/果胶核壳纳米颗粒,研究表明此纳米颗粒在pH 2~7时较稳定;在pH 4时,分别将纳米颗粒进行热处理(80 ℃、1 h)以及盐处理(NaCl浓度低于50 mmol/L)均可保持稳定,且纳米颗粒负载的白藜芦醇生物可及性、体外及细胞抗氧化活性均高于游离白藜芦醇。Liu Yuxuan等[42]研究了超声处理制备的玉米醇溶蛋白-阿拉伯胶复合颗粒对白藜芦醇包封的影响。与玉米醇溶蛋白包封白藜芦醇相比,玉米醇溶蛋白-阿拉伯胶纳米颗粒的包封率从26.19%显著提高至55.85%,在超声处理后复合颗粒的包封率进一步提高至74.20%,其载药量从2.79%上升至6.01%。Zhang Lingtuo等[43]以海藻酸钠为壳,大豆分离蛋白为核制备包封白藜芦醇的纳米颗粒,其包封率约为91.9%,且具有更好的pH值稳定性及离子稳定性。在紫外光照射30 min后,带壳纳米颗粒中反式白藜芦醇的异构化率仅为15%,比无壳纳米颗粒低约30%。纳米颗粒运载体系主要以天然大分子聚合物(蛋白、多糖)为载体对活性成分进行包埋(表2),载体本身具有良好的生物相容性,同时还可以提高活性成分的稳定性且包封率较高,因此具有广泛的应用前景。

表2 白藜芦醇纳米颗粒的特性Table 2 Characteristics of resveratrol nanoparticles
3.2 乳液
传统乳液是将油相和水相混合,添加乳化剂经高压均质、超声乳化、高压微射流等形成的分散系,根据油-水两相的相对分散性,可将其分为水包油(oil-in-water,O/W)型乳状液和油包水(water-in-oil,W/O)乳状液。乳液体系是热力学不稳定体系,在贮藏和加工过程中容易受到温度、pH值、离子强度等因素影响,会出现分层、破乳等现象[49]。针对这些问题,研究人员以纳米乳液、多重乳液、Pickering乳液等多种不同结构和性质的乳液体系包埋白藜芦醇,以提高其生物利用度。
3.2.1 纳米乳液
纳米乳液作为新型的载体体系,被认为是使用最广泛的运载体系之一,越来越多地应用于医学领域及功能性食品开发领域。该体系主要是通过水相、油相、乳化剂按适当比例在一定的外力作用混合形成热力学不稳定均相胶体分散体系。纳米乳液的粒径在50~200 nm之间,粒径的大小与乳化剂的类型、油相中油的类型和浓度以及所采用的均质方法有关。
Xiong Yun等[50]将制备了牛至精油与白藜芦醇的纳米乳液,并将纳米乳液加入到果胶基质中,涂在新鲜的猪里脊肉上,研究其对鲜猪里脊肉的保鲜影响。研究表明,该涂层具有最好的保鲜性能,可最大限度地减少里脊肉的pH值及颜色变化,延缓脂质和蛋白质氧化,延长里脊肉的保质期。研究人员使用自发乳化法制备负载白藜芦醇的低能纳米乳液,以橙油与葡萄籽油为油相封装白藜芦醇,将纳米乳液在紫外光下暴露1 h,白藜芦醇的保留率为88%,可有效防止白藜芦醇降解[51]。Zhu Peipei等[52]使用玉米醇溶蛋白-聚甘油稳定的O/W纳米乳液来包封白藜芦醇,其包封率超过90%,研究表明该体系显著提高了白藜芦醇的抗氧化活性,并且可以在34 d内保持良好的物理化学稳定性。Tsai等[53]发现负载白藜芦醇的纳米乳液在小鼠皮肤上应用24 h后,与白藜芦醇饱和溶液处理组相比,其透皮量增加约896.2 倍,皮肤内的沉积量增加约10.2 倍[53]。与传统乳液相比,该乳液体系具有粒径小、贮藏稳定性高等特点。纳米乳液运载体系可以改善活性成分的稳定性和抗氧化活性,但受自身热力学不稳定性质的影响且制备过程中需要加入表面活性剂,存在一定的安全风险,因此纳米乳液的应用受到限制。
3.2.2 多重乳液
传统乳液对功能成分进行包埋时往往出现泄漏问题,导致活性成分封装效率低,因此可利用聚电解质、蛋白质等物质通过氢键、静电和疏水相互作用对乳液进行多层修饰,这种乳液被称为多重乳液[54]。多重乳液具有更复杂的乳液体系,因此被称为“乳液中的乳液”,乳液的分散相液滴中还分散着互不相容的液滴。由于多重乳液具有两个或两个以上油-水界面,可以更好地保护活性成分,降低外界环境对包埋物的影响。
Wang Jun等[55]通过高压均质法制备了白藜芦醇的水包油包水(water-in-oil-in-water,W/O/W)乳液,与内水相为去离子水相比,内水相为乙醇时白藜芦醇的包封率(99.97%)更高。Shi Aimin等[56]发现包埋白藜芦醇的W/O/W多重乳液可在pH 2~8、温度25~70 ℃条件下保持稳定,可稳定贮存77 d,而且该体系对肠蠕动和消化液的具有良好的抵抗力,对白藜芦醇有更好地保护与缓释作用。Díaz-Ruíz等[57]研究表明,与体积比40∶60的W1/O相比,采用体积比30∶70的W1/O所制备W1/O/W2乳液具有更长时间的稳定性。以体积比80∶20的W1/O∶W2和体积比为30∶70的W1/O制备W1/O/W2多重乳液具有更好的胶体稳定性及流变特性,且白藜芦醇的包封率及质量浓度都较高,更适合用作药品或食品成分。同样,Matos等[58]通过两步机械乳化工艺制备包埋白藜芦醇的浓缩W1/O/W2双乳液,最佳配方下的浓缩W1/O/W2双乳液中,白藜芦醇质量浓度为6.2 mg/L,且具有较高的包封率、稳定性及流变特性。
3.2.3 Pickering乳液
相比于以表面活性剂稳定的传统乳液,Pickering乳液中的固体颗粒充当乳化剂[59],吸附在乳液水-油界面上的固体颗粒一般发生不可逆吸附,从而赋予Pickering乳液更好的稳定性。乳液的类型与固体颗粒在油-水中的接触角(θ)有关,若θ<90°,则颗粒亲水,可形成O/W乳液,若θ>90°,则颗粒疏水,可形成W/O乳液。近年来植物蛋白凭借绿色、天然、生物相容性好等特点被应用于食品领域[60],因此以植物蛋白[61-63]制备的食品级固体颗粒稳定的Pickering乳液的报道不断增多,且逐步深入到食品领域。鉴于Pickering乳液高稳定性、高安全性的特点,可以用来保护和递送白藜芦醇,拓宽白藜芦醇在食品领域的应用范围。
Wu Bi等[64]通过辛烯基琥珀酸淀粉酸酐(octenyl succinic anhydride,OSA)改性淀粉制备新型淀粉基Pickering乳液,用于包封白藜芦醇。该体系可以对白藜芦醇起到很好的缓释作用,显著改善白藜芦醇皮肤渗透的能力,促进白藜芦醇在皮肤中的分布,且在4 ℃和25 ℃下可保持稳定60 d,具有良好的离心和稀释稳定性。Sharkawy等[65]制备壳聚糖/阿拉伯树胶纳米粒子稳定的Pickering乳液作为反式白藜芦醇局部给药的载体,发现Pickering乳液具有更高的皮肤保留率和更低的白藜芦醇渗透率,并且可以增加反式白藜芦醇光稳定性。有学者利用OSA改性藜麦淀粉颗粒稳定的Pickering乳液包埋白藜芦醇,向乳液的分散相中添加一定比例的橙油时体系更稳定,此时白藜芦醇包封率高达98%,是表面活性剂稳定体系中包封率的两倍以上[66]。Zhang Yali等[67]以玉米醇溶蛋白/壳聚糖颗粒稳定的Pickering乳液包埋白藜芦醇,实验证明该乳液体系白藜芦醇的稳定性和缓释性均优于同一研究中纳米乳液包埋的白藜芦醇。Pickering乳液是由固体颗粒稳定的乳液,具有稳定性强、安全性好、可有效抑制液滴凝聚、抵抗奥式熟化等优点,同时具有良好的生物相容性及可食用性,可以应用于食品领域中。
不同白藜芦醇乳液的制备方法及特性如表3所示。
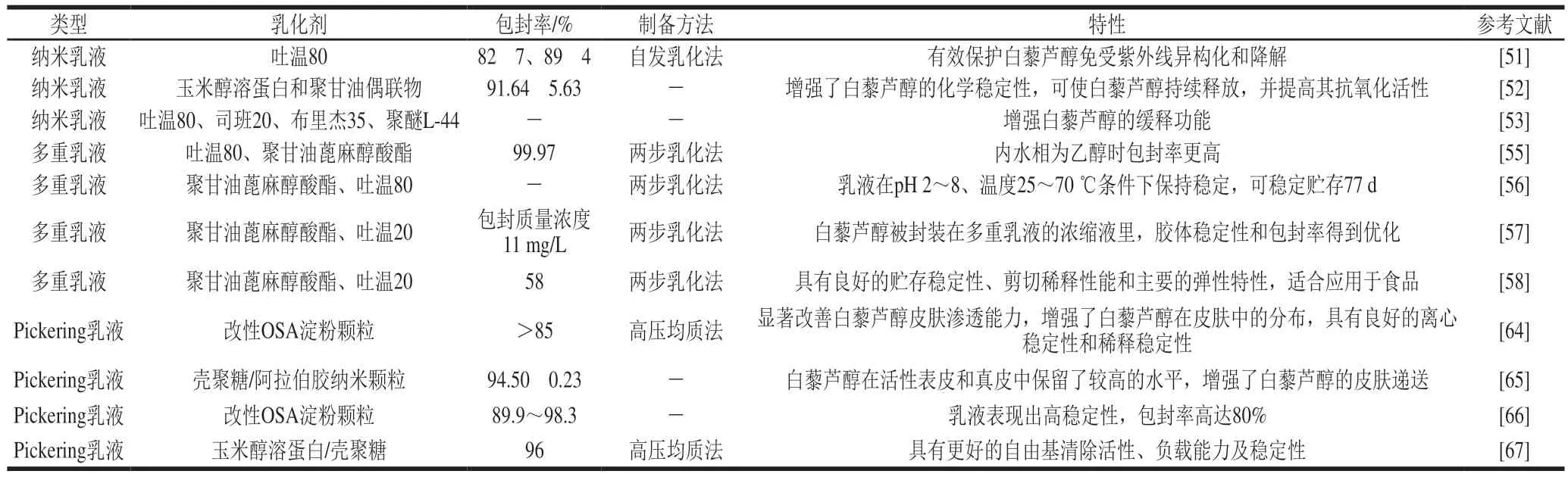
表3 白藜芦醇乳液特性Table 3 Characteristics of resveratrol emulsions
3.3 脂质体
脂质体是一种由磷脂双分子层结构组成的球形囊泡,具有疏水尾部和亲水头部,因此可以同时运载亲水性物质和亲脂性物质。脂质体可将亲水分子封装在内部水性内腔中,而亲脂性分子主要分布在脂质双层内,其粒径在几十纳米到几微米之间,具有生物相容性好的特点,可实现跨细胞转运[38]。制备方法主要有薄膜分散法、逆向蒸发法、乙醇注入法、冻融法、复乳法等。目前,脂质体已被美国食品药品监督管理局认定为安全和可生物降解的载体。许多研究表明,脂质体可以通过疏水相互作用,氢键及静电相互作用将白藜芦醇装在疏水的双分子层中,提高其溶解性及稳定性。但脂质体具有半衰期短、稳定性差等缺点,容易导致负载物的泄漏,因此研究人员常对脂质体进行修饰改性,增强体系的稳定性以及提高其适用性。
通过薄膜水合法结合超声处理制备了聚乙二醇2000修饰的白藜芦醇脂质体,修饰的脂质体包封率为85.5%左右,且贮藏6 d没有发生显著聚集现象,修饰后脂质体稳定性更高[68]。Feng Simin等[69]将白藜芦醇与表没食子儿茶素共同包封在涂有低甲氧基果胶的脂质体中,经过涂层包被的脂质体稳定性更高,巴氏杀菌后仍具有较大的抗氧化性。和其他运载体系相比,脂质体具有很好的生物相容性,可以提高活性成分的吸收与利用,同时该体系可以实现亲疏水活性成分的共同运载。
3.4 水凝胶
水凝胶是通过物理或化学交联制成的能够在水介质中膨胀的三维网络状聚合物体系,不同材料能够组合形成不同功能和性状的水凝胶。水凝胶具有高封装效率、可靠的化学稳定性以及理想的微环境,并通过响应不同的环境条件来实现靶向释放,被认为是一种有良好应用前景的递送系统[70]。交联空间网络结构赋予水凝胶优异的溶胀以及持水能力,使其成为封装生物活性成分的理想递送系统,同时可以保护活性成分免受胃肠道疾病侵害。
Wang Peng等[71]通过离子交联成功制备氧化结冷胶(oxidized gellan gum,OGG)和抗性淀粉(resistant starch,RS)组成的水凝胶,并对白藜芦醇进行包埋。通过对比发现,RS的加入明显影响了水凝胶的形态结构和溶胀能力,该凝胶具有pH值敏感性且对白藜芦醇包封率在84.95%~90.73%。体外实验结果表明,OGG/RS水凝胶珠在模拟胃液中表现出良好的稳定性,在模拟肠液中持续释放白藜芦醇。Zhao Chenchen等[72]将白藜芦醇负载到肽水凝胶上形成伤口敷料。体外细胞实验结果表明,该水凝胶没有细胞毒性,可以抑制巨噬细胞促炎细胞因子的产生,所制备敷料可以加速伤口愈合,促进胶原蛋白有序沉积,减轻炎症并最终防止疤痕形成。
3.5 环糊精包合物
CD是由葡萄糖单体(吡喃葡萄糖)通过α-1,4-糖苷键连接形成的天然环状低聚糖[73]。根据葡萄糖的数量,可分为α-CD、β-CD和γ-CD,其分别由6、7、8 个葡萄糖单体构成。CD是1 个中空的圆锥形三维结构,具有0.79 nm的锥形腔深,而顶部和底部的直径都随着葡萄糖单位的数量而增加。亲脂性的亚甲基和醚键位于CD空腔内侧,亲水性的羟基位于外侧,从而形成了“内疏水、外亲水”的结构特点[74]。目前α-CD、β-CD和γ-CD已获得美国食品药品监督管理局的安全认定,并且可以商业化生产。相比较其他几种CD,β-CD具有成本低、应用范围广的特点,因此被人们广泛研究。
Silva等[75]将游离的白藜芦醇与γ-CD-白藜芦醇加入到柠檬汁中作为功能成分,对比发现γ-CD-白藜芦醇-柠檬汁中的白藜芦醇含量约为白藜芦醇-柠檬汁的9 倍,说明γ-CD包合增加了白藜芦醇的溶解度,将两种果汁在黑暗条件下室温或4 ℃下贮藏28 d后,白藜芦醇含量差异仍然十分显著。Haley等[76]的研究表明通过CD聚合物包封白藜芦醇,可将白藜芦醇的释放时间延长至100 d,且可以使其稳定的自由基清除活性维持60 d[76]。Wang Xuechun等[77]将白藜芦醇与磺基丁基醚-β-CD络合并装载于聚合物纳米颗粒中,该包合物使白藜芦醇的水溶性提高了约66 倍。
4 结语
白藜芦醇是一种具有抗氧化、抗炎、抗菌、抗心血管疾病、抗肿瘤等多种生物活性的酚类物质,在食品中具有广阔的应用前景,但水溶性差、稳定性差等因素导致其生物利用度低,限制了其在食品中的开发与利用。为此,研究者们设计出各种白藜芦醇食品运载体系,这些运载体系可以增加白藜芦醇的溶解性、稳定性及生物利用度,但目前的研究中还存在一些不足:1)在制备纳米乳液、多重乳液运载体系时,需要加入表面活性剂,常见表面活性剂具有一定的毒副作用,如对黏膜的刺激性、对皮肤的致敏性、致癌致畸性等,因此,运载体系缺乏天然、无毒、安全的乳化剂;2)纳米颗粒递送系统比复合物运载体系更稳定,但单一蛋白颗粒对环境变化比较敏感,容易受到pH值、温度等因素影响;3)目前关于白藜芦醇在运载体系研究主要集中在体外模拟方面,且多为初级研究,而对代谢及消化吸收机制的研究相对较少;4)运载体系制备过程较复杂,生产成本较高,因此制备方法仍处于实验室研究阶段,不适合工业化生产;5)对运载体系运载白藜芦醇的靶向性研究不足,较难实现白藜芦醇的靶向释放,因此白藜芦醇的生物利用度不高,生物活性不明显。
针对上述问题,可以重点研究以下方面:1)大力开发安全、无毒的表面活性剂(蛋白质、多糖),以提高运载体系的安全性;2)深入研究多糖与蛋白质结合制备,两者可通过共价结合或非共价结合增强纳米颗粒的稳定性;3)加强对白藜芦醇代谢消化机制的研究,开展动物实验以确定其代谢途径、毒性等;4)研究适合产业化生产的制备工艺,深入并拓宽运载体系在食品领域(如功能饮料、奶茶、保健食品、3D打印等)的应用;5)对运载体系进行修饰改性或者将多种运载体系结合,更好地实现白藜芦醇的靶向缓释,进一步提高白藜芦醇的生物利用度。

