耐多药结核病治疗过程中周围神经炎发生率的Meta分析
王梦梦 沙莉 李新月 唐苏姚
周围神经炎是结核病治疗过程中常见的药物不良反应[1-2]。与非耐药结核病相比,耐多药结核病(multidrug-resistant tuberculosis,MDR-TB)患者在长期的化疗过程中需要5~6种包括针剂在内的药物联合使用,种类多、疗程长、周围神经炎发生率高且难以预测和处理[3],常会导致患者永久性残疾[1]。目前,虽有研究对MDR-TB治疗过程中药物不良反应的发生情况进行统计,但是部分研究样本量偏小,且未对周围神经炎的发生情况进行有针对性的分析;在研究地区、方法和时间等方面也存在明显差异,导致所报道的周围神经炎的发生率存在差异,难以系统地反映国内外MDR-TB患者抗结核治疗过程中周围神经炎发生率的实际水平和严重程度。为更好地了解MDR-TB患者治疗过程中周围神经炎的发生情况,笔者以MDR-TB患者为目标人群,以周围神经炎的发生率为结局指标,严格遵照纳入和排除标准,系统检索及筛选国内外相关研究,采用系统综述和Meta分析方法,对国内外MDR-TB患者治疗过程中周围神经炎的发生率进行综合分析,以为周围神经炎的预防、诊断和治疗提供参考和依据。
资料和方法
一、检索策略
系统检索PubMed、Embase、Web of Science、Cochrane Library、中国知网(CNKI)、万方、维普和中国生物医学文献数据库中关于MDR-TB治疗过程中周围神经炎发生情况的文献,检索时限从建库至2022年7月。同时,通过参考文献追溯和手工检索方法补充文献。检索采用主题词与自由词相结合的方法进行,并根据每个数据库的特点进行调整。英文检索词:tuberculosis、multidrug-resistant、MDR-TB、side effect、adverse、safety、neuritis、peripheral neuritis、multiple neuropathy;中文检索词:耐多药结核、不良反应、副反应、毒副作用、神经炎、周围神经炎、末梢神经炎、多发性神经病。
二、纳入与排除标准
1.纳入标准:(1)研究对象为MDR-TB患者;(2)干预措施为包含二线抗结核药物的治疗方案;(3)文献报告了周围神经炎不良事件发生率或提供可统计周围神经炎不良事件发生率的数据;(4)研究类型为横断面研究;(5)文献语言限定为中文或英文;(6)公开发表的学术论文。
2.排除标准:(1)重复发表或同一个研究;(2)综述、评论或讲座;(3)研究对象为特殊人群,如孕妇或儿童;(4)信息不完整或不清晰,如文献中无可统计周围神经炎发生率的数据等,与作者联系仍无法取得原始数据的文献;(5)无法获取全文。
三、文献筛选及资料提取
利用Note Express软件进行文献筛查,先去重后再根据文献标题和摘要进行初筛,然后通读全文,依据纳入和排除标准确定最终纳入文献数量。文献提取内容包括第一作者、发表年份、研究地区、研究时间、研究类型、年龄、性别、治疗方案、致病药物、致病时间、样本量、病例数、周围神经炎发生率。整个文献筛查和资料提取过程由2名研究者独立进行,若出现结论不一致,则通过讨论解决,当讨论仍不能解决分歧时,交由第三方进行判断。
四、质量评价
纳入文献采用澳大利亚Joanna Briggs Institute(JBI)循证卫生保健研究中心的横断面研究评价标准进行质量评价[4]。该评价标准共有9项,从抽样方法、研究对象、资料收集及分析方法等方面评价患病率研究的总体质量,每个条目均采用“是”“否”“不清楚”及“不适用”进行判定。根据标准确定文献质量等级,1~3分为低质量,4~6分为中等质量,≥7分为高质量。
五、统计学处理
采用Stata 16.0软件进行统计分析,采用无对照二分类数据即单个率的Meta分析进行数据分析[5-6]。异质性检验采用I2和Q检验进行评估,当P>0.10,I2<50%时,表示纳入研究之间异质性较小,采用固定效应模型进行合并;反之,当P≤0.1,I2≥50%时,表示纳入研究之间存在较大异质性,采用随机效应模型进行合并。采用亚组分析探索不同组别周围神经炎发生率的差异,并探讨异质性的来源。研究结果的稳定性采用敏感性分析检测,如某篇文献被剔除后异质性显著降低,则说明该文献是异质性来源之一。运用漏斗图分析文献是否存在发表偏倚,并通过Egger检验分析发表偏倚。Meta分析的检验水准为α=0.05。
结 果
一、文献筛选流程及结果
从检索到的1231篇文献中去除重复发表文献763篇,阅读题目和摘要排除359篇,对剩下文献进行全文阅读后,排除不符合要求文献,最终共纳入12篇文献[2,7-17]进行研究。文献筛选流程见图1。
二、文献特征和质量评价
纳入分析的12篇文献包含2726例MDR-TB患者,其中,373例发生周围神经炎;调查地区主要为亚洲和非洲地区;文献发表时间为2001—2022年;研究类型包含前瞻性研究及回顾性研究。纳入分析的文献中高质量文献10篇,中等质量文献2篇。纳入文献的基本信息见表1,质量评价结果见表2。

图1 文献筛选流程

表1 纳入分析的12篇文献的基本信息
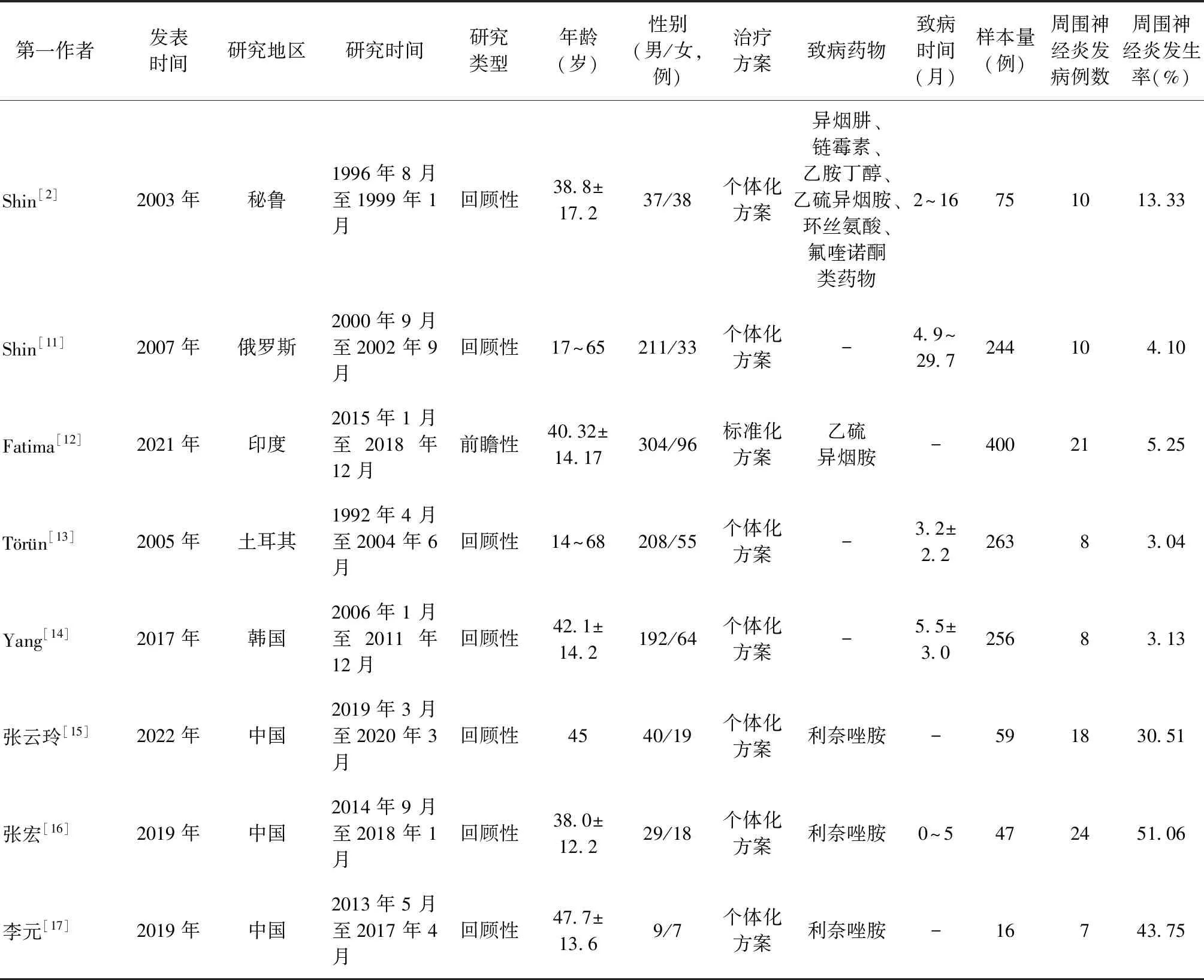
续表1
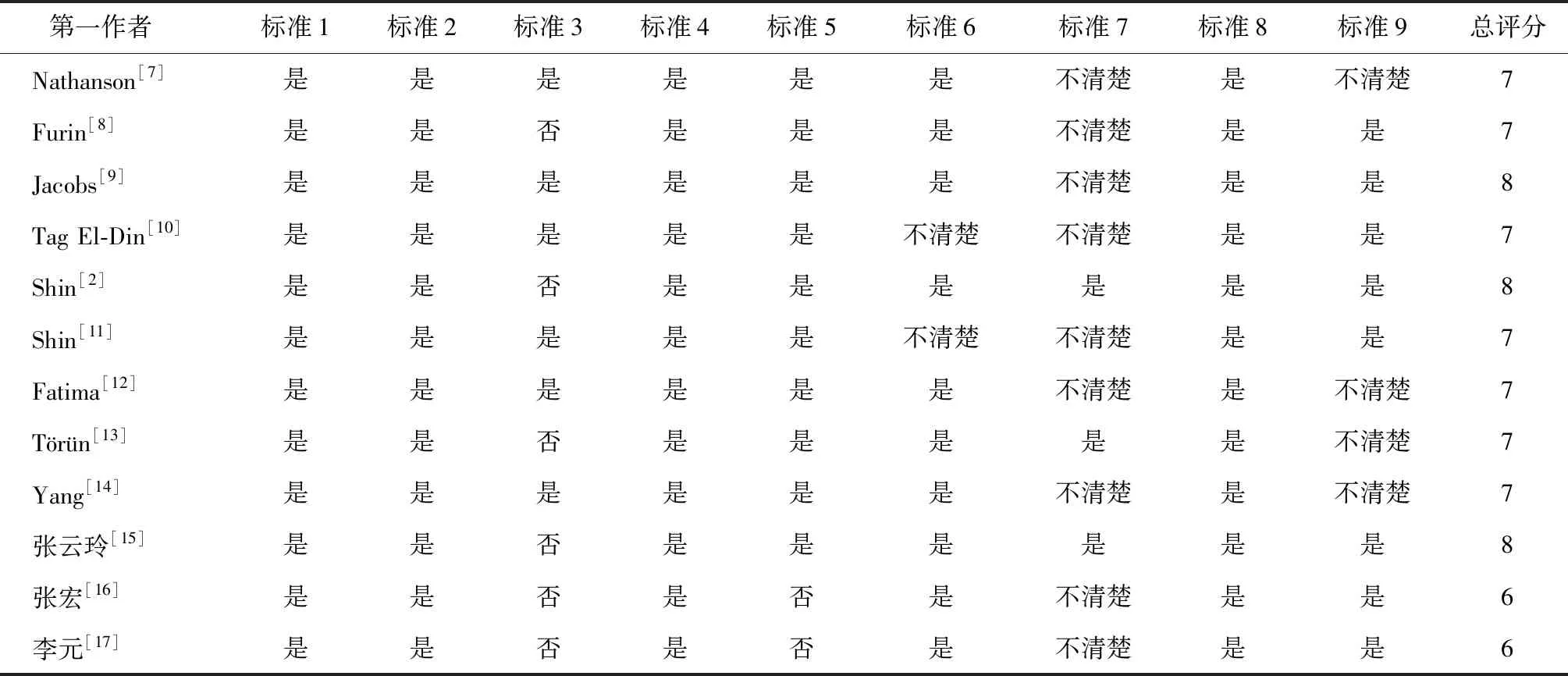
表2 纳入分析的12篇文献的质量评价
三、Meta分析结果
1.总发生率:纳入的12篇文献中,MDR-TB患者治疗过程中周围神经炎的发生率范围为3.04%~51.45%。异质性检验I2=96.7%,P<0.001,故采用随机效应模型进行总效应分析,加权合并MDR-TB治疗过程中周围神经炎的发生率为19%(95%CI:13%~25%)。具体见图2。
2.亚组分析:以研究地区、发表年份、治疗方案及样本量作为分层因素进行亚组分析,由于各组均存在较高异质性,故采用随机效应模型合并效应值。结果显示:(1)研究地区:亚洲地区的5项研究的Meta分析显示,在778例MDR-TB患者中,78例患者发生了周围神经炎,加权合并后周围神经炎发生率为21%(95%CI:12%~29%);非洲地区的2项研究加权合并后,周围神经炎发生率为43%(95%CI:26%~59%);其他地区的5项研究加权合并后的周围神经炎发生率为7%(95%CI:4%~10%)。(2)发表年份:纳入文献的发表年份主要为2000—2022年,发表年份不同,其Meta分析的结果也不同,将其分为2015年之前和2015年及之后两组,每组均包含6项研究,周围神经炎发生率分别为13%(95%CI:6%~20%)和29%(95%CI:17%~40%)。(3)治疗方案:12项研究中有3项研究使用标准化治疗方案,9项研究使用个体化治疗方案,根据不同方案进行Meta分析,周围神经炎发生率分别为16%(95%CI:4%~27%)和21%(95%CI:14%~28%)。(4)样本量:根据本次纳入研究的样本量不同,将其分为≤100例、101~399例、≥400例3个亚组,其中,有5项研究样本量≤100例,加权合并后的周围神经炎发生率为29%(95%CI:16%~43%),其余两组结果分别为18%(95%CI:8%~29%)和7%(95%CI:4%~9%)。具体见表3。
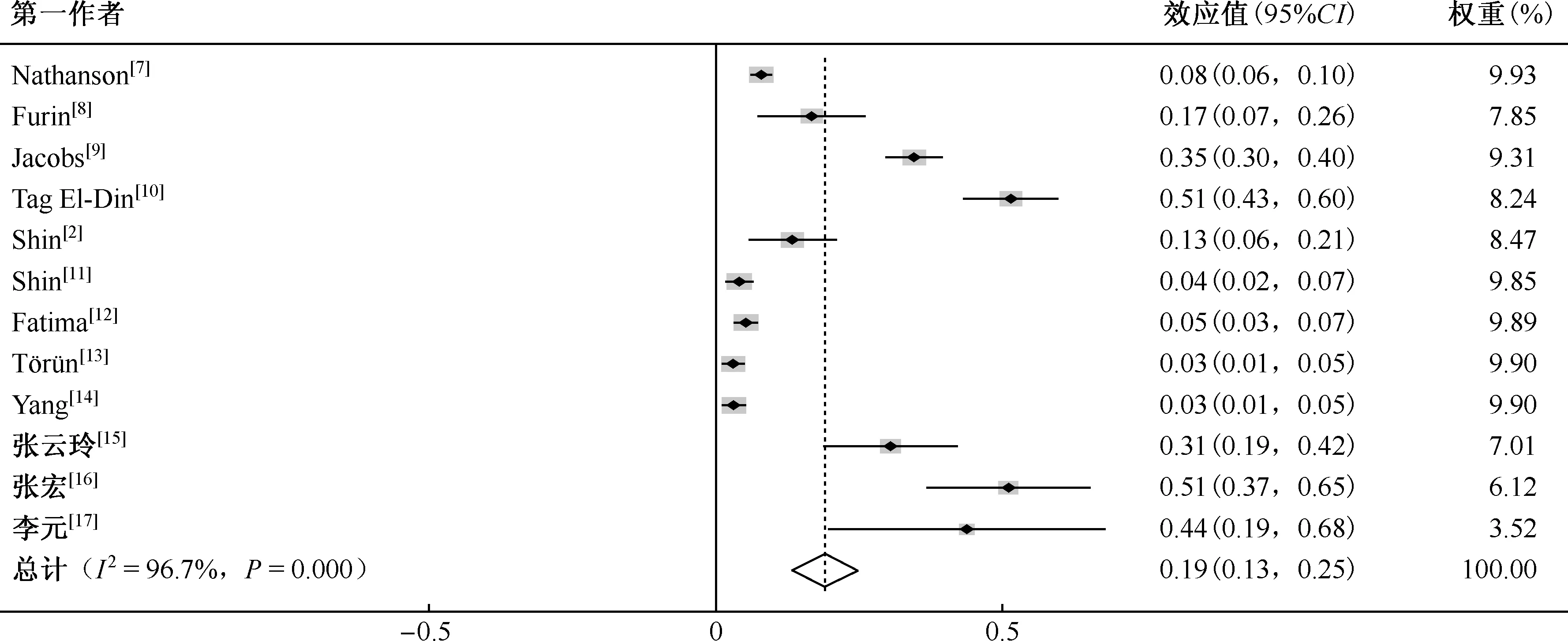
注 权重来自随机效应模型图2 耐多药结核病治疗过程中周围神经炎发生率的Meta分析森林图

表3 不同亚组耐多药结核病患者周围神经炎发生率的Meta分析
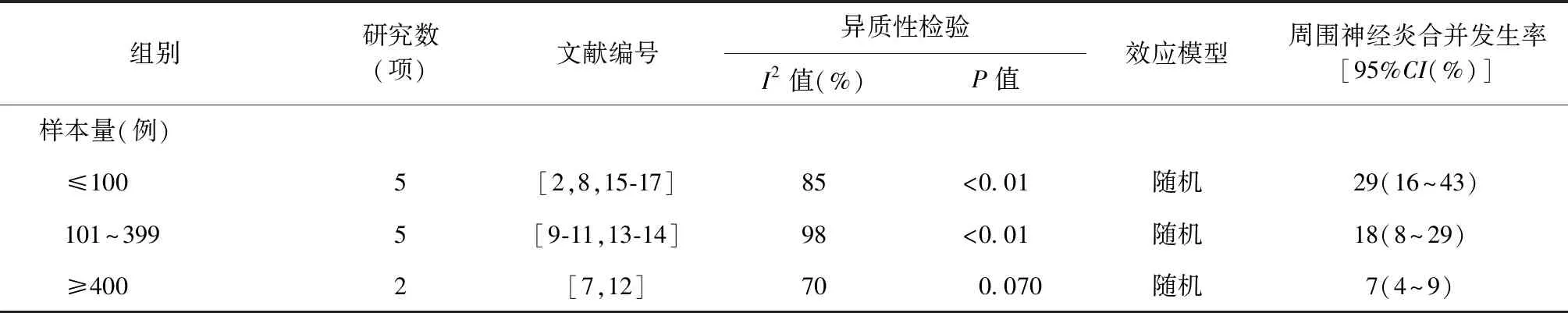
续表3
四、发表偏倚
由漏斗图可以看出,纳入文献散点分布在轴线两侧并不均匀和对称(图3)。为进一步检测,采用 Egger检验,t=3.550,P=0.005,提示可能存在发表偏倚。

图3 耐多药结核病治疗过程中周围神经炎发生率Meta分析纳入文献的漏斗图
五、敏感性分析
将纳入的12项研究采取逐一排除单个研究的方法观察单个研究对合并效应的影响,结果显示,剔出任意1篇文献其效应量未发生明显变化,说明本研究Meta分析结果稳定性较好。
讨 论
与非耐药结核病相比,MDR-TB治疗疗程长,方案复杂,需要联合应用多种毒性较强的二线抗结核药物[2,18],在整个化疗过程中周围神经炎等不良反应发生率高,难预测,且处理难度大[19]。周围神经炎临床主要表现为四肢相对对称的运动、感觉及自主神经功能障碍,症状多表现为受累肢体远端呈手套短袜型感觉减退、麻木或针刺、蚁走、烧灼、触痛和感觉过敏等刺激性症状,甚至肌肉萎缩[20],在发生后如处理不当会严重影响患者的生存质量。相关文献报道,结核病并发的周围神经炎可能不可逆转,一旦发生,将对患者造成深远的影响[3]。本次研究共纳入国内外12篇文献,共2726例MDR-TB患者,有373例在抗结核治疗过程中出现周围神经炎。Meta分析结果显示,MDR-TB患者在使用二线抗结核药物治疗过程中周围神经炎的总发生率为19%(95%CI:13%~25%),处于较高的水平。当MDR-TB患者并发糖尿病、HIV感染、酒精中毒等时,周围神经炎的发生率还会增加[3]。抗结核药物不良反应会影响患者的治疗依从性,容易造成患者治疗中断、失败,诱导或加重耐药的产生[19,21-22],导致MDR-TB患者转变为广泛耐药结核病患者[18]。
本次分析显示,非洲地区的MDR-TB患者治疗过程中周围神经炎的发生率为43%,高于亚洲及其他地区,可能由于非洲地区是结核病高发地区,且非洲结核病患者合并HIV感染者比例较大[23],地区经济相对落后,患者可能存在治疗依从性差和营养不良。相关研究也显示,并发HIV感染、药物滥用及营养缺乏尤其缺乏维生素B是周围神经炎的高发因素,导致非洲地区MDR-TB患者的周围神经炎发生率高[1]。亚洲地区MDR-TB患者周围神经炎的发生率虽然低于非洲地区,但是总体也处于较高水平。本次分析显示,2015年之前发表的文献中MDR-TB治疗过程中周围神经炎的发生率明显低于2015年及之后,可能因为随着经济社会的发展及终结结核病方案的提出,近些年患者和医务人员对抗结核药物不良反应的预防、筛查和管理意识提高,研究者对结核病的关注度逐渐提升。本次分析显示,实施标准化治疗方案和个体化治疗方案的MDR-TB患者,周围神经炎的发生率存在一定差异。实施个体化治疗方案的MDR-TB患者周围神经炎的发生率高于实施标准化治疗方案的患者。MDR-TB标准化治疗方案是依据国家或地区耐药结核病检测资料,针对不同耐药类型群体设计的统一的化学治疗方案;个体化治疗方案是依据患者药物敏感性试验结果、既往用药史及患者具体情况综合考虑后制定的治疗方案[24]。与个体化治疗方案相比,标准化治疗方案经过科学的研究,并通过大量实践证明具有高效性,药物不良反应发生率低[25]。本次分析根据各研究的样本量不同进行了分组,结果显示,样本量≤100例的研究中研究对象的周围神经炎发生率最高,周围神经炎发生率最低的为纳入≥400例样本量的研究,这可能与样本的代表性有关。
本研究具有一定的局限性:(1)为了保证研究质量,本研究未纳入低质量文献和会议论文等灰色文献,漏斗图分散且不对称,可能存在发表偏倚。(2)本研究为单个率值的Meta分析,各研究间异质性较大,虽然进行了亚组分析,但不同亚组间异质性仍较高,影响各研究间的因素无法确定,可能影响结果的准确性。(3)纳入研究为观察性研究,但对于药物不良反应的调查应首选研究设计为长期的药物不良反应检测,因此,受研究设计所限,多种偏倚无法避免。
综上所述,当前证据显示,MDR-TB患者治疗过程中周围神经炎的发生率较高。在MDR-TB治疗过程中医务人员应加强对患者的监测和管理,对患者及其家属进行相关健康宣教,提高患者自我识别能力,做到早评估、早诊断、早干预。
利益冲突所有作者均声明不存在利益冲突
作者贡献王梦梦:酝酿和设计实验、实施研究、采集数据、分析/解释数据、起草文章、统计分析;沙莉:对文章的知识性内容作批评性审阅、获取研究经费、指导、支持性贡献;李新月和唐苏姚:采集数据、统计分析、支持性贡献

