pH对罗望子胶和κ-卡拉胶复配凝胶特性的影响
李婷,王玉丽,范玉文,聂珂楠,院佩佩,吴正奇*
湖北工业大学生物工程与食品学院(武汉 430068)
罗望子胶(TSP)是从豆科罗望子属植物种子的胚乳中分离提取出来的一种中性多糖类物质。与其他动植物胶相比,TSP水溶液的黏稠性较强,黏度不受酸类和盐类等影响,具有优良的物理化学性质和热稳定性[1]*。但是罗望子胶在冷水中溶解性差,溶液浑浊,自身不成胶。卡拉胶是一种来源于红海藻的硫酸化多糖,是一种优秀的亲水性胶体[2]*。此次试验使用的是κ-卡拉胶(KC),其相对分子质量约为5×105*Da。得益于KC的凝胶性、生物相容性和生物可降解性,KC已被广泛用于食品、乳制品和医药行业[3]*。但KC溶解度相对不高,且存在不耐酸、脆性大、易脱水等缺陷[4]*。复合多糖可使多糖在不同作用机制上起效,彼此互补平衡,协同提高凝胶性质,通过不同胶体之间的复配可以提高或改善κ-卡拉胶的凝胶性质[5]*。望运滔等[6]*曾试验表明卡拉胶-仙草胶复合能形成整体性能较佳的复合膜。文章首次选取TSP与KC这两种多糖进行复合,由于TSP和KC的分子结构中都含有大量羟基,因此预测TSP会通过氢键的相互作用与KC结合。
1 材料和方法
1.1 材料与试剂
罗望子胶(河南豫中生物工程有限公司);κ型卡拉胶(河南旗诺食品配料有限公司);其他试剂均为分析纯。
1.2 仪器与设备
TA.XTplus质构分析仪(英国Stable Micro有限公司);MCR92安东帕流变仪(奥地利安东帕有限公司);JSM-5610LV型扫描电子显微镜(日本Hitachi公司);D-advance X-射线衍射分析仪(美国Bruker公司);DSC-Q10差示扫描量热仪(美国TA公司);Namo ZS MPT-2纳米粒度及电位分析仪(英国Malvern公司)。
1.3 试验方法
1.3.1 复配凝胶的制备
称取一定量TSP,加入到去离子水中快速摇匀,配制出1.5% TSP溶液,之后将事先准备定量的KC加入到TSP溶液中,使得混合溶液中的KC浓度为0.7%,复合浓度为2.2%。室温下用磁力搅拌器搅拌至溶液均匀统一。5份混合溶液分别使用HCl和NaOH溶液调节pH至2,4,6,8和10,放入85 ℃的水浴锅中加热30 min,在冷水中快速冷却,在4 ℃条件下储藏12 h,之后进行凝胶性质测定。
1.3.2 持水性(WHC)测试
参考Xia等[7]*的文献,采用离心法测定凝胶WHC。
1.3.3 流变特性测试
1.3.3.1 表观黏度测定
样品在室温下平衡2 h后恢复室温,在25±0.2 ℃下测定TSP-KC复合凝胶的表观黏度与剪切速率之间的关系。此时测定的平行板直径为40 mm,剪切速率为0.01~1 000 s-1*,狭缝间距为0.5 mm。
1.3.3.2 频率扫描
根据应变扫描测量得到的LVR,将频扫试验的应变固定在1%,使用振荡模式。具体参数:形变量为1%,频率范围为0.1~25 Hz,在25 ℃条件下测定MCPWPI复合凝胶的储能模量(G’)、损耗模量(G”)及损耗因子(tanδ=G”/G’)随角频率的变化情况。
1.3.3.3 蠕变与恢复
蠕变恢复测试根据Bi等[8]*的方法进行评估。
1.3.4 质构特性测试
复合凝胶样品在进行凝胶质构特性测试时使用P/0.5圆柱型探头,选用TPA模式,设置参数:测试前速度为1.0 mm/s,测试速度为1.0 mm/s,测试后速度为1.0 mm/s,压缩比例为30%,触发力为5 g。
1.3.5 微观结构(SEM)测试
将样品放入真空冷冻干燥机中冷冻干燥,冻干的复配凝胶样品切割成小块,将横切面积朝上固定在样品台上喷金。在30 kV的加速电压下,用扫描电子显微镜观察记录图像。
1.3.6 Zeta电位-粒径测试
将相同浓度的TSP溶液、KC溶液以及TSP/KC复合凝胶在室温下搅拌2 h后,分别用超纯水稀释100倍,之后在25±1 ℃条件下进行测定。
1.3.7 X-射线衍射(XRD)测试
参考Shahbazi等[9]*的方法,并稍作修改。冻干样品,测定条件:电压40 kV、电流40 mA、扫描速率10°/min、扫描范围2θ为5°~55°。
1.3.8 热稳定性(DSC)测试
精确称取4 mg冻干样品于铝坩埚,以空铝埚作参照样,通过差示扫描量热仪以5 ℃/min的速率从-20℃升到200 ℃,测量热焓值的变化情况。
1.3.9 数据处理
所有测定进行3次平行试验,结果以平均值±标准差的形式表示。试验数据分析使用SPSS 25.0和Origin 2021软件。P<0.05为统计学差异显著。
2 结果与分析
2.1 宏观结构
图1表明,胶体在碱性条件下随着pH的增加而变黄,推测是TSP中含有糖醛酸,醛基在氢氧化钠溶液中不稳定,会与羟基反应同时发生歧化反应,其生成的产物会使溶液发黄。此外,pH 2时凝固性较差,不成胶,其他pH条件下均形成了较为稳定的凝胶。这与孙哲浩等[10]*在对明胶和卡拉胶体系的研究结果一致,当pH低于3时,体系形成极其微弱的凝胶,这可能是酸对卡拉胶分子结构造成破坏,使大分子降解为小分子,从而影响凝胶的形成。

图1 不同pH复配凝胶外观
2.2 持水性
持水性能好的凝胶能充分溶胀但不溶解,具有很高的黏度,凝胶网络结构形成更加紧密。图2表明,pH 2时复配凝胶体系中持水性相对来说较差,其他pH条件下的复配凝胶体系持水性数值较高,无显著性差异,持水性良好。

图2 不同pH条件下复配凝胶持水性
2.3 流变特性
2.3.1 表观黏度
图3显示,当复合凝胶处在pH 2的条件下时,表观黏度极低,且不随剪切速率的变化而变化,这可能是因为卡拉胶在酸性溶液中(尤其是pH≤4.0)易发生酸水解,低pH破环了复配凝胶的结构,导致其复配凝胶性质变差[11]*。在pH 4~10条件下,复合凝胶的表观黏度都随着剪切速率的增加而明显降低,表现为剪切稀化,是胶体行为[12]*。同时,该条件下复合凝胶的表观黏度并没随着pH的变化有明显的变化,说明此范围内的pH对TSP/KC复合凝胶的黏度并没有显著影响,其表观黏度在一定范围内pH相对稳定,这可能是由于TSP/KC复配凝胶的黏度主要取决于TSP的添加与否。

图3 不同pH条件下复配凝胶表观黏度
2.3.2 动态黏弹性
图4表明,在pH 4~10条件下,G’>G”,且都随着振荡频率的提高而缓慢上升,这说明该复合凝胶体相弹性性质优于黏性,更偏向于形成弹性固体(elastic solid),呈显著性凝胶特性[13]*。在pH 6的条件下,G’和G”表现为最高,且根据计算pH 6时损耗因子tanδ最小,说明凝胶在pH 6强度相对最好。
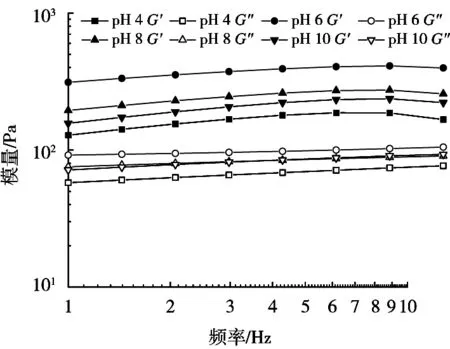
图4 不同pH条件下复配凝胶G’、G”的流变特性
2.3.3 蠕变与恢复
如图5所示,在pH 4~10范围内,凝胶随着蠕变试验的时间增加,应变值迅速增加到一定值,然后略微下降后保持线性变化。这种现象表明,黏性流效应是蠕变阶段最终变形的主要原因,这是典型的黏弹性行为。蠕变阶段结束时的最大柔度(Jmax)可以反映出凝胶体系最大的抗变形性。Jmax值越髙,表示抗变形性越弱,同时说明凝胶体系结构较弱。由图5(B)可知,pH 4时的最大柔量(Jmax)最大,pH 6时的Jmax最小,其次是pH 8和pH 10。流变学结果表明,TSP通过与KC相互作用可以形成的凝胶是黏弹性材料,其中pH 6时凝胶黏弹性与强度最佳。
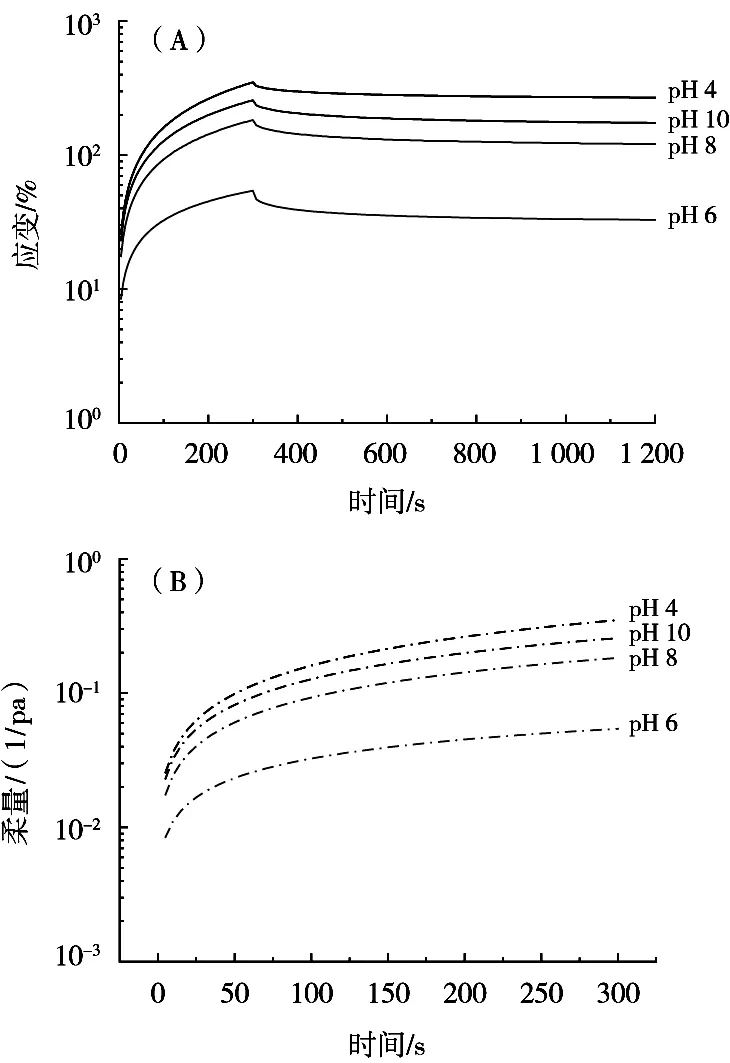
图5 不同pH条件下复配凝胶的蠕变恢复曲线
2.4 质构分析
质地特性是凝胶体系的一个重要特征。pH 2.0时,凝胶硬度最小(27.75 g)。pH 6~10时,凝胶硬度较大且无显著性差异(P>0.05),pH 4时相对较小,但也远大于pH 2。弹性与内聚性、黏附性和回弹性相关。pH 2时凝胶样品的弹性最高,在pH 4~10范围内,弹性无显著差异,均低于pH 2。内聚性是凝胶抵抗变形的紧密程度的标准。内聚性在pH 2时相对较高,在其他pH条件下无显著差异。结果与上文凝胶强度结果保持一致,在pH 4~10范围内复合凝胶相对稳定。

表1 不同pH条件下TSP/KC复合凝胶的质构参数
2.5 凝胶微观结构
由图6可以观察得到在不同pH条件下复配凝胶的微观结构发生变化。pH 2时,TSP/KC复配凝胶网络结构间距大,间壁发生破裂,凝胶的网络结构有所破坏。pH 4时,网络结构的间距变小,间壁破损显著减小,但有序性较差。当pH在中性和碱性条件下时,凝胶网络结构均匀致密而有序。酸性条件下会促进卡拉胶分子降解,碱性条件下会阻止卡拉胶分子相互缠绕[14]*。但是图像表明复配凝胶在碱性条件下相对稳定,且只在强酸性条件下,其结构会受到明显破坏,不成形。这与之前猜测的结果一致,复配凝胶能适应较为广泛的pH。

图6 不同pH条件下复配凝胶的微观结构
2.6 电位粒径
通过调节不同的pH可以改变多糖的电位粒径。如图7(A)所示,在不同pH条件下KC带负电荷,TSP基本不带电荷或者带少量电荷。TSP与金属氢氧化物或碱式盐溶液反应后,得到相应的金属络合物,能变成阴离子或阳离子衍生物。TSP/KC复配凝胶溶液带有负电且电荷量低于KC,说明除了氢键相互作用,静电相互作用在TSP/KC复配凝胶体系中可能也起着一定作用。多糖的电荷密度通过影响分子间的相互作用,进而影响多糖复配凝胶的凝胶性质。由图7(B)可见,通过调节pH可以影响多糖分子粒径,此外,所有pH条件下TSP/KC复配溶液粒径均小于单个多糖溶液。TSP与KC混合复配后粒径变小,这一现象可能是电荷中和过程中静电相互作用和氢键相互作用共同影响复配聚集体分子的收缩所导致。

图7 不同pH条件下凝胶、溶液的电位粒径图
2.7 DSC
热稳定性可以通过熔化温度来说明,DSC升温过程把热量传递给凝胶体系,可以引起胶体状态和结构发生改变,从而表明分子间是否存在相互作用[15]*。由图8可知,不同pH条件下,TSP/KC复配凝胶的变性温度(Tm)不同,其中pH 6时的Tm最高,为97.75 ℃,最低为pH 2。热变性温度越高,说明TSP/KC复配凝胶体系在加热过程中发生了交联和缠结,形成了更加稳定的结构,热稳定性越强。
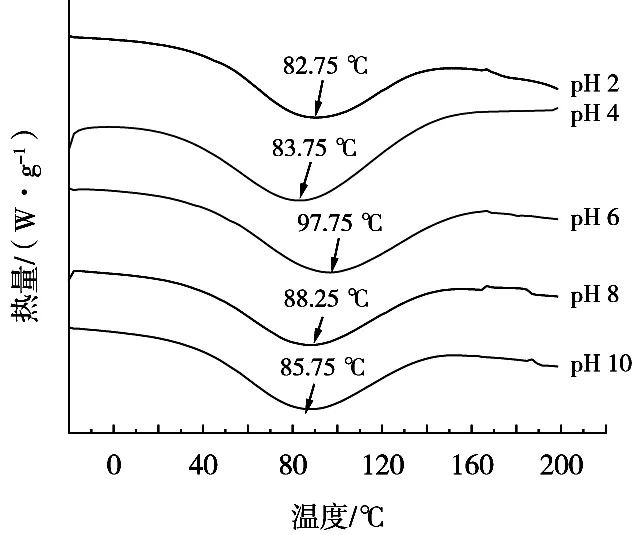
图8 不同pH条件下TSP/KC复配凝胶的热稳定性
2.8 XRD
多糖分子通过羟基形成氢键,在分子内和分子间产生连接,导致其呈现出不同程度的结晶排列以及无定型态和晶态之间的转变。如图9所示,在不同pH条件下复配凝胶的衍射强度在2θ在20°左右时,其峰面积最大,峰形圆钝,峰强度较高,因此复配凝胶中结晶区域的比例较少,主要以无定型态存在。在pH 4~10条件下TSP/KC复配凝胶有明显的特征峰,但是其特征峰在pH 2时消失,说明pH 2时,TSP/KC复配凝胶的有序性被破坏。在pH 4~10之间出现多个衍射峰且衍射峰十分相似,2θ在30°左右处有双衍射峰出现,这表明在pH 4~10间多糖凝胶中存在一定结晶性,说明多糖凝胶形成了更为有序的结构,使得结晶度上升。同时,红外吸收峰性状十分相似,且吸收峰无明显偏移,说明在pH 4~10范围内,不同pH对TSP与KC复配产生的基团无显著性影响。

图9 不同pH条件下复配凝胶X-射线衍射图谱
3 结论与讨论
TSP与KC复配凝胶在pH 4~10条件范围内持水性和凝胶性优异,凝胶特性参数相对稳定,形成了凝胶网络结构并且具有一定结晶性,且pH 6时,网络结构最致密,抗变形能力最好,热稳定性最强。TSP与KC复配凝胶可减缓酸性条件下KC分子的降解,促进碱性条件下多糖分子的相互缠绕,能在很广泛的pH范围维持复配凝胶性质的稳定性。目前国内对TSP的研究大部分是在对TSP本身性质的研究,TSP资源被综合研究利用的应用较少。此TSP复合材料产品可以进一步研究作为壁材对一些pH敏感性的生物活性物质进行包载,为探索开发出封装、保护或者递送一些敏感性的生物活性物质的产品提供思路。

