疏水淀粉皮克林乳液凝胶的稳定机理及影响因素
郭 璐,黄 亮,张 斌,扶 雄,黄 强
(华南理工大学食品科学与工程学院,广东 广州 510641)
以固体颗粒稳定的皮克林乳液,能对功能物质实现保护、控制释放等功能[1]。通过添加胶凝剂、改变油相体积分数等手段,可以将皮克林乳液转化为乳液凝胶[2]。皮克林乳液凝胶具有独特的三维网络结构和可调的力学性质,兼具了皮克林乳液和凝胶的优点,如贮存稳定性高、环境污染小、稳定剂使用量少等[3],具有良好的应用前景,可用于包埋和递送活性物质[4]、抑制脂肪氧化[5]、新型材料制备[6]等。食品领域中,已有不少研究者利用纤维素、蛋白质、复合颗粒等食品级颗粒制备出皮克林乳液凝胶[7-8]。Dai Lei等[9]利用玉米醇溶蛋白和阿拉伯胶的氢键和静电相互作用,制备了复合胶体纳米颗粒,并用其制备出能长期稳定的皮克林乳液凝胶;Zhang Bao等[10]将玉米醇溶蛋白/羧甲基糊精颗粒稳定的皮克林乳液加入卡拉胶基质中,通过共价交联制备出了皮克林乳液凝胶并用于稳定姜黄素,结果显示姜黄素的光热稳定性和生物可及性显著提高。
淀粉是食品的重要成分之一,通过改性可制备出稳定皮克林乳液凝胶的食品级固体颗粒[11]。此外,淀粉独特的半结晶结构、糊化等特性为调控乳液凝胶的乳化性和凝胶性提供了更多的可能。目前,对淀粉进行疏水改性[12]、复合其他聚合物[13]、调节环境因素[14]等方式都能有效提高淀粉颗粒的乳化性能。而将淀粉与脂质进行复合是一种绿色安全的淀粉疏水改性手段,可以有效改善淀粉颗粒的疏水性能,是一种极具潜力的皮克林乳化剂[15]。已有研究表明,月桂酸可以在温度高于熔点的反应体系中进入V型淀粉的单螺旋空腔中形成I型复合物,月桂酸的加入可以有效改善淀粉颗粒的表面性能[16]。Lu Xuanxuan等[17]将高直链玉米淀粉与月桂酸复合,并利用该复合物制备了皮克林乳液,所制乳液在不同离子强度和pH值条件下都有一定的稳定性。
食品行业中,皮克林乳液凝胶在包埋递送活性物质、作为固体脂肪代替物等方面有很大的应用前景,可用于焙烤食品、调味酱料等产品[18],但这些产品会暴露在不同食品体系和环境中,因此了解不同因素对乳液凝胶的影响十分重要。目前,鲜见不同因素对淀粉-脂质复合物(starch-fatty acid complex,SFAC)稳定的皮克林乳液凝胶影响的研究。环境条件不同会影响SFAC颗粒的结构、性质等,进而影响其乳化行为,改变其吸附于油水界面的能力,影响乳液凝胶网络结构的稳定性等。
本研究阐述疏水淀粉皮克林乳液凝胶的制备及其稳定性评价;设置不同的环境条件(贮藏温度、pH值及离子强度),通过微观观察、粒径分析及电位分析等方式探究其对皮克林乳液凝胶的影响,并将其应用于不同油相,为乳液凝胶体系的应用提供一定理论指导。
1 材料与方法
1.1 材料与试剂
普通玉米淀粉(直链淀粉质量分数23%,食用级)吉林天成玉米开发有限公司;月桂酸(纯度≥99%,食用级) 上海凌峰化学试剂有限公司;大豆油、玉米油、葵花籽油、亚麻籽油(均为食用级) 上海益海嘉里食品有限公司;尼罗河红、尼罗河蓝(均为分析纯)美国Sigma-Aldrich公司;NaOH、浓盐酸、NaCl、正己烷(均为分析纯) 国药集团化学试剂有限公司。
1.2 仪器与设备
BS201S电子分析天平 德国Starorius公司;Silent Crusher M高速剪切机 德国Heidolph公司;BH-2光学显微镜 日本Olympus公司;Mastersizer 3000激光粒度仪、Zetasizer Nano ZS纳米激光粒度电位仪 英国马尔文仪器有限公司;SP8激光共聚焦扫描显微镜(confocal laser scanning microscope,CLSM) 德国Leika公司;DF-1018磁力搅拌器 河南予华仪器有限公司;EVO18扫描电子显微镜(scanning electron microscope,SEM)德国ZEISS公司。
1.3 方法
1.3.1 疏水淀粉纳米粒子制备及复合指数测定
参考Huang Liang等[16]的方法制备SFAC。将3 g普通玉米淀粉分散于100 mL蒸馏水中配制3%淀粉分散液,沸水浴加热1 h,保持搅拌,完全糊化后冷却至室温。将2 倍体积的无水乙醇逐滴滴加至上述淀粉糊中,4000 r/min离心10 min。用无水乙醇清洗沉淀3 遍,将沉淀物置于40 ℃烘箱干燥,粉碎后过100 目筛,得到V型淀粉纳米粒子。采用干法制备SFAC,称取一定质量V型淀粉纳米粒子,加入淀粉质量分数10%的熔融月桂酸,在60 ℃封闭体系下干法反应48 h,粉碎后过100 目筛,得到SFAC。
参考Jia Xiangze等[19]的方法测定SFAC复合指数。取0.1 g样品,加入10 mL水,沸水浴下搅拌30 min,冷却后于3000 r/min离心10 min。取上清液50 μL,加入4 mL I2-KI溶液(0.1% I2和2% KI溶解于100 mL水),振荡混合后,用紫外分光光度计于690 nm波长下测定吸光度。通过下式计算,得到V型淀粉与月桂酸的复合指数为34.3%。
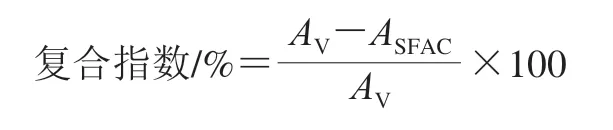
式中:AV、ASFAC分别为V型淀粉纳米粒子和淀粉-月桂酸复合物在690 nm波长下的吸光度。
1.3.2 皮克林乳液凝胶的制备
选取不同种类食用油作为油相:大豆油、玉米油、葵花籽油和亚麻籽油。皮克林乳液凝胶体积为10 mL,SFAC添加量为4 g/100 mL,油相体积分数为50%。加5 mL蒸馏水(水相)于淀粉样品,磁力搅拌过夜,再加入油相,20000 r/min高速剪切2 min,得到皮克林乳液凝胶。
1.3.3 不同处理后皮克林乳凝胶的制备
将1.3.2节制备的皮克林乳液凝胶分别置于不同温度(-20、4、25、60 ℃和100 ℃)下处理6 h,得到不同温度处理后的皮克林乳液凝胶。
配制0.1 mol/L NaOH溶液和0.1 mol/L HCl溶液,制备6 个pH值(pH 3、5、7、9、11和13)梯度的溶液,各取5 mL作水相,按照1.3.2节步骤制备不同pH值处理后的皮克林乳液凝胶。
配制0(对照)、0.1、0.3、0.5、0.7 mol/L和0.9 mol/L 6 个浓度梯度的NaCl溶液,各取5 mL作水相,按照1.3.2节步骤制备不同离子强度处理后的皮克林乳液凝胶。
将油相替换为正己烷,按照1.3.2节步骤制备皮克林乳液凝胶,真空干燥10 h,得到干燥皮克林乳液凝胶[20]。
1.3.4 皮克林乳液凝胶的微观形态观察
取少量皮克林乳液凝胶样品滴于载玻片上,盖上盖玻片后,置于光学显微镜下观察并拍照记录。
取皮克林乳液凝胶0.5 mL,加入100 μL尼罗蓝、尼罗红混合染色剂,混合振荡,于避光低温下放置过夜。取一滴滴于载玻片,盖上盖玻片后用精油涂抹封边,置于CLSM下进行观察。尼罗红、尼罗蓝的荧光激发波长分别为488、633 nm。
1.3.5 皮克林乳液凝胶的粒径测定
取适量皮克林乳液凝胶样品放入蒸馏水分散容器中,系统遮光背景强度达到6%~12%时使用激光粒度仪进行测试,得到乳液凝胶粒径分布曲线和数据。淀粉折光度为1.54,蒸馏水折光度为1.33。
1.3.6 皮克林乳液凝胶的Zeta电位测定
用滴管取少量皮克林乳液凝胶样品分散于蒸馏水中,将其缓慢注入干净的样品池,避免产生气泡,放入纳米激光粒度电位仪中测试样品的Zeta电位。
1.3.7 皮克林乳液凝胶的SEM测定
用导电胶将上述干燥皮克林乳液凝胶样品固定于测试台,真空条件下进行喷金,放入SEM中,加速电压为10 kV,调节合适的放大倍数进行观察、拍摄。
1.4 数据分析
所有实验均重复3 次,通过SPSS 18.0软件对数据进行差异显著性分析,并用Excel、Origin 2021软件作图。
2 结果与分析
2.1 贮存温度对皮克林乳液凝胶稳定的影响
由图1可知,皮克林乳液凝胶经-20 ℃处理6 h后,乳液结构被破坏,这可能是因为连续相冻结后,冰晶的形成破坏了SFAC形成的界面屏障,解冻之后,SFAC颗粒无法再吸附于油水界面,导致油滴聚集上浮,乳液体系失稳,出现分层。皮克林乳液凝胶经4、25、60 ℃处理后体系稳定,均可维持乳液凝胶网络结构且具有良好的胶凝性;100 ℃处理后乳液凝胶黏度下降,出现流动性,而光学显微镜结果表明乳液结构并未明显被破坏,静置降温后又可重新呈现凝胶状态,并在贮藏60 d后保持倒置不流动(图2)。由于SFAC的熔融解旋温度在105~114 ℃之间[16],高于100 ℃,这可能是SFAC稳定的乳液凝胶在高温处理下仍保持结构稳定的原因。高温处理使得分子间相互作用力减弱,覆盖在油滴表面的SFAC颗粒之间的交联作用减弱,降低了整体的凝胶强度,出现流动性。冷却后,分子间相互作用力恢复,重新形成凝胶,倒置不流动。Li Ruyi等[21]用单宁酸和β-葡聚糖复配稳定的皮克林乳液;Liu Yikun等[22]用辛烯基琥珀酸改性淀粉和单宁酸协同稳定的高内相乳液都有类似现象,当加热超过60~70 ℃时,由于氢键减弱、凝胶强度减弱,冷却后氢键恢复,乳液样品再次变得凝固。由此可见,本实验的皮克林乳液凝胶是具有热可逆性的半固体材料,温度升高,乳液凝胶变得容易流动,而温度降低则再次呈现胶凝性,该特性可使乳液凝胶在温度波动的场景中有潜在应用。如图2所示,贮藏60 d后,-20 ℃处理后的皮克林乳液凝胶由于乳液结构在水相结冰又解冻后被破坏,油相漏出,体系表观松散无定形。其余温度处理后乳液凝胶可倒置,仍表现出良好的凝胶性质。其中4 ℃处理的与室温处理的乳液凝胶质地、表观等表现一致,说明适度的低温处理基本不会影响乳液凝胶的结构和性能。

图1 不同温度处理后皮克林乳液凝胶光学显微镜图(A)和CLSM图(B)Fig.1 Microscope (A) and CLSM images (B) of Pickering emulsion gel treated at different temperatures

图2 不同温度处理后新鲜的(A)和贮藏60 d的(B)皮克林乳液凝胶表观Fig.2 Appearance of fresh (A) and 60-day stored (B) Pickering emulsion gel treated at different temperatures
由图3可知,以25 ℃常温处理为对照,高温处理和低温处理都明显增大了乳液凝胶的粒径。结合光学显微镜观察结果(图1A),-20 ℃处理后的乳液凝胶粒径明显增大,这是由于乳液结构被破坏,SFAC颗粒无法吸附于油水界面层,形成稳定的三维网络结构以阻止油滴大量聚集。60 ℃和100 ℃处理后的乳液凝胶粒径明显增大,结合图1可知,60 ℃和100 ℃处理后的乳液凝胶结构并未被破坏,其原因是高温处理会使体系界面张力降低,小乳滴更趋于形成大乳滴以缩小表面积,维持体系稳定,因此高温处理会使乳滴少量聚集,形成较大乳滴。此外,高温处理也会加剧分子的布朗运动,增加乳滴合并的趋势,但SFAC颗粒仍能通过重组和桥联作用,重新分布并吸附于油水界面,稳定较大的乳滴并维持乳液凝胶结构[23]。

图3 不同温度处理后皮克林乳液凝胶粒径分布Fig.3 Droplet size distribution of Pickering emulsion gel treated at different temperatures
2.2 皮克林乳液凝胶在不同pH值下的稳定性
如图4所示,从表观形态看,pH 13下出现明显分层,无法形成乳液凝胶,其他pH值条件下均能形成乳液凝胶。由图5可知,pH 3、5、7和9处理后的样品都形成了淀粉颗粒包裹油相的乳滴。pH 11处理后的样品虽然能形成乳滴,但乳滴尺寸差异明显且乳滴间存在较大空隙,可见pH 11条件下虽然不影响乳液凝胶表观形态,但高碱性对其微观结构有显著影响。继续提高pH值至13时无法形成乳液凝胶,乳滴尺寸最大。有研究表明,改性纳米淀粉颗粒在高pH值下会发生水解反应导致乳液的失稳和相分离[24]。此外,SFAC稳定的皮克林乳液凝胶在pH 3~11范围内能保持60 d长期稳定(图4),乳液凝胶一旦形成,在长期贮藏中,其形态和结构不会轻易改变。

图4 不同pH值处理后新鲜的(A)和贮藏60 d的(B)皮克林乳液凝胶表观Fig.4 Appearance of fresh (A) and 60-day stored (B) Pickering emulsion gel treated at different pH conditions

图5 不同pH值处理后皮克林乳液凝胶光学显微镜图Fig.5 Light microscopic images of Pickering emulsion gels treated at different pH conditions
皮克林乳液凝胶在中性及酸性条件下的粒径分布和Zeta电位结果接近。由图6A可知,弱碱条件下(pH 9),乳液凝胶的粒径反而减小,可能是淀粉颗粒与界面之间存在一定的静电相互作用,帮助加强乳液凝胶的稳定性[25]。pH 11时粒径分布有较大差异,出现粒径较小和较大两个峰,这与光学显微镜结果一致(图5),说明部分乳滴出现聚集。pH 13处理的样品明显出现了两个粒径分布峰,结合表观形态看,第1个粒径峰可能是淀粉颗粒的聚集或少量乳滴的粒径,第2个粒径峰可能是被分散的油滴的粒径。由此可知,碱性条件易对皮克林乳液凝胶的粒径造成极大影响。Ko等[26]也发现随着pH值增加,淀粉纳米颗粒在碱性条件下发生不均匀溶解,导致皮克林乳液的稳定性显著降低。此外,由图6B可知,强碱条件下,随着pH值增加,乳滴电位绝对值大幅上升,这可能是由于淀粉颗粒在碱性条件下发生去质子化反应,破坏了SFAC颗粒间的相互作用,颗粒在乳滴表面的聚集导致界面膜强度减弱,造成乳液凝胶体系失稳。Liu Yikun等[22]用单宁酸和辛烯基琥珀酸改性淀粉协同稳定的高内相乳液在pH 7处也发现了相似现象。Zhang Cuige[27]和Kargar[28]等分别对复合纳米颗粒和微晶纤维素颗粒进行研究,发现颗粒的Zeta电位绝对值都随着体系中pH值的上升而增加,这与本实验的Zeta电位分析结果相似。

图6 不同pH值处理后皮克林乳液凝胶粒径分布(A)及Zeta电位(B)Fig.6 Droplet size distribution (A) and zeta potential (B) of Pickering emulsion gel treated at different pH conditions
2.3 皮克林乳液凝胶在不同离子强度下的稳定性
如图7、8所示,不同离子强度下皮克林乳液凝胶中乳滴大小均一且堆积密集,形成了颗粒型乳液凝胶网络结构,无乳析分层现象,贮藏60 d后仍具有良好的稳定性。由图9A可知,皮克林乳液凝胶平均粒径(D50)在11.5~13.5 μm之间,不同离子强度下乳液凝胶粒径分布无明显差异,说明不同离子强度处理对乳液凝胶的结构影响较小,这与Lee等[29]用淀粉纳米粒子与甲壳素纤维协同稳定的乳液粒径的研究结果相似。

图7 不同离子强度处理皮克林乳液凝胶光学显微镜图Fig.7 Light microscopic images of Pickering emulsion gel treated with different ionic strengths

图8 不同离子强度处理后新鲜的(A)和贮藏60 d的(B)皮克林乳液凝胶表观Fig.8 Appearance of fresh (A) and 60-day stored (B) Pickering emulsion gel treated with different ionic strengths

图9 不同离子强度处理后皮克林乳液凝胶粒径分布(A)及Zeta电位(B)Fig.9 Droplet size distribution (A) and zeta potential (B) of Pickering emulsion gel treated with different ionic strengths
由图9B可知,对照样品的Zeta电位为-10.3 mV,经不同离子强度处理后Zeta电位绝对值减小,在-2~-4 mV间浮动但无明显差异,可能是因为当NaCl浓度为0.1 mol/L时已经能达到静电屏蔽的效果。许多皮克林乳液体系中,离子强度的静电屏蔽作用可以减弱乳滴之间的静电相互作用,从而影响乳液体系的稳定性[30-31]。如酸水解淀粉纳米晶体稳定的皮克林乳液凝胶体系中,NaCl产生的静电屏蔽会使颗粒集聚进而导致乳液体系失稳[32]。然而有趣的是,结合乳液凝胶微观、表观形态及粒径分布(图7、8、9A)结果可知,离子强度并不能影响该疏水淀粉乳液凝胶的稳定性,可见静电相互作用力也许并不是疏水淀粉皮克林乳液凝胶体系中阻碍乳滴聚集、维持乳液凝胶网络结构的主要作用力,而是SFAC颗粒在油水界面的紧密排布及其产生的空间位阻,阻止了乳滴的聚集[29]。因此,本实验的皮克林乳液凝胶的耐盐能力极强,在复杂的食品体系中有潜在的应用价值。
2.4 疏水淀粉皮克林乳液凝胶在不同油相中的应用
如图10所示,SFAC颗粒能稳定不同油相皮克林乳液凝胶,乳滴粒径大小均一且分布均匀。SFAC颗粒在油水界面形成一层屏障,阻碍了油滴之间的聚集(图10B)。此外,乳滴周围还有少量淀粉颗粒分布,说明4%淀粉添加量足以满足稳定50%油相的需要,处于连续相中的游离淀粉颗粒可以通过桥联作用增强乳液凝胶网络结构以阻止乳滴的合并[33]。由表观形态可知(图11),皮克林乳液凝胶呈现出具有良好胶凝性和黏性的软固体状态,质地均一、表面光滑,具有塑造立体形状的效果。说明SFAC颗粒具有稳定不同油相形成皮克林乳液凝胶的能力,可以广泛用于不同油相的乳化和稳定。

图10 不同油相的皮克林乳液凝胶光学显微镜图(A)和CLSM图(B)Fig.10 Microscope (A) and CLSM images (B) of Pickering emulsion gel with different oil phases

图11 不同油相的新鲜的皮克林乳液凝胶表观Fig.11 Appearance of fresh Pickering emulsion gels with different oil phases
2.5 疏水淀粉皮克林乳液凝胶网络结构及稳定机理
用正己烷替代植物油制备乳液凝胶,将正己烷烘干蒸发后,留下形状如蜂巢的乳液凝胶网络,如图12所示,乳滴之间连接紧密,凝胶网络表面密实无孔,形成了一层结实的保护层。将该网络结构再放大,可观察到网络内表面由淀粉颗粒所呈现的不规则凸起的颗粒感,进一步佐证了该体系是由淀粉颗粒包裹分散的油滴并通过相互作用密集堆积而形成,与CLSM观察结果(图1B、10B)相吻合。因此,由SFAC颗粒稳定的皮克林乳液凝胶体系中,SFAC颗粒在高速剪切下自发移动至油水界面并紧密排布,形成一层致密的屏障包裹油滴,阻碍油滴的聚集,维持乳液凝胶结构的稳定;同时通过不同乳滴间的相互交联作用与空间位阻以及水相中SFAC颗粒之间的桥联作用,形成紧密的乳液凝胶三维网络结构,阻止了油滴的碰撞和合并,使其在不同环境条件(温度、pH值及离子强度)下都具有优良的稳定性[23]。由于乳滴间的紧密堆积和相互交联作用截留住了作为连续相的水,使乳液凝胶流动性大大降低,从而呈现良好的胶凝性及半固体状态。

图12 皮克林乳液凝胶网络结构SEM图Fig.12 SEM images of Pickering emulsion gel network structure
3 结论
SFAC颗粒在高速剪切过程中自主吸附到油水界面上,紧密地包裹油滴,形成一层机械屏障稳定乳液凝胶结构。-20 ℃低温下,SFAC颗粒形成的屏障被破坏,油滴大量聚集,乳液分层;100 ℃下乳液凝胶出现流动性,冷却后能重新恢复胶凝性,具有热可逆性功能。高碱性条件下(pH 13),淀粉颗粒发生去质子化,无法维持本身的吸附性能,乳液凝胶结构被破坏,但在pH 3~9范围内,乳液凝胶的性质和结构受影响较小。离子强度的变化对皮克林乳液凝胶影响不明显。总体而言,SFAC颗粒稳定的皮克林乳液凝胶在多种不同环境条件下都可以维持其良好的稳定性与结构性能,在复杂的食品体系中有良好的应用前景。

