医用镁合金表面阳极氧化/茶多酚复合转化层耐腐蚀性能研究
李浩,张皓,申孝龙,李栋梁,杨成
医用镁合金表面阳极氧化/茶多酚复合转化层耐腐蚀性能研究
李浩a,张皓a,申孝龙b,李栋梁a,杨成a
(攀枝花学院 a.钒钛学院 b.生物与化工学院,四川 攀枝花 610000)
在AZ31镁合金表面制备阳极氧化/茶多酚复合转化层,解决医用镁合金在植入环境中降解过快、易导致炎症等问题。使用阳极氧化法在镁合金表面构建阳极氧化(Anodization)层,之后在阳极氧化层上通过浸泡法制备多酚转化层,得到复合转化层,多酚选择表没食子儿茶素没食子酸酯(EGCG)。通过SEM、EDS、XRD、FTIR和XPS对转化层的表面形貌、成分结构进行分析,利用极化曲线、电化学阻抗谱、长期浸泡试验评价转化层的耐腐蚀行为。阳极氧化层内层致密,外层多孔,主要成分为MgO和MgSiO3。在阳极氧化层表面构建EGCG转化层形成复合层后,外层孔洞被填补,且FTIR图谱中出现了EGCG的特征峰。电化学评价结果显示,与AZ31相比,复合转化层的自腐蚀电流密度降低了约2个数量级,高频容抗弧半径显著增大,等效电路模拟后所得极化电阻(p)为179.425 kΩ·cm2,远大于裸材。长期浸泡试验结果显示,复合层可明显控制浸泡过程中溶液pH值的增加,且明显低于其他对照组。浸泡160 h后,表面腐蚀产物最少,具有良好的耐腐蚀性能。采用阳极氧化法和浸泡法在AZ31镁合金表面成功制备了阳极氧化/茶多酚复合层,明显提高了镁基底的耐蚀性能。选用的EGCG来源绿色、价格低廉,且具有抗氧化、抗炎等多重功效,为医用镁合金表面改性提供了一种新方案。
镁合金;医用材料;阳极氧化;EGCG;耐腐蚀能力
镁及镁合金由于具备可生物降解性、良好的生物相容性和接近天然皮质骨的理想杨氏模量,被广泛认为是一种具有潜在革命性的骨科植入材料[1-5]。更重要的是,研究表明,镁基骨植入物植入后释放的镁离子可以促进骨再生,并加速愈合[6-7]。理想的镁基骨植入物在支撑时间和降解行为层面应该和骨组织愈合的过程相匹配[8]。然而,限制镁及镁合金临床应用的主要问题是其在生理环境中具有高反应性,由于降解过快导致的机械完整性过快丢失、大量氢气、局部碱性环境以及腐蚀产物的堆积均会对骨组织的修复产生不同程度的负面影响。为了解决这些缺陷,并开发临床上可行的镁基骨植入物,减缓和控制镁基骨植入物的生物降解速率至关重要。
表面改性层可在早期保护镁基底,减缓镁基底的降解速率,从而减少早期机械损失,以适应现阶段的承重要求。在减缓降解速率的基础上,表面涂层可以为细胞和组织提供稳定的弱碱性表面微环境,以适应细胞粘附和组织生长[9]。近年来,已有大量关于镁基骨植入物表面改性的研究,如阳极氧化层、仿生矿化沉积钙磷涂层、电沉积涂层和化学转化层等[10]。其中阳极氧化(AO)是常用的表面处理技术之一,通过电解在金属表面形成一层氧化层,以增强金属的耐腐蚀性能[11]。然而,阳极氧化层具有多孔结构,孔隙处容易侵入腐蚀介质,导致保护失效。同时,对于医用骨植入物表面改性,在提高镁基底耐腐蚀能力的基础上,还需要兼顾生物功能。因此,需要通过复合层的构建来改善AO层的耐腐蚀能力,并兼顾生物相容性的提高。
近年来,将茶多酚引入骨植入物的表面改性成为研究热点。大量研究表明,多酚化合物具有抗氧化、抗菌、抗炎、降血脂等多种生物活性,这些生物活性主要是来自多酚类物质的氧化能力[12-13]。其次,将绿茶中的多酚提取物用于钛合金表面改性,该表面能够诱导羟磷灰石沉积,促进成骨细胞分化和矿化[14-15]。同时,茶多酚可以与多种金属离子络合,形成稳定的络合物,并覆盖在金属表面,这为构建茶多酚转化层,提高镁基底的耐腐蚀能力提供了理论基础[16-21]。前期研究表明,在医用镁合金表面构建多酚转化层可有效提高镁基底的耐腐蚀能力[22]。更重要的是,将茶多酚用于表面改性,可在表面成功引入活性位点(酚羟基和醌基),可用于后续生物功能的修饰[23-24]。
因此,本研究把阳极氧化和化学转化相结合,在镁合金表面通过阳极氧化制备OA层的基础上,采用浸泡法制得OA-EGCG复合层,提高镁基底的耐腐蚀能力和生物相容性,为可降解镁基骨植入物表面改性提供了一种新思路。
1 试验
1.1 制备方法
基底样品准备。将AZ31镁合金切割为10 mm× 10 mm×1 mm的方形试样,打磨抛光,清洗干燥备用。AZ31镁合金的化学成分见表1。

表1 AZ31镁合金的化学成分
阳极氧化层(AO)制备。电解液由40 g/L NaOH、30 g/L Na2B4O7·10H2O、90 g/L NaSiO3组成,溶液用去离子水配制。试验电源为WYK-K系列直流稳压稳流电源,使用阳极氧化电压70 V制备阳极氧化层。样品标记为AZ31-OA。
阳极氧化/多酚复合层(OA-EGCG)制备。将EGCG溶解于Tris缓冲液(10 mmol/L,pH=8.5)中,得到1 mg/mL的EGCG转化液。将AZ31-OA置于该转化液中,室温下反应12 h后取出,超声清洗并干燥后,保存于真空干燥箱中。样品标记为AZ31-OA- EGCG。制备流程如图1所示。
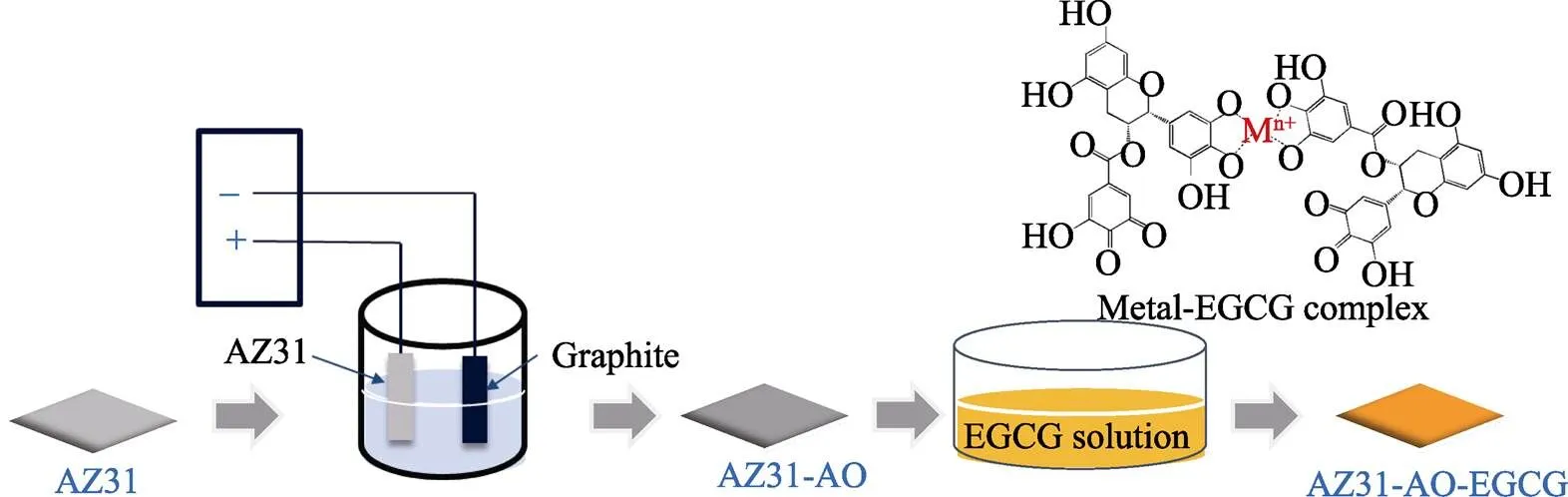
图1 OA-EGCG复合层制备流程
1.2 检测与分析
使用场发射扫描电子显微镜(FESEM,JSM- 7401F,JEOL,日本)对样品表面及截面形貌进行观察,结合EDS能谱仪分析样品组成元素。通过XRD进行物相分析。采用傅里叶红外分析仪(NicoletiS50)结合衰减全反射附件,波数范围为4 000~500 cm–1,测定样品表面成膜前后表面官能团的变化。通过X 射线光电子能谱(XPS)测定材料表面的元素组成及元素键合状态,并用C1s 峰(284.6 eV)的标准结合能校正。使用3M胶带对样品表面进行粘揭,直接观察样品表面层的结合情况。
电化学测试包括动电位极化(PDP)和电化学阻抗谱(EIS)。测试在电化学工作站(IM6,Zahner,德国)上进行,三电极单元组成:样品作为工作电极,铂片为对电极,饱和甘汞电极 SCE为参比电极。使用硅橡胶封装试样,留出带有涂层的表面作为工作电极。电化学测试的腐蚀介质为磷酸盐缓冲液(PBS),测试温度通过水浴锅稳定在37 ℃左右。测试开始前,样品在PBS中浸泡10 min,以稳定开路电位(OCP)。动电位极化曲线扫描范围为–2.0~–1.0 V,扫描速率为1 mV/s。自腐蚀电位(corr)和自腐蚀电流密度(corr)由Tafel外推法确定。电化学阻抗谱(EIS)测试的频率范围为10–1~105Hz,正弦幅度为 20 mV。使用相应的等效电路模拟奈奎斯特图,重复测试不少于3次。
将样品用环氧树脂密封后浸泡在(37±0.5) ℃的PBS缓冲液(pH=7.4)中,每4个总表面积为4 cm2的样品浸泡在160 mL PBS中作为1组,设置3组平行样。浸泡160 h,每隔12 h使用PHS-3C pH计(Lei-ci,China)记录溶液的 pH 值,并观察浸泡后表面形貌。
同样将密封好的测试样品浸泡在250 mL PBS 中,样品面积与PBS 溶液体积比约为0.01 cm2/mL,平行样设置3组,每组4个样品。样品放置于析氢装置中,并置于37 ℃恒温水浴锅中保温,每间隔固定时间,通过析氢装置中玻璃管内液面下降刻度,估读析氢量,并记录。
2 结果与讨论
2.1 复合层微观形貌
AZ31、AZ31-AO、AZ31-AO-EGCG样品的表面SEM形貌如图2所示。可以看到,在AZ31表面,仍可见抛光后的划痕。经阳极氧化处理后的AZ31-AO样品,表面可见阳极氧化层的形成,该氧化层的表面显示出大量的孔隙。镁合金的阳极氧化层内层薄且致密,外层较厚但多孔。因此,从表面SEM的结果来看,AZ31-AO显示出多孔隙的状态。在AZ31-AO的基础上,进一步进行EGCG转化液的浸泡后,得到的AZ31-AO-EGCG表面明显无孔洞的存在。可以看到,形成的EGCG转化层覆盖填补了AZ31-AO的孔洞结构。但是AZ31-AO-EGCG表面仍可见均匀的裂纹,这是由于EGCG分子中含有刚性结构,当转化层中EGCG的含量较多,会导致涂层在干燥状态下,由于应力变化发生开裂。
为观察涂层的厚度及进一步印证阳极氧化层的孔隙被EGCG转化层填补,对AZ31-AO和AZ31-AO- EGCG这2组样品的截面进行的SEM形貌观察,结果如图3所示。AZ31-AO的截面明显出现阳极氧化产生的多孔形貌,氧化层厚度在1.39 μm左右。在AZ31-AO表面再次沉积EGCG转化层后,AZ31-AO- EGCG表面的涂层厚度明显增加,约2.11 μm。同时,截面看不到微孔形貌,说明形成的EGCG转化层覆盖填补了阳极氧化形成的孔洞结构。
通过简单的3M胶带粘揭测试样品表面涂层结合力,试验结果如图4所示。通过对比AZ31-EGCG(即在AZ31表面直接沉积EGCG转化层)和AZ31- OA-EGCG这2组样品的表面涂层结合力可以看到,阳极氧化层作为中间层,可以有效提高EGCG转化层的结合力。AZ31-EGCG表面的涂层在胶带粘揭后出现大面积的脱落,而AZ31-AO-EGCG表面的涂层仅在边缘部分出现涂层粘揭。这是由于在制备样品时,边缘部分的AO层受到一定破坏导致的。该结果显示了AZ31-AO-EGCG涂层较好的结合力。
2.2 复合层组成成分
为检测阳极氧化层中的元素成分及含量,对样品AZ31-AO进行EDS点扫描,结果如图5所示。AZ31-AO的表面存在较多孔洞,因此分别对阳极氧化层实体和孔洞处进行EDS检测。可以看到,阳极氧化层的实体部分含有大量的O、Mg和Si,而孔洞处主要是Mg和少量的O。这说明阳极氧化层中应该含有氧化镁和硅镁盐,而孔洞处主要显示基底的镁和少量氧化镁。

图2 AZ31、AZ31-AO、AZ31-AO-EGCG样品表面的电镜形貌

图3 AZ31-AO和AZ31-AO-EGCG截面电镜形貌

图4 AZ31-EGCG和AZ31-AO-EGCG样品表面涂层粘揭3M胶带前后的形貌对比
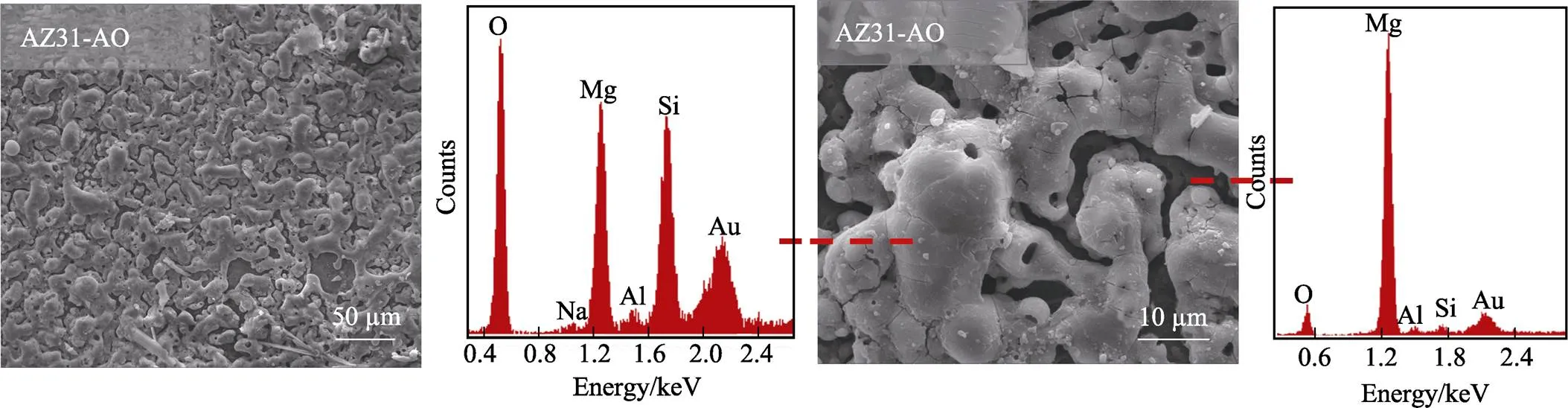
图5 AZ31-AO表面EDS元素分析
为进一步对阳极氧化层的成分进行确定,通过XRD检测AZ31-AO和AZ31-AO-EGCG,结果如图6所示。图6中,2值为20.08°、31.22°、57.58°、63.18°和68.88°的衍射峰可分别标定为MgSiO3的(0,2,0)、(6,1,0)、(8,3,2)、(10,2,1)、(1,4,3)晶面。2值为36.67°的衍射峰可标定为MgO的(1,1,1)晶面,其余衍射峰均为Mg的晶面信息。可以看到,AZ31-AO表面的阳极氧化层和AZ31-AO-EGCG表面涂层中均主要含有MgSiO3和MgO成分。AZ31-AO-EGCG表面的MgSiO3衍射峰减少,说明表面EGCG转化层覆盖在AZ31-AO阳极氧化层表面。
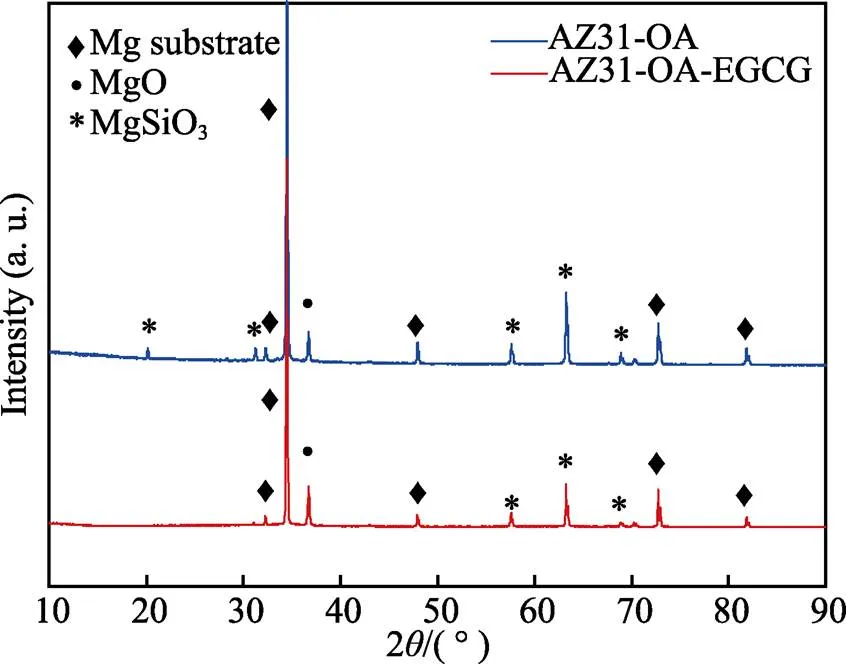
图6 AZ31-AO和AZ31-AO-EGCG表面XRD检测分析
通过ATR-FTIR光谱分析AZ31、AZ31-AO、AZ31-AO-EGCG表面的化学成分,结果如图7所示。可以看到,与AZ31相比,AZ31-AO在3 756 cm–1附近显示尖峰,对应反应形成的阳极氧化层中Mg(OH)2的—OH[25]。AZ31-AO-EGCG样品同样显示有Mg(OH)2中的—OH。AZ31-A-E的红外图谱出现宽峰,为酚羟基—O—H的伸缩振动[26]。另外,C—O伸缩振动峰(1 265 cm–1)和苯环骨架C峰(1 605 cm–1)的出现[24],说明AZ31-AO-EGCG表面转化层中含有EGCG成分。红外分析表明,在AZ31合金上成功制备了阳极氧化层,并在阳极氧化层表面成功沉积了EGCG转化层,转化层中可能含有Mg(OH)2和EGCG与金属的络合物。
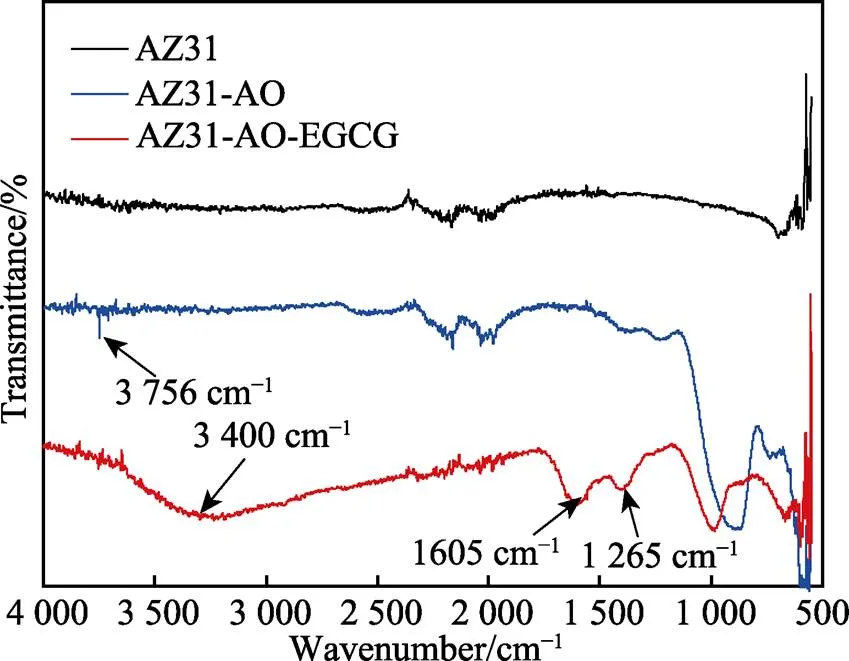
图7 AZ31、AZ31-AO、AZ31-AO-EGCG的表面红外光谱分析对比
为研究AO-EGCG复合层中EGCG层在AO层表面的结合形式,对AZ31-AO-EGCG样品表面进行XPS检测,并对涂层中的Mg和O元素的高分辨图谱进行了拟合分析[24,26]。图8显示了AZ31-AO-EGCG样品表面Mg1s和O1s的拟合结果。Mg元素拟合为3种键合状态:1 304.2 eV处的Mg2+,来自镁盐和络合态的镁离子;1 303.5 eV处的MgO及络合态MgO;1 302.8 eV处的Mg(OH)2及络合Mg(OH)2。O元素拟合为4种键合形式:酚羟基(532.9 eV),来自镁盐或其他金属盐的O=C—O(–531.9 eV),Mg(OH)2(531.1 eV)以及醌基和MgO(530.2 eV)。将镁合金浸泡在EGCG转化液中,可以在表面形成EGCG转化层,转化层中含有酚镁络合物[22]。AZ31-AO- EGCG样品表面Mg和O元素的XPS高分辨图拟合结果显示,EGCG层是以转化层的形式结合在AO层表面,形成的AO-EGCG复合层。
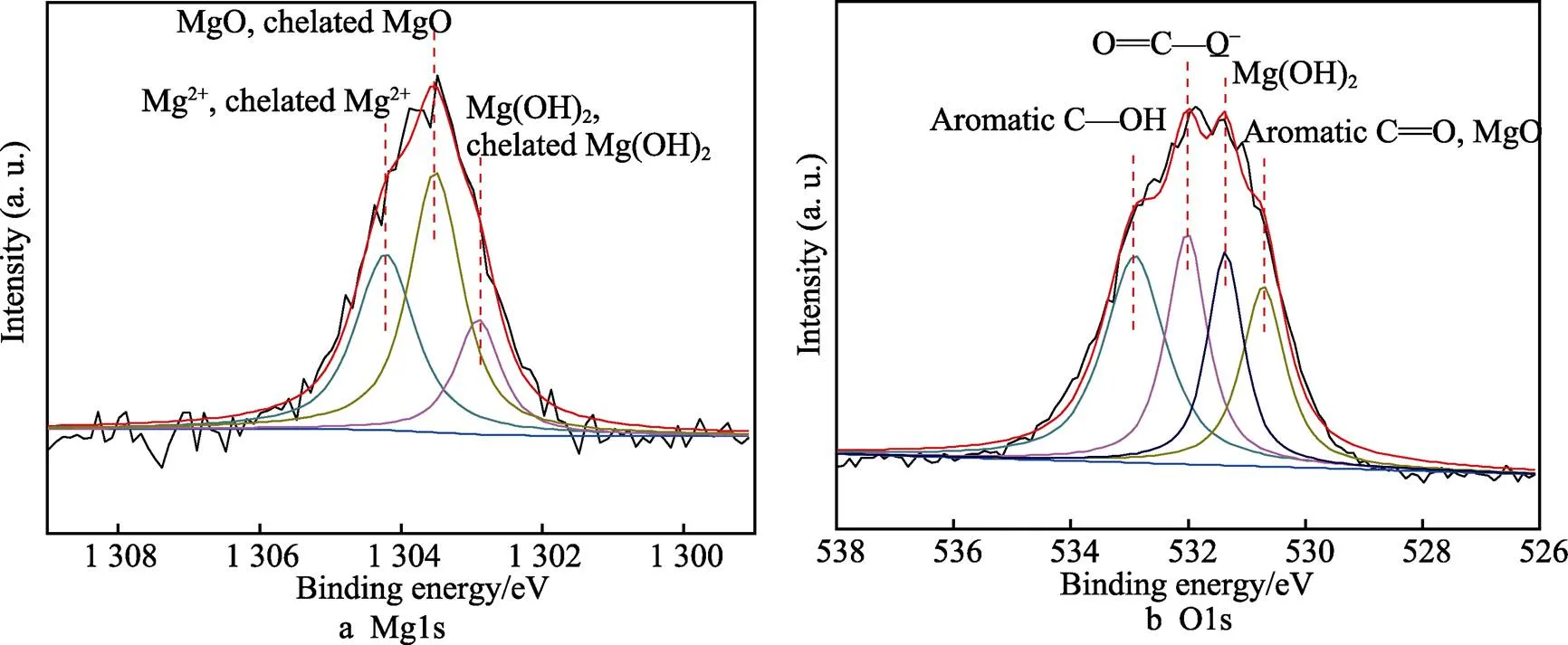
图8 AZ31-AO-EGCG样品表面的Mg1s和O1s的XPS高分辨图谱拟合结果
2.3 耐腐蚀行为评价
为评价OA-EGCG复合层对AZ31的腐蚀保护行为,对AZ31、AZ31-AO、AZ31-AO-EGCG进行了电化学评价,包括PDP和EIS测试。另外,进行了长期浸泡测pH值变化的试验。
2.3.1 极化曲线分析
所有样品的动电位极化曲线如图9所示。通过Tafel外推法测得corr和corr,见表2,而平均腐蚀速率i则可以通过公式i=22.85corr计算得到[27]。AZ31、AZ31-AO、AZ31-AO-EGCG的corr大致相近。从自腐蚀电流密度来看,AZ31-OA的自腐蚀电流密度corr相较AZ31明显减小,从2 454.71 μA/cm2减小至154.88 μA/cm2,说明阳极氧化层对基底的耐腐蚀能力实现了一定程度的提高。AZ31-AO-EGCG呈现最小的自腐蚀电流密度(17.78 μA/cm2),比裸材小2个数量级。这说明,在AZ31-AO表面构建EGCG转化层,可以进一步提高材料的耐腐蚀性能。
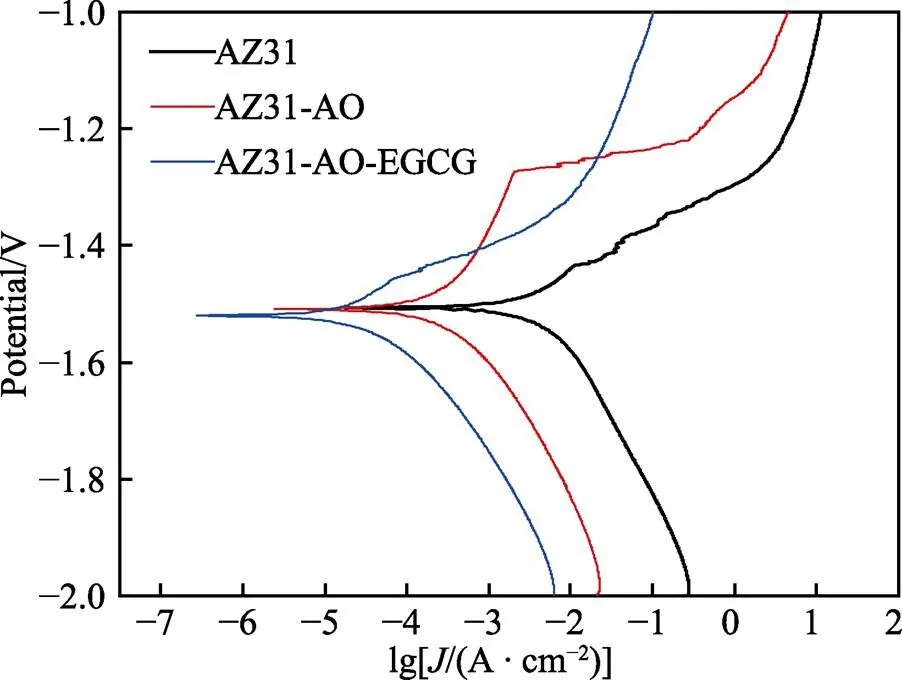
图9 AZ31、AZ31-AO、AZ31-AO-EGCG的动电位极化曲线

表2 AZ31、AZ31-AO、AZ31-AO-EGCG在PBS 中的自腐蚀电位Ecorr、自腐蚀电流Jcorr及腐蚀速率Pi
对样品极化前后的形貌进行了对比,如图10所示。AZ31在进行极化测试前呈现金属光泽的表面,而极化后的表面明显被破坏,且有大量白色腐蚀产物堆积,说明表面发生了相对严重的点蚀。AZ31-AO样品,极化前的表面呈现阳极氧化层的白色,极化后的表面可见少量的腐蚀点,且无明显的腐蚀产物堆积。AZ31-AO-EGCG的表面呈现出棕色,这是由于表面覆盖的EGCG转化层带来的,EGCG转化层的形成过程就是它氧化自聚合的过程。极化测试后,AZ31- AO-EGCG的表面同样无明显变化,只出现了少数腐蚀点,说明AO-EGCG改性层对基底腐蚀保护的有效性。

图10 各样品极化测试前后的表面形貌对比
2.3.2 EIS阻抗图谱分析
3种样品的EIS阻抗图谱(Nyquist图和Bode图)如图11所示。研究表明,不同镁基材料的高频容抗半圆与腐蚀速率密切相关,高频容抗半圆的半径越大,其腐蚀速率越小,样品的耐蚀能力越好。由Nyquist图(见图11a、b)可知,AZ31-AO-EGCG显示出最大的高频容抗弧半径,AZ31-AO次之,但二者都明显大于AZ31的高频容抗弧半径,表明改性层显著提高了基底的耐腐蚀能力。AZ31的Nyquist图(见图11b)显示出2个时间常数,分别是高频区的电容和低频区的电感回路,电容回路对应镁基底与PBS溶液之间的界面电荷转移,可由电荷转移电阻(ct)并联双层电容(dl)表示;电感回路涉及镁表面腐蚀产物的形成,由局部缺陷位点吸附物质的电感()和电阻(L)串联模拟。AZ31-AO和AZ31-AO-EGCG的Nyquist图(见图11a)显示出2个时间常数,分别是高频电容回路和低频电容回路,高频电容回路与涂层或腐蚀产物层的缝隙相关,由代表涂层缺陷的电阻(pore)和电容(f)并联拟合;中频电容回路与界面电荷转移过程有关,由电荷转移电阻(ct)和电容(dl)并联拟合。Nyquist图谱中没有电感回路,Bode图中没有正相位角的标志性特征。用于拟合的等效电路如图12所示,其中图12a为AZ31的EIS数据等效电路,图12b为AZ31-AO和AZ31-AO-EGCG的EIS数据等效电路。拟合结果见表3,s为溶液电阻。腐蚀系统的极化电阻p与腐蚀速率成反比,根据等效电路可计算求得腐蚀系统的极化电阻p,计算结果见表3。
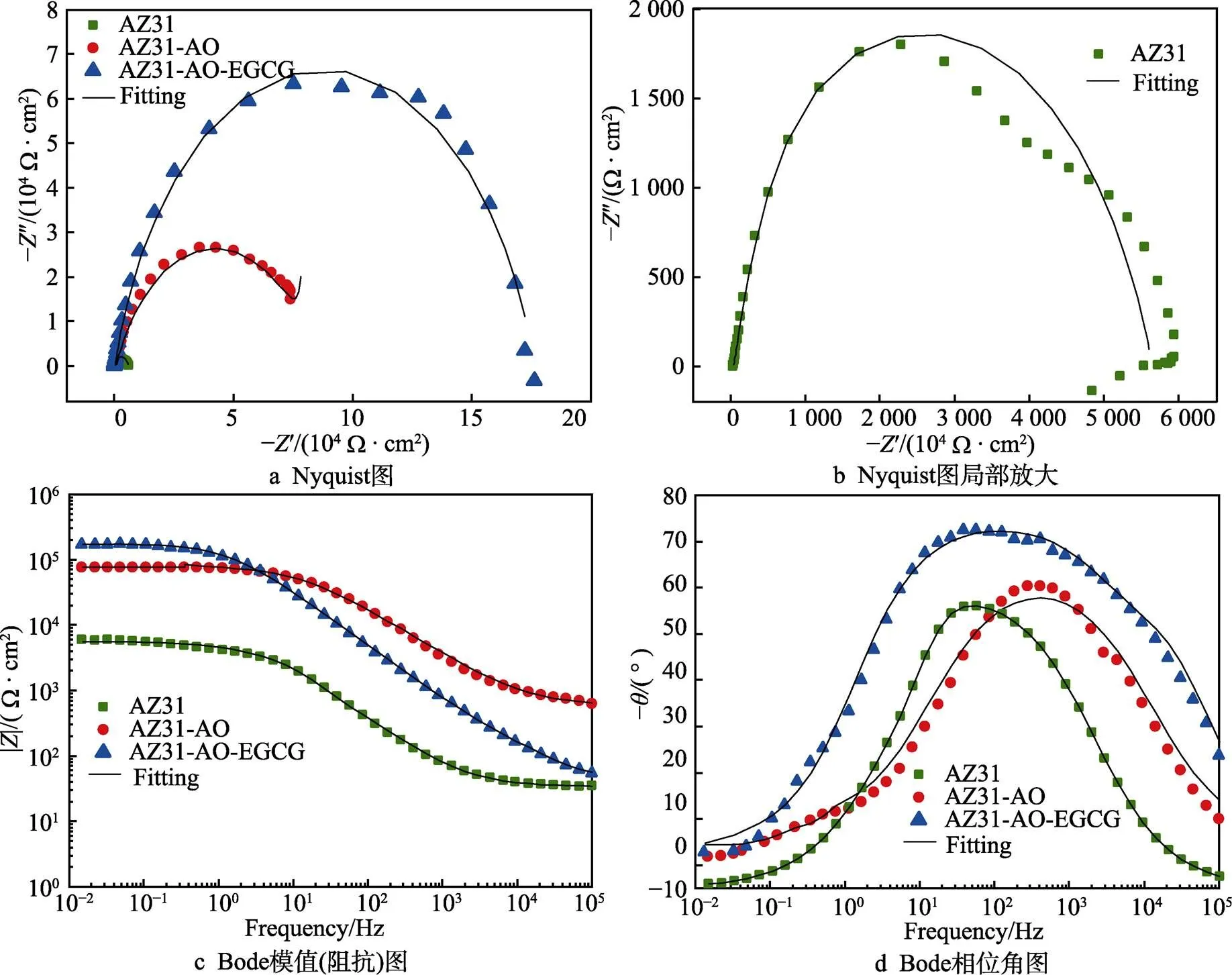
图11 AZ31、AZ31-AO、AZ31-AO-EGCG样品的EIS阻抗图谱
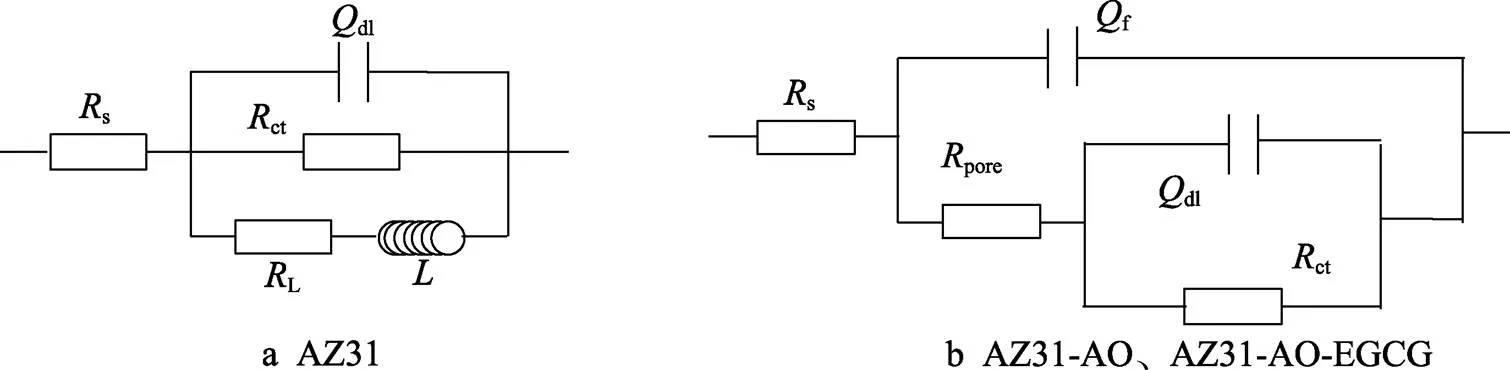
图12 等效电路
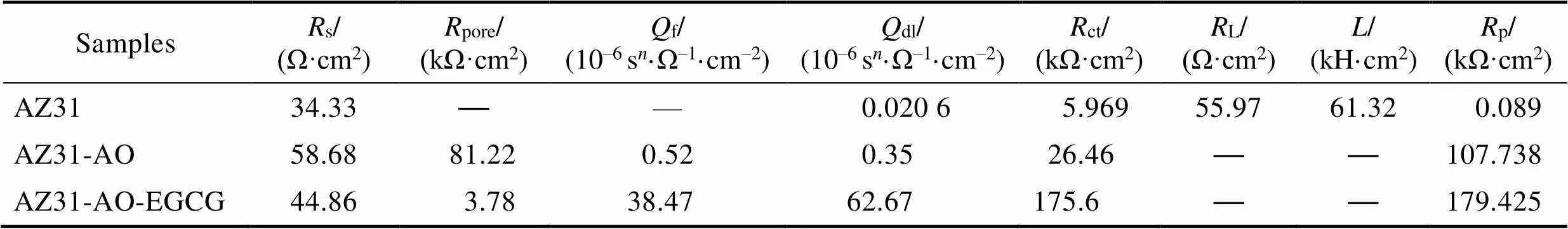
表3 AZ31、AZ31-AO和AZ31-AO-EGCG阻抗图谱拟合参数
对于AZ31:
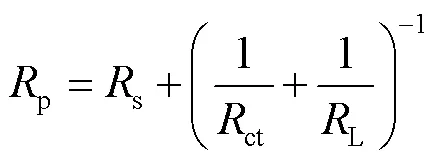
对于AZ31-AO和AZ31-AO-EGCG:
从表3的数据可以看到,AZ31-AO-EGCG的p最高,为179.425 kΩ·cm2,显著高于裸材AZ31的p(89 Ω·cm2)。p的显著增加可归因于转化层的覆盖消除了活性表面积,腐蚀过程受到有效阻碍。
2.3.3 长期浸泡试验
当镁与生理环境接触时,腐蚀反应发生并产生氢气和氢氧化镁,而生理环境中含有大量氯离子,较高浓度的氯离子,使得产生的氢氧化镁极易溶解,生成氯化镁,并产生大量OH–,从而引起环境pH值的增加。因而,溶液pH值的变化可以直接反映出样品腐蚀速率的大小。同时,镁在水溶液中的腐蚀反应产生H2,析出的氢气量也可反应腐蚀程度。因此,将AZ31、AZ31-AO和AZ31-AO-EGCG在(37±0.5) ℃的PBS中浸泡160 h后,对浸泡液pH值的变化和析出的氢气量变化进行检测,结果如图13所示。从图13a中可以看到,在浸泡初期(0~20 h),AZ31的pH值迅速从7.5升至10.5,说明其在PBS中发生了较快速的腐蚀,而AZ31-AO和AZ31-AO-EGCG样品组的pH值均只升高至9左右,说明改性后样品在浸泡初期均有效抑制了基底的快速腐蚀。随着浸泡时间从20 h增加至60 h,AZ31的pH值逐渐趋于平稳,保持在10.5左右。这说明AZ31在PBS浸泡的过程中,表面逐渐形成了腐蚀产物层,使得pH值不再发生较大的变化。AZ31-AO的pH值则在这段时间内表现出快速增长,从8.5升至10.5。这表明AZ31-AO表面的阳极氧化层只能在短期提供有效的防腐蚀功能,浸泡时间过长,阳极氧化层的保护作用丢失,使得环境pH值迅速增大,并与AZ31相当。AZ31-AO-EGCG样品组的pH值在这段时间内只从8.5升至9.5左右,这说明AO-EGCG复合层相比于单一的OA层提供了更加有效的保护,并且在后续浸泡至160 h的过程中,pH值始终保持在10左右,明显低于AZ31和AZ31- AO样品组。
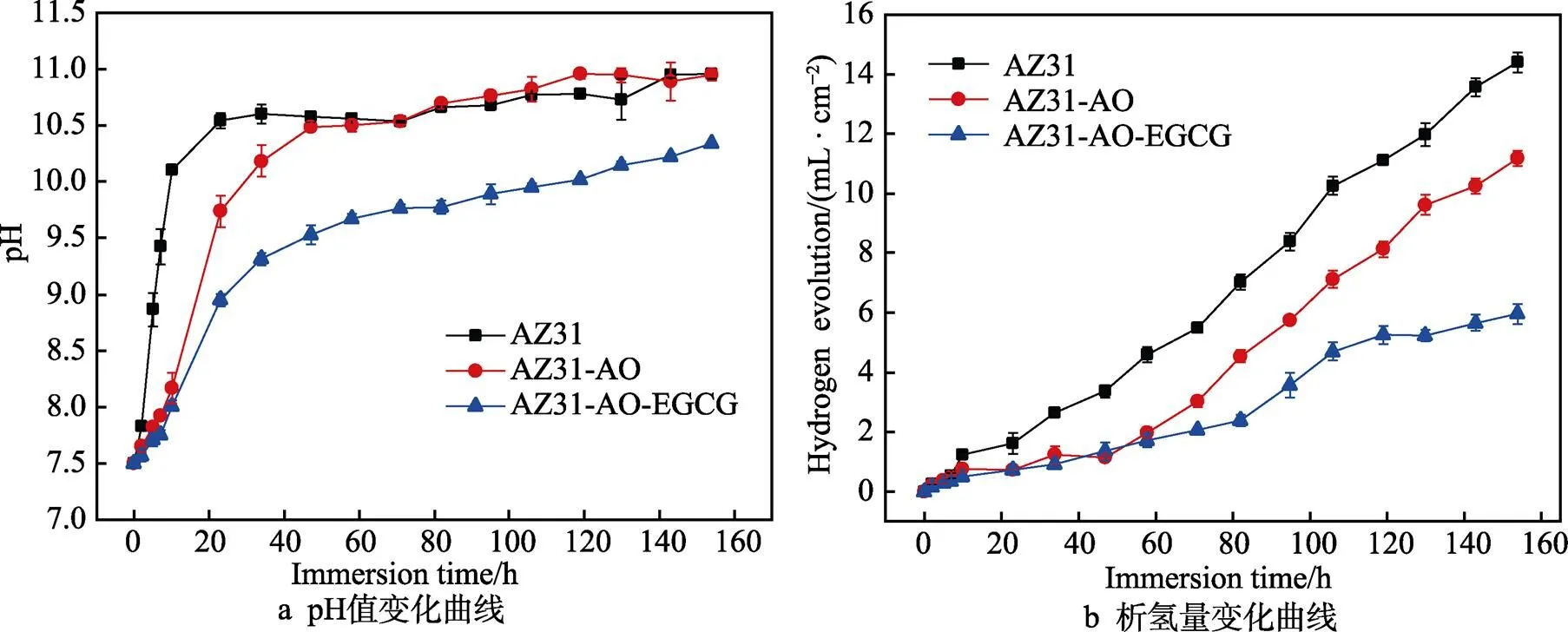
图13 AZ31、AZ31-AO和AZ31-AO-EGCG在PBS缓冲液中长期浸泡的 pH值变化曲线和析氢量变化曲线
长期浸泡析氢结果(见图13b)显示,AZ31样品在160 h内累积释放约14 mL/cm2氢气,AZ31-AO和AZ31-AO-EGCG样品组分别释放约11、6 mL/cm2氢气。在前60 h的浸泡过程中,AZ31-AO和AZ31- AO-EGCG样品组均明显抑制氢气析出,析出量控制在2 mL/cm2左右,AZ31样品的析出量在4.6 mL/cm2左右。浸泡60~160 h,AZ31-AO组的氢气析出量相较于AZ31-AO- EGCG明显增大,但该2组样品均低于裸材AZ31的析出量。该结果与pH值的浸泡变化情况相对应。长期浸泡试验结果说明,AZ31-AO- EGCG表面的改性层具有更加持久的耐腐蚀能力,EGCG转化层的复合对单一阳极氧化层的耐腐蚀能力有更好的提升。
为了更加直观地观察长期浸泡后样品的腐蚀情况,将浸泡160 h后的各组样品取出进行肉眼观察和光镜形貌观察,如图14所示。可以看到,AZ31表面出现大量的白色腐蚀产物堆积,说明其发生了较严重的腐蚀。AZ31-AO表面同样可见白色腐蚀产物,而AZ31-AO-EGCG表面显现出最少的腐蚀产物形成,且仍可见结晶产物下方的样品表面。该结果说明,AZ31-AO-EGCG可以为镁基底提供相对于单纯阳极氧化层更持久的防腐蚀能力。

图14 AZ31、AZ31-AO和AZ31-AO-EGCG样品长期浸泡后样品表面形貌
3 结论
1)通过阳极氧化与化学转化法相结合的方式,在AZ31镁合金表面制备了具有良好耐腐蚀能力的AO-EGCG复合转化层。
2)通过XRD、FTIR及XPS分析,发现阳极氧化层主要由MgO和MgSiO3组成,AZ31-AO-EGCG表面酚羟基等官能团的出现以及酚镁键合形式的出现,表明EGCG转化层能够成功生长在AO层表面。
3)电化学测试和长期浸泡试验结果表明,AZ31-AO-EGCG的自腐蚀电流密度(17.78 μA/cm2)相对于AZ31-AO明显减小,并且比AZ31减小了2个数量级。AO-EGCG复合层的阻抗值也远大于AZ31和单一的AO层。浸泡160 h后,复合层的长期耐腐蚀能力明显优于裸材和单一的阳极氧化层。
[1] ZHAO De-wei, WITTE F, LU Fa-qiang, et al. Current Status on Clinical Applications of Magnesium-Based Orthopaedic Implants: A Review from Clinical Translational Perspective[J]. Biomaterials, 2017, 112: 287-302.
[2] ZHANG Yi-feng, XU Jian-kun, RUAN Ye chun, et al. Implant-Derived Magnesium Induces Local Neuronal Production of CGRP to Improve Bone-Fracture Healing in Rats[J]. Nature Medicine, 2016, 22(10): 1160-1169.
[3] MARRELLA A, LEE T Y, LEE D H, et al. Engineering Vascularized and Innervated Bone Biomaterials for Improved Skeletal Tissue Regeneration[J]. Materials Today, 2018, 21(4): 362-376.
[4] HAN H S, LOFFREDO S, JUN I, et al. Current Status and Outlook on the Clinical Translation of Biodegradable Metals[J]. Materials Today, 2019, 23: 57-71.
[5] SEKAR P, S N, DESAI V. Recent Progress inStudies and Clinical Applications of Magnesium Based Biodegradable Implants-a Review[J]. Journal of Magnesium and Alloys, 2021, 9(4): 1147-1163.
[6] ZHAO De-wei, HUANG Shi-bo, LU Fa-qiang, et al. Vascularized Bone Grafting Fixed by Biodegradable Magnesium Screw for Treating Osteonecrosis of the Femoral Head[J]. Biomaterials, 2016, 81: 84-92.
[7] ZHOU Hang, LIANG Bing, JIANG Hai-tao, et al. Magnesium-Based Biomaterials as Emerging Agents for Bone Repair and Regeneration: From Mechanism to Application[J]. Journal of Magnesium and Alloys, 2021, 9(3): 779-804.
[8] FROST H M. The Biology of Fracture Healing. an Overview for Clinicians. Part II[J]. Clinical Orthopaedics and Related Research, 1989(248): 294-309.
[9] WAN Peng, TAN Li-li, YANG Ke. Surface Modification on Biodegradable Magnesium Alloys as Orthopedic Implant Materials to Improve the Bio-Adaptability: A Review[J]. Journal of Materials Science & Technology, 2016, 32(9): 827-834.
[10] RAHMAN M, DUTTA N K, ROY CHOUDHURY N. Magnesium Alloys with Tunable Interfaces as Bone Implant Materials[J]. Frontiers in Bioengineering and Biotechnology, 2020, 8: 564.
[11] CAI Jing-shun, CAO Fa-he, CHANG Lin-rong, et al. The Preparation and Corrosion Behaviors of MAO Coating on AZ91D with Rare Earth Conversion Precursor Film[J]. Applied Surface Science, 2011, 257(8): 3804-3811.
[12] 何知恩, 孜力汗, 刘源涛, 等. 多酚类材料的应用研究及前景展望[J]. 生命的化学, 2017, 37(6): 919-924.
HE Zhi-en, ZI Li-han, LIU Yuan-tao, et al. Application and Research Progress on Polyphenols Material[J]. Chemistry of Life, 2017, 37(6): 919-924.
[13] CHU K O, CHAN S O, PANG C P, et al. Pro-Oxidative and Antioxidative Controls and Signaling Modification of Polyphenolic Phytochemicals: Contribution to Health Promotion and Disease Prevention?[J]. Journal of Agricultural and Food Chemistry, 2014, 62(18): 4026-4038.
[14] CAZZOLA M, FERRARIS S, BOSCHETTO F, et al. Green Tea Polyphenols Coupled with a Bioactive Titanium Alloy Surface: In Vitro Characterization of Osteoinductive Behavior through a KUSA A1 Cell Study[J]. International Journal of Molecular Sciences, 2018, 19(8): 2255.
[15] HE Li-bang, DENG Dong-mei, ZHOU Xue-dong, et al. Novel Tea Polyphenol-Modified Calcium Phosphate Nanoparticle and Its Remineralization Potential[J]. Journal of Biomedical Materials Research Part B, Applied Biomaterials, 2015, 103(8): 1525-1531.
[16] SILEIKA T S, BARRETT D G, ZHANG Ran, et al. Colorless Multifunctional Coatings Inspired by Polyphenols Found in Tea, Chocolate, and Wine[J]. Angewandte Chemie (International Ed in English), 2013, 52(41): 10766-10770.
[17] EJIMA H, RICHARDSON J J, LIANG Kang, et al. One-Step Assembly of Coordination Complexes for Versatile Film and Particle Engineering[J]. Science, 2013, 341(6142): 154-157.
[18] JEON J R, KIM J H, CHANG Y S. Enzymatic Polymerization of Plant-Derived Phenols for Material-Independent and Multifunctional Coating[J]. Journal of Materials Chemistry B, 2013, 1(47): 6501-6509.
[19] KIM S, KIM D S, KANG S M. Reversible Layer- by-Layer Deposition on Solid Substrates Inspired by Mussel Byssus Cuticle[J]. Chemistry, an Asian Journal, 2014, 9(1): 63-66.
[20] XU Li-qun, PRANANTYO D, NEOH K G, et al. Tea Stains-Inspired Antifouling Coatings Based on Tannic Acid-Functionalized Agarose[J]. ACS Sustainable Chemistry & Engineering, 2017, 5(4): 3055-3062.
[21] CHEN Yu-peng, MENG Jing-xin, ZHU Zhong-peng, et al. Bio-Inspired Underwater Super Oil-Repellent Coatings for Anti-Oil Pollution[J]. Langmuir: the ACS Journal of Surfaces and Colloids, 2018, 34(21): 6063-6069.
[22] ZHANG Hao, LUO Ri-fang, LI Wen-jun, et al. Epigallocatechin Gallate (EGCG) Induced Chemical Conversion Coatings for Corrosion Protection of Biomedical MGZNMN Alloys[J]. Corrosion Science, 2015, 94: 305-315.
[23] ZHANG Hao, XIE Ling-xia, SHEN Xiao-long, et al. Catechol/Polyethyleneimine Conversion Coating with Enhanced Corrosion Protection of Magnesium Alloys: Potential Applications for Vascular Implants[J]. Journal of Materials Chemistry B, 2018, 6(43): 6936-6949.
[24] ZHANG Hao, SHEN Xiao-long, WANG Jin, et al. Multistep Instead of One-Step: A Versatile and Multifunctional Coating Platform for Biocompatible Corrosion Protection[J]. ACS Biomaterials Science & Engineering, 2019, 5(12): 6541-6556.
[25] CHEN Ying-qi, ZHANG Xuan, ZHAO Sheng, et al. In Situ Incorporation of Heparin/Bivalirudin into a Phytic Acid Coating on Biodegradable Magnesium with Improved Anticorrosion and Biocompatible Properties[J]. Journal of Materials Chemistry B, 2017, 5(22): 4162-4176.
[26] CHEN Si, ZHANG Jiang, CHEN Ying-qi, et al. Application of Phenol/Amine Copolymerized Film Modified Magnesium Alloys: Anticorrosion and Surface Biofunctionalization[J]. ACS Applied Materials & Interfaces, 2015, 7(44): 24510-24522.
[27] WANG Juan, HE Yong-hui, MAITZ M F, et al. A Surface- Eroding Poly(1, 3-trimethylene carbonate) Coating for Fully Biodegradable Magnesium-Based Stent Applications: Toward Better Biofunction, Biodegradation and Biocompatibility[J]. Acta Biomaterialia, 2013, 9(10): 8678-8689.
Corrosion Resistance of Anodic Oxidation/Polyphenol Conversion Composite Coating on Biomedical Magnesium Alloy
a,a,b,a,a
(a. College of Vanadium and Titanium, b. College of Biology and Chemical Engineering, Panzhihua University, Sichuan Panzhihua 610000, China)
Magnesium and its alloys are widely regarded as potentially revolutionary orthopaedic implant materials due to their biodegradability, good biocompatibility and ideal Young's modulus close to that of natural cortical bone. However, the clinical application of magnesium implants is limited by their high reactivity in the physiological environment. Rapid degradation of magnesium alloys in physiological environments can lead to rapid loss of implant mechanical integrity, large amounts of hydrogen, localized alkaline environments, and enrichment of corrosion products.To address these issues and develop clinically viable magnesium-based bone implants, slowing and controlling the biodegradation rate of magnesium- based bone implants is critical. The work aims to prepare an anodic oxidation/polyphenol conversion composite coating on AZ31 Mg alloy surface to solve the problems such as fast degradation and easy to cause inflammation of medical magnesium alloy in implantation environment.
In this work, an anodic oxidation/polyphenol conversion composite coating was prepared on AZ31 alloy, and its corrosion resistance and was evaluated. Anodic oxidation (OA) coating was prepared by anodization method, then a polyphenol conversion coating was prepared on the OA coating by immersing in EGCG (epigallocatechin gallate) solution, and finally the OA-EGCG composite conversion coating was obtained. The surface morphology and composition structure of the coating were analyzed by SEM, EDS, XRD, FTIR and XPS. The polarization curve, electrochemical impedance spectroscopy, and long-term immersion test were used to evaluate the corrosion resistance of the composite coating. The results showed that the main components of anodic oxide coating were MgO and MgSiO3. After the EGCG conversion coating constructed, the porous morphology of the AO coating was filled. The characteristic peaks of EGCG appeared in the FTIR spectrum, indicating the successful construction of the OA-EGCG composite coating. The fitting results of XPS high-resolution images of Mg and O elements on the AZ31-AO-EGCG showed that the EGCG was combined on the AZ31-AO surface by conversion to form an AO-EGCG composite coating. The anodic oxide coating acts as an intermediate layer, which can effectively improve the binding force of the EGCG conversion coating to the substrate. Electrochemical evaluation results showed that the corrosion current density of OA-EGCG coating was reduced about 2 orders of magnitude compared with AZ31. The arc radius of the high-frequency capacitive reactance was significantly increased, and the polarization resistance (p) obtained after the equivalent circuit simulation was 179.425 kΩ·cm2, which was much larger than that of the AZ31. After immersion for 160 h, the OA-EGCG composite coating could obviously control the increase of pH value of the solution, and significantly lower than other controls. The corrosion products formed on the AZ31-OA-EGCG was the least. The hydrogen evolution results showed that the AZ31 released about 14 mL/cm2of hydrogen within 160 hours, and the AZ31-AO and AZ31-AO-EGCG sample groups released about 11 mL/cm2and 6 mL/cm2of hydrogen, respectively. This result corresponded to the immersion changes in pH. By combining the anodization and the polyphenol conversion coating, the corrosion resistance of the single anodized coating was improved, and the bonding force of the single polyphenol coating was improved.
The anodic oxidation/tea polyphenol composite coating is successfully prepared on the AZ31 Mg alloy surface by anodic oxidation and immersion methods, which significantly improves the corrosion resistance of the magnesium substrate. The selected EGCG source is green, low in price, and has multiple functions such as anti-oxidation and anti-inflammatory. This study provides a new solution for the surface modification of medical magnesium alloys.
magnesium alloy; biomedical material; anodic oxidation; EGCG; corrosion resistance
TG174.4
A
1001-3660(2023)01-0196-10
10.16490/j.cnki.issn.1001-3660.2023.01.020
2021–11–11;
2022–03–21
2021-11-11;
2022-03-21
国家自然科学基金(52101286);四川省自然科学基金项目(2022NSFSC2011);国家级大学生创新创业训练计划项目(202011360001)
The National Natural Science Foundation of China (52101286); Natural Science Foundation of Sichuan Province (2022NSFSC2011); National College Student Innovation and Entrepreneurship Training Program (202011360001)
李浩(2000—),男,主要研究方向为镁合金表面改性。
LI Hao (2000-), Male, Research focus: surface modification of magnesium.
张皓(1991—),女,博士,讲师,主要研究方向为医用材料表面改性。
ZHANG Hao (1991-), Female, Doctor, Lecturer, Research focus: surface modification of biological materials.
李浩, 张皓, 申孝龙, 等. 医用镁合金表面阳极氧化/茶多酚复合转化层耐腐蚀性能研究[J]. 表面技术, 2023, 52(1): 196-205.
LI Hao, ZHANG Hao, SHEN Xiao-long, et al. Corrosion Resistance of Anodic Oxidation/Polyphenol Conversion Composite Coating on Biomedical Magnesium Alloy[J]. Surface Technology, 2023, 52(1): 196-205.
责任编辑:刘世忠

