瞬时受体电位锚蛋白亚型1受体在远端创伤预处理保护心肌缺血/再灌注损伤中的作用
宋美先,吴 云,张 野
(安徽医科大学第二附属医院麻醉与围术期医学科,安徽医科大学麻醉与围术期医学安徽普通高校重点实验室,安徽 合肥 230601)
缺血性心脏病已成为全球致死的首要原因,血流再灌注治疗是拯救濒临梗死心肌的最有效方法,而减少血流恢复后存活心肌的继发性损伤仍然是至今难以攻克的难题[1]。研究表明,腹部浅表手术切口的伤害性刺激对心肌缺血/再灌注损伤具有保护作用,这种心肌保护策略被称为远端创伤预处理(RPCT)[2]。RPCT具体的分子机制尚未明确,可能与皮肤痛觉信号的传递相关,因此,有必要研究疼痛信号相关的受体TRPA1与RPCT之间的关联。
瞬时受体电位锚蛋白亚型1(transient receptor potential ankyrin 1,TRPA1)是机体感受伤害性刺激的主要感受器,针对外科手术切皮等伤害性刺激,TRPA1受体抑制剂可以从源头处阻断痛觉信号的传递,有望成为新型镇痛药物[3]。然而,除了调控痛觉信号,TRPA1受体同样在心肌细胞中表达[4]。因此,明确TRPA1受体能否介导RPCT的心肌保护效应及其相关机制,将有利于提高临床镇痛过程中的心血管安全性。越来越多的证据表明,ALDH2是心脏保护作用的关键下游酶,ALDH2过表达可通过减少4-HNE的含量改善心肌缺血/再灌注损伤[5]。但RPCT的心肌保护作用是否与ALDH2的活性和表达相关,目前尚不清楚。本研究旨在探讨TRPA1能否介导远端创伤预处理的心肌保护作用以及其对心脏组织ALDH2的影响。
1 材料
1.1 动物健康♂ SD大鼠购于安徽医科大学实验中心,体质量(250~300) g,实验动物合格证号为:SYXK(皖)2017-006。大鼠被饲养在清洁级动物房中,饮食水充足,环境温度设置为(22 ± 1) ℃,湿度设置为(40 ± 15)%,昼夜周期为12/12 h。
1.2 主要试剂和仪器TRPA1抑制剂(TCS,货号5861528)购自美国MCE公司;氯化三苯基四氮唑(TTC)和伊文思蓝均购自美国Sigma公司;TUNEL染色试剂盒购自瑞士Roche公司;ALDH2活性试剂盒购自美国Abcam公司;组织裂解液、蛋白酶抑制剂和蛋白定量试剂盒等均购自碧云天科技研究所;兔抗ALDH2(DF6358)购自中国Affinity Biosciences公司;兔抗4-HNE(ab46545)、兔抗GAPDH(ab9485)均购自美国Abcam公司;山羊抗兔二抗购自美国Thermo公司。大鼠呼吸机购自成都泰盟公司;血流动力学数据采集系统购于澳大利亚AD公司;电泳仪购自美国Bio-RAD公司。
2 方法
2.1 心肌缺血/再灌注模型和远端创伤预处理模型大鼠腹腔注射3%戊巴比妥钠50 mg·kg-1,待其充分麻醉后放在保温垫上。分离颈部肌肉,切开气管,连接动物呼吸机。根据大鼠胸廓起伏程度设置呼吸频率约为65~70次/min,潮气量约为20~30 mL·kg-1。右颈总动脉和右颈内静脉置管,用于监测血流动力学及给药。在左侧胸部平腋下肋间用撑开器撑开胸腔,撕开心包膜后显露出心脏。用6-0带针线在左心耳下缘进针,从肺动脉圆锥旁出针。随后将结扎线的两端依次穿过圆形橡胶垫和自制的阻断器,心肌缺血时将血管钳向下推移,使阻断器和圆形橡胶垫压向心肌表面并夹紧,即可压迫冠状动脉致血流中断,松开血管钳即可解除压迫恢复血流。若MI/R模型建立成功,压迫冠状动脉后则可观察到心尖组织变为苍白或暗紫色,同时,心电图ST段明显抬高,解除压迫后再灌注的心尖组织变为红润。大鼠远端创伤预处理模型参照文献[6],即在大鼠腹部中线水平,用手术刀划开皮肤,做一长度为4 cm的横行切口。
2.2 实验分组大鼠随机分为5组(n=10):假手术组(Sham组)、模型组(IR组)、远端创伤预处理组(RPCT组)、TRPA1抑制剂+远端创伤预处理组(TCS+RPCT组)和TRPA1抑制剂组(TCS组)。Sham组:仅穿线,不进行缺血/再灌注;IR组:阻断冠状动脉缺血30 min后再灌注120 min;RPCT组:缺血前15 min于腹部正中切开腹壁4 cm,随后建立缺血/再灌注模型;TCS+RPCT组:远端创伤预处理前 10 min静脉注射TCS 1 mg·kg-1,其余处理同RPCT组;TCS组:缺血前25 min静脉注射TCS 1 mg·kg-1,随后进行缺血/再灌注损伤。
2.3 血流动力学监测颈总动脉插管成功后连接PowerLab系统,监测血流动力学,于结扎线缝好后平衡30 min(基础值)、缺血15 min和再灌注完成3个时间点,记录平均动脉压(MAP)及心率(HR),并计算血压心率乘积(RPP)。
2.4 心肌梗死面积的测量再灌注完成后,阻断冠状动脉血流,将3%伊文思蓝约2 mL从颈内静脉快速推入,当大鼠四肢皮肤染为蓝色时,立即摘除心脏,剪去心房和右心室。将左心室结扎线以下的心肌组织切成5等分的心肌切片,随后把切片置于1%TTC溶液里,37 ℃孵育20 min后以组织固定液固定。24 h后可观察到缺血危险区中的活组织被染成红色,梗死组织被染为白色,非缺血区被染成蓝色。用刀片依次切下红色、白色和蓝色区域并称质量,得到梗死区质量(IS,白色区)、缺血区质量(AAR,白色区+红色区)以及结扎线下左心室质量(LV,白色区+红色区+蓝色区),并求出IS/AAR及AAR/LV比值。
2.5 TUNEL染色再灌注结束后取下大鼠心脏,PBS冲洗后进行固定、蔗糖梯度脱水、OCT包埋,随后进行冷冻切片。切片在室温复温后,用PBS洗去包埋剂,加入透膜液通透2 min。再次用PBS洗去透膜液,滴加TUNEL反应液,置于37 ℃暗湿盒中孵育1 h。切片以PBS清洗后加入DAPI封片,荧光显微镜下观察,计算视野中阳性细胞数/总细胞数。
2.6 ALDH2活性检测再灌注完成后留取心脏组织,采用ALDH2活性检测试剂盒测定ALDH2活性。按照说明书步骤进行操作,加入的蛋白质样品浓度为0.1 g·L-1。最后避光孵育30 min,测量450 nm处的吸光度值。结果将Sham组ALDH2活性标准化为1,计算其余组ALDH2的相对活性。
2.7 Western blot取左心室心尖组织,加入RIPA裂解液,放在研磨器中研磨,离心后得到组织总蛋白。获取的蛋白经蛋白浓度测定后按相应比例加入上样缓冲液,100 ℃金属浴10 min后取30 μg蛋白进行凝胶电泳。随后进行切胶、转膜,把膜放入快速封闭液中封闭15 min。按蛋白分子量裁出相应蛋白条带,然后分别放入GAPDH(1 ∶2 000)、ALDH2(1 ∶1 000)和4-HNE(1 ∶2 000)的抗体稀释液中,4 ℃摇床孵育过夜。TBST洗膜后加入二抗(1 ∶10 000)稀释液,室温孵育1 h。再次洗膜后滴加显影剂反应1 min,最后在成像系统上显出蛋白条带。
Tab 1 Hemodynamic data in rats
3 结果
3.1 血流动力学数据比较5组大鼠MAP、HR和RPP的基线值间无明显差异(P>0.05)。相比于Sham组,其余4组的MAP、HR和RPP在缺血15 min和再灌注完成时刻均下降(P<0.05);与IR组相比,RPCT组在缺血15 min和再灌注完成时刻的MAP、HR和RPP均升高(P<0.05);而IR组、TCS+RPCT组和TCS组间的血流动力学无明显差异(P>0.05)。见Tab 1。
3.2 心肌梗死面积的比较5组大鼠的AAR/LV比值间无明显差异(P<0.05),说明结扎位置基本一致。与Sham组相比,其余各组出现白色梗死区;与IR组相比,RPCT组的IS/AAR百分比明显减小(P<0.05);与RPCT组相比,TCS+RPCT组的IS/AAR百分比明显增加(P<0.05)。结果表明,RPCT能有效地降低大鼠MI/R损伤后的心肌梗死面积,而TRPA1抑制剂消除了RPCT 的保护作用。见Fig 1。
3.3 心肌细胞凋亡水平的比较相比于Sham组,其余4组心肌细胞凋亡水平明显增加(P<0.05);RPCT组相比于IR组,心肌凋亡细胞减少(P<0.05);与RPCT组相比,TCS+RPCT组的心肌凋亡细胞增加(P<0.05),说明预先给予TRPA1抑制剂使远端创伤预处理减少心肌细胞凋亡的作用降低。见Fig 2,3。
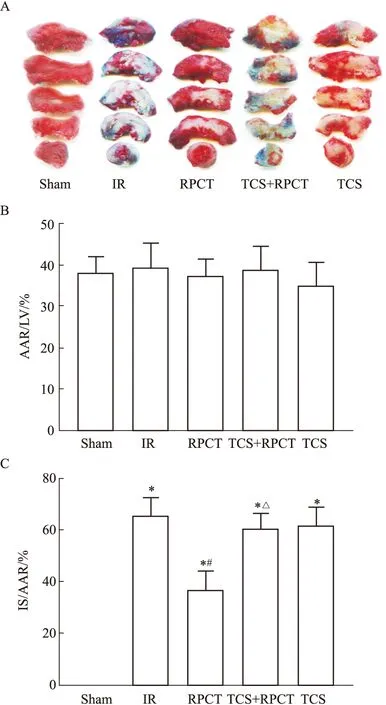
Fig 1 Myocardial infarct size in rats A:Representative images for ischemic risk area for each experimental group.Infarcted tissue remains unstained (white) while viable tissue is stained red.B:Area at risk/left ventricle.C:The myocardial infarction area / ischemic risk area.*P<0.05 vs sham;#P<0.05 vs IR;△P<0.05 vs RPCT.
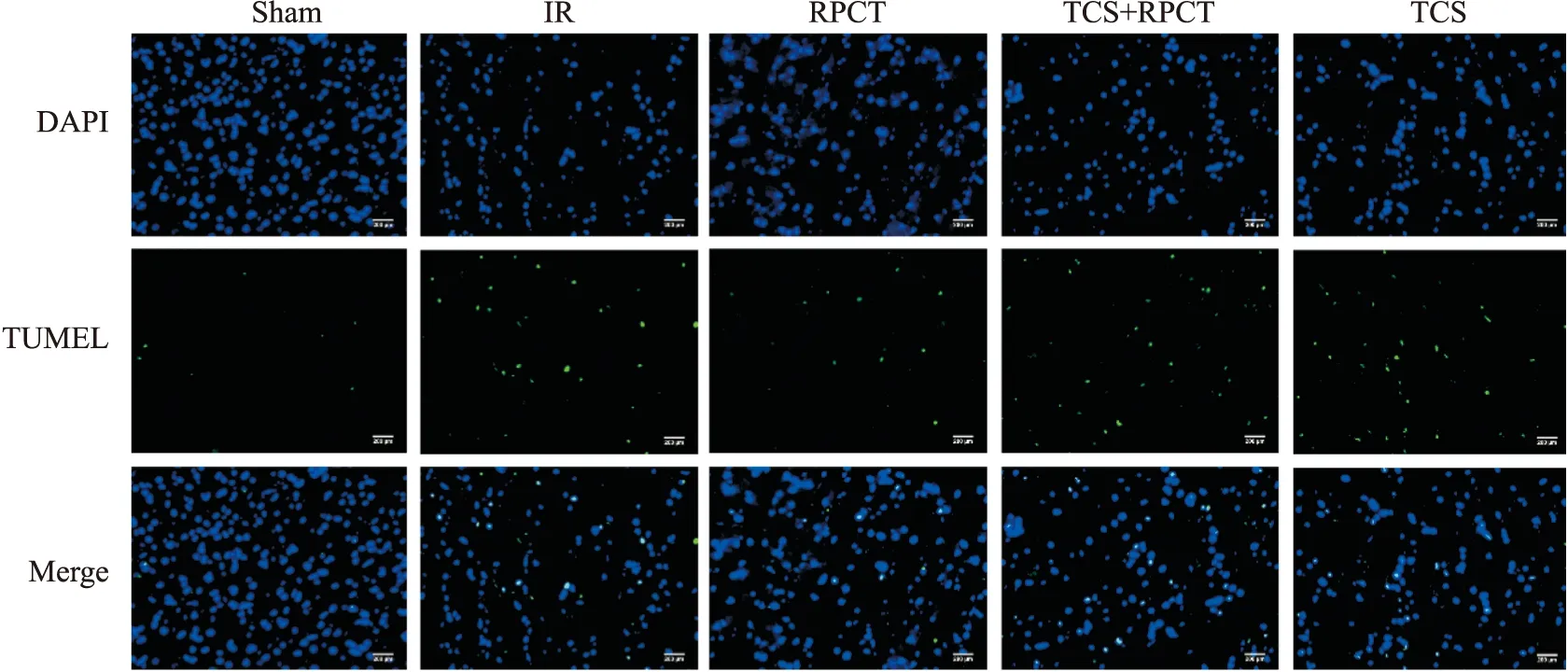
Fig 2 Representative images of TUNEL staining in each group
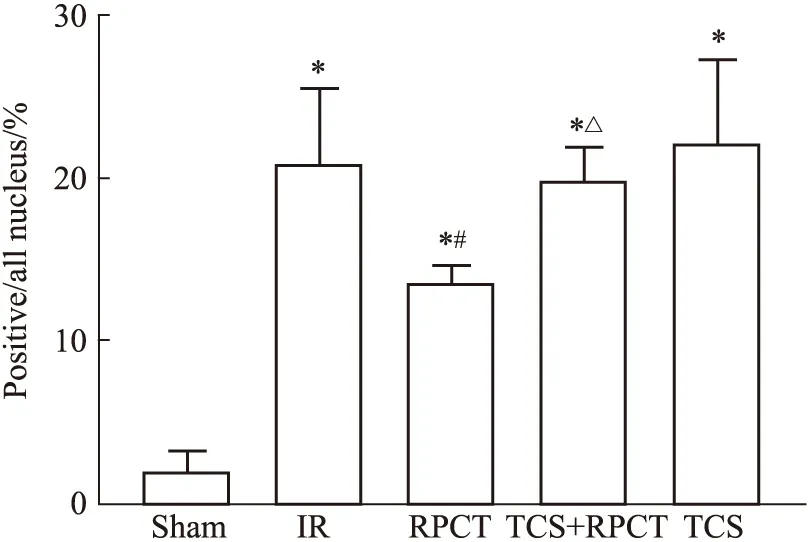
Fig 3 The statistical results of TUNEL staining *P<0.05 vs sham;#P<0.05 vs IR;△P<0.05 vs RPCT.
3.4 ALDH2活性和蛋白表达以及4-HNE蛋白表达情况与Sham组比较,IR组的ALDH2活性和蛋白表达降低,4-HNE含量增加(P<0.05);与IR组比较,RPCT组的ALDH2活性和表达升高,4-HNE含量减少(P<0.05);相比于RPCT组,TCS+RPCT组的ALDH2活性和表达降低,4-HNE含量增加(P<0.05),表明抑制TRPA1受体减弱了远端创伤预处理升高心肌组织ALDH2活性和蛋白表达的作用。见Fig 4,5。
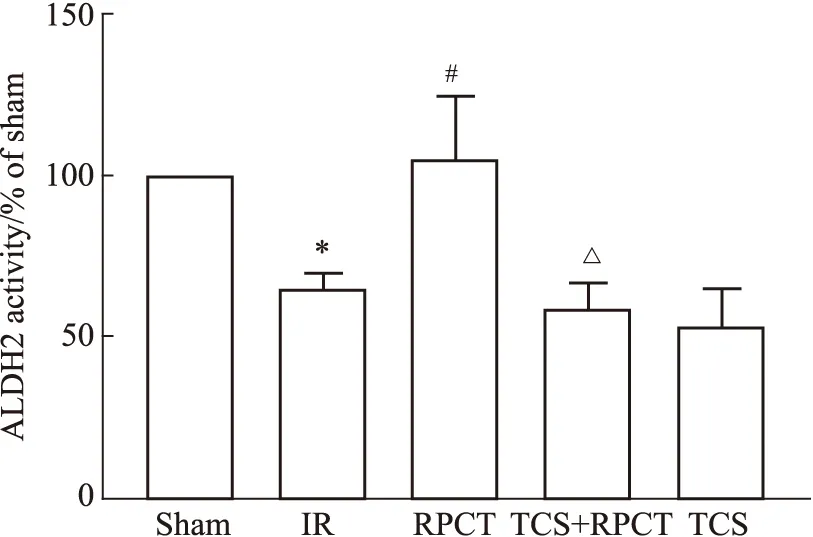
Fig 4 ALDH2 activity in each group n=6)*P<0.05 vs sham;#P<0.05 vs IR;△P<0.05 vs RPCT.
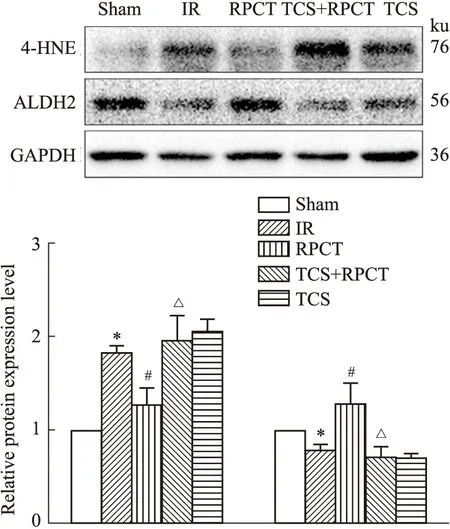
Fig 5 The protein expression of 4-HNE and ALDH2 *P<0.05 vs sham;#P<0.05 vs IR;△P<0.05 vs RPCT
4 讨论
远端创伤预处理是一种有效的心脏保护方法,由Ren等[7]于2004年首次报道,并在小鼠和大鼠心肌缺血/再灌注模型中得到证实[8-9]。本研究参照文献[6]构建大鼠远端创伤预处理模型和心肌缺血/再灌注模型。结果观察到心肌缺血时心尖组织明显发绀,心电图ST段明显抬高。而且,RPCT组较IR组的IS/AAR百分比、心肌细胞凋亡水平明显减少,证明远端创伤预处理降低了心肌缺血/再灌注损伤。
TRPA1受体属于瞬时受体电位通道超家族,是细胞膜上的一种钙通透性非选择性阳离子通道,作为机体感受温度、化学以及机械等伤害性刺激的主要感受器[10]。研究证实,心肌细胞中存在TRPA1,且TRPA1的激活介导了阿片类药物的心肌保护作用[4]。本课题组前期研究发现缺血前于大鼠腹部涂抹冬青油(水杨酸甲酯,TRPA1激动剂)软膏能够减少心肌缺血/再灌注损伤[11]。这些结果强烈提示TRPA1在介导心肌保护作用中发挥着关键作用。TCS 5861528是一种选择性TRPA1通道拮抗剂,可抑制AITC(TRPA1激活剂)诱导的钙内流[12],被广泛用于研究TRPA1功能实验中。在本实验中,为了研究TRPA1是否参与远端创伤预处理对大鼠MI/R的保护作用,进行了TCS+ RPCT组实验。结果发现,与RPCT组比较,TCS+RPCT组可明显增加IS/AAR比值和心肌细胞凋亡水平,说明TRPA1受体拮抗剂TCS可消除远端创伤预处理的心肌保护效应,提示TRPA1受体在远端创伤预处理降低大鼠MI/R损伤的过程中发挥重要作用。
缺血心肌血流恢复后,生成活性氧簇(ROS),并通过脂质过氧化反应生成大量毒性醛如4-HNE,诱导细胞损伤[13]。ALDH2是醛脱氢酶家族成员,可以将脂质过氧化过程中产生的毒性醛分解为无毒的羧酸,降低细胞毒性和氧化损伤[14]。大量数据表明,ALDH2的活性和表达增加可以增强其代谢4-HNE的能力,导致4-HNE的含量减少,从而减轻心肌缺血/再灌注损伤[5,15]。Chaudhuri等[16]发现TRPA1可通过钙调激酶信号通路激活核因子E2相关因子(Nrf2),Nrf2已被证实可调控ALDH2的表达[17]。因此,我们推测药物抑制TRPA1受体可能会影响ALDH2的活性和表达。本研究观察到心肌经历缺血/再灌注损伤后ALDH2活性和表达下降,毒性物质4-HNE表达升高,而远端创伤预处理可上调ALDH2的活性和表达,减少4-HNE含量。但当给予TRPA1受体特异性拮抗剂后,远端创伤预处理上调ALDH2活性和表达的作用消失。该结果提示TRPA1受体可能是通过调控ALDH2活性和表达,影响4-HNE含量,从而介导了远端创伤预处理对大鼠MI/R损伤的保护作用。
目前,关于TRPA1的研究主要集中在神经源性炎症反应、慢性疼痛治疗方面,TRPA1抑制剂未来有望成为新的临床镇痛药物[3,18]。研究发现远端的疼痛刺激能够对缺血心肌产生保护作用,这说明疼痛信号通路与心脏保护之间存在关联[2]。因此,在开发直接阻断TRPA1通道的临床用非麻醉性止痛药之前,需考虑TRPA1在介导特异性心脏保护和一般器官保护方面的贡献。本研究提示TRPA1受体在心肌保护中具有重要作用,这表明如果在围术期通过阻断TRPA1进行镇痛治疗,将可能对缺血性心脏病患者或是行心脏手术患者带来安全隐患。
综上所述,远端创伤预处理可减轻大鼠心肌缺血/再灌注损伤,而药物拮抗TRPA1受体阻断了远端创伤预处理的心肌保护作用,其机制可能与调控ALDH2活性和表达,影响4-HNE含量有关。

