改性镍铁渣吸附剂对Cr(VI)吸附性能的影响及机理分析
陆 艳,刘 钦,罗中秋,周新涛,赵晓腾,兰 雄
(昆明理工大学化学工程学院,昆明 650500)
0 引 言
随着工业快速发展,人类生产活动频繁,导致许多污染物进入自然环境,增加了环境质量负荷,影响周边生态系统的稳定性,威胁人类健康[1-2]。重金属因来源广、毒性大、持续时间长、不可降解、易生物累积等特点而受到广泛关注[3]。合金制造、电镀、纺织、电子等行业会产生大量的含铬废水,铬作为一种强毒性物质会对土壤、水环境和人类健康造成极其严重的危害[4-6]。因此,对铬进行有效净化处理迫在眉睫。目前水体重金属铬污染的治理方法主要有离子交换[7-8]、膜分离[9-11]、化学沉淀[12]、吸附[13]等。离子交换法去除率较高但只能在低浓度下有效去除铬且操作成本昂贵[14-16];化学沉淀法会产生大量污泥,容易造成二次污染[17];吸附法因其处理效果好、适应范围广、吸附质便于回收利用、吸附剂来源广泛等优点,在重金属处理中有巨大优势[18-21]。吸附法处理效果主要取决于所用的吸附剂,因此开发高效、低成本、可再生的吸附剂是目前吸附法处理铬废水的重要研究课题。目前,有学者利用四硅酸四乙酯、四乙氧基硅烷等纯物质制备功能性介孔二氧化硅,对重金属进行吸附处理[22-25],但其制备成本高且吸附容量小。寻找合适硅源以制备高吸附容量二氧化硅吸附剂成为重要研究方向。
镍铁渣是冶炼镍铁合金过程中形成的固体废渣,据统计,每生产1 t镍将产生约14 t的镍铁渣[26],其主要化学组成为SiO2、MgO、Fe2O3、CaO、Al2O3,其中SiO2含量高达55%(质量分数)[27]。目前对镍铁渣的主要处理方式仍为堆存处理[28-29],少量资源化利用主要为镁的提取回收,对SiO2利用极少。SiO2因表面积高和机械强度高而在吸附领域具有广阔的应用前景。基于此,以镍铁渣为低廉硅源,通过硝酸酸浸提高镍铁渣中镁橄榄石活性,制备无定形SiO2,同时利用表面活性剂将疏水官能团引入,改变其表面性能和结构,提高对Cr(VI)的吸附能力,并通过批量吸附试验研究不同因素对吸附重金属Cr(VI)的影响。采用XRD、BET、SEM-EDS、FTIR、XPS等测试手段对改性吸附剂进行表征分析,确定其吸附机理。
1 实 验
1.1 原料与试剂
所用原料为电炉镍铁渣(ferronickel slag, FS),取自广西北海某镍业责任有限公司,其化学组成如表1所示。十六烷基三甲基溴化铵(C19H42NBr, CTAB)、十二烷基硫酸钠(CH3(CH2)11OSO3Na, SDS)、聚乙二醇-6000(HO(CH2CH2O)nH, PEG6000)、重铬酸钾(K2Cr2O7)、硝酸(HNO3)、氢氧化钠(NaOH)、盐酸(HCl)购买于天津市风船化学试剂科技有限公司。

表1 镍铁渣的主要化学组成Table 1 Main chemical composition of ferronickel slag
1.2 改性FS制备
将FS置于80 ℃干燥箱中干燥24 h,用滚筒式球磨机粉磨2 h后,用48 μm筛筛分,得到FS粉末;在烧杯中加入100 mL 4 mol/L硝酸,再加入0.6 g阳离子表面活性剂,升高温度到40 ℃,搅拌溶解,即为改性混合液;将3 g FS粉末加入改性混合液中,在油浴锅中加热搅拌,冷凝回流状态下90 ℃反应24 h,过滤并洗涤滤渣至中性,烘干即得到改性FS粉末吸附剂。
1.3 批量吸附试验
用1 000 mL容量瓶溶解2.829 g K2Cr2O7配制1 000 mg/L Cr(VI)溶液,通过稀释获得不同浓度梯度以便于下一步吸附试验。将100 mg吸附剂加入到装有100 mL 100 mg/L Cr(VI)溶液的烧瓶中,在温度为25 ℃、振幅为160 r/min的振荡器中进行振荡吸附。考察吸附时间(0~3 h)、pH值(1~7)和Cr(VI)浓度(60~200 mg/L)对吸附过程的影响。溶液pH值通过添加0.1 mol/L HCl和0.1 mol/L NaOH溶液进行调节。
根据二苯碳酰二肼分光光度法测定滤液中Cr(VI)的浓度。Cr(VI)去除率(ω)和吸附容量(Qt)根据式(1)、式(2)计算[30]。
ω=(C0-Ct)/C0×100%
(1)
Qt=(C0-Ct)V/m
(2)
式中:C0和Ct分别为吸附初始时刻和t时刻的Cr(VI)浓度,C0为100 mg/L;V为溶液的体积,L;m为吸附剂质量,g。每个方案进行3组平行试验,相关图中的误差线代表数据的标准偏差。
1.4 测试与表征
使用德国Bruker D8 Advance型X射线衍射仪(XRD)分析吸附剂晶体结构及组成,扫描角度(2θ)为10°~80°。利用美国Micromeritics ASAP 2020气体吸附仪(BET)分析氮气吸附-脱附曲线,测得吸附剂的比表面积、孔径分布和孔容等参数,脱气环境温度为200 ℃,最大脱气持续时间为4 h。采用日本Hitachi S-4800场发射扫描电子显微镜(FTSEM)对原料和改性FS粉末的微观形貌进行分析。使用德国Bruker Vertex 80V傅里叶变换红外光谱(FT-IR)在400~4 000 cm-1的范围内分析样品所含基团种类,确定其化学组成。通过美国赛默飞VG MULTILAB 2000型X射线光电子能谱(XPS)测定样品表面化学性质。
2 结果与讨论
2.1 吸附剂表征分析
图1为FS改性前后的XRD谱。如图1所示,原料FS主要矿物相为镁橄榄石(Mg2SiO4)。经酸化和CTAB联合改性后镁橄榄石特征峰消失,在23°左右出现了二氧化硅的无定形峰,说明FS经酸化-CTAB联合改性后,原料中的硅质组分转化为了无定形SiO2。
图2为FS改性前后的N2吸附-脱附等温线。由图2可知,原料FS呈现Ⅲ型等温线,没有明显的滞后回线,表明其对N2的吸附能力较低,与N2的相关力较弱。FS改性后显示出了与典型的IV等温线和H3磁滞回线耦合的相似之处,即FS改性后为介孔结构。表2对FS改性前后的比表面积和孔结构参数进行了对比,FS比表面积从11.64 m2/g增加到180.60 m2/g,得到较大提升,根据扫描电子显微镜照片可明显看出改性混合液将FS紧实的块状镁橄榄石结构转变为了松散的无定形二氧化硅,其高比表面积为Cr(IV)吸附提供了大量吸附位点。
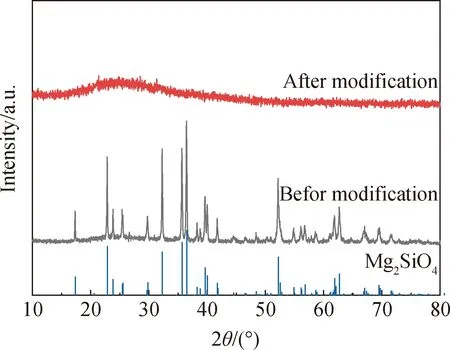
图1 FS改性前后的XRD谱Fig.1 XRD patterns of FS before and after modification
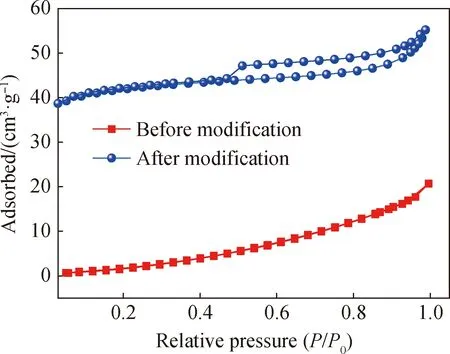
图2 FS改性前后的N2吸附-脱附等温线Fig.2 N2 adsorption-desorption isotherms of FS before and after modification

表2 FS改性前后的比表面积与孔隙结构Table 2 Specific surface area and pore structure of FS before and after modification
图3为FS改性前后的SEM照片和EDS能谱。由图3可以观察到:原料FS以结晶相为主,形态为不规则的块状结构;改性后FS主要由1 μm左右的分散板状颗粒组成,颗粒之间出现团聚现象,这是因为改性后FS中的镁橄榄石由原来的稳定状态转变为活性较大的无定形二氧化硅,此外CTAB使颗粒表面极性增加,彼此之间易发生反应,团聚在一起。从EDS分析可看出Mg含量急剧下降,C含量有所增加,N含量也有所增加,这是因为镁橄榄石在酸性条件下溶解,形成了无定形二氧化硅,这与XRD分析一致,而CTAB表面活性剂附着在二氧化硅表面导致其C含量明显增加。
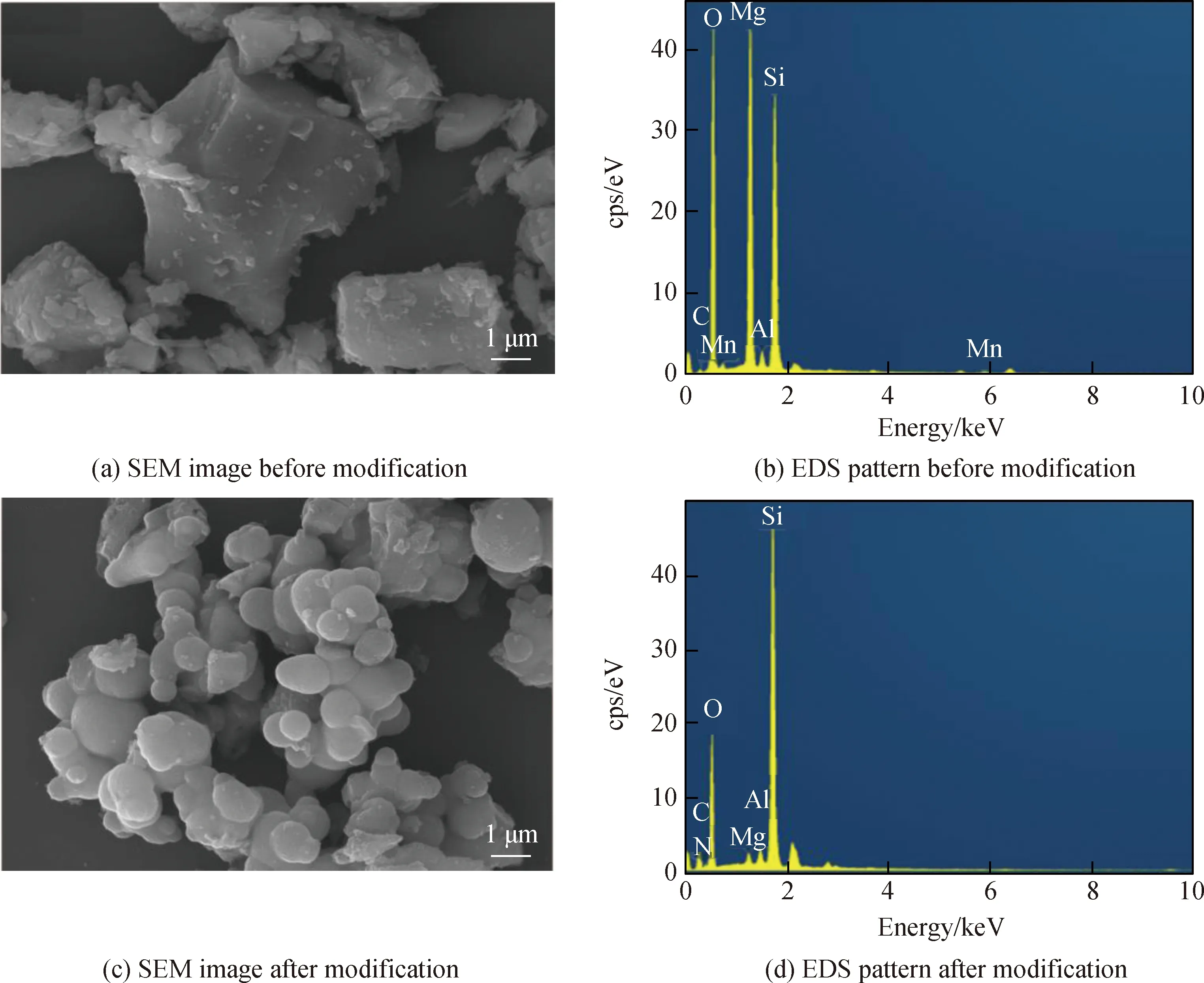
图3 FS改性前后的SEM照片和EDS能谱Fig.3 SEM images and EDS patterns of FS before and after modification
2.2 Cr(VI)的吸附性能研究
2.2.1 表面活性剂对Cr(VI)吸附效果的影响
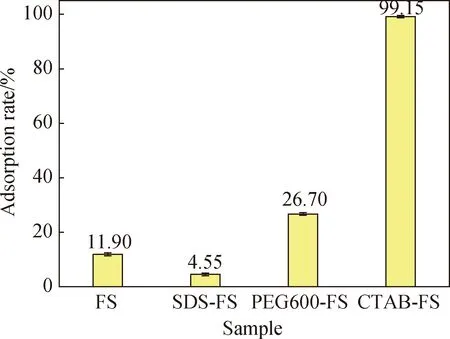
图4 CTAB、SDS和PEG6000表面活性剂对 Cr(VI)吸附效果的影响Fig.4 Effects of CTAB, SDS and PEG6000 surfactants on Cr(VI) adsorption
在Cr(VI)溶液浓度为100 mg/L、初始pH值为2、接触时间为2 h条件下,考察三种不同离子种类的表面活性剂(阳离子表面活性剂CTAB、阴离子表面活性剂SDS、非离子表面活性剂PEG6000)对酸化FS吸附Cr(VI)效果的影响,结果见图4。由图4可知,采用阴离子表面活性剂SDS制备的吸附剂对Cr(VI)的吸附效果最差,这是因为Cr(VI)在水体中主要以含氧阴离子形式存在,阴离子表面活性剂对同属于阴离子的铬酸根离子具有排斥作用。非离子表面活性剂PEG6000改性FS的吸附效果有所提高,但提高效果并不理想,效果的提高归因于表面活性剂对SiO2有分散作用,增加了吸附位点。CTAB改性的FS吸附效果最好,高达99.15%,由于CTAB表面活性剂属于阳离子表面活性剂,改性过程附着在酸化FS产生的无定形二氧化硅表面,对溶液中的铬酸根离子具有静电吸引作用,因此吸附效果得到明显提高。
2.2.2 CTAB掺量对Cr(VI)吸附效果的影响
在初始Cr(VI)浓度为100 mg/L、初始pH值为2、接触时间为2 h条件下,研究CTAB掺量对Cr(VI)吸附效果的影响(见图5)。从图5中可以看出,随着CTAB掺量增加,对Cr(VI)的去除率也越来越大,当CTAB含量为20%(质量分数)时,Cr(VI)去除率达最大,为99.15%。这可能归因于随着CTAB含量增加,附着在SiO2表面的CTAB增多,吸附剂所带极性增强,对铬酸根离子的静电吸引力增大,吸附效果得到加强。此外,CTAB可增加SiO2分散性,随着CTAB含量增加,吸附剂比表面积增大,吸附位点增多,吸附效果得到大幅度提升。
2.2.3 吸附剂掺量对Cr(VI)吸附效果的影响
吸附剂用量是影响吸附过程的重要因素,吸附剂用量决定了恒定离子浓度的吸附剂容量。在Cr(VI)浓度为100 mg/L、初始pH值为2、接触时间为2 h条件下,考察吸附剂掺量(0.05~0.30 g)对Cr(VI)吸附效果的影响,结果见图6。由图6可知,随着吸附剂掺量增加,Cr(VI)吸附率从40.15%迅速增加到99.15%。这是因为随着吸附剂质量增加,吸附位点增加,吸附剂与Cr(VI)接触面积增加,增大了Cr(VI)与吸附剂结合的可能性。然而,当吸附剂掺量较高时,吸附率基本保持不变,吸附容量却从40.15 mg/g降低到了16.67mg/g,这是因为吸附剂活性位点饱和度降低,吸附剂颗粒易团聚,从而导致可用表面积减少和扩散路径长度增加。
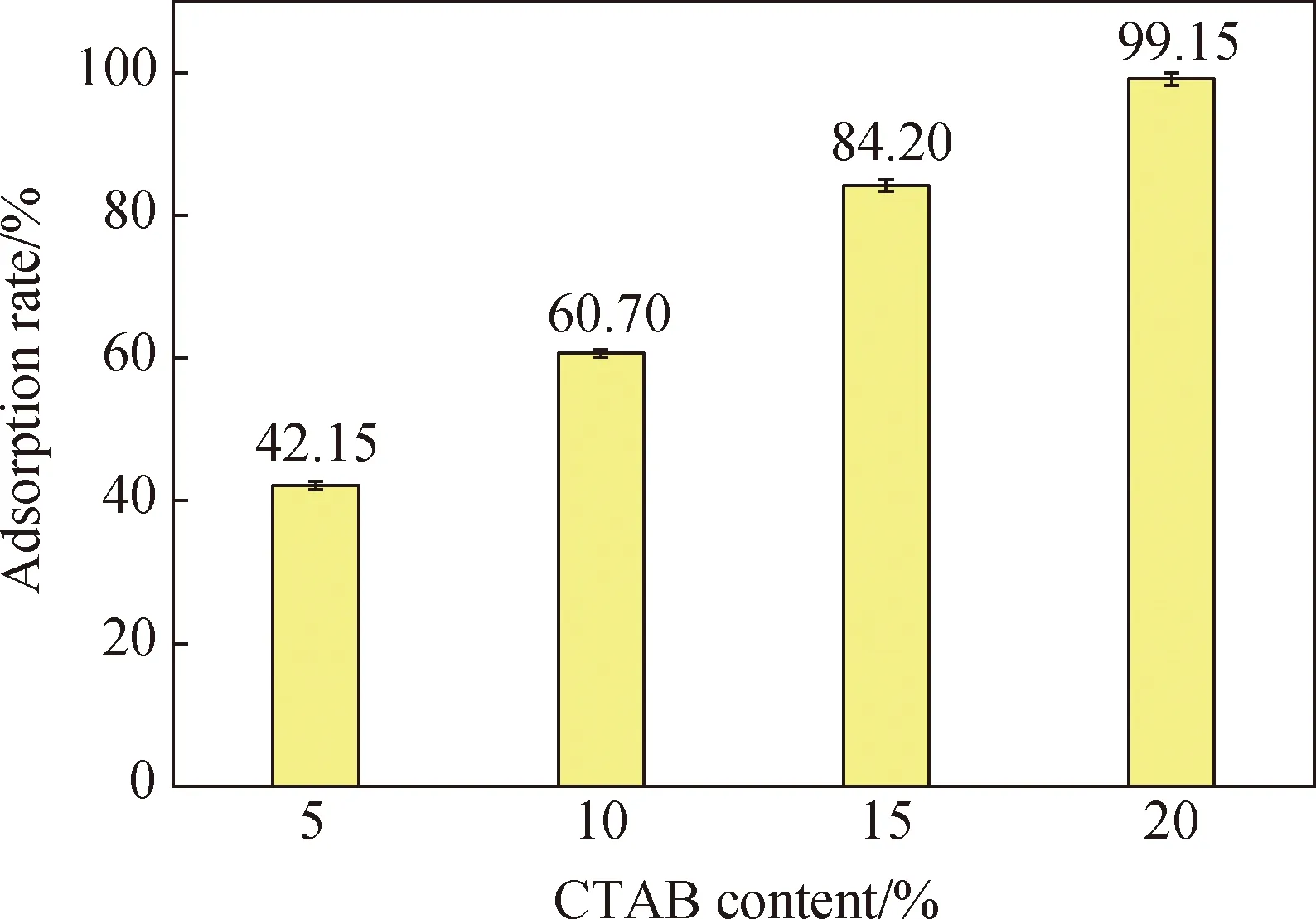
图5 CTAB掺量对Cr(VI)吸附效果的影响Fig.5 Effect of CTAB content on Cr(VI) adsorption
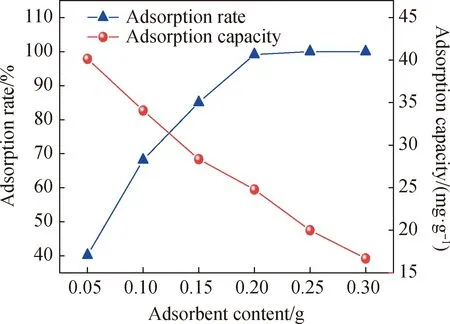
图6 吸附剂掺量对Cr(VI)吸附效果的影响Fig.6 Effect of adsorbent content on Cr(VI) adsorption
2.2.4 溶液初始pH值对Cr(VI)吸附效果的影响
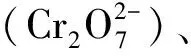
2.2.5 Cr(VI)浓度对Cr(VI)吸附效果的影响
在pH值为2、接触时间为2 h条件下,考察Cr(VI)初始浓度对Cr(VI)吸附效果的影响(见图8)。从图8可以看出,随着Cr(VI)从60 mg/L增加到180 mg/L,吸附剂对Cr(VI)的吸附率从100%降到了90.9%,吸附容量从15.00 mg/g增加到了40.91 mg/g。吸附容量随着浓度的增加而增加是因为Cr(VI)的转移驱动力增强和扩散阻力降低以及Cr(VI)与吸附剂表面之间的有效碰撞增加。吸附率的降低是因为离子浓度增加,吸附剂活性位点总量不变。
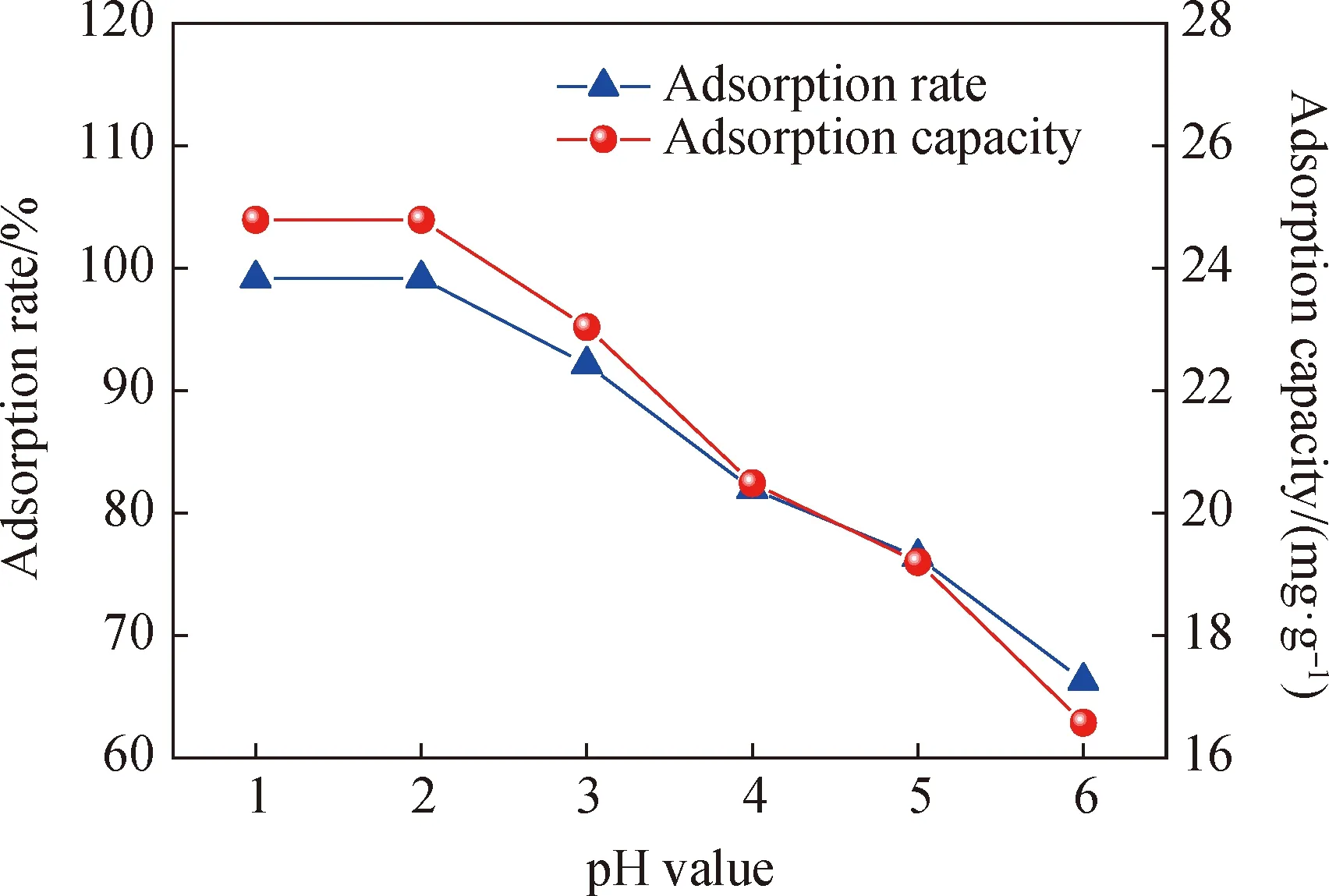
图7 溶液初始pH值对Cr(VI)吸附效果的影响Fig.7 Effect of initial solution pH value on Cr(VI) adsorption
2.3 Cr(VI)吸附模型
2.3.1 Cr(VI)等温吸附
吸附平衡等温线能评估吸附剂的最大吸附容量(qm),还能解释吸附分子与吸附剂表面的相互作用方式。其中,Langmuir等温方程用于描述Cr(VI)在吸附剂表面的单分子层吸附现象,相当于假设饱和位点的数量有限;Freundlich等温方程是一个经验方程,用于描述Cr(VI)在吸附剂表面的多层吸附现象,并考虑在吸附剂表面发生了异质性吸附;Tempkin等温方程用于观察吸附Cr(VI)过程的焓;而Dubinin-Radushkevich(D-R)等温方程用于分析Cr(VI)和吸附剂之间的相互作用,通过高斯能量分布在非均质表面上描述吸附机理。等温方程如式(3)~(8)所示。
(3)
(4)
Tempkin等温方程:
qe=BlnA+BlnCe
(5)
(6)
(7)
(8)
式中:Ce为Cr(VI)溶液的平衡浓度,mg/L;qe为平衡时吸附剂对Cr(VI)的吸附容量,mg/g;qm为对Cr(VI)理论最大吸附容量,mg/g;KL为Langmuir常数,L/mg;KF为与温度、吸附剂性质有关的常数,mg1-n·Ln·g-1;n为与温度有关且大于1的常数;A和B为Tempkin常数;R为通用气体常数,J·mol-1·K-1;T为绝对温度,K;Z为Tempkin等温线吸附热,J/mol;β为D-R吸附等温线常数,mol2/J2;ε为Polanic吸附势能,J/mol;E为吸附过程自由能,J/mol。
根据初始浓度对Cr(VI)吸附效果的影响,在100~180 mg/L条件下根据其吸附率和吸附容量结果按照不同等温线方程进行拟合,拟合曲线见图9,拟合参数见表3。根据图9的R2值可知,与Freundlich、Tempkin和D-R吸附等温模型相比,Langmuir等温模型的相关系数更高,表明Cr(VI)的吸附等温线数据在Langmuir等温模型中更合适。结果表明Cr(VI)在吸附剂上的吸附是单分子层吸附,从Langmuir等温模型获得的Cr(VI)最大吸附容量为42.553 1 mg/g。
在Freundlich等温模型中,1/n的数值一般在0与1之间,1/n越小,表示吸附剂对Cr(VI)的吸附效果越好,一般来说,1/n在0.1~0.5时,表示吸附易于发生,表中Freundlich常数n为5.977 3,表明吸附剂对Cr(VI)有着较好的吸附效果。Tempkin模型可以描述Cr(VI)和吸附剂之间的间接相互作用以及吸附过程的焓。Tempkin模型与Cr(VI)的吸附过程匹配,表明改性FS吸附剂的吸附热和温度在吸附过程中呈良好的线性关系,A与吸附热有关。D-R模型相关系数(R2=0.819 4)较低,拟合结果较差。
综上,Cr(VI)吸附等温线更符合Langmuir等温模型,表明其吸附主要为单分子层吸附,改性FS对Cr(VI)有明显的吸附效果。
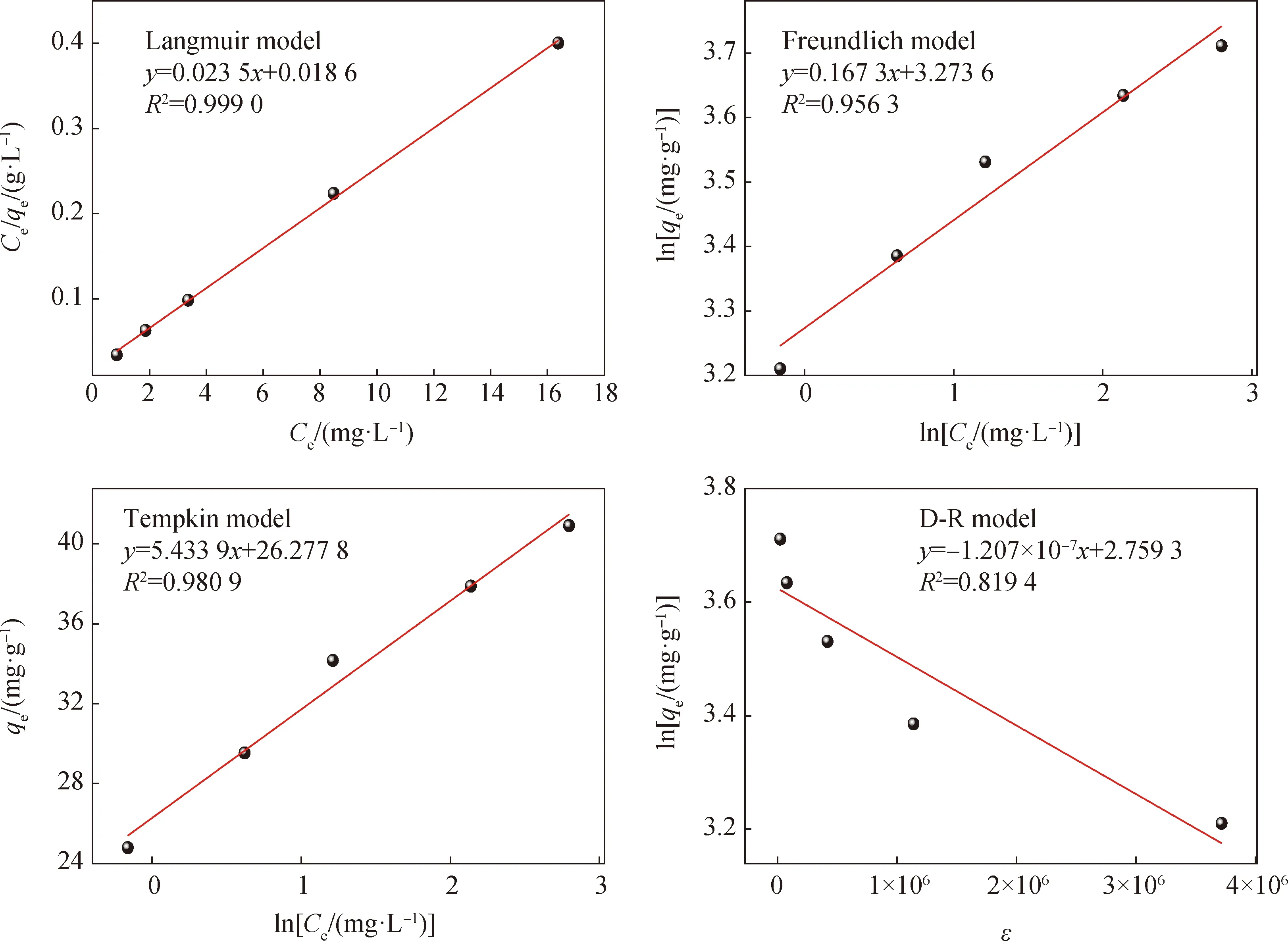
图9 Cr(VI)吸附等温线模型Fig.9 Isothermal models of Cr(VI) adsorption

表3 Cr(VI)等温线模型拟合参数Table 3 Isothermal model fitting parameters of Cr(VI) adsorption
2.3.2 Cr(VI)吸附动力学
吸附动力学主要用来描述吸附剂吸附Cr(VI)速率的大小。在温度为25 ℃、吸附剂掺量为0.2 g、Cr(VI)浓度为 100 mg/L条件下,对不同时间吸附容量进行测定,通过动力学模型对试验数据进行拟合,从而探讨其吸附机理。常用的吸附动力学拟合模型有拟一级动力学模型、拟二级动力学模型、Elovich动力学模型和颗粒内扩散模型。如果吸附控制剂分散在边界层中,则吸附动力学通常遵循拟一级动力学模型,其中吸附速率随时间的变化与吸附剂表面中未占据位点的数量成正比;拟二级动力学模型基于固相吸附,其中吸附位的占有率与空位数成正比。式(9)~(12)为拟一级动力学模型、拟二级动力学模型、Elovich动力学模型和颗粒内扩散模型线性方程。
拟一级动力学模型:
ln(qe-qt)=lnqe-k1t
(9)
(10)
(11)
颗粒内扩散模型:
qt=kit0.5+C
(12)
式中:qe为平衡吸附容量,mg/g;qt为t时刻的吸附容量,mg/g;k1为拟一级动力学的吸附速率常数,1/min;k2为拟二级动力学的吸附速率常数, g/(mg·min);α为初始吸附速率,mg/(g·min);γ为解吸常数,g/mg;ki为颗粒内扩散速率常数,mg/(g·min0.5);C的值给出了边界层厚度的概念,边界层效应与切割区域的大小成正比。
在Cr(VI)浓度为100 mg/L、pH值为2、吸附剂掺量为0.2 g条件下,对不同时间吸附效果进行研究,测定其吸附容量并按照四种动力学模型进行拟合,拟合结果见图10,相关参数见表4。由图10的R2值可知,与拟一级动力学模型、Elovich动力学模型和颗粒内扩散模型相比,吸附Cr(VI)时拟二级动力学模型具有更高的R2值,说明改性FS吸附剂对Cr(VI)的吸附更符合拟二级动力学模型。此外,拟二级动力学模型计算出来的平衡吸附容量Cr(VI)为24.875 6 mg/g,与最佳条件下的试验结果相近,表明吸附剂与Cr(VI)之间的吸附机制主要是静电作用。
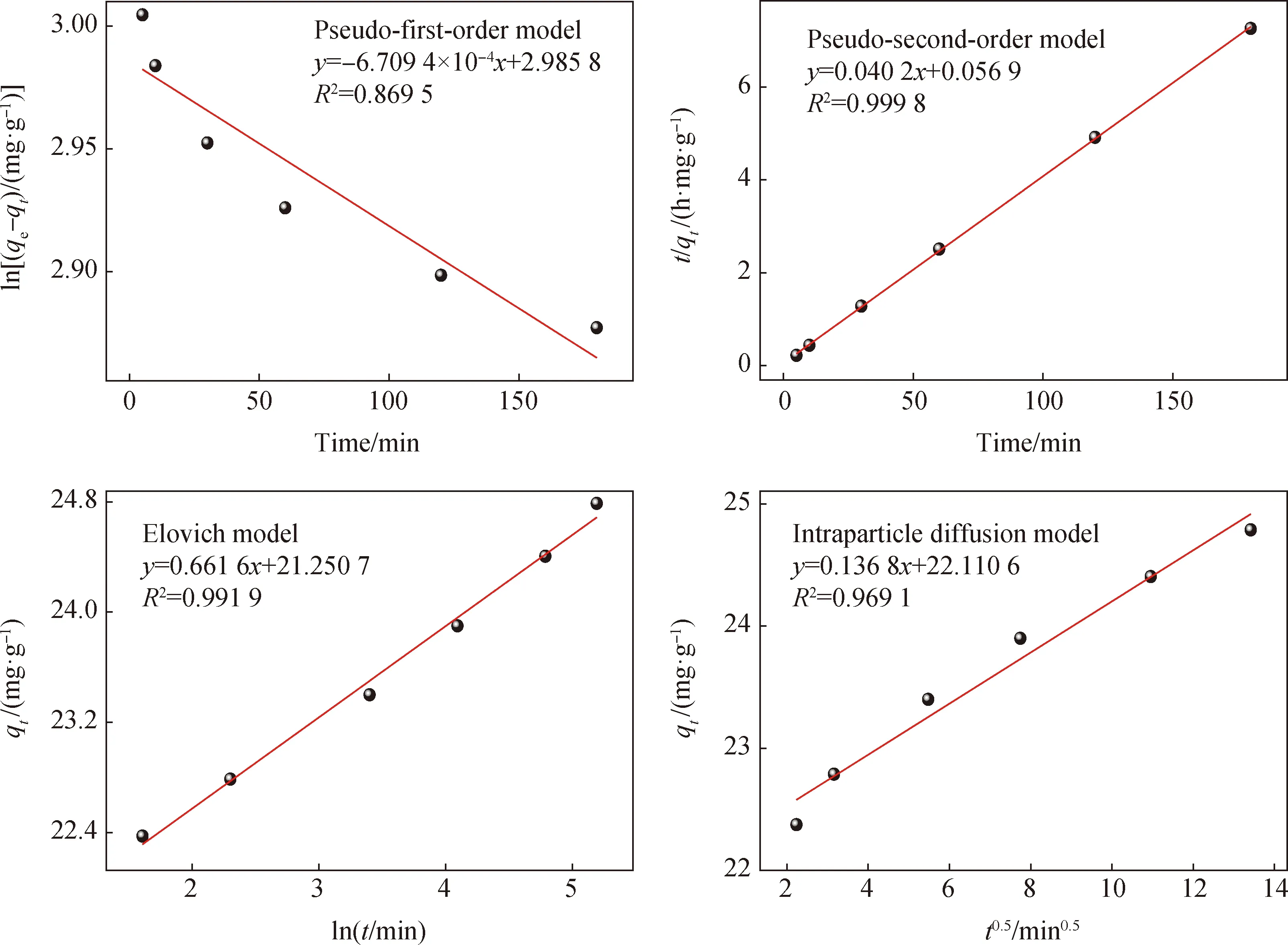
图10 Cr(VI)吸附动力学模型拟合曲线Fig.10 Cr(VI) fitting curves of adsorption kinetic models
Elovich动力学模型用于描述Cr(VI)在非均匀固体吸附表面的吸附行为,揭示了其他动力学方程所忽视的数据的不规则性,适用于反应过程中活化能较大的过程,通过Elovich动力学模型可以看出吸附剂对Cr(VI)有着极大的吸附率,在5 min内吸附率达到了89.50%,此后吸附率随着时间延长慢慢增加到99.15%。吸附机制的描述是研究污染物吸附过程的重要步骤,可知晓反应的限制步骤。一般来说,吸附在四个连续的阶段中展开:(1)将溶质输送到液相中;(2)通过吸附剂表面周围的液膜扩散;(3)吸附剂颗粒内部的扩散;(4)吸附剂和吸附物的化学基团之间的吸附反应。通常,各种机制控制吸附动力学中限制最大的是扩散机制,其包括外部扩散、边界层扩散和颗粒内扩散。因此,为了确定吸附过程中的限制性步骤,颗粒内扩散模型被应用于动力学数据;其中C值有助于确定边界厚度,较大的C值对应较大的边界层扩散效应。改性FS吸附剂对于Cr(VI)吸附过程中,颗粒内扩散模型具有较高的R2值(0.969 1),但qt与t0.5的线性拟合曲线未通过原点,表明吸附涉及颗粒内扩散,但这不是唯一的速率控制步骤。
综上,改性FS对Cr(VI)的吸附更符合拟二级动力学模型,表明其吸附以化学吸附为主导,吸附过程中涉及颗粒内扩散,速率控制步骤不由内扩散单一控制。

表4 Cr(VI)动力学模型拟合参数Table 4 Cr(VI) fitting parameters of adsorption kinetic models
2.4 吸附机理分析
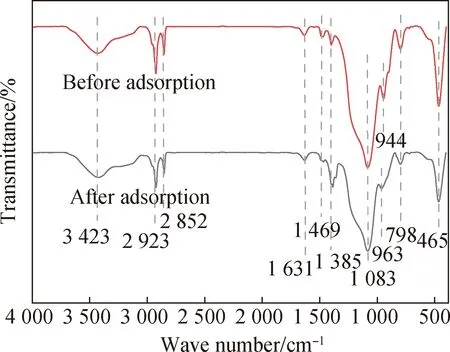
图11 吸附Cr(VI)前后吸附剂的FTIR谱Fig.11 FTIR spectra of absorbent before and after Cr(VI) adsorption
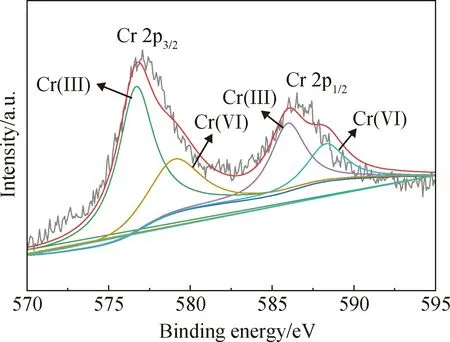
图12 吸附Cr(VI)后Cr价态的XPS分析Fig.12 XPS analysis of Cr valence state after Cr(VI) adsorption
3 结 论
(1)酸化-CTAB联合改性FS制备Cr(VI)吸附剂,吸附剂分析表征表明电炉镍铁渣经改性转化为无定形二氧化硅,其比表面积从11.64 m2/g增加到180.6 m2/g,比表面积极大提高。
(2)吸附试验表明,吸附剂掺量为0.2 g、pH值为2时,改性FS吸附剂对Cr(VI)的吸附过程更符合Langmuir模型和拟二级动力学模型,说明吸附以单分子层化学吸附为主,理论最大吸附容量为42.553 1 mg/g。