细菌纤维素膜纯化条件的优化及性能表征
王耀强,王 涛,李旖曦,张 虹,张 勇,李家兵,韩永和
(1.福建师范大学环境与资源学院、碳中和现代产业学院,福建 福州 350117;2.福建省污染控制与资源循环利用重点实验室,福建 福州 350117)
纤维素(cellulose)是一种以葡萄糖为基本单元组成的生物高分子材料,其分子式和相对分子质量分别为(C6H10O5)n和50 000~2 500 000[1].作为木材、亚麻、大麻等植物的主要成分,纤维素与果胶、木质素和半纤维素共同构成植物细胞壁[2].植物源纤维素是制备纸张、纺织品、全纤维素复合物等产品的主要原料[3-5].但植物纤维素的纯化需经酶或机械预处理以去除木质素、半纤维素和其他杂质,该过程成本较高且可能改变纤维性能,进而限制了其在某些领域的应用[6-9].除植物外,多种微生物也具备产纤维素能力,此类纤维素被称为细菌纤维素(bacterial cellulose,BC)[10].Cladophora、Vallonia等微藻,Dictyostelium、Saprolegnia等真菌和Acetobacter、Achromobacter、Aerobacter、Agrobacterium、Asaia、Gluconobacter、Gluconacetobacter、Komagataeibacter、Rhizobium、Saccharibacter、Sarcina、Tanticharoenia等细菌均具备良好的产纤维素能力[10].与植物纤维素相比,BC的纯度和结晶度更高、持水能力更强、纤维尺寸更小(30~50 nm)且生物相容性更好[11-13].因此,BC已被广泛用于食品、水凝胶、高强度可再生纸、乐器膜、滤膜、医用材料等产品的开发,具有广阔的市场前景[14-19].
BC是微生物以葡萄糖为底物通过β-1,4-糖苷键合成的生物高分子材料.因BC不含木质素和半纤维素,其纯化成本更低,也更受企业欢迎[20-23].然而,BC是伴随着微生物二分裂繁殖过程产生的纳米纤维,因此BC网状结构中分布着大量菌体[10,24].尽管在食品开发过程中一般不对BC进行除菌处理[25-26],菌体等杂质的存在会影响BC在生物医学、膜和电化学等领域的应用[14,27-29].已报道的纯化方法包括机械破碎处理、低温破碎处理、超声处理、强酸处理、碱处理和生物预处理等,这些方法对纤维素微观形貌和理化性能产生的影响有较大差异[27-28].碱处理作为BC纯化的常用手段,其原理是将BC糖苷链中的范德华力和纤维束层中的氢键打开以降低机械强度[30].例如,Rachtanapun等[31]研究了0.20~0.60 g·mL-1NaOH对以椰果为原料纯化制备羧甲基纤维素(carboxymethyl cellulose,CMC)的影响,发现0.30 g·mL-1NaOH处理下CMC的产率较高,但产物的微观形貌发生了较大变化.研究表明,当NaOH体积分数为6%~18%时,微波加热处理8 min还可实现Ⅰ型纤维素向Ⅱ型纤维素的转化[32].采用0.1 mol·L-1NaOH水浴煮沸2 h是目前BC纯化的常规参考条件[33],但鲜有研究者系统地考察不同NaOH浓度和处理时间对BC微观形貌、晶体结构等性质的影响.通过优化NaOH浓度和处理时间以获得高纯度BC样品是提高其应用价值的重要前提.
本研究以不同NaOH浓度和处理时间为主要优化条件,对BC进行纯化,通过SEM、XRD、FTIR等表征手段探讨纯化条件对BC材料性能的影响.具体包括:设置不同NaOH浓度(0、0.1、0.2、0.5、1.0、2.0 mol·L-1)和处理时间(30、60、120、240 min),分别采用SEM、XRD和FTIR分析BC的微观形貌、晶体结构和表面官能团,探讨纯化BC的最适NaOH浓度和处理时间.结果有望为BC的纯化制备提供参考,为医药、化学等领域提供可靠的BC基生物高分子材料.
1 材料与方法
1.1 实验菌株和培养基
菌株Komagataeibactersp.W1分离自福建省泉州市某食醋有限公司的食醋发酵池,由本实验室保存[33].实验HS培养基组分包括(g·L-1):葡萄糖20、酵母膏5、蛋白胨5、十二水磷酸氢二钠6.8、一水柠檬酸1.15和七水硫酸镁0.51,并利用1.0 mol·L-1NaOH或HCl将培养基pH调至6.0[34].培养基经115 ℃灭菌30 min,备用.
1.2 细菌纤维素膜的制备与纯化
取一环Komagataeibactersp.W1菌株单克隆,接种至灭菌的HS培养基中,30 ℃静置培养7 d.收集培养基表面的BC膜,备用.
用去离子水反复冲洗BC膜,沥干.将BC膜分别浸泡于0、0.1、0.2、0.5、1.0、2.0 mol·L-1NaOH溶液中,100 ℃水浴煮沸2 h;随后,将BC膜转移至去离子水中继续煮沸2 h以彻底除去膜中的菌体和残留培养基.根据NaOH浓度的优化结果,选取最适NaOH浓度重复上述纯化过程,控制水浴煮沸时间(30、60、120、240 min),获得最优处理时间.
将纯化后的BC膜转移至清水中浸泡24 h,沥干后通过美国Labconco FreeZone 6 plus冷冻干燥机对样品进行冷冻干燥48 h直至恒质量.
1.3 细菌纤维素膜的微观形貌与理化性能表征
将少量冷冻干燥的BC样品置于样品台的导电胶上,喷金处理后采用S-4800场发射扫描电子显微镜(SEM,QuantaTM250 FEG,FEI,美国)观察BC膜表面的微观结构.SEM参数为:斑点3.0,电压15 keV,放大倍数×10 000.为分析BC表面的聚集性颗粒物是否为NaOH晶体,同时对BC进行SEM-EDS(能谱)分析,通过面扫描模式计算各元素的相对原子含量(以百分比计).
采用X’Pert Pro型粉末X射线衍射仪(XRD,Bruker D8 ADVANCE,德国)分析BC膜的晶体结构.首先,选择BC膜中较平整的测试面,以带有镍过滤的铜Kα(λ= 0.154 06 nm)为辐射条件,设置电压为40 keV、灯丝发射电流为30 mA、扫描步长为0.1°、扫描角度为11°~30°(2θ).为消除背景干扰,以硅零背景板为对照采集干扰信号响应值,实际测量值与硅零背景板干扰信号的差值即为样品的XRD吸收值.BC膜的晶面距离(d)和表观晶粒度近似值分别根据Bragg方程(式1)和Scherrer公式(式2)进行计算[35].
(1)
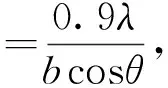
(2)
其中,λ为X射线的波长,θ表示平面与衍射或入射光束之间的角度(即Bragg角),半峰全宽b是最大吸收峰一半处的峰宽.半峰全宽数值由OriginPro 9.0软件的峰值和基线模块(the Peaks and Baseline module)中的综合峰值分析(Integrated Peaks analysis)计算而得.通过公式(3)和(4)计算BC的结晶指数和结晶度[36].
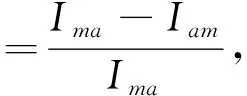
(3)
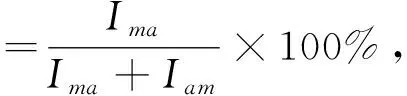
(4)
其中,Ima表示2θ在22°~24°处晶格峰的最大衍射强度,Iam表示2θ在18°~19°处非晶相的最小衍射强度.
除SEM和XRD分析外,本文还采用FTIR(Thermo Scientific Nicolet iS5,美国)研究BC膜的表面官能团.采用衰减全反射模式,每次测量进行32次扫描,扫描范围为400~4 000 cm,分辨率为0.5 cm-1.
2 结果与讨论
2.1 不同NaOH处理浓度对BC形貌的影响
NaOH作为一种常用的BC纯化试剂,在合适的浓度范围内可通过影响范德华力和氢键使BC膜呈松散结构,但过高的浓度会破坏纳米纤维的微观结构[30].本研究设置NaOH浓度为0、0.1、0.2、0.5、1.0、2.0 mol·L-1,观察不同NaOH浓度对BC膜的表观和微观形貌的影响.结果显示,对照组BC膜呈黄色且不透明,其纳米纤维表面可见大量附着物,说明膜内存在较多菌体和杂质(图1a).当NaOH处理浓度为0.1 mol·L-1时,BC膜的杂质显著减少,但仍可见典型的菌体附着(图1b).随着NaOH浓度继续提高至0.2和0.5 mol·L-1,BC膜呈现良好的透明度,SEM显示BC纤维分布均匀且未见明显的菌体或杂质(图1c、1d).其中,0.5 mol·L-1NaOH处理时BC膜出现皱缩现象,且其微观形貌呈现更高的致密性(图1d),说明该浓度下BC的结构已有明显变化.NaOH浓度进一步提高至1.0 mol·L-1会加剧BC膜的皱缩现象,同时可见纳米纤维表面附着菌体和大颗粒杂质(图1e).当NaOH浓度达2.0 mol·L-1时,样品已失去膜状外观,SEM分析亦未见典型的纳米纤维结构(图1f).以上结果表明,0.1 mol·L-1NaOH仍难满足BC膜的纯化要求(图1b),表现出前期研究中常见的菌体残留现象[33].尽管高浓度NaOH(0.20~0.60 g·mL-1)处理有利于制备羧甲基纤维素,但所制备的产物的晶体结构已发生显著改变[31,37-39].结合本研究结果,说明NaOH浓度过低或过高均不是获得高纯度BC膜的理想条件,而0.2 mol·L-1可作为BC膜纯化的最优参考浓度.
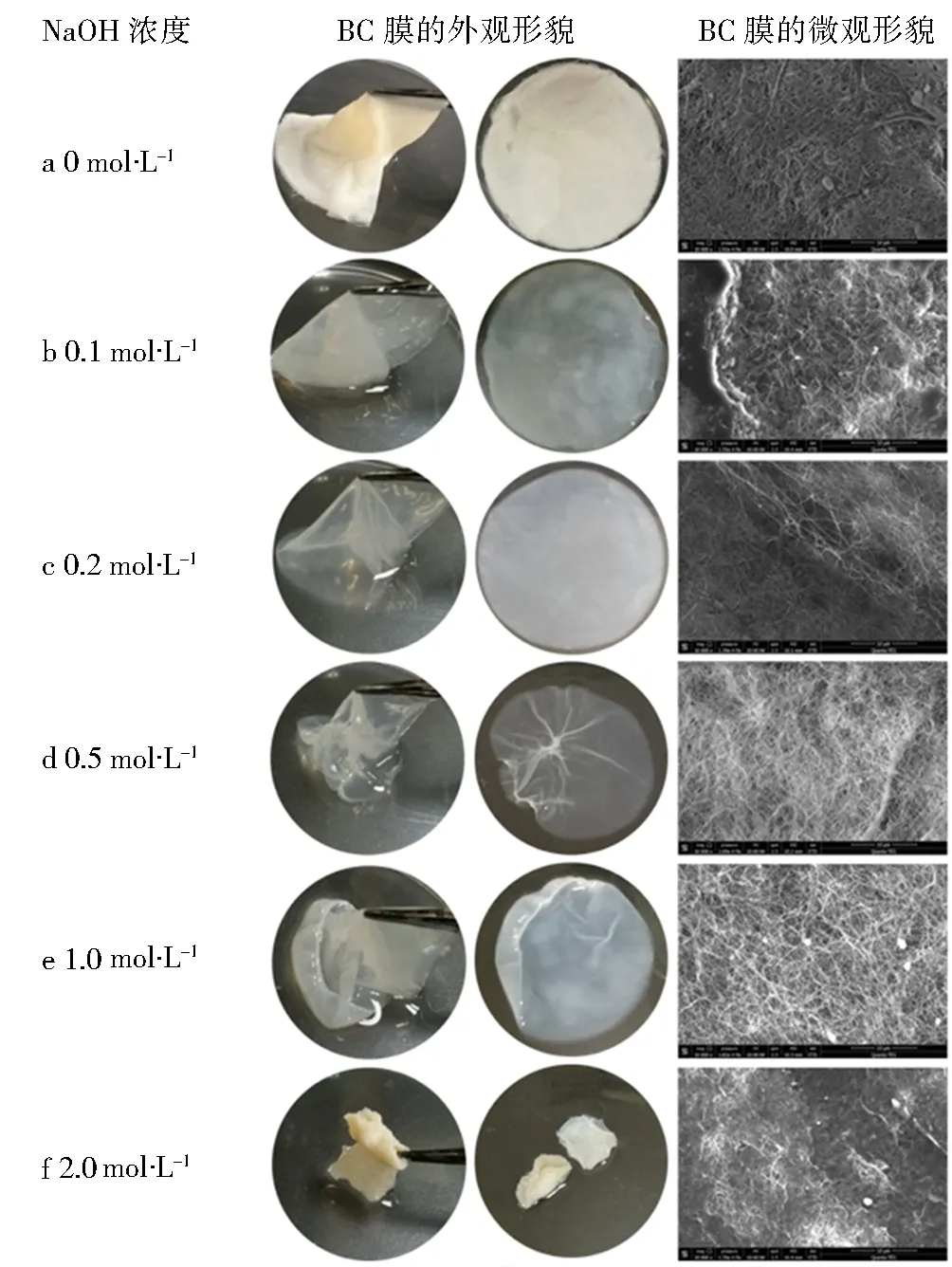
图1 在不同NaOH浓度(左)处理下BC膜的外观形貌(中)和微观形貌(右,SEM:×10 000)Fig.1 The apparent morphology (middle) and micromorphology (right,SEM:×10 000 ) of BC membranes treated with different NaOH concentrations (left)
如图1e、1f所示,在进行SEM分析时发现,NaOH浓度过高会导致BC纤维表面附着大量颗粒物.该颗粒物呈白色长条状,在纤维表面成堆随机分布(图2a).为探讨其成分,在SEM基础上选取区域Spectrum 9进行EDS分析.结果表明,该区域内的元素组成主要为O(45.5%)、C(37.4%)和Na(17.1%),散布的Au峰为喷金导致的信号值(图2b).由此可见,除影响BC膜的正常纳米纤维结构外,过量的NaOH还会以晶体形式析出.在进行BC膜纯化处理时,尽管菌体和杂质的去除是主要目的[40-41],但NaOH结晶析出也会影响材料的纯度和性质,该结果提示NaOH浓度需控制在一个合适范围内.
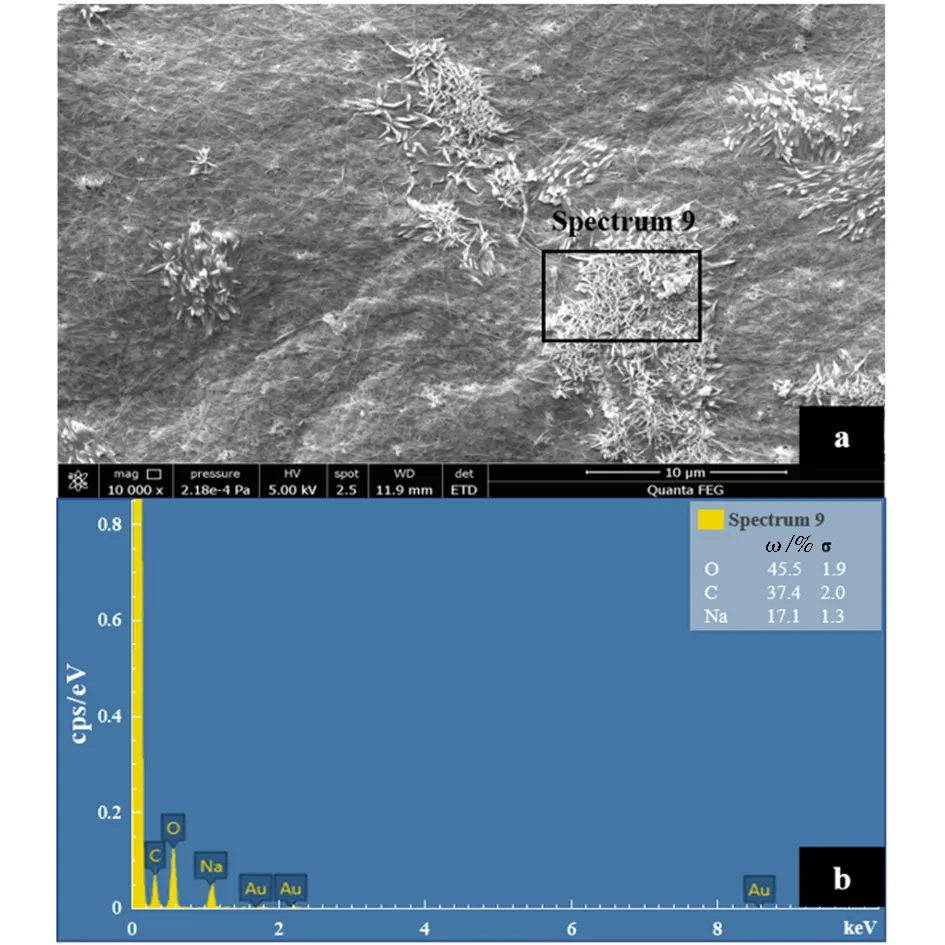
(a) SEM图(×10 000);(b) 基于图a中区域Spectrum 9的EDS扫描结果图2 基于SEM-EDS解析BC膜上元素的相对原子含量Fig.2 SEM-EDS-based analysis of the relative atomic content of elements on the BC membrane
2.2 不同处理时间对BC形貌的影响
水浴加热是BC膜纯化的关键步骤,处理时间的长短不仅会影响NaOH与样品的充分接触,同时可影响NaOH的浓度.为探究不同处理时间对BC形貌的影响,以0.2 mol·L-1NaOH为处理浓度,采用SEM分析了在30、60、120、240 min时BC膜的微观形貌差异.如图3a所示,处理30 min未能有效去除BC膜表面及网状结构中的菌体和杂质,纳米纤维呈致密结构且纤维网络不清晰.将处理时间提高至60 min时,BC膜纤维网络均匀性大幅提升,但纤维表面及网络中仍附着大量菌体和杂质(图3b).当处理时间达120 min时,BC纳米纤维尺寸均匀、纤维网络清晰,说明该处理时间可有效去除菌体和杂质(图3c).但处理时间过长(240 min)时BC纤维的均匀性较差,且可见明显的杂质堆积,可能与长时间水分蒸发导致的NaOH浓度增加有关(图3d).
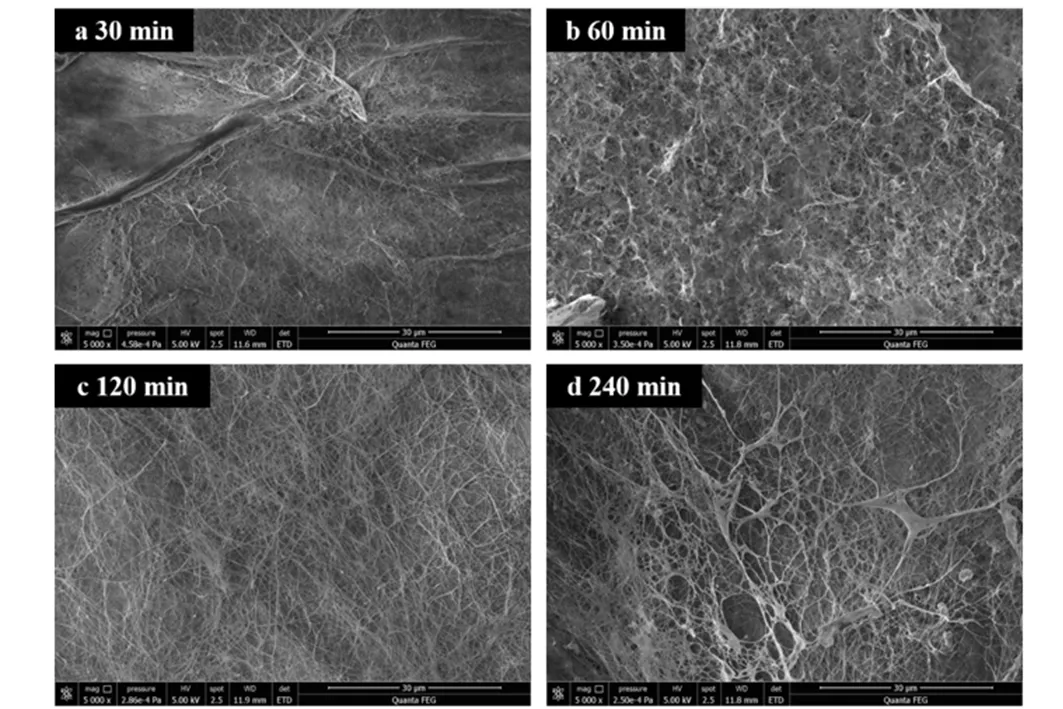
图3 基于SEM分析不同处理时间对BC膜微观形貌的影响(×5 000)Fig.3 Effects of pretreatment time on the micro-morphology of BC membrane based on SEM analysis (×5 000)
BC含有大量氢键,确保恰当的水浴时间内经适当浓度的NaOH处理有助于打开分子间氢键[30,33],进而使附着其上的菌体和杂质脱落.Li等[23]指出,处理时长是破坏BC纤维键能进而打开纤维网络的关键因素之一.但处理时间过长会导致NaOH浓度升高并破坏BC的晶体结构[42].结果说明,仅当NaOH浓度为0.2 mol·L-1、处理时间为120 min时,BC膜的纯化效果才比较理想(图3c).
2.3 基于XRD分析不同纯化条件对BC晶体结构的影响
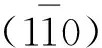
本研究结果显示,不同NaOH浓度和处理时间会显著影响BC的晶体衍射峰强度,且前者对纤维素的典型晶体峰影响比后者大(图4).在各处理组中,BC膜在2θ为14.5°、16.6°和22.7°均出现了典型衍射峰,表明存在纤维素晶体结构(图4).当NaOH浓度为0 mol·L-1时,BC膜的XRD衍射峰强度较弱,且在2θ为16.6°处未出现典型吸收峰(图4a).随着NaOH浓度升高,BC膜的XRD衍射峰强度呈现先增强后减弱的趋势;其中,NaOH浓度为0.1~0.2 mol·L-1时衍射峰较明显(图4a),但NaOH浓度达1.0 mol·L-1之后衍射峰逐渐消失(图4a).因此,NaOH浓度过低或过高不仅不利于菌体和杂质的去除(图1),而且对纤维素的晶体结构会产生显著影响.
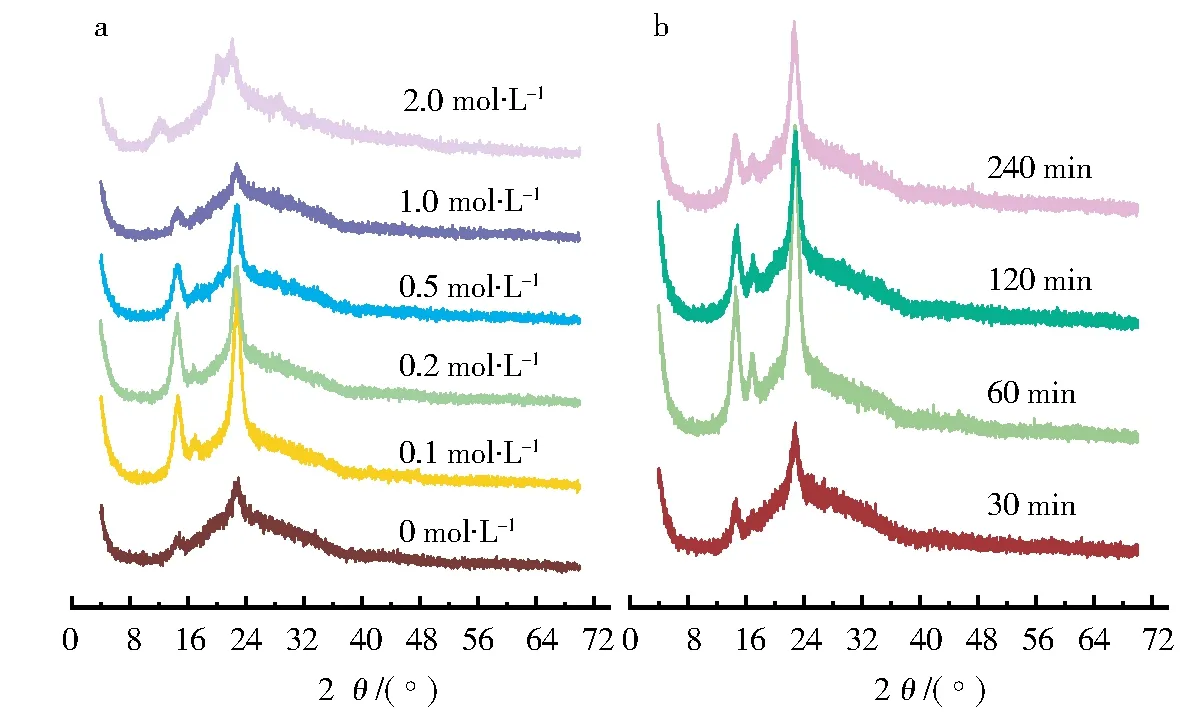
图4 不同NaOH浓度(a)和处理时间(b)对BC晶体结构的影响Fig.4 Effects of different NaOH concentrations (a) and treatment time (b) on the crystal structure of BC
当处理时间为30 min时,BC膜的XRD衍射峰强度与低浓度NaOH处理结果类似(图4b),说明短时间处理未能将BC内大分子间的氢键打开[47].尽管60~240 min处理时间对BC膜的微观形貌产生了较大影响(图3b、3c、3d),但BC膜均含有典型的纤维素晶体衍射峰(图4b).结合SEM结果可知,在0.2 mol·L-1NaOH和120 min处理条件下,BC膜呈现出较好的纤维结构和晶体特征.
为进一步探讨不同NaOH浓度和处理时间对BC晶体特性的影响,系统分析了BC的d值、表观晶粒度、结晶指数和结晶度.如表1所示,NaOH浓度为0~1.0 mol·L-1时,峰1(14.5°)对应的d值为0.606~0.610,与报道的结果一致[33,49],说明各样品的Iα含量相近[48].但当NaOH达2.0 mol·L-1时,d值为0.731(表1),表明BC晶体结构已被破坏.尽管不同浓度NaOH对峰3(22.7°)的d值影响不大(0.388~0.398;表1),但峰2(16.6°)的d值在高浓度NaOH处理组中无法计算获得(表1),说明NaOH浓度主要影响BC在14.5°和16.6°处的晶体结构.与d值不同的是,表观晶粒度在各处理组中差异较大且没有明显规律(表1),可能与BC膜中微纤维的不规则特性和杂质的干扰有关[49].因此,NaOH浓度过低或过高均会破坏BC晶体结构的稳定性,当NaOH浓度为0.1~0.5 mol·L-1时,BC结晶度较高(结晶指数为0.75~0.82,结晶度为80%~85%;表1).
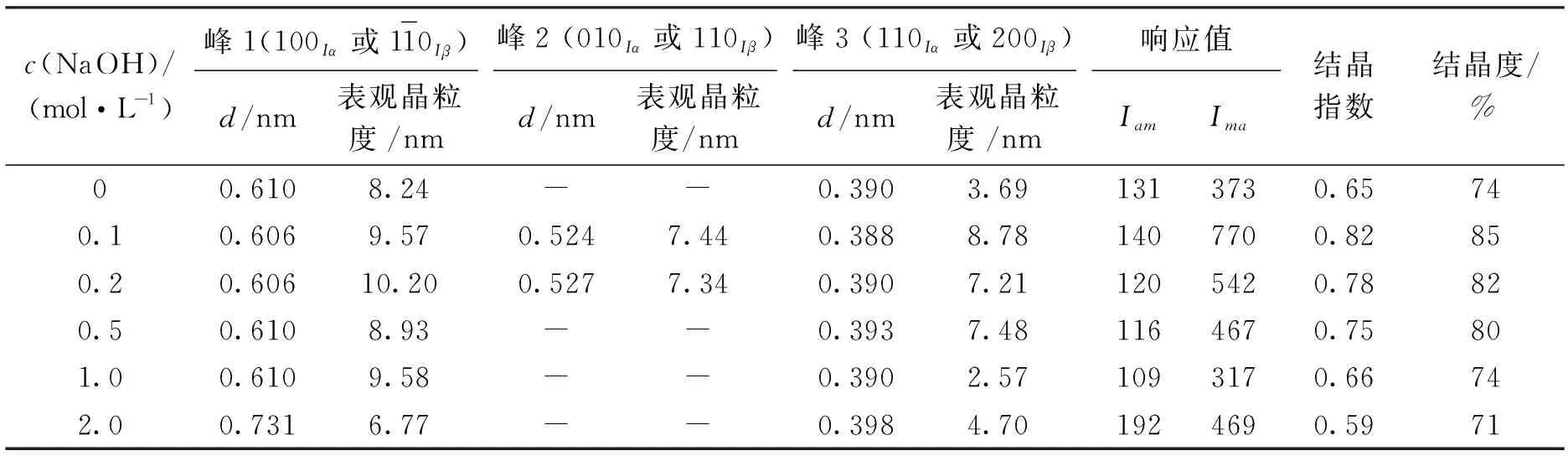
表1 不同NaOH浓度处理时BC膜的d、表观晶粒度、结晶指数和结晶度Tab.1 d-spacing,apparent crystal size,crystallinity index and crystalline of BC membrane pretreated with different concentrations of NaOH
经不同处理时间纯化时,BC膜的3个XRD衍射峰所对应的d值与NaOH处理组相当,区别在于各峰的d值未受处理时间的显著影响(表2).然而,处理时间对表观晶粒度的影响呈现出与NaOH浓度相似的趋势.此外,不同处理时间纯化时BC膜的结晶指数(0.73~0.84)和结晶度百分比(79%~86%)均较高(表2).结合表1结果,说明BC晶体结构主要受起始NaOH浓度影响,但处理时间过长也能通过影响NaOH浓度而间接影响BC膜的晶体结构.基于BC膜微观形貌和纤维的晶体特性,采用0.2 mol·L-1NaOH水浴煮沸120 min是比较理想的BC膜纯化条件.
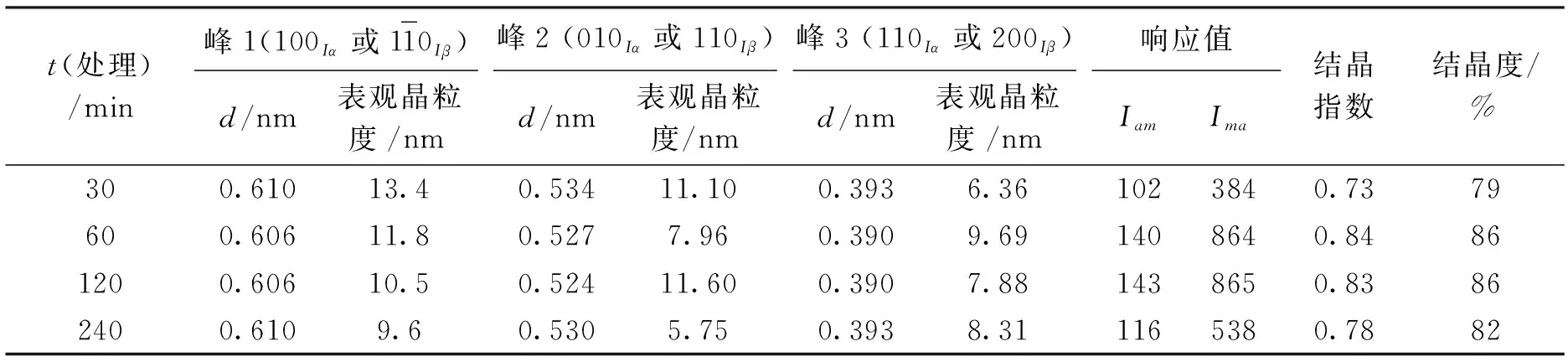
表2 处理时间对BC膜d值、表观晶粒度、结晶指数和结晶度的影响Tab.2 Effects of the treatment time on d-spacing,apparent crystal size,crystallinity index and crystalline of BC membrane
2.4 基于FTIR解析不同纯化条件下BC表面官能团的变化
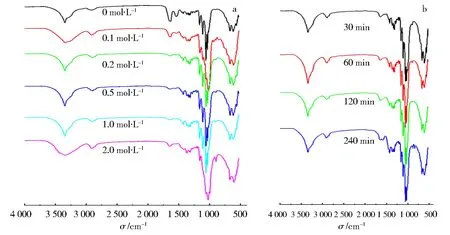
图5 不同浓度NaOH(a)和处理时间(b)下的BC表面官能团差异分析Fig.5 Differential analysis of the surface functional groups of BC treated with different concentrations of NaOH (a) and treatment time (b)
3 结论
本研究设置不同浓度NaOH溶液和处理时间,通过SEM、XRD、FTIR等考察纯化条件对BC膜外观形貌、微观结构和表面官能团的影响.结果表明,NaOH溶液浓度太低或处理时间不足不能有效去除BC膜中的菌体和杂质,该条件下制备的BC膜在2θ为14.5°、16.6°和22.7°处的吸收峰不显著且结晶度低于85%,而NaOH浓度太高或处理时间太长会破坏BC晶体结构.当NaOH浓度和处理时间分别为0.2 mol·L-1和120 min时,所制备的BC材料纯度较高、纤维结构规整、晶体特征明显.但NaOH浓度和处理时间对BC膜的表面官能团影响较小.本研究优化了BC膜的纯化条件,结果可为获得纯度更高、性能更好的BC材料提供理论依据.

