基于推土距离(EMD)算法的群体生物等效性统计方法评价眼用乳剂粒径分布的一致性
徐千姿,梁月茹,赵忠卫,沈 雁**
(1中国药科大学药学院药剂系,南京 210009;2深圳奥祺生物医药有限公司,深圳 518057)
近年来,随着人们生活水平的提高,健康意识的不断增强,药品需求随之越来越大。仿制药是医疗保障系统中的重要组成部分,其价格相对低廉,拥有良好的经济效益和社会效益[1]。生物等效性(bioequivalence,BE)评价是批准仿制药的重要步骤之一[2]。体外生物等效性研究是BE研究的重要组成部分,它通常有两种统计分析方法,平均生物等效性(average bioequivalence,ABE)和群体生物等效性(population bioequivalence,PBE)[3]。PBE计算方法最早由安德森和霍克提出[4],是对ABE方法的补充,这是由于在实际中有许多药物可能存在方差非齐性,相比于ABE 检测只比较药代动力学参数的平均水平,PBE统计方法还考虑了参比制剂和受试制剂样本间、样本内所有变异,计算更加严谨[5]。
粒径分布(PSD)通常用直方图表示,通过粒子大小和范围的信息可用于描述一些物质物理和化学特性。PSD 的分析在建立复杂药品的BE 方面已引起了广泛的关注。在FDA 官方指南中已建议使用PBE 方法对多种纳米制剂的粒径开展体外生物等效性研究,如氢氧化铁蔗糖复合物注射液[6]、二氟泼尼松眼用制剂[7]、盐酸多柔比星脂质体注射剂[8]、妥布霉素/地塞米松眼用悬浮液[9]。对于这些制剂,PBE 考察主要参数为D50、Span 或多分散系数,其中D50 指有一半的粒径直径分布小于该值,Span 用来描述分布的区间,但这些参数只局限于粒径分布是单一峰的情况[10],当PSD图形是复杂的(即非单峰),D50/SPAN 将不足以进行分析。例如,对于存在双峰的PSD 图形,D50 可能位于两个峰之间的谷从而导致误差。针对这一问 题,FDA 在《Draft Guidance on Cyclosporine》[11]中提出了一种度量方法,称为推土距离(Earth Mover‘s Distance,EMD)算法。目前在计算机领域,已有不少研究将EMD 算法应用于图像检索、分析和模式识别等[12-13]。EMD 定义两个直方图之间的距离为一个运输问题,可用于度量两个相似分布间的差异[14],因此可将EMD 应用于PSD 图形相似度比较,为进一步评价粒径生物等效性提供数据分析基础。
环孢素眼用乳剂(商品名:Restasis)于2002年被FDA 批准在美国上市用于干眼症的治疗[15],获得了良好的疗效,但市场上很少有其仿制制剂,其中一个关键问题是生物等效性研究[16]。本研究以Restasis 作为研究对象,应用基于EMD 算法的PBE统计计算软件,检验开发的软件是否能通过参比制剂自身等效,并评价不同工艺下受试制剂粒径分布与参比制剂是否具有等效性,本研究不仅解决环孢素眼用乳剂控制体外生物等效性关键问题,同时也为其他乳剂、胶束、脂质体、纳米粒、微球、纳米囊等复杂仿制制剂的PSD 及PBE 评价提供参考。
1 材 料
1.1 药品与试剂
环孢素眼用乳剂参比制剂(商品名Restasis,规格0.4 mL∶0.2 mg,美国Allergan 公司);甘油(南京化学试剂股份有限公司);蓖麻油[罗辅医药科技(上海)有限公司];聚山梨酯80(南京威尔药业股份有限公司);卡波姆共聚物A 型(美国Lubrizol 公司);氢氧化钠(西陇科学股份有限公司);环孢素(浙江瑞邦药业股份有限公司)。
1.2 仪 器
电子分析天平(上海舜宇恒平科学仪器有限公司);pH计(瑞士Mettler toledo公司);恒温水浴锅(上海力辰邦西仪器科技有限公司);Malvern nano ZSE 动态光散射仪(英国马尔文仪器有限公司);Wiggens高速剪切机[维根技术(北京)有限公司]。
2 方 法
2.1 EMD算法
EMD 算法[10]起源于经典的货物搬运问题。对于两个离散分布P和Q,如果把这两个分布看作是总量为1 的一堆“土”的形状,那么EMD 算法反映的就是在一定限制条件下把这堆“土”从P状态搬运到Q状态所做的最小工作量。已知原始位置(xi)有“土”(pi),目标位置(yj)需求“土”(qj),则表 示 从pi运 往qj的“土”的数量;dij表示pi与qj两地的距离)。一旦找到最优解
2.2 群体生物等效性
体外群体生物等效性统计分析的研究方法是基于比较准则,计算其95%的置信区间的上限值θ,如果θ小于或等于预设的界限值θp,则表示受试制剂与参比制剂具有生物等效性。FDA 提出混合标度法[17]作为体外群体生物等效性比较的准则(population bioequivalence criterion,PBC)。

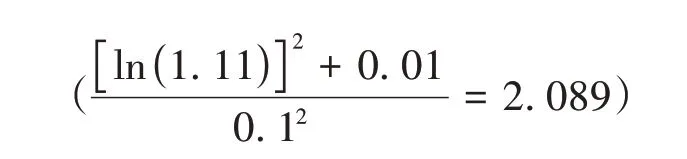
将式(1)转化为线性形式:
当σR>σT0时选用参比标准,即η1;当σR≤σT0时,选用常数标准,即η2
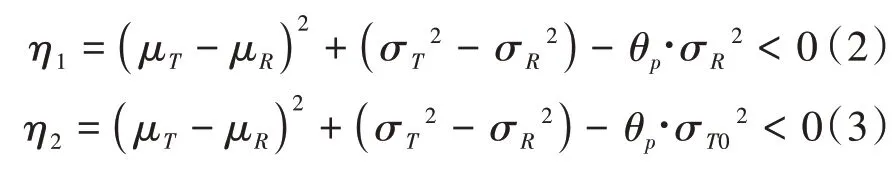
为使受试产品通过PBE 试验,线性化标准(η1或η2)的95%置信上限(Hη1或Hη2)不得大于0。
2.3 环孢素眼用乳剂的制备
2.3.1 处方 参考原研制剂处方组成,制备3 批处方量为100 g 的0.05%环孢素眼用乳剂,根据前期实验结果,改变蓖麻油、吐温用量及制备工艺参数,以获得不同粒径大小及分布的制剂。
2.3.2 制备工艺 按照表1 中处方组成及用量,用20%注射用水分散卡波姆共聚物A 型作为水相1;另取70%注射用水作为水相2;将蓖麻油、聚山梨酯80、甘油、环孢素搅拌溶解均匀后作为油相;油相与水相2混合,在45 ℃条件下按表2工艺参数以高速剪切制备初乳,而后加入水相1,调节溶液pH至6.0 ~ 8.0,加注射用水至终重后即得终乳。
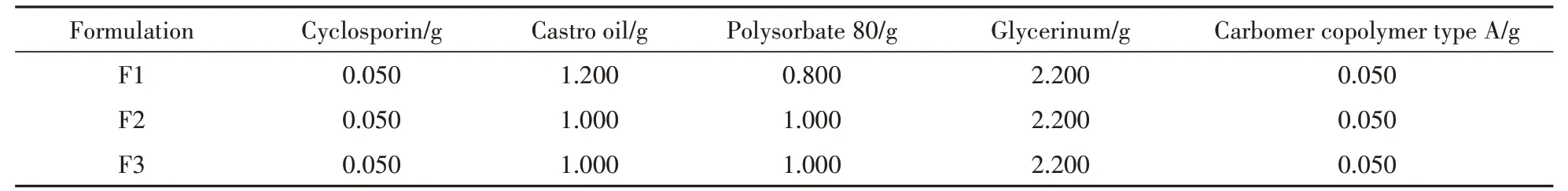
Table 1 Prescription composition and dosage of cyclosporin ophthalmic emulsion
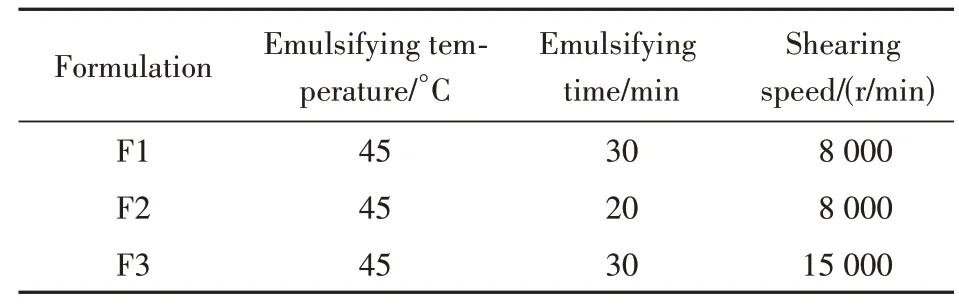
Table 2 Technological parameters of cyclosporin ophthalmic emulsion
2.4 EMD-PBE统计方法
对给定的参比制剂和受试制剂PSD 数据集,首先对所有参比样本PSD 求取平均值从而得到平均参比样本PSD,作为参比中心。然后应用EMD计算单个参比样本的PSD 到参比中心的距离,如[dR1,1,1,.....,dRi,j,k,.....],表示单个参比样本与参比中心之间的偏差。同样地,利用EMD 计算每个受试样本到参比中心之间的距离,如[dT1,1,1,.......,dTi,j,k,......],表示单个受试样本与参考中心之间的偏差(其中i、j、k分别表示批次、样本数、重复测量次数)。随后,利用PBE 对两组EMD 进行统计检验,以建立受试制剂和参比制剂之间的BE(图1)。利用PBE 处理一个多层次的数据结构(即,批次 × 样本 × 重复测量次数)。相比于直接比较两组PSD 曲线,本文中所使用的方法通过计算EMD 降低数据的维度,由此绕过多变量比较,并且比较了受试和参比之间的差异与参比内部的差异,所得粒径等效性结果具有真实性。
在此项研究中,采用动态光散射仪,以25 ℃测量角度173 ℃条件测定制剂粒径;所有样品均用超纯水稀释10倍后置于DTS0012样品池中。每批参比制剂取3 个样本,每个样本重复测定5 次。按照以下流程进行粒径PBE计算。
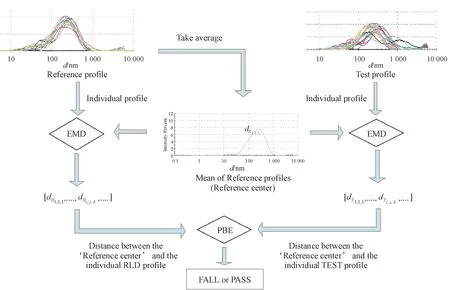
Figure 1 Schematic diagram of the proposed equivalence approach
3 结 果
3.1 参比制剂内部等效性结果
在本节中,在4 批参比粒径数据集中任选2 批作为R(R:参比样本),其余2 批作为T(T:受试样本),检查所提出的方法接受等效产品的能力(例如,参比制剂本身)。图2-A 显示了将参比制剂与自身进行比较的测试结果。可以看出,两个粒径分布图是重合的,有一些局部的变化,这表明即使参比制剂本身也存在一定程度的变化。然后将所提出的方法应用于选定的两组数据。图2-B 显示了参比样本粒径分布图(橙色)和受试样本粒径分布图(青色)到参比中心(即参考样本的平均值)计算的EMD距离。可以看到两组距离具有相似的范围(即低于0.28)。最后,将PBE 应用于两组EMD距离,根据判别标准,当σR< 0.1 时,选用常数标准,即Hη2= -0.019 12 < 0。参比制剂自身通过生物等效性验证,由此说明本研究应用的开发软件是可靠。
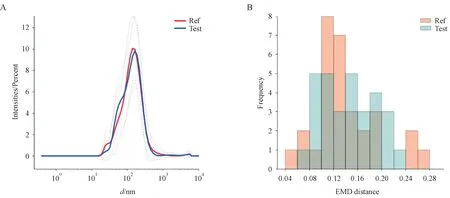
Figure 2 Comparison between two sets of the reference samples (two lots) by treating one of them as Test
3.2 受试制剂等效性结果
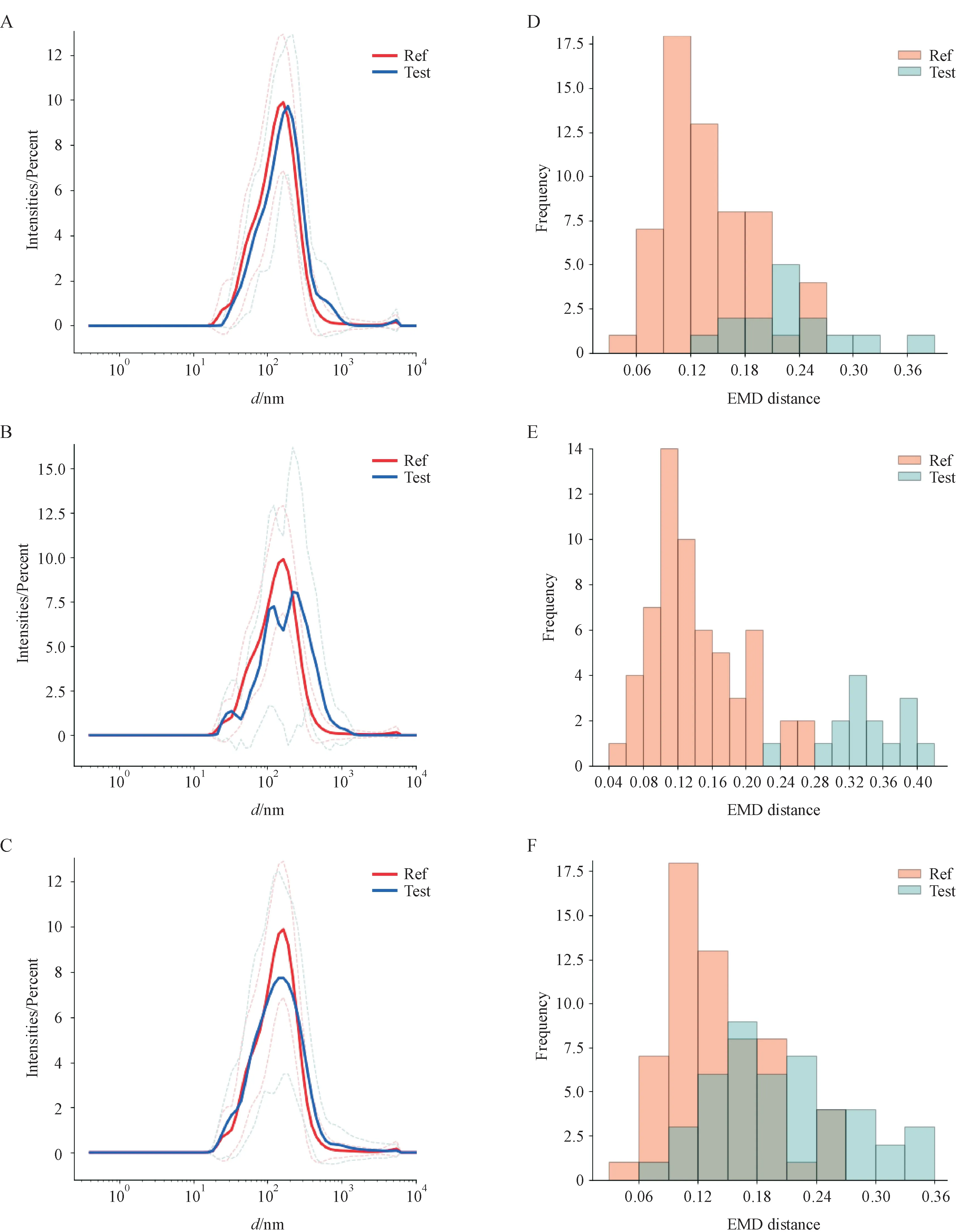
Figure 3 Comparison between the reference samples and test samples (F1-F3)
实验中,制备了不同处方用量和工艺参数的受试制剂,按照上述参数测定粒径,获得3 个受试制剂数据集,同时以4 批参比粒径数据参比数据集,分别应用EMD-PBE 统计软件进行分析。图3中A ~ C 分别表示处方F1 ~ F3 与参比制剂的PSD分布图;D ~ F 表示处方F1 ~ F3 与参比制剂EMD计算结果,可以看出,处方F1 和F2 与参比制剂的PSD 是不同的并且两者EMD 的范围也有很大的差异,同时计算结果显示两者均满足σR< 0.1,Hη2分别为0.005 102和0.035 99,均大于0,故未通过BE测试,由此也说明该方法具有良好的拒绝不等效产品的能力。处方F3 通过BE 测试,满足σR< 0.1,Hη2= -0.010 20 < 0。受试制剂F1 ~ F3处方用量及工艺参数的改变对粒径大小及粒径等效性均产生影响,借助EMD-PBE 统计分析方法,为仿制药开发中处方和工艺筛选提供一定的帮助。
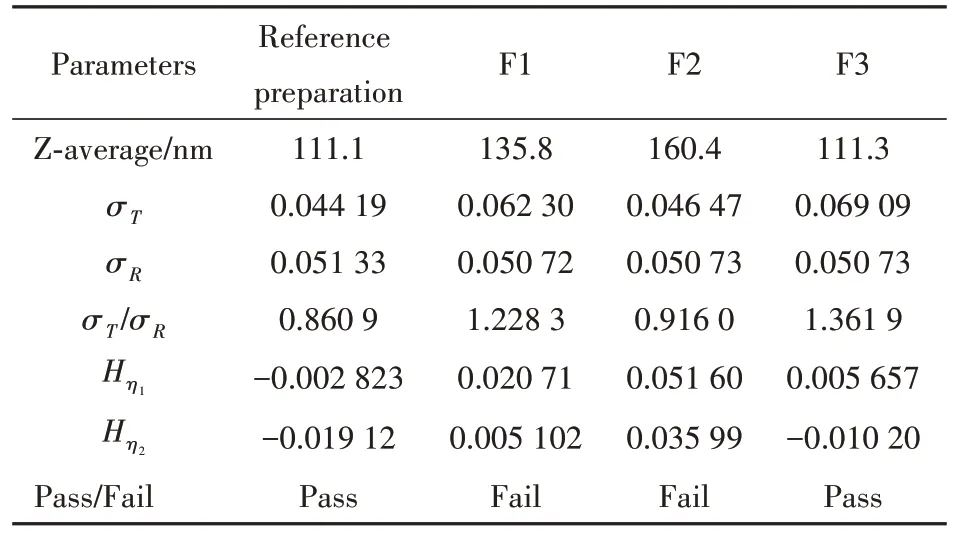
Table 3 Calculation results of equivalence parameters of test and reference preparations
4 讨 论
EMD 是衡量图像之间相似性的有效方法,虽广泛应用于计算机视觉应用,但使用EMD 来比较PSD 等效性未见文献报道。本研究应用基于Python 语言开发的EMD-PBE 统计分析软件,操作简单快捷,从上述结果可知该分析方法可有效通过粒径等效产品,拒绝不等效产品,为仿制制剂处方及工艺开发提供依据。
基于EMD的体外群体生物等效性的统计分析中,还有一部分内容可进一步深入研究:一是研究对象的选择,二是样本量的确定。本研究对象环孢素眼用乳剂粒径范围广泛[18](从几纳米到几十微米不等),导致其PSD 非完全单峰,故应用该统计方法分析PSD 是准确且可信的。在后续研究中,可选择更多其他呈现复杂粒径分布的纳米制剂进行评价。FDA 在布地奈德吸入剂草案(draft)中指出样本数量应选择不少于受试制剂和参比制剂各3 个批次,每个批次10 个样品数(即≥30 个样品)进行统计分析,并且每个样本进行3个阶段(包括制剂寿命初期、中期和末期)的研究,但是Chow等[19]认为 30 个样品数并不足以达到期望功效(80%),提高功效的方法有增加样品量或对于每个样品重复测量,目前对于样品量的计算暂无特定的指导标准。本研究中,由于参比制剂数量受限,故对每批参比制剂的每个样本重复测定5 次以提高功效,此外结合Hu 等[10]的计算,笔者认为这里的生命周期可以理解为重复测定次数。

