顶空-气相色谱法测定烷基糖苷中2种典型的残留脂肪醇
赵 静,卢 科,黄 飞
(浙江传化股份有限公司,浙江杭州 311215)
烷基糖苷(APG)是一种环境友好型的表面活性剂,由原料淀粉(或者葡萄糖)和脂肪醇通过直接苷化法制取;直接苷化法合成的产物必须经过脱醇和后处理等才能制成烷基糖苷成品[1]。APG 具有表面活性极佳、去污力强、复配性能好、对人体友好、生物降解迅速完全等优点[1-3]。脂肪醇的价格较高,残留的脂肪醇不仅会影响产品品质,也会增加生产成本。
残留脂肪醇含量是衡量APG 品质的重要指标之一,而关于测定APG 中残留脂肪醇含量的方法文献报道较少。目前主要参考GB/T 19464—2014《烷基糖苷》检测APG 中各残留脂肪醇的含量:利用萃取和气相色谱分析相结合的方法,对APG 中残留的脂肪醇组分进行分离和定量测定。该方法以正十一醇(C11)为内标物,用50 mL 含有二氯甲烷的石油醚在自制硅藻土层析柱内洗脱,接受液水浴蒸发至1~2 mL 后,进行气相色谱分析。该方法耗时费力、消耗大量有机溶剂、成本高,难以实现大批量检测[4]。另有相关文献报道了采用全挥发顶空-气相色谱法测定APG 中残留的脂肪醇(正辛醇与正葵醇)[5],该方法使实验操作变得简便,但是以异丙醇作为溶剂提取APG 中的残留脂肪醇,取上清液进行全挥发顶空-气相色谱法分析,预处理复杂,而且样品检测难以平行,对实验人员的要求过高,不利于日常常规检测。
本实验利用50%的N,N-二甲基甲酰胺-水混合溶液溶解稀释APG 样品后,经顶空恒温加热后自动进样进行气相色谱分析,建立了一种快速、简便、有效测定APG 中残留正辛醇(C8)与正葵醇(C10)的部分挥发顶空-气相色谱分析方法。
1 实验
1.1 试剂与仪器
试剂:N,N-二甲基甲酰胺(DMF,分析纯,西陇科学股份有限公司),正辛醇(C8)、正葵醇(C10)标准品(质量分数大于等于99.5%,上海麦克林生化科技有限公司),APG0810 系列小试样品(浙江传化化学集团),去离子水。
仪器:GC-2030 型气相色谱仪[岛津公司,配备氢火焰离子检测器(FID)和HS-10 型顶空自动进样器],DB-624 色谱柱(30.00 m×0.53 mm×3.00 μm)、20 mL 顶空瓶(美国Agilent 公司),高纯氮气瓶(N2纯度为99.999%,杭州今工特种气体有限公司),1 mL 移液枪(Eppendorf公司)。
1.2 溶液的配制
溶剂:用量筒分别量取等体积的N,N-二甲基甲酰胺和去离子水混合在烧杯里,搅拌均匀后冷却至室温,配制成50%的DMF 水溶液,作为本实验溶剂。
混合标准储备液(800 mg/L):分别准确称取0.08 g(精确至0.1 mg)正辛醇与正葵醇标准品于100 mL容量瓶,加入配制好的溶剂稀释、定容并混合均匀。
标准工作溶液:用溶剂将混合标准储备液稀释成40、80、200、300、400、600 和800 mg/L 系列溶液,建立标准工作曲线。
1.3 样品预处理
称取4.0 g(精确至0.1 mg)样品于50 mL 容量瓶中,用溶剂稀释、定容并混合均匀。用1 mL 移液枪移取1.0 mL 稀释液于20 mL 顶空瓶中,加盖密封,采用顶空-气相色谱仪进行检测。
1.4 色谱分析条件
顶空条件:平衡温度80 ℃,平衡时间30 min,样品流路温度120 ℃,样品传输线温度130 ℃,GC 循环时间50 min。
色谱条件:载气为氮气(纯度大于等于99.999%),恒流模式,流量1 mL/min;进样口温度300 ℃;FID 检测器温度300 ℃;分流比10∶1;色谱柱程序升温(初始温度100 ℃,保持1 min,以5 ℃/min 升温至260 ℃,保持10 min);进样量1 mL。
在该条件下,正辛醇与正葵醇的色谱分离保留时间分别为9.906、15.351 min。
2 结果与讨论
2.1 溶剂组成
正辛醇、正葵醇在水中的溶解度都非常小,而APG 分子由于具有高度亲水的基团易溶于水,不溶于普通溶剂[1]。因此,选择合适的溶剂尤为重要。结合溶剂沸点与对样品的溶解性2 方面的因素,选择50%的DMF-水混合溶液作为溶剂。此时DMF 能够有效地把2 种残留脂肪醇提取出来,而水分子可以有效地分散溶解APG 基质。
2.2 顶空平衡温度和时间
样品是否达到气液平衡与平衡温度和平衡时间都有关,考虑到温度过高会导致APG 样品分解,造成检测结果偏差,确定80 ℃为实验的顶空平衡温度。
不同顶空平衡时间下C8、C10 标准溶液顶空-气相色谱图见图1。
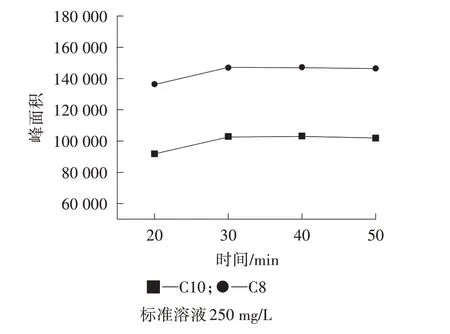
图1 不同顶空平衡时间下C8、C10 标准溶液顶空-气相色谱图
由图1 可以看出,在80 ℃平衡温度下,APG 样品中的2 种残留脂肪醇峰面积开始随着平衡时间的延长而明显增加(20~30 min);30 min 后,峰面积不再增加;50 min 时,峰面积减小,可能是因为平衡时间过长,顶空瓶内气密性变差。为了提高效率和响应灵敏度,保证气-液两相完全达到平衡,可以选择30 min作为顶空平衡时间。
2.3 毛细管柱
同时考察了市面上常见的RTX-1(非极性)、DB-624(中等极性)和DB-WAX(强极性)3 种毛细管柱对2 种残留脂肪醇的分离效果,结果如图2 所示。使用RTX-1 柱分析时,色谱峰灵敏度差、基线漂移严重;使用DB-WAX 柱分析时,保留时间长、灵敏度差;使用DB-624 柱对残留脂肪醇进行分析时,基线稳定,保留时间适中,灵敏度高,具有较好的分离效果,因此选择DB-624型毛细管柱作为分析柱。
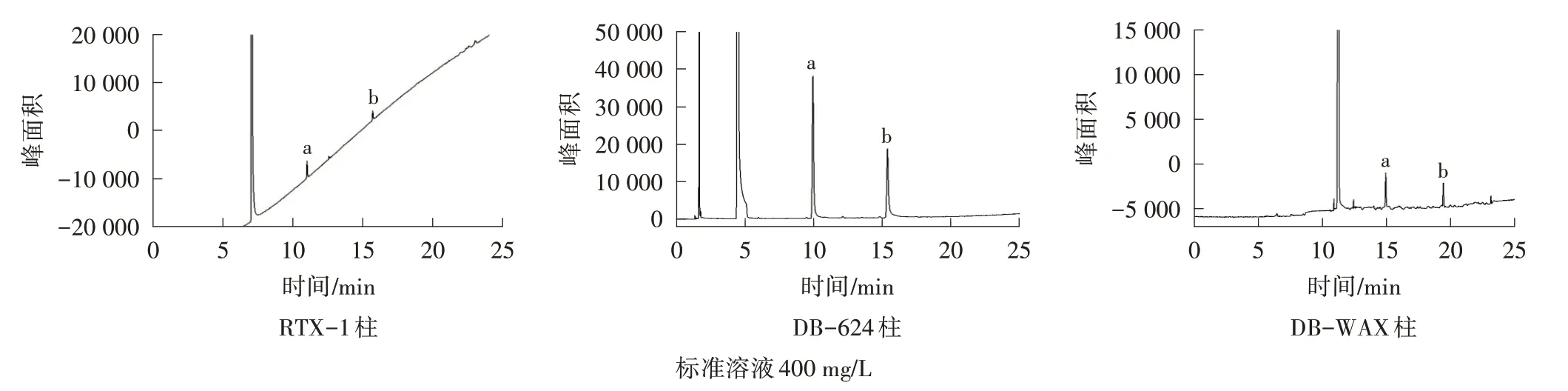
图2 3 种色谱柱条件下C8(a)和C10(b)标准溶液的顶空-气相色谱图
2.4 方法评估
2.4.1 线性方程、检出限、定量限以及精密度
由表1 可看出,2 种目标残留脂肪醇在一定质量浓度范围内均具有良好的线性关系,相关系数R2值均大于0.999 0。该方法C8 的检出限(S/N=3)与定量限(S/N=10)分别为2、10 mg/L,相对标准偏差(RSD,n=6)为1.1%;C10 的检出限(S/N=3)与定量限(S/N=10)分别为10、20 mg/L,相对标准偏差(RSD,n=6)为2.4%。说明本文建立的检测方法灵敏度较高、重复性较好,符合实际样品检测要求。

表1 HS-GC 方法的回归方程、相关系数、线性范围和检出限
2.4.2 加标回收率及精密度
取APG0810 系列小试样品,分别检测2 种残留脂肪醇的含量,APG 样品平行测定5 次。根据样品中2种残留脂肪醇的本底浓度值,向其中加入50%~150%水平的残留脂肪醇标准物质,考察方法的加标回收率和相对标准偏差(RSD)。由表2 可看出,APG 样品中C8 的加标回收率为95.5%~100.7%,相对标准偏差(RSD,n=5)为2.4%;C10 的加标回收率为90.1%~100.2%,相对标准偏差(RSD,n=5)为4.3%,符合日常检测准确度和精密度需求。
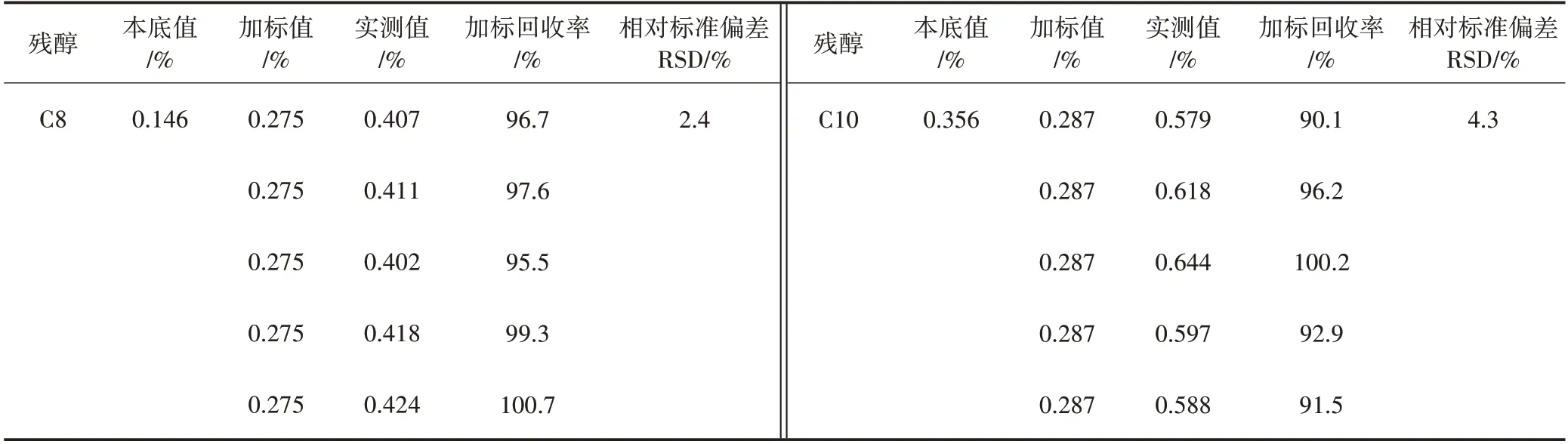
表2 HS-GC 方法检测APG 样品的加标回收率和精密度
2.5 实际样品检测
为了进一步验证方法的准确性,取5 个APG0810系列小试样品,分别参考本文所建方法(顶空-气相进样法)和GB/T 19464—2014 方法(国标法)检测2 种残留脂肪醇含量,对检测数据进行比较,以国标法检测的残留脂肪醇含量作为基准值计算相对偏差。由表3 可以看出,顶空-气相进样法和GB/T 19464—2014 检测2 种残留脂肪醇的含量具有一致性,相对偏差在可接受范围内,证明了方法的可行性。

表3 顶空-气相法和GB/T 19464—2014 检测2 种残留脂肪醇含量数据
3 结论
建立了一种有效检测APG 中残留脂肪醇[正辛醇(C8)与正葵醇(C10)]的方法。该方法利用50%的N,N-二甲基甲酰胺-水混合溶液作为溶剂溶解稀释APG 样品,结合部分挥发气相顶空进样的分析方法进行检测,具有快速、简便、环境友好等优点,适用于日常大批量检测APG 中的残留脂肪醇。

