利用MODDE软件全因子分析优化乙脑灭活疫苗的纯化工艺
李庆岸,于海,曹鹏,康文哲
(辽宁成大生物股份有限公司,辽宁沈阳 110179)
现行的乙脑灭活疫苗多采用生物反应器、细胞工厂或转瓶培养生产[1]。用生物反应器进行高密度微载体细胞培养乙脑灭活疫苗质量较高,而且已经实现疫苗生产的工业化和标准化[2-3]。但根据《中国药典》(2020版)三部的规定,其细胞蛋白质残留量不得高于2 μg/mL,细胞DNA残留量每剂应小于100 pg[4]。一般采用浓缩至一定体积后密度梯度离心或凝胶过滤层析的方法进行纯化,能去除大量的分子差异较大的细胞蛋白[5]。但对于分子大小或聚集体接近病毒分子的杂质,去除能力较差。因此,近年来研究人员聚焦于纯化工艺的创新,已经开发出一些现代化纯化工艺,比如离子交换、疏水/亲和层析方法等。
实验设计法(Design of Experiment,DOE)是一种基于统计学原理的设计实验的技术,可以用最少的实验确定关键性因素及其相互作用。本研究使用MODDE软件中全因子分析方法摸索Sartobind Q膜层析的工艺条件,以筛选Sartobind Q膜层析的关键工艺参数,并初步确定工艺参数范围
1 材料与方法
1.1 毒株及细胞
乙型脑炎毒种,P3株,中国药品生物制品检定所提供;Vero细胞,美国标准菌种保藏中心(ATCC)。
1.2 仪器与试剂
Sartobind Q膜,德国Sartorius Stedim公司;AKTA pure 150层析系统,美国GE公司;ABI 7500实时荧光定量PCR仪,美国Thermo Fisher公司;Vero残留DNA-154检测试剂盒,湖州申科生物技术有限公司;300 kDa的膜包,美国Millipore公司。
1.3 病毒原液的制备
Vero细胞使用微载体Cytodex1在7.5 L生物反应器内大规模培养,获得病毒收获液。
1.4 病毒灭活
将病毒收获液澄清后,经过300 kDa膜包浓缩约20倍,按β-丙内酯∶浓缩液=1∶4 000的体积比向病毒浓缩液中加入β-丙内酯;将病毒浓缩液在2~8 ℃冷库搅拌灭活24 h;灭活结束后,置于37 ℃下水解2 h,获得病毒灭活液。
1.5 疫苗纯化
将乙脑灭活液经过Sepharose 6 FF层析,洗脱液为 PBS缓冲液(含 0.3~0.7 mol/L NaCl,pH7.5),紫外280 nm下收集第一个吸收峰,即得乙脑病毒蛋白初步纯化液(S0)。
1.6 实验设计
对乙脑病毒蛋白初步纯化液(S0)进行Sartobind Q膜层析实验设计,如表1所示,采用4因素3水平全因子分析DOE模型进行实验,输入因子为上样量(40 mL 、70 mL 和 100 mL)、盐浓度(0.3 mol/L、0.5 mol/L和 0.7 mol/L)、pH(6.0、7.0和 8.0)、流速(1.0 mL/min、10.5 mL/min和20.0 mL/min),输出响应值为抗原回收率、细胞残留DNA去除率。本文所用Sartobind Q膜体积(CV)为1 mL,即上样量为40~100 mL,流速为 1~20 mL/min。

表1 乙脑病毒蛋白初步纯化液Sartobind Q膜层析DOE
1.7 中间产品成分检测[4]
1.7.1 乙脑残留DNA含量检测
PCR-荧光探针法检测Vero细胞宿主DNA。
1.7.2 乙脑灭活液、纯化液抗原含量检测
根据《中国药典》(2020版)三部的方法和标准,对乙型脑炎病毒抗原进行ELISA实验检测。
1.8 数据处理
使用层析系统控制软件自带的数据处理功能模块(赛多利斯MODDE®集成DOE软件包),将检测数据逐一输入对应的实验条件下,生成箱线图及响应曲面图并进行系统分析。
2 结果与分析
2.1 实验结果
实验的抗原回收率及DNA去除率如表2所示。使用Sartobind Q膜层析的目的是将细胞残留DNA从前一步纯化液中捕获出来。由于纯化液一般成分较复杂,病毒蛋白中混有宿主细胞残留蛋白、人血白蛋白和牛血清残留成分等,且样品体积较大,因此对于收率的要求为>90%,细胞残留DNA的去除率>90%。从表2的实验结果可以看出,在实验参数范围内,获得的产品纯度无显著差异,抗原回收率为100%,DNA去除率均在90%以上,满足Sartobind Q膜层析设计的要求。

表2 实验结果
2.2 输入因子与输出变量箱线图分析
图1为影响DNA去除率的因素箱线图。由图1可知,对于细胞残留DNA去除率,盐浓度是显著影响因子,盐浓度越接近0.3 mol/L,去除率越高,且上样量、盐浓度、pH、流速两两之间没有明显的交互作用;根据实验室多次测定结果,对于抗原回收率来说,上样量、盐浓度、pH、流速无显著影响,抗原回收率均达到90%以上(所用方法为半定量,数据未展示)。
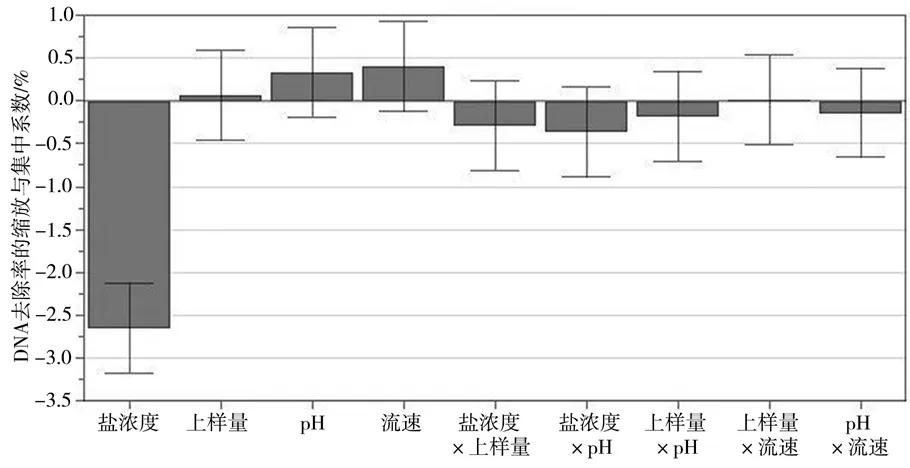
图1 影响DNA去除率的因素箱线图
2.3 响应曲面分析
从图2中可以看出,对于DNA去除率,盐浓度在0.3~0.7 mol/L、上样量40~100 倍膜体积范围内,宿主细胞DNA去除率在90%以上,盐浓度越趋向于0.3 mol/L,去除率越高,可以达到96%以上。

图2 DNA去除率的响应曲面图
3 结论
此纯化平台工艺是在原有乙脑灭活疫苗纯化工艺基础上,增加了Sartobind Q膜阴离子交换层析。利用细胞残留DNA在接近中性条件下大多带负电荷的特性,进一步去除原液中Vero细胞残余DNA,工艺去除率在90%以上;利用完整乙脑病毒颗粒分子量较大、不易结合在介质上的特点,采用直接流穿模式即可达到分离的目的,简化了实验参数设置。本实验通过DOE实验设计,成功地建立了一种乙脑灭活疫苗层析纯化工艺平台,使得产品的安全性得到了进一步的提高,而且减少了样品收集和上样的步骤,生产过程简单,优化了传统工艺,可用于Vero细胞大规模培养的乙脑灭活疫苗生产。

