腐植酸氧化还原特性的量子化学预测
T.A.Yarkova,A.M.Gyul’maliev 著 沈天瑞 周霞萍*译
1 莫斯科国立科技与管理大学 俄罗斯莫斯科 123110
2 俄罗斯科学院托普切夫石化合成研究所 俄罗斯莫斯科 119999
3 上海臻衍生物科技有限公司 上海 201700
腐植酸制剂的独特性质被广泛应用于国民经济的各个领域。腐植酸(HA)是一种多功能大分子混合物;在实际应用中,它们可以同时表现出氧化剂和还原剂的特性。HA 属于一类所谓的氧化还原聚合物,它可以从与其接触的离子或分子中动态可逆地转移电子。一些研究人员认为HA 是电子和自由基的供体或受体,而另一些人则认为HA 的标准氧化电位由顺磁中心的数量决定。有文献报道了有关HA 显著还原特性的数据:它能够还原金属离子,归因于它的碳水化合物成分。通过气体体积法研究,天然褐煤HA 及其酰化衍生物表现出抗氧化活性,与O2对异丙苯和乙苯的液相氧化有关。检测到HA 对碳氢化合物底物的氧化抑制作用,观察到的效果随着HA 浓度的增加而增强。抗氧化活性及其对浓度的依赖性也通过电流分析法和测压法确认。来源于各种类型泥炭的HA 对O2电还原的催化活性增加,这种实验方法很有趣,因为它允许使用电流强度-电压坐标曲线(伏安图)来获得微电极上被还原或氧化的电活性物质的定量信息。研究发现,随着抗氧化剂的加入,电活性成分(O2分子及其活性自由基,超氧阴离子O2-)产生的电流降低。我们假设这种抗氧化活性与O2和HA 中络合的中心金属原子的相互作用有关。在HA 的储存过程中,检测到抗氧化活性增加。有研究者将这种抗氧化活性与活性中心的释放联系起来。还有研究者假设络合形式的金属在引发或抑制氧化反应的过程中起主导作用。
HA 的高抗氧化活性使人们可以将它作为有前途的天然来源的纳米级抗氧化剂,并为开发用于生物医学目的的新型药物和新型纳米材料提供基础。它可用来治疗与身体氧化还原稳态破坏相关的病症。
在对HA 抗氧化活性进行广泛实验研究的背景下,阐明氧化还原过程中O2分子被HA 激活和抑制的机制无疑具有重要意义。有研究者详细研究了酶对分子O2的激活以及生物化学系统中自由基过程的启动和抑制。在一般情况下,氧化剂可以是亲电分子,例如中性的分子、自由基阴离子、自由基阳离子和Lewis 酸。
这项工作的目的是使用现代量子化学方法,从电子结构的角度研究HA 的氧化还原特性。这些方法以前应用于天然物质。为此,我们研究了HA 有机部分在分子O2氧化反应中的抗氧化性能的理论。由于O2分子负责生化过程中活性自由基的形成,因此有必要确定一种物质是否能够在其表面吸附(化学吸附)O2,并抑制自由基的形成。为了估算天然聚合物表面上O2分子的吸附能,实验使用了具有经验式C32H15O13N 的HA 结构片段模型。为了简化量子化学计算过程,测试片段(与先前提出的HA 的典型结构模型相反)主要由含O 和含N 的稠环、杂环和芳香环组成,分子O2可与之积极作用。为了比较HA 与其他物质的抗氧化性能,使用先前提出的方法,该方法通过量子化学反应活性指数来评估分子的抗氧化性能。
基于量子化学DFT ub3lyp/6-31g(d,p)方法使用软件包计算的最高占据分子轨道的能量EHOMO和最低未占据分子轨道的能量ELUMO,可确定以下反应活性指数:
绝对化学硬度按公式(1)计算。

绝对电负性按公式(2)计算。
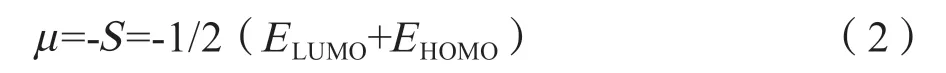
亲电性指数按公式(3)计算。

能量特性由以下众所周知的方程公式(4)(5)(6)(7)确定:
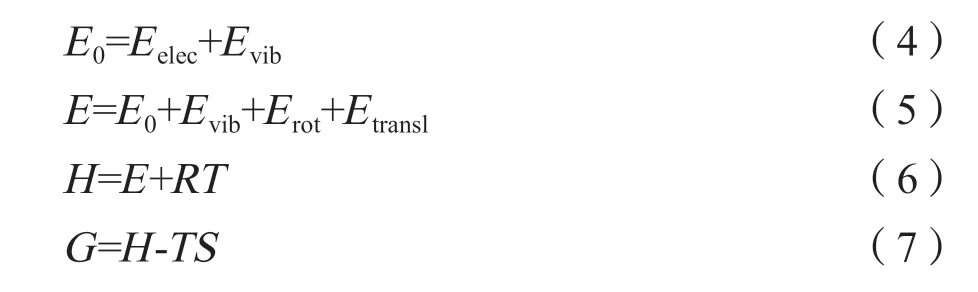
其中,Eelec是分子的电子能,E0是零振动能,Evib是分子在T=298 K 时的振动能,Erot是转动能,Etransl是平动能,H是焓,S是熵,G是吉布斯自由能。在软件包中,以上所有数值都以原子单位(a.u.)计算,1 a.u.=627.5095 kcal/mol。
表1 总结了采用量子化学DFT ub3lyp/6-31g(d,p)方法测定的HA 的结构片段、O 原子(O原子的基态术语符号为3P2)、多重性M=3 的分子O2和多重性M=2 的超氧阴离子O2-的反应活性指数(图1),以及一般公认为是抗氧化剂的反应活性指数。图1 显示了分子O2和超氧阴离子O2-稳定的能级以及电荷q和多重性M的变化。

表1 抗氧化剂的反应活性指数Tab.1 Antioxidant reactivity indices
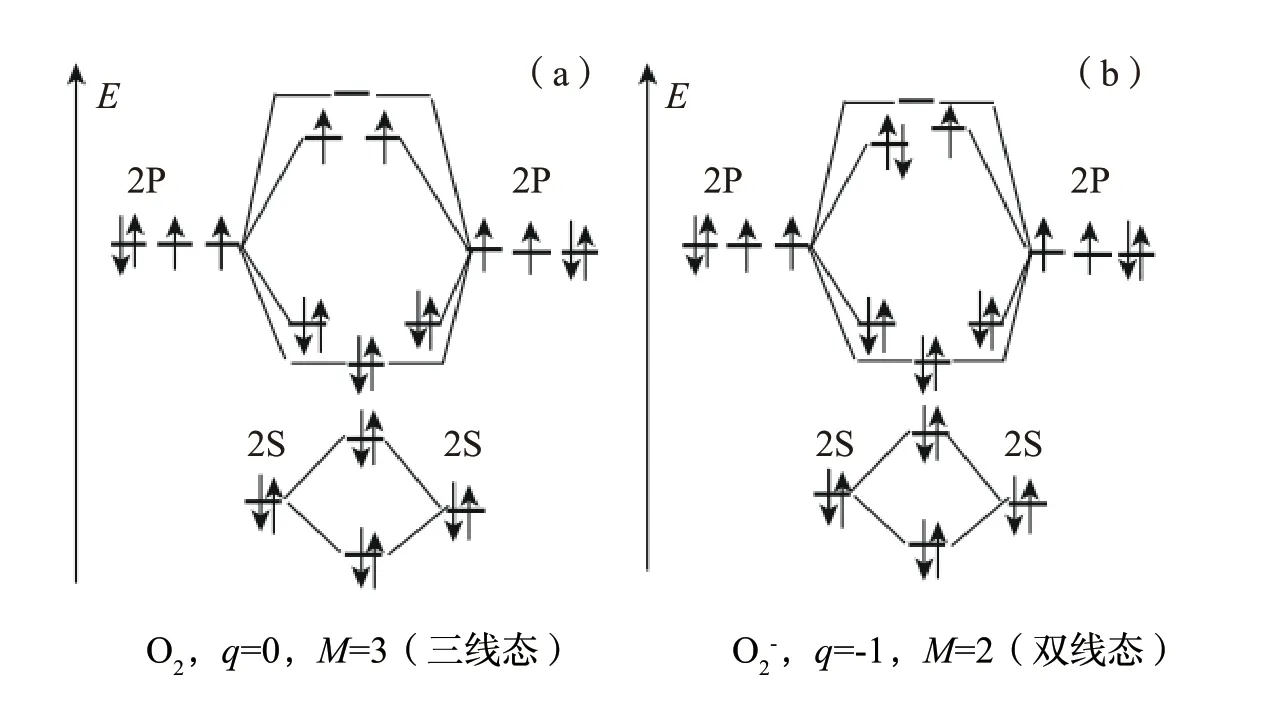
图1 分子O2(a)和超氧阴离子O2-(b)的电子构型Fig.1 Electronic conf igurations of (a) the molecule O2 and (b) the superoxide anion O2-
有趣的是,根据表1 和图2,O、O2和O2-的反应活性指数是不同的,它们在相关线上占据的位置也不同。因此,他们以不同的方式参与反应。表2 总结了氧的能量特性。
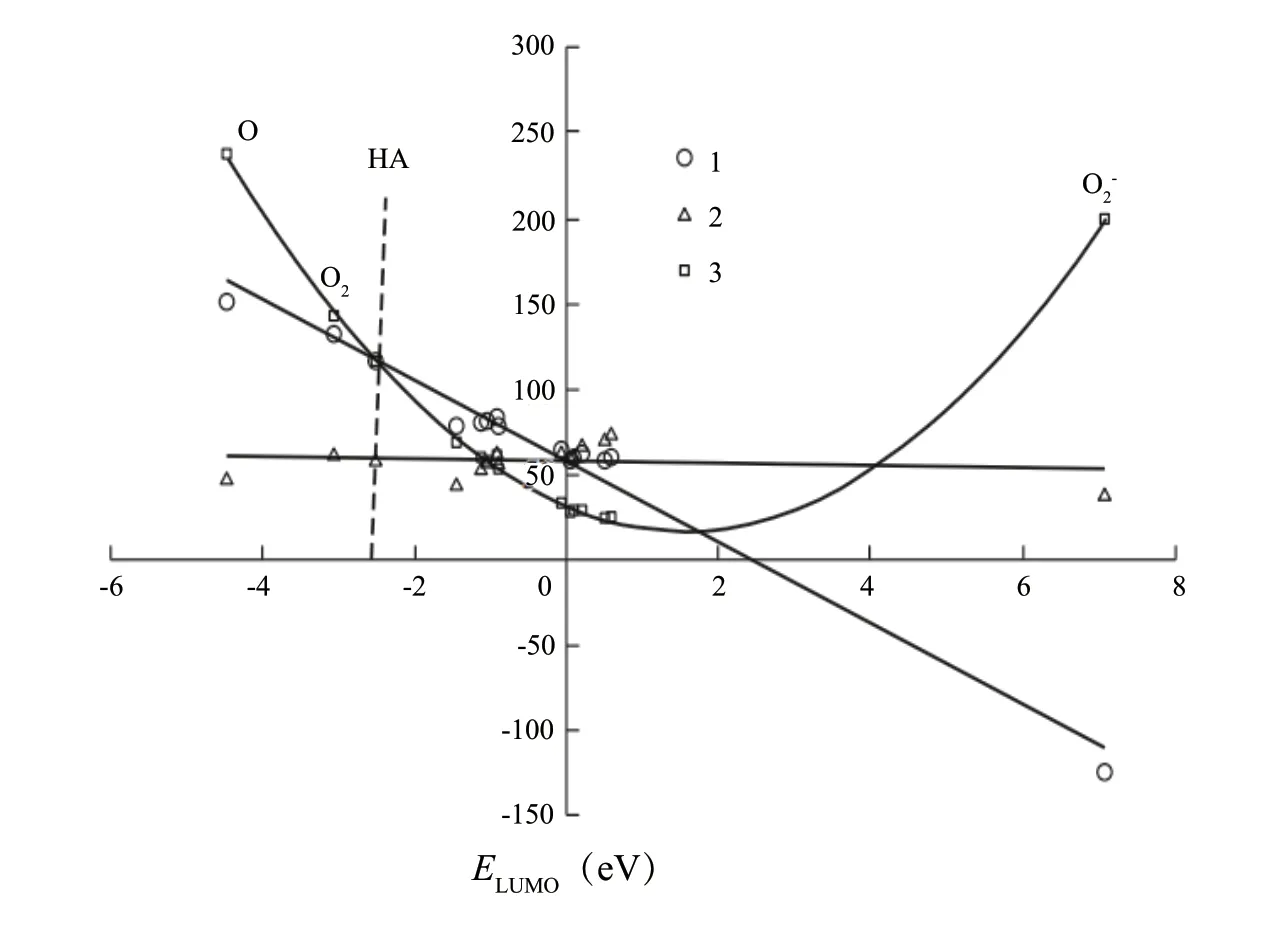
图2 抗氧化剂反应活性指数的比较分析:(1)电负性χ,(2)绝对化学硬度η 和(3)亲电性指数ωFig.2 Comparative analysis of the reactivity indices of antioxidants: (1) electronegativity χ,(2)absolute chemical hardness η,and (3) electrophilicity index ω

表2 O2、O2-和O 的能量特性Tab.2 Energy characteristics of O2,O2-,and O
图2 显示了电负性χ对能量ELUMO的依赖性,由以下具有良好相关系数的线性方程(8)描述:

根据定义,化学物质的电负性意味着吸引电子的能力,它随着ELUMO的降低而增加。电负性函数通过坐标系的原点,在那里ELUMO改变符号。添加超氧阴离子O2-后(表1),亲电指数ω对ELUMO的依赖性由以下二次函数方程(9)描述,其相关系数高于先前的报道:
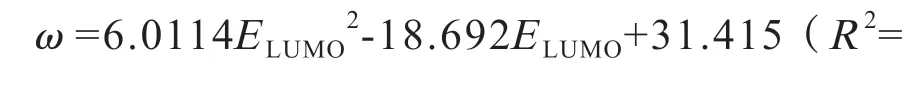

分析表明,电子受体分子(促氧化剂)和电子供体分子(抗氧化剂)都位于由函数χ=f(ELUMO)描述的直线上。负能量ELUMO的绝对值越大,物种的吸电子能力越明显。方程(8)和(9)以类似的方式描述了在本质上非常不同的化学物质的电负性和亲电性,具体为分子、超氧阴离子、O 原子、各种抗氧化剂和HA。在电子受体特性方面,HA 类似于分子O2。一个合理的问题产生了:由实验确定的HA 分子抗氧化特性(其抑制分子O2参与的氧化过程)是仅源于其组成中的金属离子的氧化还原反应性,还是源于其有机部分?HA 吸附活性O2分子并可以降低它们在反应介质中的浓度,起到氧化抑制剂的作用。该过程中HA 的活性由反应活性指数决定。分子O2在HA 上的吸附能通过量子化学方法pm6 计算。为此,研究了通过在HA的不同化学位点吸附O2而形成的络合物[HA…O2]以确定最低的电子能。但未能在文献中找到有关HA 吸附O2的实验数据。
所有情况下的O2分子都以三线态的基态出现。HA 与O2分子的结合能ΔE由下式(10)估算。
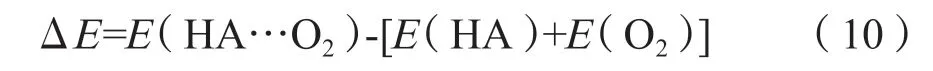
其中ΔE为HA 与O2分子的结合能,E(HA…O2)为络合物的总能量,E(HA)和E(O2)分别为HA 与O2的总能量。图3 中,∑E对应于独自的HA 和O2分子的能量之和,作为此后的参考点。在络合物(2)中,O2分子吸附在苯环的碳-碳键上(ΔE=-25.8 kcal/mol);在络合物(3)中,1 个O 原子指向3 个H 原子(ΔE=-62.8 kcal/mol);在络合物(4)中,O 原子指向苯环和羟基(ΔE=-4.4 kcal/mol);在络合物(5)中,O原子指向羟基(ΔE= -70.5 kcal/mol);在络合物(6)中,O 原子指向吡啶环的N 和H 原子(ΔE=-62.4 kcal/mol)。
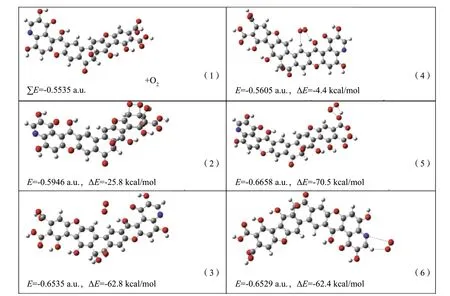
图3 在不同HA 位点O2 分子的配位能计算Fig.3 Evaluation of the coordination energies of O2 molecules at diff erent HA sites
因此,上述数据表明,O2在HA 分子不同位点上的吸附能有时是与化学键[络合物(3)、(5)和(6)]的能量相当。由此,可以得出结论,除了参与氧化还原反应之外,HA 在与分子O2的氧化反应中也表现出抑制剂的特性。这种可能性的出现是由于O2在天然聚合物的有机部分上的吸附(化学吸附),更具体的是在苯、吡啶环和羟基上的吸附。
参考文献(略)

