土壤铵态氮中氮稳定同位素比值测定前处理方法优化研究
袁红朝 贺 珍 张丽萍 耿梅梅 许丽卫 陈 闻 彭 灿 李春勇 王久荣*
(1. 中国科学院 亚热带农业生态研究所,亚热带农业生态过程重点实验室,长沙 410125;2.农业生态工程湖南省重点实验室,长沙 410125)
土壤中铵态氮以铵根离子(NH4+)形态存在,是植物可吸收利用的主要氮素形态之一[1],也是水体环境污染的主要来源[2]。稳定同位素氮示踪技术包括N自然丰度技术和富集标记技术,在土壤有机氮的周转、氮肥的使用效率、农产品的产地朔源以及氮素的淋失和面源污染等研究中得到广泛应用[3-8],而其中涉及NH4+—N同位素比值的精准测定。
目前,土壤铵态氮提取后不能直接进行稳定同位素比值检测,需要进行前处理。土壤铵态氮中氮稳定同位素比值测定的前处理流程主要包括:1)铵态氮的分离与吸收;2)将铵态氮制备成可供同位素质谱仪检测的样品。合适的样品前处理方法对样品质谱分析检测结果的准确性起着至关重要的作用[9-12]。其中,土壤铵态氮分离吸收的主要方法有:蒸气蒸馏法[13]和微扩散法[14]。传统蒸馏法单个样品的处理时间短,效率比较高,但实验过程操作繁琐、样品蒸馏之间会产生交叉污染,且无法实现批量样品处理;而扩散法仪器操作简单,可实现样品的批处理,但扩散培养耗时长(需要48 h及以上)。通过分离浓缩后的铵盐可通过元素分析仪-稳定同位素质谱仪联用进行15N丰度检测[9-10,15]或用化学方法将微量的铵转化为N2O气体,然后用带自动预浓缩装置的同位素比值质谱仪测定N2O 中的15N丰度[11-12]。相较于元素分析仪-稳定同位素质谱仪联用法进行15N丰度检测,需要50 μg氮量所产生的氮气才能进行15N丰度的精准测定,而通过化学方法将微量的铵转化为N2O气体再利带自动预浓缩装置的同位素比值质谱仪测定N2O 中的15N 丰度,检测限降低1个数量级[11,15]。但该方法N2O的产率最高仅为25%左右,有待进一步优化。
针对以上问题,本研究在上述方法[11-12,15-16]的基础上创新了蒸馏方法,大幅提高了样品的批处理效率,并对化学转化方法的条件进行了探索优化,建立一种快速蒸馏法结合高效化学转化的N2O发生的铵态氮中氮稳定同位素比值测定前处理方法。通过考察不同反应条件对铵态氮转化N2O产率的影响,明确了最适宜的方法条件。通过分析不同浓度条件下自然丰度、15N富集和标记的NH4+—N标准溶液对整个分析流程进行了方法学验证。同时还考察了该方法对于两种不同土地利用类型土壤铵态氮中氮稳定同位素比值测定的适用性。
1 实验部分
1.1 主要仪器与装置
PreCon痕量气体预浓缩装置配备(T1~T3冷阱),Combi PAL 自动进样器,96位气体样品盘,顶空瓶(12 mL),化学阱(填充高氯酸镁和碱石灰),PoraPLOT Q 色谱柱,He载气(气体纯度均>99.999%)。
稳定同位素比质谱仪MAT253:高灵敏度电子轰击离子源,10 kV 加速电压,C/N法拉第杯。质谱仪主机与外设的系统控制、数据采集和处理均由Isodat NT软件自动完成。
以上仪器均购自美国Thermo Fisher Scientific公司。
SEAL AA3流动注射仪(德国Norderstedt公司),Agilent 7890A气相色谱仪(美国安捷伦科技有限公司)。
全自动微量氮转化-N2O发生装置[15]:配备自动进样器,120位气体样品盘(与12 mL顶空瓶匹配),自动气体置换及注入系统和自动加液系统等。
全玻璃的半微量蒸气蒸馏器:全玻璃封闭型的半微量蒸气蒸馏器。
XS3DU百万分之一天平(梅特勒-托利多,感量0.001 mg)。
快速蒸气蒸馏及吸收装置(见图1):装置使用12 mL螺纹玻璃瓶作为反应瓶,配套螺纹密封盖;氨蒸气吸收器分为两部分,其中吸收槽为一体成型的丁腈橡胶空心柱体,柱体有内凹槽,可放置6~10 mm的玻璃纤维滤片,滤片上滴加30~50 μL H2SO4-Cu2+吸收液(1 mol/L),柱体的底部覆膜,可通气但不通水;顶部设计为密封垫片,防止氨蒸气逸散;干式恒温器配备64位的加热盘,与反应瓶匹配,控温范围为室温~150 ℃,温度为精度1 ℃。
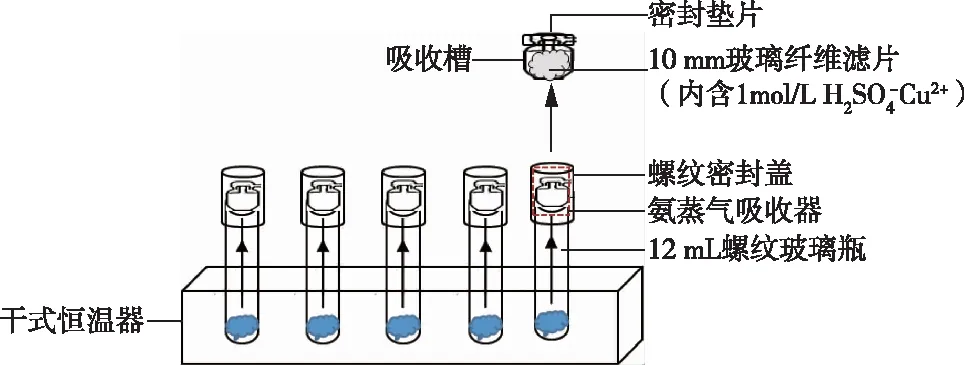
图1 NH4+—N 快速蒸气蒸馏及吸收装置 Figure 1 Fast steam distillation and absorption unit for ammonium-nitrogen.
1.2 主要试剂与材料
1.2.1 标准品
硫酸铵国际标准品:IAEA-N2(δ15Nair=20.3‰)、IAEA 305B(δ15Nair=375.3‰)和IAEA 311(15N=2.05 atom%),购于IAEA国际原子能机构。
硫酸铵实验室标准品(参考值为δ15NAir‰=-2.7),购于Sigma-Aldrich,纯度≥99.9%。
15N -硫酸铵标记材料:15N的丰度10.1 atom%(纯度≥99.5%;Sigma-Aldrich)。
硫酸铵标记溶液:用低丰度的标准溶液作为稀释剂,将10.1 atom%15N标准溶液制备成15N丰度2.0 atom%左右的硫酸铵标记溶液,其参考值为2.1 atom%。
氨基酸混和标准品:纯度≥99.5%,美国CIL剑桥同位素实验室公司。
1.2.2 前处理试剂及材料
氯化钾溶液(1 mol/L),氧化镁,碱性次溴酸钠溶液(含2 mmol/L Cu2+),具体配制参考已发表文章[15]。以上所需试剂均购于国药集团,为分析纯试剂;次氯酸钠溶液(有效氯4%~5%,Sigma-Aldrich)。玻璃纤维GF/D型滤片(Cat No.1823-142,Watman),实验用水均为超纯水(ELGA OQ015MMX1,电阻率18.2 MΩ.cm@25 ℃)。
1.2.3 土壤提取液制备
土壤样品采自中国科学院亚热带农业生态研究所桃源农业生态试验站的长期定位试验田(111°26′E,28°55′N)的稻田和旱地土壤,土壤具体信息参见表1。

表1 土壤基本理化性质
称取20.00 g(精确至0.001 g)土壤样品(研磨过2 mm筛,土壤含水量30%)于250 mL螺口聚乙烯瓶中,加入1 mL标记硫酸铵溶液(2.1 atom%,约1.0 mg铵态氮),然后立即加入100 mL氯化钾 (1mol/L)提取液,旋紧瓶盖,置于温控摇床中,在(20±2) ℃条件下以(220±20) r/min的频率振荡1 h,滤液保存于150 mL聚乙烯瓶备用,铵态氮含量用AA3流动注射仪测定。
1.3.4 参比气体
N2O 参比气体:参考值可溯源至法国液空公司的N2O 标准气体(Lot. 160-401912433-1),该N2O 参比气体的δ15NAir‰值为2.2‰±0.3‰。
1.4 实验条件及优化
1.4.1 铵态氮蒸馏
蒸气蒸馏法:土壤提取液中加入MgO,在弱碱性条件下铵态氮经蒸气蒸馏分离出铵态氮,铵态氮被滤片中硫酸溶液接收成铵盐。
反应方程式为:[NH4+]+[OH-]→H2O + NH3↑;NH3+[H+]→[NH4+]
本研究利用特制的快速蒸气蒸馏及吸收装置(见图1)替代了传统的半微量蒸气蒸馏法,分别选择硫酸铵和混合氨基酸标准品进行蒸馏时间和温度的实验,检验改进后方法的蒸馏效率。其中混合氨基酸较易高温水解为NH3,可作为主要的土壤可溶性有机态氮干扰源,评价检验改进后方法的蒸馏效率和有机态氮热水解的干扰程度。
1.4.2 铵态氮-N2O转化
铵态氮的转化-N2O产生法[11]:真空条件下,溶液中的铵态氮与碱性次溴酸钠反应,主要产生N2,另外产生一部分N2O。
反应方程式为:[NH4+]+[BrO-]→[Br-]+H2O + N2↑+N2O↑
参考ZHANG等[16-17]研究中次氯酸盐对[NH4+]具有更强氧化性能的表现,本研究选择次氯酸盐替代原方法的次溴酸盐,对化学转化反应条件进行摸索。由曹亚澄等[11]研究可知,该反应过程被Cu2 +催化,受氧化试剂浓度影响并与pH值有关。因此,考察了室温条件下,不同碱度和浓度的碱性次氯酸钠溶液条件下反应生成的N2O气体的浓度,以确定影响N2O产率的参数及最优反应条件。
1.5 铵态氮标准溶液及土壤样品前处理转化
在确定最优转化反应体系的基础上,对不同浓度梯度和15N丰度的硫酸铵标准溶液进行前处理。具体操作步骤如下:吸取15N系列硫酸铵溶液置于反应瓶中(12 mL螺纹玻璃瓶),反应瓶中氮量分别0.5和1.0 μmol,称取3 mg MgO(按照3 g/L用量)加入反应瓶后安装好氨蒸气吸收器及螺纹密封盖。将反应瓶放置在干式恒温器上120 ℃下蒸馏20 min。蒸馏结束冷却后,用镊子将滤片取出放入另一洁净的反应瓶中盖上密封瓶盖,转移至全自动微量氮转化-N2O发生装置抽真空后,利用装置的加液模式向反应瓶中依次加入1 mL反应试剂(碱性次氯酸钠溶液或碱性次溴酸钠),最后注入20 mL的惰性He气。每组标准样品重复6次。反应生成的N2O气体的浓度和15N丰度分别用气相色谱仪和带自动预浓缩装置的同位素比值质谱仪测定。
依据土壤铵态氮含量,取1~2 mL土壤浸提液(pH值范围6.0~8.0,否则需要调节pH值,或者加入合适的pH值缓冲溶液)置于12 mL反应瓶中,操作同标准样品,每组样品重复6次,同时做试剂空白(本研究中试剂空白本底未检出)。
1.6 PreCon-IRMS测定15N—N2O丰度的仪器工作条件
预浓缩装置气体流速(He载气:20 mL/min),冷阱T2浓缩时间180 s,冷阱T3浓缩时间300 s,色谱柱温度30 ℃。待仪器稳定后,将气体样品置于Combi PAL 自动进样器上,气体样品经过化学阱除去大部分的水汽及二氧化碳干扰气体后依次通过T2/T3冷阱浓缩。浓缩后的含N2O的混合气通过气相色谱柱分离,依次进入稳定同位素质谱仪检测N2O得到15N丰度。
1.7 统计分析
所有测定结果均为6次重复的平均值。使用SPSS 16.0统计软件,数据采用统计描述、方差分析(one-way ANOVA)和Duncan检验。
2 结果与讨论
2.1 铵态氮的蒸馏效率
不同蒸馏条件下,铵态氮标准溶液的回收率为35.3%~100.1%(见表2)。铵态氮的回收率同时受蒸馏温度和时间的影响。一般情况下,提高蒸馏温度和延长蒸馏时间可提高铵态氮的回收率,当温度达到120 ℃及蒸馏时间为20 min时,回收率可达99.6%~100%,延长蒸馏时间,铵态氮的回收率没有显著变化。此外,在相同蒸馏条件下,不同氮含量硫酸铵标准样品的蒸馏回收率基本一致。混合氨基酸样品在80 ℃下未发现明显水解现象,当温度达到100至120 ℃后,水解程度逐渐增加,在温度120 ℃和蒸馏时间为30 min时达到最大值1.1%左右,并已对铵态氮蒸馏提纯产生干扰。因此,最优蒸馏条件为:120 ℃下蒸馏20 min。本研究确认的最优蒸馏时间与传统蒸馏法单个样品的处理时间基本一致,但提高了前处理的样品通量和分析效率。
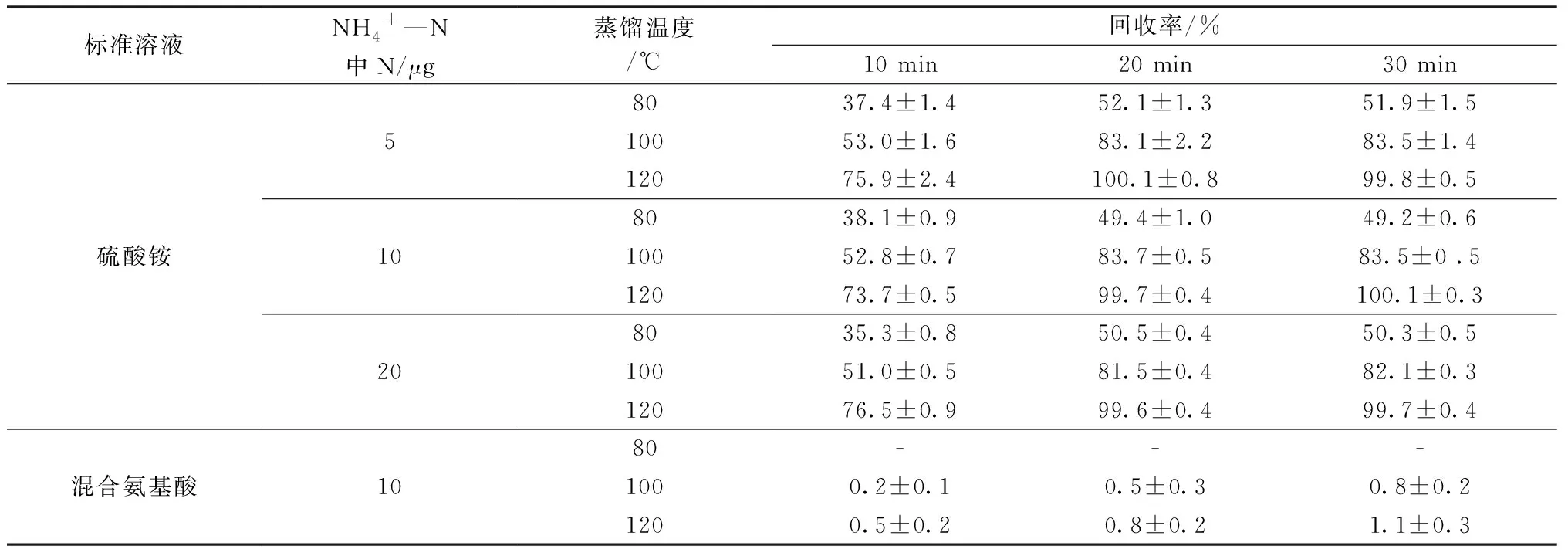
表2 不同蒸馏条件下铵态氮的回收率
2.2 铵态氮化学转化过程中N2O产率的影响因素
研究中采用氧化性更强的次氯酸盐替代原方法的次溴酸盐,考察了不同次氯酸钠浓度和碱度对铵态氮转化生成的N2O气体产率的影响,结果见表3。
研究发现碱性次氯酸钠反应体系中,不同反应条件下铵态氮转化生成的N2O气体产率在20.5%~62.3%(表3)。同等碱度条件下(NaOH浓度10 mol/L),次氯酸钠浓度对铵态氮转化生成的N2O气体产率影响显著,其中30 mmol/L氯酸钠浓度的N2O气体产率最高,而降低或者升高氯酸钠浓度,铵态氮转化生成的N2O气体产率均会显著下降,与ZHANG等[16]的研究结果一致。铵态氮转化生成的N2O气体的产率同时还受反应体系碱度的显著影响,当升高NaOH浓度,铵态氮转化生成的N2O气体产率升高,并在10 mol/L时达到最大值,与曹亚澄等[11 ]和LAUGHLIN[12]结果一致,但产率较原方法的25%提升至60%以上。而当继续提高NaOH浓度,铵态氮转化生成的N2O气体产率显著下降。因此,实验最终选择氯酸钠浓度为30 mmol/L,NaOH浓度为10 mol/L。
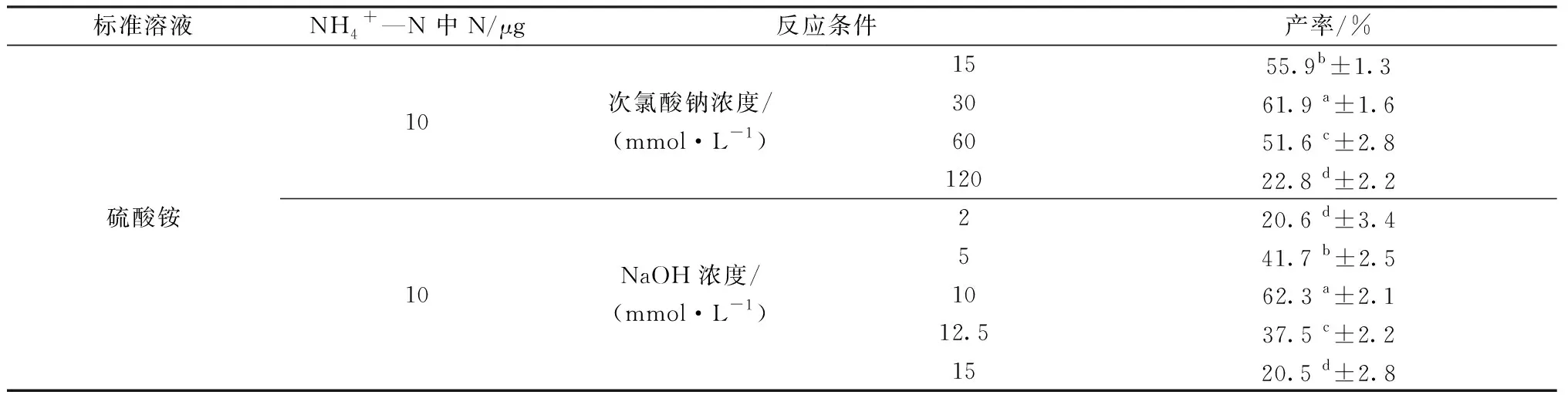
表3 不同反应条件下铵态氮转化生成的N2O气体产率
另外,本研究还考察了最优反应条件下,不同浓度的铵态氮标准溶液转化生成的N2O气体的产率,结果见图2。铵态氮转化生成的N2O气体产率为25.1%~62.1%,且随反应体系中铵态氮浓度的增加而升高,当反应体系N终浓度为0.5 μmol/mL 时,铵态氮转化生成的N2O气体产率达到最大值,且基本稳定,不再受铵态氮N浓度的影响。此外,在保证质谱最低检测限的基础上(12 mL进样体积,保证N2O气体浓度为1.0 μmol/mL以上),反应体系中总氮量不再是铵态氮转化生成的N2O气体产率的制约因子。当总氮量小于0.5 μmol时可考虑减少反应体系体积以增加体系中铵态氮浓度,保证铵态氮转化生成的N2O气体产率最高。

图2 不同浓度的铵态氮标准溶液转化生成的N2O气体产率Figure 2 Yields of N2O production under different concentrations of NH4+—N.不同字母代表处理之间差异显著,p<0.05Letters a,b,c represent significant differences of individual parameters between different treatments by Duncan′s test (p<0.05)
2.3 测定铵态氮中15N比值的精密度和准确度
不同氮含量和15N丰度的硫酸铵标准溶液经过前处理后结合气体预浓缩装置与稳定同位素质谱仪(PreCon-IRMS)联用系统测定其15N丰度,每组测试6 次,获得的测定结果见表4。当体系中的NH4+—N浓度不低于0.5 μmol/mL时,所有标准硫酸铵样品15N比值均能获得较好的精密度和准确度。其中自然丰度和低富集样品的精密度为0.2‰~0.4‰。对于高丰度的标记样品,精密度为0.001 atom%~0.003 atom%(CV在0.1%~0.3%之间)。所有标准品的15N丰度测定值均与参考值一致。
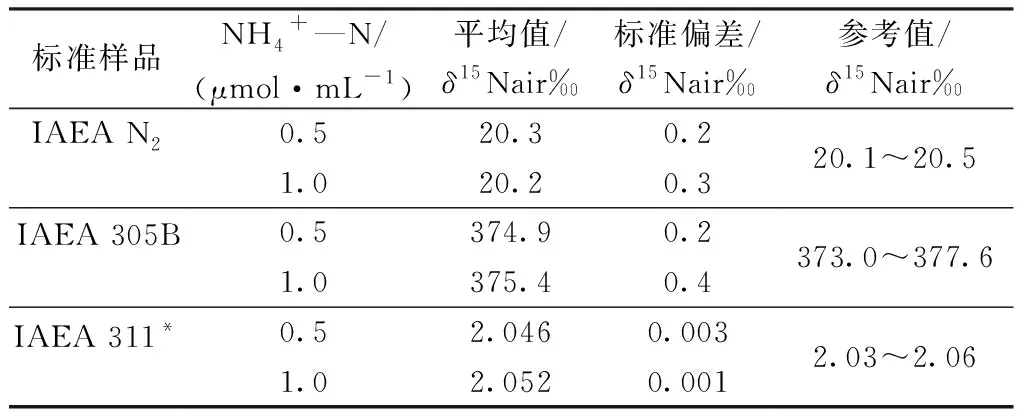
表4 不同铵态氮含量和15N丰度的硫酸铵标准溶液15N比值测定的精密度和准确度
2.4 土壤浸提液铵态氮中15N丰度的测定
分别采用新建的方法和原方法对两种不同土地类型稻田和旱地土壤的铵态氮进行前处理后测定其15N丰度,结果见表5。两种土壤的15N丰度值在2.067 atom%~2.081 atom%,与添加的外源氮15N丰度值基本一致(2.1 atom%),土壤本底NH4+—N对其的稀释作用较小。两种前处理测定土壤浸提液铵态氮中15N丰度的精度均较为理想,为0.002 atom%~0.013 atom%,其中新方法的精度(CV<0.2%)优于原方法(CV>0. 5%),可完全满足相关科研工作的需求。
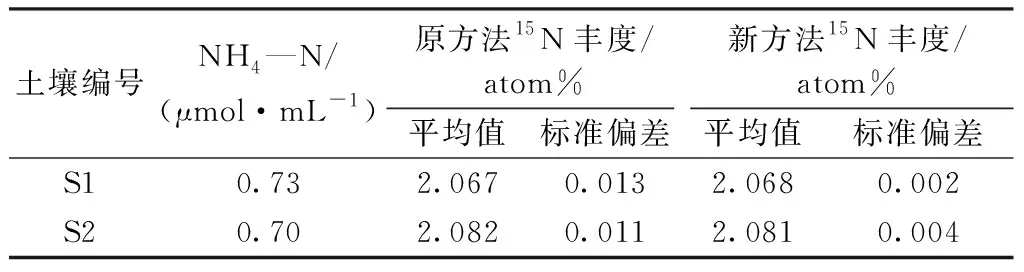
表5 新方法和原方法测定两种不同土地利用类型土壤浸提液铵态氮中15N丰度
3 结论
蒸馏法结合N2O 产生法是目前应用较广泛的土壤铵态氮15N同位素丰度测定前处理方法。改进后的蒸馏法在120 ℃,蒸馏20 min条件下的铵盐回收效率可达99%以上,且可以实现批量铵态氮的分离纯化,减少了样品之间的交叉污染。优化后N2O 产生法的最优条件为次氯酸钠浓度为30 mmol/L,NaOH浓度为10 mol/L。反应体系中总氮量不再是铵态氮转化生成的N2O气体产率的制约因子,仅需保证反应体系铵态氮浓度为5 μmol/mL及以上,铵态氮转化为N2O的产率可达60%以上,且测定不同15N丰度的标准样品均能获得较理想的分析精度和准确度,无分馏现象发生。基于优化后的前处理方法建立的铵态氮中氮稳定同位素丰度分析系统测定精度优于原方法,且前处理分析时间短,测试样品通量大,降低了测试精密度对人员操作熟练程度的依赖。新方法的建立将有助于推进土壤有机氮矿化、周转及其影响机制等研究的开展。

