超声引导下经皮经肝注射吲哚青绿在腹腔镜解剖性肝切除中的应用
罗水莲,柯茜茜,黎 萍(通信作者)
(武汉大学中南医院综合超声医学科 湖北 武汉 430071)
解剖性肝切除术,包括切除所有由门静脉分支供应至肿瘤所在区域的肝实质,是治疗肝细胞癌的有效方法,它提高了患者总生存率,可减少局部复发,改善预后[1-2]。实施解剖性肝切除术面临的一个主要问题是要切除体积的肝表面及节段间的分界。既往研究表明通过注射染色剂能够解决这一难题。Takeshi Aoki等研究结果显示通过门静脉注射吲哚青绿(indocyanine green,ICG)的红外观察摄像系统是一种可靠的术中鉴别肝段和亚段的技术,可用于解剖性肝切除[2]。基于肝脏解剖结构的个体差异,肝内血管变异较多,结构复杂,超声引导下精准定位并成功引导穿刺目标肿块所在肝段门静脉及其分支仍具挑战。自2019年起,武汉大学中南医院采用了在超声引导下经皮经肝注射吲哚青绿联合腹腔镜技术对肝癌患者进行解剖性肝切除术,取得良好效果,超声引导技术不断改进。本文回顾了2019年1月—2022年6月20例在武汉大学中南医院肝胆胰外科行腹腔镜技术联合超声引导经皮经肝门静脉注射吲哚青绿解剖性肝切除病人的临床资料。探讨超声引导下经皮经肝注射吲哚青绿技术在腹腔镜下解剖性肝切除术手术中的应用价值。
1 资料与方法
1.1 一般资料
选取武汉大学中南医院2019年1月—2022年6月期间在超声引导下经皮经肝注射ICG荧光成像指导腹腔镜下肝脏肿块切除术的20例患者为研究对象,其中男性14例,女性6例;年龄为44~69,平均(56.22±8.26)岁;乙型肝炎表面抗原(HBsAg)均为阳性,病理检查结果均为Ⅱ级肝细胞肝癌,其余肝实质呈肝硬化图像;肿块均为单发结节,平均大小为(3.78±1.55)cm,大多位于肝右叶,其中2例位于左内叶,7例位于右前叶下段,8例位于右后叶下段,3例位于右后叶上段。
1.2 方法
使用的彩色多普勒超声诊断仪为GE,型号LOGIQ E9,C5-1探头,探头频率为(1.0~5.0)MHz。超声引导经皮经肝注射吲哚青绿方法及操作:结合磁共振图像,超声重点观察肿块大小、肿块及其所在肝段供血门静脉主支及其侧支、拟穿刺门静脉最佳穿刺点及该处内径、穿刺途径血管分布情况。调节患者体位,在避开途径血管的前提下,选择最佳皮表穿刺点和穿刺路径,采用22G-PTC-B针,针尖斜面朝向门静脉远心端的穿刺方向,在实时超声监测下穿刺针尖依次穿过皮层、肝实质到达目标门静脉,拔出导丝可见血液回流,连接吲哚青绿注射剂,在3~5 min内匀速缓慢推注染色剂1 mL。注射过程中根据染色剂自显影情况在二维灰阶图像条件下实时监测门静脉内染色剂流向,观察是否存在反流。拟穿刺目标门静脉均注射后,于腹腔镜荧光成像系统下观察目标肝段染色效果,肝表面分界及肝段分界情况。
1.3 术后处理
观察随访患者术后转归情况;术后肿瘤病理组织学类型及相关分级。
2 结果
20例患者在超声引导下实行了经皮经肝吲哚青绿门静脉注射,18例目标节段肝表面分界及肝段分界较明确,成功指导了腹腔镜下解剖性肝切除术的顺利实施;2例则全肝染色,未达到目标肝段阳性染色结果,且术中出现大出血现象,实施了中转开腹手术,其中1例因失血过多失血性休克死亡。
超声引导吲哚青绿注射门静脉穿刺点的选择:4例选择了4支肿块所在门静脉,10例选择了3支肿块所在肝段直接供血门静脉,6例选择了2支肿块所在肝段直接供血门静脉,20例均选择了肿块主要供血门静脉;超声所见肝脏肝段解剖学分界为起点,均以门静脉入目标肝段起始点约1 cm以内为穿刺点,针尖斜面朝向门静脉远心端,穿刺方向与所穿刺门静脉长轴角度介于30°~45°。二维灰阶超声实时监测吲哚青绿注射期间穿刺针针尖于门静脉管腔内均可清晰显示,均可见从针尖向目标门静脉远心端流向的染色剂自显影,其中1例可见沿门静脉近心段流向显影,1例可见肝静脉显影。见图1、图2。
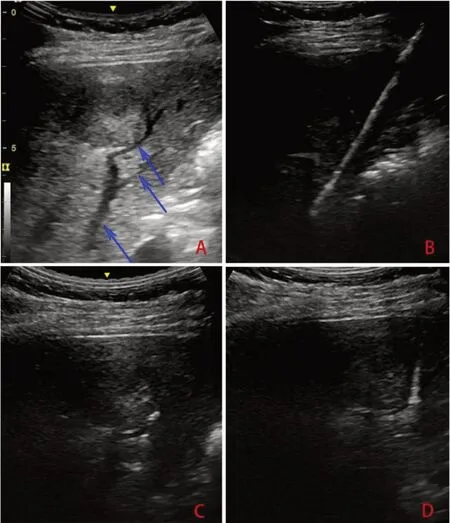
图1 二维超声评估显示目标门静脉及穿刺成功图
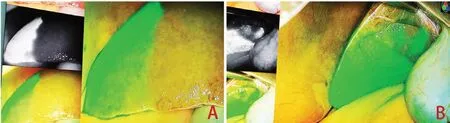
图2 荧光影像系统下目标肝段脏面及膈面吲哚青绿染色效果图
3 讨论
肝细胞肝癌(hepatocellular carcinoma,HCC)是世界上第六大最常见的恶性肿瘤,也是癌症相关死亡的第四大原因[3]。解剖性肝切除术(anatomical liver resection,ALR)是原发性肝肿瘤的既定手术,在保留残肝结构完整性的同时,完全切除携带肿瘤的肝段,有利于提高患者的生存率,改善预后。为了提高解剖性肝切除术的可行性和准确性,既往研究探索了不同染色剂在手术过程中的应用,对比显示,吲哚青绿(indocyanine green,ICG)在解剖性肝切除术中具有更大的应用潜能和更高的成功率[1-2,4-6]。2008年Aoki率先报道了ICG在开腹解剖性肝切除术中的应用[4],而后Ishizawa于2012年首次报道了ICG于腹腔镜下解剖性肝切除的使用[6]。ICG染色的基本策略包括反染法(负染法)和正染法。李等报道了通过阻断目标肝段肝蒂后经外周静脉注射ICG,除荷瘤区外对整个肝脏进行染色(反染),应用荧光成像指导有助于腹腔镜肝段切除术的安全实施[7]。但是反染法不能充分划分节段间平面、精确划分实质,时常肝蒂阻断区域可见染色或荧光染色渗透扩散,该方法更适用于较大范围的肝切除术。而术中穿刺目标肝段门静脉分支并注射ICG(正染),更有助于肝段分界和节段间分界,有利于肝段和亚肝段切除术。但是正染法对于目标门静脉的选择和成功穿刺具有较高的要求,存在因目标肿块分支较多或门静脉分支较细等穿刺困难或目标区域不染色等问题[8]。管加福等运用3D可视化技术重建病人肝脏及血管虚拟模型,并利用虚拟模型指导术中超声引导下向目标门静脉并注射ICG,降低术中穿刺染色的技术难度,保证解剖性肝脏切除的完成[9]。本文通过对正染法指导的腹腔镜解剖性肝切除病例回顾性研究分析认为,术前结合增强CT、磁共振等影像技术,在超声下寻找目标肝段主要供血门静脉及其分支,评估拟穿刺门静脉数量及穿刺路径,对于术中穿刺成功具有重要的指导意义。术中穿刺过程中选择粗细合适的穿刺针及穿刺角度,即22G的PTC-B针,在30°~45°之间的角度进针,能够提高目标门静脉的穿刺成功率。在目标门静脉分支根部以远0.5~1.0 cm部位点穿刺,针尖斜面朝向门静脉远心端,3~5 min内缓慢推注ICG,同时根据二维超声染色剂自显影现象观察染色剂流向,一旦发现反流则立即停止注射,能够较好地避免染色剂反流、染色效果不均匀、目标肝段不明确或因操作不当导致的全肝染色问题,提高染色成功率。
吲哚青绿染色指导的解剖性肝切除术优于常规的肝切除术,吲哚菁绿荧光染色已成为精准腹腔镜解剖性肝切除术的重要技术手段[10-13]。隋明昊等研究显示,吲哚青绿荧光融合影像技术对于腹腔镜肝切除术中肝段边界的清晰显示可达95%[14]。同时,相关报道表明,在肝切除术中,ICG荧光染色总体成功率可至88.0%[15]。本研究共纳入ICG染色指导的腹腔镜解剖性肝切除患者20 例,18例染色效果较好,具有较清晰的目标肝段染色分界,其中2例则染色失败,明显的全肝染色。回顾分析,其中1例在术中经皮经肝超声引导穿刺过程中将肝中静脉误认成门静脉。众所周知,肝静脉为出肝血流,因此,即使术中我们在二维超声染色剂自显影下及时发现反流且意识到目标静脉错误并立即停止ICG注射,但仍造成了不可逆性的全肝染色。另1例全肝染色患者,术前评估以及术中穿刺均成功,按常规速度及浓度推注ICG时,每一支目标门静脉在二维超声染色剂自显影下均可见少许反流,虽及时停止,依旧导致全肝染色。全肝染色的2例患者在术中均出现了大出血现象,施行了中转开腹手术,始终存在少许反流的全肝染色患者发生了失血性休克,最终死亡。结合患者肝硬化病史特征,我们猜测该患者可能存在门静脉-肝静脉瘘,或由于先天血管发育异常或因门脉压力过高所致。在肝硬化门脉高压症患者中,门静脉到腔静脉系统的分流非常常见,肝内门静脉-腔静脉之间的分流可能是先天性的,也可能为肝硬化、门脉瘤破裂等后天形成[16-17]。本研究样本量纳入过少,该类染色失败原因有待进一步的研究及探索。
综上所述,超声引导经皮经肝注射ICG是一种简单、有效、方便的方法,可在肝表面和节段间形成较清晰的目标肝段ICG阳性染色荧光成像,能够提高肿瘤所在节段腹腔镜解剖性肝切除术的准确性,有助于手术的安全实施。ICG肝段染色技术仍处于探索阶段,本研究患者例数较少,有待更大样本的研究。

