生物表面活性剂稳定的纳米铁溶胶的制备与破乳性能评价*
邹 静,胡语婕,佘跃惠,张 凡,黄培秀,曲瑞雪,王正良
(1.长江大学化学与环境工程学院,湖北荆州 434100;2.长江大学石油工程学院,湖北武汉 430100;3.中国地质大学(北京)能源学院,北京 100083;4.非常规油气湖北省协同创新中心,湖北武汉 430100)
0 前言
在石油和石化行业中,各种破乳剂受到极大的关注[1]。油水乳化液在运输过程中会加快管道腐蚀[1-3],并在石油炼制精炼过程中导致催化剂中毒[4-11]。在许多行业中,特别是在石油和天然气行业,破乳是非常重要的。已有很多关于物理和化学处理破坏高度稳定的乳液并实现油水分离的研究[5,12-20],但物理方法昂贵,化学方法污染严重。因此,需要找到经济且环保的破乳方法和破乳剂,以实现工业化应用。
近年来,磁性纳米粒子作为破乳剂应用的研究进展迅速[21]。磁性纳米粒子对外部磁场快速响应,容易被磁力从复杂的环境中分离出来,因此其在处理含油废水方面受到了很大关注[6,22-29]。用溶剂热合成法获得的磁性纳米粒子已很好地应用于乳化油水混合物的处理和分离[21]。Li 等[30]通过该方法合成了Fe3O4磁性纳米粒子,实现了石油和水的分离。溶胶-凝胶法通常对合成温度的要求不高,比物理方法经济[31]。研究表明,溶胶-凝胶法能很好地控制纳米材料的形状和大小[32-34]。
虽然纳米颗粒的应用取得了一些进展,但在控制纳米颗粒尺寸、稳定性、形状和分散性方面仍面临挑战,因为纳米颗粒的聚集影响了它们的高比表面积、高反应活性和杀菌性能[35-36]。现已有各种化学表面活性剂,如十二烷基硫酸钠(SDS)[37-38]和聚乙烯吡咯烷酮(PVP)[39]被用作纳米颗粒的稳定剂。尽管化学合成的表面活性剂和聚合物的应用广泛,但其为石油衍生产品,很难被生物降解,会对环境和生物造成危害[36,40]。使用生物表面活性剂作为封端剂是制造可持续、环保、具有生物相容性的金属纳米粒子的良好方法[36,41-42]。此外,生物表面活性剂具有生物相容性、低毒性及可在极端条件下应用的优点[36]。
本文研发了一种新的适用于油田污水破乳的新型绿色破乳药剂。将溶剂热法和溶胶凝胶法相结合,以铜绿假单胞菌发酵离心后的上清液为分散剂和稳定剂,上清液内含的活性成分生物表面活性剂为封端剂和分散剂,制备纳米级铁溶胶,在制备纳米金属氧化物的同时完成生物表面活性剂的包覆,使纳米颗粒有效分散,提高稳定性。
1 实验部分
1.1 材料与仪器
实验室自分离菌株T,属于铜绿假单胞菌,好氧菌属,在特定发酵培养基中产生物表面活性剂;水合柠檬酸(C6H8O7·H2O)、十二烷基硫酸钠(SDS)、NaCl、CaCl2、MgCl2、Na2SO4、NaHCO3,分析纯,上海国药集团化学试剂有限公司;九水合硝酸铁(Fe(NO3)3·9H2O),分析纯,上海晶纯生化科技股份有限公司;涠洲上岸油水混合物;发酵培养基,将20 g 蔗糖、7 g L-谷氨酸钠、6.8 g KH2PO4、0.5 g KCl、0.2 g MgSO4、11 mg FeSO4、0.5 mg MnSO4、0.09 mg ZnSO4、0.07 g CuSO4、1.4 g NaOH溶于1 L去离子水中,调节pH=7。
THZ-C 恒温摇床,常州金坛宏华仪器厂;HD-1360超净工作台,河南信陵仪器设备有限公司;LS-B50L 立式压力蒸汽灭菌器,江阴滨江医疗设备厂;H2050R 高速离心机,湘潭湘仪仪器有限公司;BSA224S电子分析天平,赛利斯科学仪器(北京)有限公司;PT-9030G 烘箱,广东普赛特电子科技股份有限公司;Zeiss SIGMA 场发射扫描电子显微镜(SEM),英国卡尔蔡司公司;傅立叶红外光谱分析仪(FTIR),美国Thermo公司;Bettersize2600激光粒度分布仪(湿法),深圳市力达信仪器有限公司;Zetasizer Nano ZSP纳米粒度电位仪,英国马尔文仪器有限公司;锐影Empyrean 粉末X 射线衍射仪(XRD),荷兰帕纳科公司;XH-C 涡旋混合器,金坛区白塔新宝仪器厂;HH.B11-500 电热恒温培养箱,天津市中环实验电炉有限公司;ALPHA1-2 真空冷冻干燥机,德国Chtist公司。
1.2 实验方法
(1)纳米级铁溶胶的制备
将特定发酵培养基在灭菌锅中于121 ℃下灭菌15 min,然后在超净台中接种菌株T,接种量为2%(体积分数)。将接种后的锥形瓶放入摇床中培养,培养条件为37 ℃、150 r/min、培养时间6 d。取发酵液以10 000 r/min 转速离心10 min 除去菌体,留上清液备用。
在100 mL 蒸馏水中加入3.84 g C6H8O7·H2O 和4 g Fe(NO3)3·9H2O,90 ℃水浴锅中持续老化16 h,与大气接触,合成铁溶胶。分别将水替换成20%~100%T 发酵上清液,观察其是否影响产物形貌和尺寸[43]。
(2)纳米级铁溶胶的表征
SEM测试。用无水乙醇对溶胶产物进行洗涤,每次洗涤后以4000 r/min 转速离心10 min,共3 次。离心结束后取少量样品滴加于抛光的硅片上,室温下置于空气中数分钟晾干,用SEM观察样品的形貌。
粒度和Zeta 电位测定。用无水乙醇洗涤以不同浓度发酵上清液作为溶剂制备的溶胶产物,4000 r/min 离心,重复3 次,取洗涤完成的样品进行Zeta电位测试;用超声波分散产物5 min,取样进行粒度测试。
FTIR测试。取适量样品于敞口玻璃瓶中,在烘箱中105 ℃干燥2 d,用FTIR 在4000~400 cm-1范围进行扫描。
XRD测试。将产物置于105 ℃干燥箱中烘干,得到粉末制品,用XRD进行广角扫描测试。
活性成分定量。根据T菌发酵上清液的红外光谱结果,确定用于合成铁溶胶的T 菌发酵上清液中的活性成分,并根据标准物质进行定量。
(3)破乳脱水率的测定
在1 L蒸馏水中加入17.787 g NaCl、1.143 CaCl2、0.864 MgCl2、0.133 Na2SO4、0.551 NaHCO3,配制成模拟地层水。称取微热后呈液体状态的涠洲上岸油水约400 mg,与1 L 模拟地层水混合均匀制得模拟污水。将各合成的干燥好的溶胶分别以400 mg/L的量加入乳化油水混合物中,其中空白组污水不加任何药剂,T组只加T菌发酵液离心后的上清液(仍按400 mg/L加量)。用涡旋仪震荡5 min,室温下静置24 h,观察脱出水色泽。根据石油天然气行业标准SY/T 5281—2000《原油破乳剂使用性能检测方法(瓶试法)》,记录脱水量和乳液中水的总量,计算破乳剂的脱水率[44]。
(4)破乳条件优化
破乳剂用量和涡旋时间不变,选取以上破乳实验脱水率最高的破乳剂组,缩短破乳实验时间至10、20、30 min,探索在恒定低温(10~30 ℃)下南海终端现场乳状液污水的破乳效果。
2 结果与讨论
2.1 发酵液浓度对铁溶胶的影响
根据不同浓度发酵液作溶剂反应产物的结果,可以看出空白组、20%、40%、60%发酵液组产物的颜色均为红黑色,主要组成成分相似,而80%和100%发酵液组产物的颜色分别为砖红色和卡其色,与前4组成分大不相同,表明发酵液作为溶剂,对溶剂热法合成铁溶胶产生了较大影响,且浓度改变,产物溶胶物质组分也发生改变。
2.2 表征结果
2.2.1 扫描电镜结果分析
以5 K倍放大,由图1可见,空白组中未加入发酵上清液,其产物为不规则形貌,表面较光滑,长径大于10 μm,体积较大。当溶剂为60%T发酵液时,用溶胶凝胶法合成的产物粒径为400~600 nm,主要为球形,大小不一致,上百个小颗粒聚集成为团簇,团簇间存在空洞使得颗粒分布不均一。当溶剂为80%T 发酵液时,用溶胶凝胶法合成的产物粒径可以达到200 nm左右,大量纳米小球被一层膜包裹紧密排列在一起,分散在溶胶中,颗粒间无明显孔隙,说明铁颗粒之间的分散程度可能与发酵液浓度有关。加入了100%T 发酵液制成的铁溶胶基本为类似于球状的小颗粒,产物形貌较一致,且这些小球均包裹着一层薄膜,成百上千个聚结在一起,呈大团簇状态,小球粒径基本全部在40~200 nm范围内。由此可见,该发酵液对纳米材料的合成产生了诱导和分散作用。这可能是由于细菌代谢物对铁溶胶的形貌和尺寸产生了影响,浓度越高,产生的纳米颗粒平均粒径越小,颗粒表面包覆的有机膜越厚,无水乙醇难以洗脱,纳米材料不易聚集。铁纳米材料表面的膜可能不是普通的物理包覆,而是通过化学键接枝聚合相连,或已形成新的共聚物。
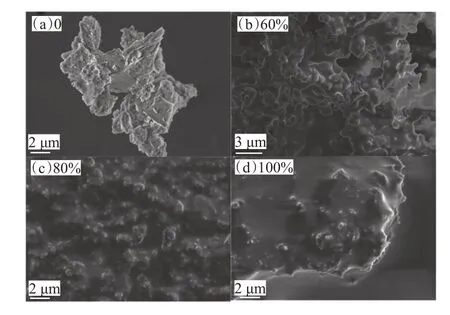
图1 不同浓度发酵液作为溶剂的产物SEM图
2.2.2 粒径和Zeta电位分析
由表1 可见,空白组和20%发酵液组的产物平均粒径均大于1 μm,空白组甚至达到27.5 μm,与该组SEM图显示结果较一致;而20%发酵液组产物的平均粒径为5.3 μm;40%、60%、80%、100%发酵液组产物的平均粒径均在700 nm 左右,与SEM 测定结果不太一致。这可能由于包覆的有机膜难以在超声波下分散开,因此测得的粒径偏大,且浓度越高的发酵上清液组,SEM测定结果与粒度仪测得的粒径结果相差越大。

表1 不同浓度发酵上清液作为溶剂的产物平均粒径和Zeta电位
80%和100%T 发酵液作为溶剂的产物Zeta 电位为正值,铁溶胶胶体颗粒带正电。根据样品产物的颜色,估计产物可能为Fe(OH)3、Fe3O4、Fe2O3。这两组产物的Zeta电位绝对值分别为10.6、6.5 mV,溶胶稳定性一般。0、20%、40%、60%T 发酵液作为溶剂合成的铁溶胶的Zeta 电位均为负值。根据胶体粒子带电性,可能生成了硫化亚铁或羟基氧化铁之类的物质,需进一步探究产物具体的组成成分。由此可知,铁溶胶产物的Zeta 电位正负性随着溶剂T发酵上清液含量的变化而变化,即产物成分和含量随发酵上清液中的有效成分(生物表面活性剂)含量的变化而变化。在胶体粒子电性相同时,即0~60%条件下,根据Zeta电位可以得知,60%组开始变得不稳定,0 和40%组稳定性一般,20%组产物的稳定性较好。这可能是由于20%发酵上清液包覆膜的厚度适中,既不会因为膜厚度较高而使颗粒团聚沉降,也比纯水作为溶剂(发酵上清液加量为0)组产物完全无膜包覆的稳定性高。从SEM 图中可以看出,纯水作溶剂的产物尺寸属于数十微米级,没有分散剂或改善分散状况的物质存在。
Zeta 电位依赖于粒子表面和分散剂的化学性质,是粒子间静电力相互作用的标尺,不受粒子尺寸的影响。Zeta 电位的影响因素有:pH 变化、电导率(由浓度、盐的类型决定)、组成成分(如高分子、表面活性剂)浓度的变化。这些溶胶产物均是由细菌发酵上清液作为溶剂合成的,因此Zeta电位测试结果不能完全确定胶体产物的稳定性。无法测定Zeta电位的实验组可能受产物中含有的表面活性剂影响。
2.2.3 傅里叶红外光谱分析
由图2 可见,T 细菌的发酵上清液干燥样品在3384.5 cm-1出现一个较宽的强吸收峰,表明存在O—H、N—H;2931.3 cm-1为糖类的特征峰;1579.4 cm-1附近为双键伸缩振动区;1407.8 cm-1处为脂肪酸碳链上C—H 键的伸缩振动峰;1114.7、1041.4 cm-1附近出现C—O和酯的特征峰,表明T发酵液上清液中含有糖脂类物质。该物质与已鉴定的鼠李糖脂的红外光谱[45]有差别,因此推断T 发酵产物为一种新型的糖脂类生物表面活性剂。

图2 T菌发酵上清液样品的红外光谱图
不同浓度T发酵液作为溶剂的条件下,柠檬酸和硝酸铁反应产物的红外吸收光谱图极其相似,可能有相同的特征官能团[46]。以60%T发酵上清液的红外光谱图(图3)为例,在3440.4 cm-1附近出现吸收峰,透过率较T 发酵上清液的3384.5 cm-1处有所下降,峰位置也有所偏移;合成产物在2626.6 cm-1出现了弱峰,可能是O=C=O;1729.9~1058.7 cm-1之间的峰均指向T发酵上清液的表面活性剂成分。指纹区内599.8~416.6 cm-1范围内的振动带表明存在Fe—O,说明产物中含有铁氧化物。
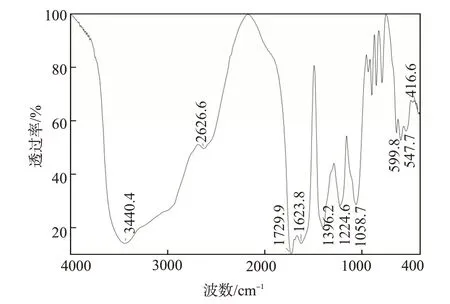
图3 以60% T发酵上清液为溶剂的产物的红外光谱图
2.2.4 XRD测试结果分析
合成产物的XRD 谱图表现为弥散峰。对比6个样品的XRD图可见,产物很有可能为相同或相似结构的铁溶胶,由于成分含量不一而呈现不同的颜色。经XRD 分析软件Jade6.5 拟合得出,不同浓度发酵液参与合成的铁溶胶物相及晶面。其中,部分三氧化二铁晶相为γ-Fe2O3,与四氧化三铁峰的位置重合,FeO(OH)与FeOOH 统一用FeO(OH)表示。通过半定量分析可以发现各组产物中含量较高的物质依次为Fe2O3、FeO(OH)、Fe3O4,另有Fe(OH)2、Fe、FeO也出现了特征峰,但含量较少。
根据上述实验结果,可以初步判定T 菌合成的生物表面活性剂为糖脂,即用于铁溶胶合成的活性成分为糖脂。用蒽酮-硫酸法测定发酵上清液中糖脂的总含量[47]。按1.2.1中的发酵条件,T菌在特定的发酵培养基中发酵6 d后,以10 000 r/min转速离心10 min,取上清液测得其糖脂含量为0.99~1.08 g/L。
2.3 破乳实验结果分析
乳化液震荡后,部分组上层出现澄清现象。震荡结束后于室温下放置24 h,60%组上清液的高度最大,破乳效果最好最稳定;不加药剂的空白组在该环境下不能自发破乳,加T 菌发酵上清液的组无明显破乳层。根据破乳层厚度(上清液高度)计算破乳系数,结果如表2所示。
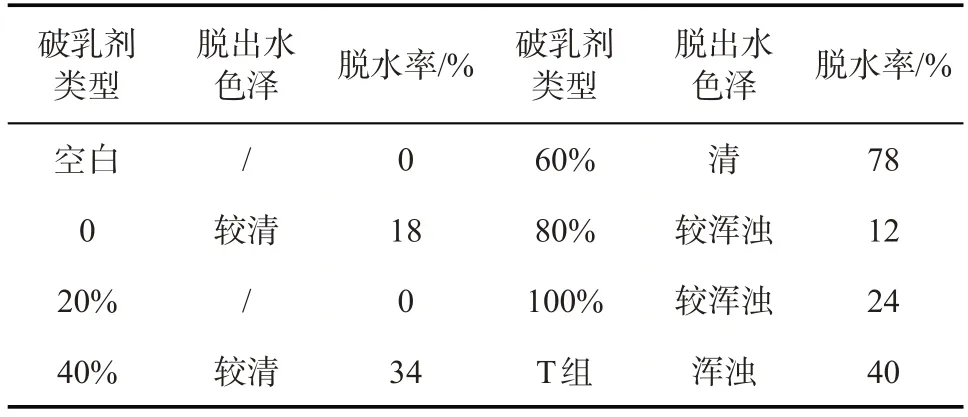
表2 不同比例T发酵液作为溶剂的铁溶胶对破乳效果的影响
破乳实验结果表明,纯水作为溶剂的铁溶胶对模拟油田污水具有一定的破乳效果,室温放置24 h后能保持在18%;发酵上清液(T 组)对乳化油水的破乳系数为40%,说明纯发酵上清液即表面活性剂对乳化油水也存在一定的破乳作用。加表面活性剂稳定的铁溶胶对模拟油田污水有不同程度的破乳影响。室温下能保持稳定破乳效果的有40%、60%、80%、100%发酵上清液组。其中效果优于纯水作为溶剂合成的溶胶的有40%、60%、100%发酵上清液组,且60%发酵上清液组合成的铁溶胶的破乳效果持久,在平均约10 ℃的温度下静置24 h 仍能保持78%的破乳系数,可以考虑后续用于低温油藏环境中的油水分离。由图1 可见,60%发酵上清液合成的产物中,铁颗粒表面包覆有机物较少,颗粒分明,与80%和100%发酵上清液组相比,颗粒之间分开程度高,没有以团簇形式被包裹,因此在投入乳化油水混合物中时,铁颗粒与乳状液的接触面积大,这可能是其破乳性能好的原因。另一方面,合成的生物表面活性剂稳定的铁溶胶结构可能随着发酵上清液中糖脂含量的变化而发生改变,整体来说由60%发酵上清液制备的铁溶胶产物的Zeta电位绝对值更低,因而比80%和100%发酵上清液组的纳米铁颗粒稳定,破乳效果更好。
本实验所用的T菌发酵液无需分离提纯即可直接应用于合成纳米铁溶胶,成本较低。工业级柠檬酸和硝酸铁价格分别约为295 元/500 g 和41 元/500 g,则合成1 g成品破乳剂约需成本0.3元。
选用60%发酵上清液合成的铁溶胶和南海终端现场污水作为待处理的乳化废水进行优化实验。破乳实验结果表明,按400 mg/L药剂投加后再涡旋5 min使其充分混合,污水温度为10、20、30 ℃时,静置20 min 均可使污水澄清,脱水率为100%,下层无沉淀和絮状物,破乳效果好。
3 结论与展望
以T菌株微生物在培养基中好氧培养6 d,取发酵离心上清液与水混合,分别制得体积比为0、20%、40%、60%、80%、100%的离心上清液,以上清液作为溶剂,采用溶剂热法和溶胶-凝胶法合成了生物表面活性剂稳定的铁溶胶。由于生物产表面活性剂有复杂的代谢途径,这些代谢途径可能会因环境的外部变化而发生突变,从而导致代谢产物产量的表述不明确。建议研究致突变物种以及控制方法,以进一步研究外部条件优化对生物内部代谢活性的影响。
制备的铁溶胶的主要无机相成分为铁氧化物Fe2O3、FeO(OH)、Fe3O4,铁颗粒外包覆的有机组分为一种新型的糖脂类生物表面活性剂。20%发酵上清液作溶剂时合成的铁溶胶的Zeta 电位电负性最强,胶体稳定性最高。
生物表面活性剂稳定的铁溶胶可以用于低温油水混合物的破乳,60%发酵上清液(糖脂)稳定的铁溶胶的破乳效果最好,低温下放置24 h后的破乳系数为78%,破乳效果好于纯水作溶剂合成的产物。表面活性剂的包覆增加了铁纳米的生物相容性,后续处理简单环保,可降低污染。用制备的破乳剂进行南海终端现场乳状液的破乳,效果明显。
制备纳米铁溶胶时使用离心后的发酵上清液,未全部利用发酵液中的培养基成分,如菌体蛋白等,后续也可单独研究其对纳米铁溶胶合成和稳定性的影响。未来应加强生物稳定破乳剂的研究,同时关注破乳后破乳材料的再生和可回收性,以期在污水处理尤其是破乳除油方面产生较稳定持久的效果,实现药剂残留对后续生化处理污水中有机污染物的微生物向无毒害化转变。

