顺序萃取法研究浸渍炭金属组分和防护反应产物
崔 洪,赵 晴,裴 佩,温宇慧
(山西新华防化装备研究院有限公司催化剂研究所,山西 太原 030008)
ASC型浸渍炭是一种防护化学毒剂和工业有毒有害气体的活性炭催化剂[1],负载不同含量的金属Cu、Cr和Ag。常采用浸渍法制备,将浸渍液成分(碱式碳酸铜、铬酸酐、硝酸银和碳酸铵的氨水溶液)负载到活性炭表面,经煅烧[(140~170) ℃]将浸渍物转化成更稳定的金属氧化物。一般认为,浸渍炭表面的金属氧化物可能包括CuCrO4·2CuO、CrO3、Cr2O3、CuO、Cu2O、Ag2O等物种[2-3],其中氧化态的Cu(Ⅱ)、Cr(Ⅵ)和Ag(Ⅰ)被公认是吸附和催化的活性金属形态[3],主要用来防护HCN、CNCl等难以通过物理吸附手段消除的酸性毒气。
ASC型浸渍炭对HCN和CNCl的防护是多种金属共同作用的结果,存在水解、酸碱中和、催化氧化等多种反应形式[3-9]。研究者[5,8,10]应用X射线光电子能谱技术对浸渍炭的表面进行分析,并结合其它方法来研究防护机理,认为导致其防护性能下降的原因有:(1)Cr(Ⅵ) 被还原成Cr(Ⅲ),表现为Cr6+/Cr3+比值的下降;(2)某些反应生成物沉积在炭表面,或覆盖了活性位点[8]。然而该结论仍缺乏来自体相元素或成分分析数据的支持。
本文以ASC型浸渍炭为调查对象,采用H2O-H2SO4和H2O-NaOH顺序萃取的方法,将浸渍炭或染毒(HCN和CNCl)浸渍炭表面的金属成分分类提取,再通过定性和定量分析,明确浸渍炭表面活性金属成分的形态,以及染毒后的金属成分形态变化和所出现的反应产物。
1 实验部分
1.1 样品制备方法
研究的样品主要包括实验室制备的ASC型浸渍炭、浸渍液(剂)和染毒浸渍炭等类型。样品及其制备方法见表1。
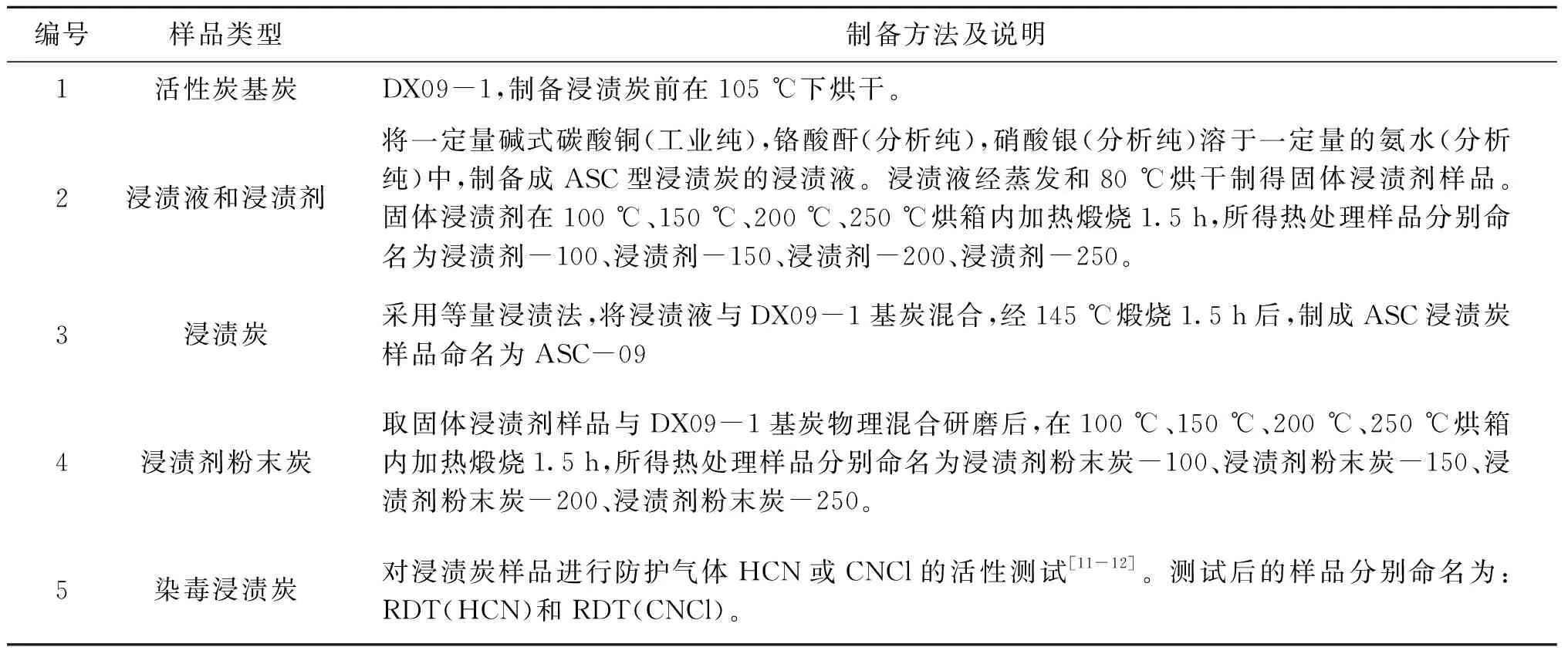
表1 样品及制备方法
1.2 样品萃取及分析方法
采用H2O-H2SO4和H2O-NaOH顺序萃取方法研究样品。萃取方法依次按照水萃取和酸(碱)萃取的顺序进行。萃取产物分别定义为“水溶态”、“酸溶态”和“碱溶态”,以及未萃取出的“残渣态”。
(1)水萃取。首先将固体样品研磨成粒度为(75~150) μm的粉末,并在105 ℃烘箱中干燥3 h。取粉末样品(0.1±0.000 1)g,置于100 mL聚乙烯离心管中,依次进行3次超声萃取和离心分离。第一次加40 mL去离子水,将离心管室温超声萃取40 min,再进行20 min(转速为4 000 r·min-1)的离心分离,取出上层清液,置于100 mL容量瓶中。第二次加入20 mL去离子水于离心管中,超声萃取40 min,离心分离20 min,取上层清液转移至100 mL容量瓶中。第三次萃取离心过程与第二次操作相同。将以上三次操作的萃取液在100 mL容量瓶中定容,作为水萃取液样品待分析。离心管中的水萃取残渣留待进行下一步的酸萃取或碱萃取。
(2)酸(碱)液萃取。将上述水溶剂替换为0.1 mol·L-1H2SO4溶液或0.1 mol·L-1NaOH溶液,对水萃取残渣重复以上相同的超声萃取和固液分离步骤,获得100 mL的酸(碱)萃取液和相对应的萃取残渣。
上述萃取样品、萃取液及萃取残渣中的金属(Cu、Cr和Ag)含量采用等离子体发射光谱仪(Thermo IRIS Intrepid Ⅱ XSP)进行测试。萃取过程的元素质量平衡按式1计算。

(1)
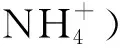
对浸渍炭、浸渍剂和浸渍剂粉末炭样品进行XRD分析。所用仪器为日本Rigaku Ultimate Ⅳ X射线衍射仪,扫描范围5°~60°,扫描速率10°·min-1,Cu Kα靶。XRD数据分析采用MDI JADE软件。
2 结果与讨论
2.1 浸渍炭表面的金属活性组分
2.1.1 浸渍炭表面金属活性组分的推测
在氨水体系中,ASC型浸渍炭所负载前驱物形态可以推断为铜氨络合物、碳酸氢铵、铬酸铵、银氨络合物。在(140~170) ℃空气煅烧环境中,这些前驱物会发生分解和氧化,在浸渍炭表面形成金属氧化物。在这些金属氧化物中,铜的氧化物分别有CuO和Cu2O两种形态。舒世立等[13]认为当煅烧温度较低时,铜主要是以CuO的形式出现,只有经高温(>300℃)处理,CuO才有可能被活性炭还原成Cu2O。胡玉良等[10]用XPS技术研究了浸渍炭中铜的氧化物形态,发现铜在浸渍炭表面以CuO的形式出现,在内部则以Cu2O形式出现。这也说明在活性炭内部,被活性炭包围的CuO可能更容易被还原成Cu2O。图1(A)和(B)分别是不同煅烧温度处理的浸渍剂(浸渍液的固体样品)和浸渍剂粉末炭(模拟浸渍炭配方)的XRD图。从图1可以发现,浸渍剂样品中主要成分是Cu(NH3)2CO3。在不同的煅烧温度下,Cu(NH3)2CO3的衍射峰(100 ℃)发生了变强(150 ℃)、变弱(200 ℃)和消失(250 ℃)的过程。浸渍剂粉末炭样品中的Cu(NH3)2CO3的衍射峰也出现了相似的历程。二者不同之处主要在于CuO衍射峰出现的温度。浸渍剂与活性炭粉末混合后,Cu(NH3)2CO3分解速率加快,CuO衍射峰出现的温度由250 ℃提前至200 ℃。另外,在图中没有发现与Cu2O相关的衍射峰。表明在浸渍炭煅烧环境和温度下,铜氧化物形态应该以CuO为主。
从图1还可以看出,浸渍剂和浸渍剂粉末炭样品XRD图中都没有出现含Cr和Ag的组分,包括浸渍炭(ASC-09)XRD图也没有。这可能是由于浸渍炭表面的金属氧化物分散均匀、结晶度差或者所形成晶粒太小的缘故[13]。Smith J W H等[14]认为粒度为(12±1) nm的CuO会出现显著的X射线衍射峰,但当颗粒尺寸小于(5±1) nm时,CuO的衍射峰会变宽且强度变弱,甚至无法辨析。
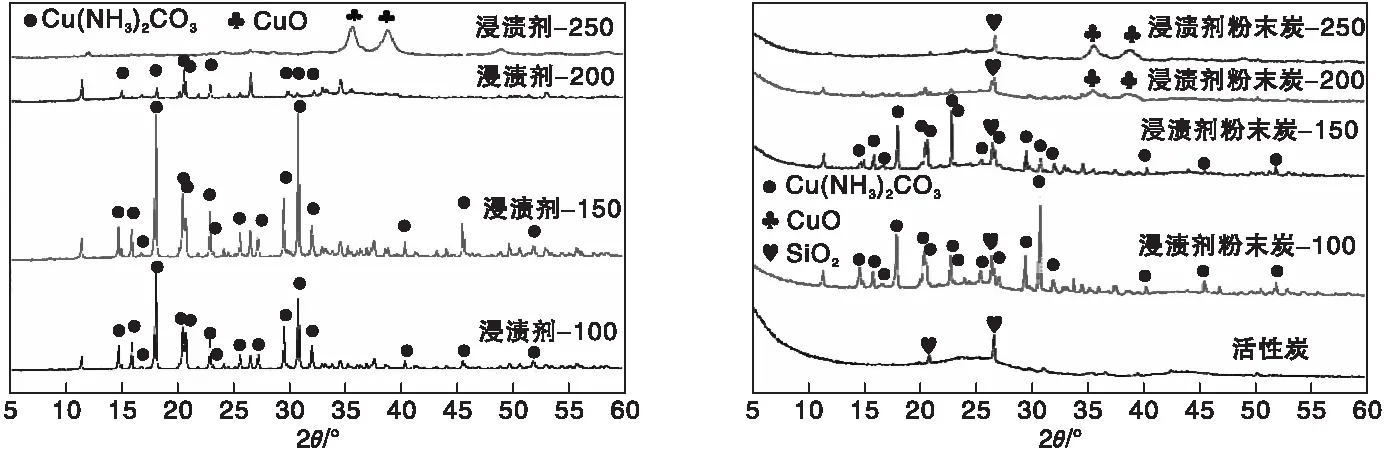
图1 不同煅烧温度下浸渍剂和浸渍剂粉末炭样品的XRD图Figure 1 XRD patterns of the impregnant and the impregnant powder activated carbon calcinated at varied temperatures
铬的氧化物[15-17]分别有CrO、Cr2O3和CrO3三种形态。浸渍液中的前驱物是铬酸酐(CrO3),在氨水环境中会以铬酸铵[(NH4)2CrO4]的形式存在。铬酸铵负载到活性炭表面后,经煅烧重新分解为CrO3。由于CrO3具有强氧化性,在活性炭表面也有可能部分被还原成Cr2O3。Cr2O3不溶于水,与酸反应,微溶于碱液,因此可通过顺序萃取的方法将Cr2O3与CrO3区分开。CrO因具有强还原性,在浸渍炭制备条件下生成的可能性极低。
银的氧化物主要是Ag2O。前驱物AgNO3在氨水中会形成银氨络合物[Ag(NH3)2OH],然后在空气煅烧过程中分解为AgOH和NH3,AgOH又进一步分解为Ag2O。
表2为浸渍炭ASC-09表面可能存在的金属前驱物煅烧后的氧化物,以及相对于H2O、H2SO4和NaOH溶液的可溶解能力。

表2 浸渍炭ASC-09样品表面负载的金属前驱物和煅烧后的氧化物形态
2.1.2 对浸渍炭表面金属活性组分的顺序萃取
对浸渍炭ASC-09的顺序萃取结果见表3,并按照式(1)计算出金属(Cu、Cr和Ag)在各萃取阶段的质量平衡数据在98.7%~108.3%之间。将表3的数据进行归一化处理,得到金属组分在各萃取产物中的百分含量分布,结果见表4。
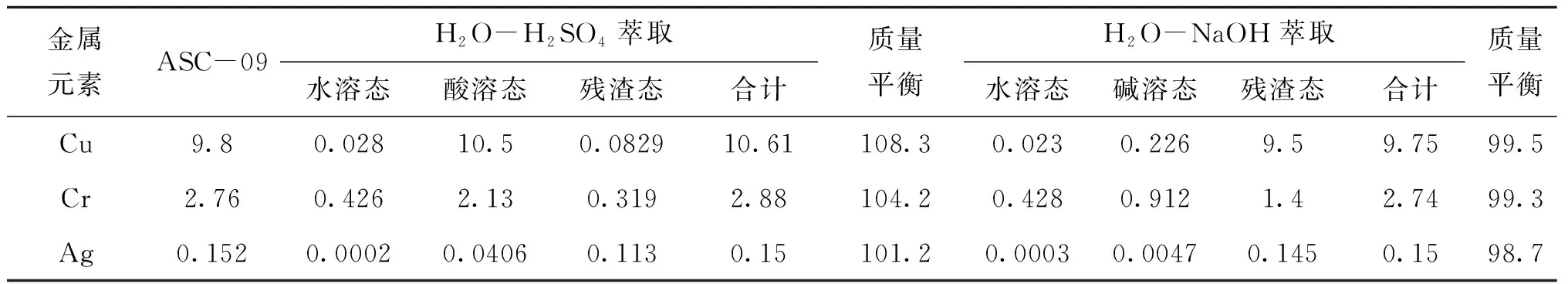
表3 顺序萃取产物中的金属含量(g·100g-浸渍炭-1)及质量平衡(%)
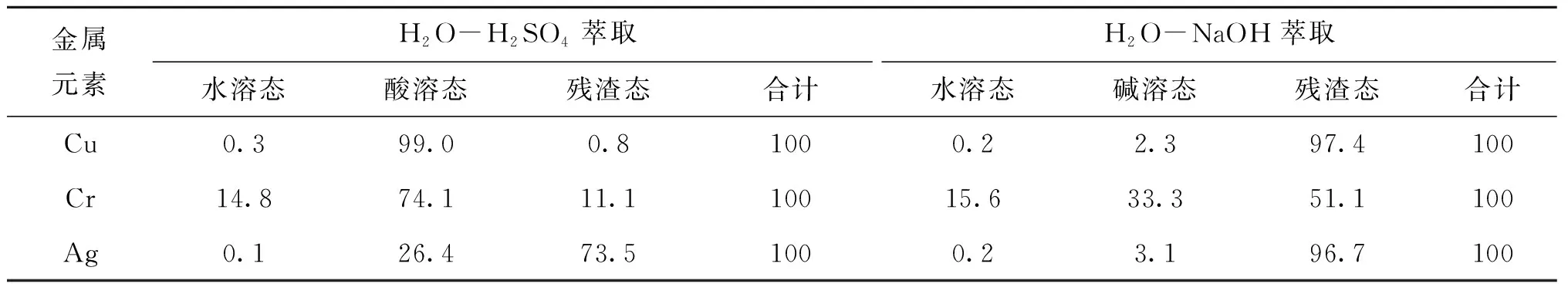
表4 萃取产物中的各金属形态的含量分布(归一化处理,%)
表4数据表明,负载在浸渍炭ASC-09表面的Cu几乎不溶于水,其中有99%的Cu属“酸溶态”,2.3%的Cu属“碱溶态”。由此可以判定浸渍炭表面的Cu组分主要是CuO。由于有2.3%的“碱溶态”Cu的出现,所以也不排除少量Cu(NH3)2CO3存在的可能性。

元素Ag的“水溶态”极少,说明其前驱物银氨络合物已转化为酸溶的氧化物(26.4%)Ag2O,而酸不溶部分(73.5%的残渣态)可推测为单质Ag。因此,Ag的最终转化形态除了氧化态Ag2O之外,还存在单质态的Ag。
由以上分析可以推测出,浸渍炭ASC-09负载的元素Cu以CuO为主,元素Ag以Ag2O和Ag为主,元素Cr存在有CrO3和Cr2O3两种形态,其中CrO3以(NH4)2CrO4的形式存在。另外,从“水溶态”金属的含量分布来看,元素Cu和Ag的前驱物在煅烧阶段分解基本完全,而元素Cr的前驱物(NH4)2CrO4未能完全分解,仍有部分留存在浸渍炭表面。
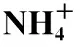
表5 对浸渍炭ASC-09水萃取产物中Cr和的分析结果(g·100g-浸渍炭-1)
2.2 染毒浸渍炭表面的金属活性组分及反应产物
表6是浸渍炭ASC-09染毒(HCN 或CNCl)前后“水溶态”组分的元素含量和浓度。
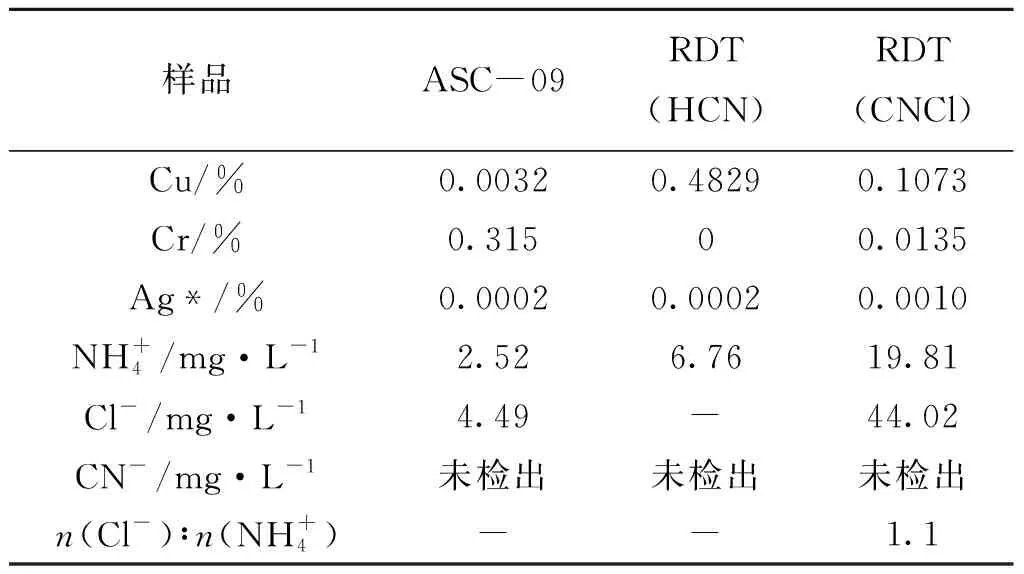
表6 浸渍炭ASC-09染毒(HCN 或CNCl)前后“水溶态”组分的元素含量(%)和浓度(mg·L-1)
2.2.1 对HCN的防护
文献[4,6,18]对ASC浸渍炭防护HCN的机理描述不尽相同,但对CuO在防护HCN过程中扮演反应物和催化剂的二元角色并无异议。一般认为,CuO和HCN首先会反应生成不稳定的Cu(CN)2,然后形成CuCN,释放出(CN)2,随后(CN)2水解生成异氰酸(HOCN)和氢氰酸(HCN)。所发生的化学反应如式(2)和式(3)所示。

(2)

(3)
生成的异氰酸(HOCN)在Cu2+/Cr6+催化体系下,或水解后形成有机胺,如草酰胺[4];或形成甲酸铵(HCOONH4)[6];或直接生成CO2和NH3[18]。
同时,Cr6+也会按照式(4)被还原成Cr3+。

(4)
因此,HCN的演变路径可以简化为:
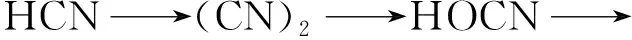
(5)
从以上反应可以看到,活性金属Cr和Cu都会发生相应的化学变化。

以上分析验证了浸渍炭在防护HCN过程中CrO3向Cr2O3的转化和有机胺或铵盐的生成。另外还发现CuO不仅与HCN反应生成CuCN,而且还生成一种非氰化物类型的离子化合物。这一新产物的发现和验证将进一步完善和补充浸渍炭防护HCN的反应机理和途径。
2.2.2 对CNCl的防护
浸渍炭在防护CNCl气体的反应路径与HCN的类似,也是多种金属共同作用的结果。首先,CNCl在ASC浸渍炭表面在金属离子Cu2+/Cr6+的催化下发生以下水解反应[7]:
(6)
随后,异氰酸(HOCN)进一步被催化水解生成NH3和H2O,而HCl可与浸渍炭中的NH4HCO3、CuO和Cr2O3发生反应,生成NH4Cl、CuCl2和CrCl3等氯化物。
从表6可以看到,浸渍炭在防护CNCl毒剂后,浸渍炭中“水溶态”Cu的含量从0.0032%上升到0.1073%,这可归因于水溶性CuCl2的生成。浸渍炭中的“水溶态”Cr含量从0.315%下降到0.0135%,表明部分水溶性的Cr6+被还原成了不溶于水的Cr3+。虽然CrCl3也是水溶性的,但仍需其它实验证据对CrCl3生成的确认。

3 结 论


