全氟化合物在北江顺德水道表层水、悬浮颗粒物以及沉积物中的污染特征及风险评估
乔 磊, 张汝频, 杨 余, 冉 勇*
全氟化合物在北江顺德水道表层水、悬浮颗粒物以及沉积物中的污染特征及风险评估
乔 磊1, 2, 张汝频1, 2, 杨 余1, 冉 勇1*
(1. 中国科学院 广州地球化学研究所, 有机地球化学国家重点实验室/广东省环境资源利用与保护重点实验室, 广东 广州 510640; 2. 中国科学院大学, 北京 100049)
在北江顺德水道采集表层水、悬浮颗粒物(SPM)和沉积物样品, 分析其中全氟化合物(PFASs)的残留水平和污染特征。结果表明, 溶解相、悬浮颗粒相以及沉积物中∑PFASs的浓度范围分别为135~192、96.7~185、0.794~2.26 ng/g。溶解相以全氟辛酸(PFOA)为主, 贡献率为91.7%~95.0%; SPM以PFOA和全氟癸酸(PFDA)为主; 沉积物以PFOA和全氟辛烷磺酸(PFOS)为主。中短链PFASs更多存在于溶解相中随着水流迁移, 长链PFASs则更易与SPM以及沉积物结合。与其他河流相比, 北江顺德水道中PFASs处于中等污染水平。周边的电器工厂和货轮码头可能是区域水环境PFASs的重要来源。此外, 北江顺德水道暂无水生生态风险, 但按照较严格的饮用水PFASs健康参考值, 该水域作为饮用水源地存在一定程度的健康风险。
全氟化合物; 北江顺德水道; 表层水; 悬浮颗粒物; 沉积物; 污染特征; 危害评估
0 引 言
全氟化合物(perfluoroalkyl substances, PFASs)是一类由人工合成的有机物, 它们通常被用于防水织物、纸制品、日常消费品、消防和清洗溶液等领域(Nguyen et al., 2017)。PFASs由非极性的全氟碳链和阴离子官能团组成, 其中C链上与C原子连接的H原子完全或部分被F原子取代。高能的碳氟共轭键使得PFASs难以受亲核物质攻击, 从而具有热稳定性和化学稳定性。同时疏水疏油的全氟碳链和亲水性的带电基团使得PFASs成为了良好的表面活性剂。全氟羧酸(PFCAs)和全氟磺酸(PFSAs)是两大类主要的全氟化合物。由于PFASs具有难降解性和良好的水溶性, 它可通过自然水体进行远距离运输, 并能借助食物链在生物体内积累、放大。各种环境介质中都有PFASs的残留检出(Ahrens et al., 2009; Naile et al., 2010), 使其受到人们的日益关注。水环境中PFASs主要来源于工业废水和生活污水的排放。研究表明, 拥有部分官能团和特定链长的PFASs具有生殖毒性、神经毒性等特性和干扰人体内分泌的作用。2009年5月, 《斯德哥尔摩公约》将全氟辛烷磺酸(PFOS)及其盐类加入了持久性有机污染物的行列, 也因此PFOS等PFASs由于对人类的潜在危害性引起了全球范围内的广泛关注。近年来, 我国实体经济发展良好, 许多行业大量使用全氟化合物, 与其相关的环境问题也日趋严重(Xie et al., 2013b)。
大部分PFASs在正常环境的pH值下会发生离解, 形成离子型PFASs。离子型PFASs的蒸气压低、溶解性高, 使水体成为PFASs在环境中的重要汇集介质(Prevedouros et al., 2006), 因此了解PFASs在水环境中的分布特征显得尤为重要。珠江流域是中国南部最大的河网, 珠江河口是河网的交汇口, 连接着珠江流域和中国南海。珠江三角洲的经济快速发展已经产生了大量污染物。同时, 这个进程也涉及了工业中PFASs的集约化生产、使用和处置, 因此区域水环境PFASs污染是不可避免的(Xie et al., 2013b)。So et al. (2007)在对珠江流域水体中PFASs的污染调查发现, 东江(东莞段)的∑PFASs浓度为95.0 ng/L, 是整个珠江流域水系中污染最高的河段。在炊具制造过程中, 特氟龙(聚四氟乙烯)被用作不粘锅涂料(Xie et al., 2013a), 而佛山市顺德区是全球最大的电饭煲供应基地。但到目前为止, 针对北江顺德水道的PFASs研究仍然相对匮乏。
饮用水的PFASs污染主要是由于水源地的污染和饮用水处理工艺的局限性。去除PFASs的方法有吸附法、膜分离法、高级氧化法和生物去除等, 其中用于自来水中去除PFASs的方法主要是活性炭吸附、纳滤和反渗透。但是目前的自来水处理工艺并不能有效去除PFASs。例如李玉娜(2019)在对天津某自来水处理厂的研究中发现, ∑PFASs的去除效率仅为11.3%; 张鸿等(2013)对深圳某自来水处理厂进行调研, 发现出水∑PFASs浓度高出原水的10%~44%, 尽管此厂的水处理工艺中包含活性炭吸附。
本研究对北江顺德水道水体中11种目标PFASs进行测定, 探讨它们在不同介质中的分配特征和污染来源, 并对其危害进行风险评价, 希望为该河段和同类水体今后的水环境保护提供详实基础资料。
1 材料和方法
1.1 标准样品和试剂
11种PFASs标准溶液和2种内标(加拿大Wellington实验室), 包括PFHpA、PFOA、PFNA、PFDA、PFUnDA、PFDoDA、PFBS、PFHS、PFOS、PFDS、FOSA和13C标记的PFOA和PFOS(表1)。所有分析标准品的纯度均≥98%。在整个实验过程中使用Milli-Q纯净水, 甲醇(HPLC级)购自Merck(德国), 醋酸铵(HPLC级)纯度≥97%。
1.2 样品采集与处理
本研究于2019年12月进行野外采样, 在北江顺德水道的8个采样点采集8个表层水、8个悬浮颗粒物(suspended particles material, SPM)和6个表层沉积物样品(图1; 表2)。每个采样点取10 L表层水(水深0.5 m处), 收集在聚丙烯(PP)瓶中。带回实验室后, 过0.45 μm玻璃纤维滤膜(GFF, GC/C, Whatman,=142 mm), 收集SPM样品。取500 mL过膜水样, 加入2.5 ng内标(13C4PFOA和13C4PFOS), 过HLB固相萃取柱(6 mL, 500 mg), 然后用5 mL、20%甲醇水溶液清除杂质, 真空抽至干燥。用10 mL的甲醇洗脱目标化合物, 洗脱液使用N2吹干, 再用500 μL甲醇复溶, 过0.22 μm有机相针式滤膜。最后将溶解相转移到1 mL PP瓶中, 进行高效液相色谱–串联质谱分析。

表1 目标全氟化合物的物理化学性质
注: NA. 未报道。

图1 北江顺德水道采样点图
1.3 色谱分析
色谱分析采用高效液相色谱–串联三重四级杆质谱仪(Agilent 1200-HPLC 6460-TQMS)。色谱柱为Thermo FisherTMBETASIL C18柱(2.1 mm×50 mm×5 μm)。在流动相通过BETASIL C18色谱柱之前, 使用AgilentTMZORBAX SB-C8(2.1 mm×50 mm×3.5 μm)除去溶剂杂质。流动相分别为甲醇(流动相A)和2 mmol/L醋酸铵水溶液(流动相B), 流速为250 μL/min。梯度洗脱, 洗脱程序为, 初始状态: 10%流动相A; 0~0.1 min: 35%流动相A; 0.1~7 min: 35%~55%流动相A; 7~17 min: 55%~95%流动相A; 17~18 min: 95%流动相A; 18~20 min: 95%~100%流动相A。柱温保持在40 ℃, 进样体积为10.0 μL, 采用电喷雾电离源(ESI), 动态多反应监测模式(DMRM)检测, 扫描负离子, 脱溶剂气流速为800 L/h, 碰撞气(Ar)流量为0.15 mL/min, 毛细管电压为3.0 kV, 锥孔气流量为30 L/h, 脱溶剂温度为500 ℃, 离子源温度为150 ℃。
1.4 质量控制与保证
整个实验过程避免聚四氟乙烯材质的器皿, 以降低PFASs的背景值。样品检测同时以超纯水作为空白基质完成方法空白, 所有空白样品的浓度均低于定量限。11种PFASs在0.05~200 μg/L范围的线性相关系数()为0.996~0.999, 检测限在0.030~0.080 ng/L。3种环境介质样品中11种PFASs的加标回收率在61%~125%, 符合分析要求(60%~140%)。
1.5 危害商
如果在一个水样中同时检测到了多种PFASs, 并且多种PFASs对人体的危害反应终端相同, 那可以通过计算危害商(hazard index, HI)来表示多种PFASs的饮用水综合风险, 当HI超过1时, 说明需要采取措施对饮用水水质进行管理。研究表明多种PFASs的生物体危害反应终端有一定程度的吻合, 故通过计算危害商来估算PFASs的饮用水综合风险(Zhuang et al., 2014)。危害商的计算方法为: HI=∑(单个PFAS的浓度/对应的饮用水健康参考值)。

表2 北江顺德水道采样点信息
1.6 统计分析
样品浓度介于检出限和定量限之间计为0.5倍定量限浓度, 用Pearson相关系数分析样品中各类PFASs浓度的相关性, 用SPSS软件分析数据。
2 结果与讨论
2.1 顺德水道环境介质中PFASs污染水平
2.1.1 溶解相中PFASs
从PFASs的浓度水平来看, 顺德水道中∑PFASs浓度为135~192 ng/L, 平均值为164 ng/L, 且所有站点的浓度分布较平均, 并无显著差别。除了PFUnDA未检出外, 其余10种PFASs均不同程度地检出, 其中长链PFCAs的检出率明显低于其他化合物。6种PFASs(PFHpA、PFOA、PFBS、PFHS、PFOS、FOSA)在所有样品中都被检出。PFOA是顺德水道溶解相中最主要的PFASs, 贡献率在91.7%~95.0%(图2)。佛山顺德地区分布着密集的电器工业园, 高浓度的PFOA可能来源于其工业生产过程中的污水排放。同时, PFOA的直接排放可能不是其在环境中被检出高浓度的唯一原因, 来自其前体物质的降解也起到了一定的贡献。PFOS是仅次于PFOA的化合物, 平均贡献率为3.53%。
顺德水道表层水中PFASs的浓度水平高于文献报道的中国长江和黄河流域、德国易北河、越南河流以及瑞典河流等(Theobald et al., 2011; Pan et al., 2014; Zhao et al., 2016; Lam et al., 2017; Nguyen et al., 2017), 与日本南坎河、大阪河、图千河以及东京湾流域等相当(Tseng et al., 2006; Takagi et al., 2008; Pignotti et al., 2017), 但低于污染较为严重的日本鹤见川流域和西班牙略布雷加特河流域(Zushi et al., 2008, 2011; Pignotti et al., 2017)(表3)。总体来说, 本研究表层水中PFASs的污染处于中等水平。
2.1.2 悬浮颗粒相中PFASs
顺德水道SPM中PFASs的总浓度为96.7~185 ng/g (干重), 平均浓度为133 ng/g。同样, SPM中也未检出PFUnDA, 但是相比于溶解相, 其他长链PFCAs的检出率有所提高。从化合物组成来看, PFOA和PFOS是SPM中主要的PFASs, 平均浓度分别是48.1 ng/g和46.3 ng/g。与溶解相比, PFDA、PFNA和PFDoDA的比例有所增加。BJ 5站点SPM中检测出高浓度PFDoDA(88.0 ng/g; 图3), 表明该站点附近存在负载高浓度PFDoDA的点源污染。BJ 5站点上游的勒流港是国家二级口岸, 有大量的货轮来往, 是潜在的PFASs污染来源。根据单位换算后的结果, 表层水中超过99%的PFASs分布在溶解相中, 结合在SPM中的不足1%, 符合之前的研究(Zushi et al., 2012; Chen et al., 2015; Munoz et al., 2015; Liu Y Q et al., 2019), 但是其中有44.2%的较长链PFCAs(C10~12)结合在SPM中, 所以忽略悬浮颗粒相, 可能使得水中长链PFCAs的含量被严重低估。
本研究SPM中的PFASs浓度高于法国的Gironde河口以及我国的黄河与辽河流域(Chen et al., 2015; Munoz et al., 2015; Zhao et al., 2016), 但低于日本的东京湾流域和我国的渤海湾流域(Zushi et al., 2012; Liu Y Q et al., 2019)。在全球范围内, 北江顺德水道SPM中PFASs处于中等污染水平。
2.1.3 表层沉积相中PFASs
沉积物中PFASs的浓度低了2个数量级, 总浓度为0.790~2.26 ng/g, 平均浓度为1.38 ng/g。11种目标化合物均有不同程度地检出。PFOA和PFDA是沉积物中主要的PFASs, 平均浓度分别是0.453 ng/g和0.353 ng/g。相比于SPM, PFHpA和PFBS的比例略有上升。BJ 4站点检出较高浓度的PFDoDA(图4), 可能是受到上游BJ 5站点的点源污染影响, 一部分高PFDoDA负荷的颗粒物沉降到了表层沉积物中。根据碳链长度把PFASs分成3类, 全氟碳链数≤6为短链, 碳链数≥11为长链, 6<碳链数<11为中链。本研究在北江水体中检出的PFASs多为中短链, 长链的检出率和残留水平都较低, 与前人研究一致(Taniyasu et al., 2005), 可能是由于相比于长链, 中短链PFASs具有高水溶性和低logow, 因此在水体中迁移能力更强, 且长链PFASs更易结合在SPM和沉积物上(Ahrens et al., 2010; Liu Y Q et al., 2019)。

图2 北江顺德水道表层水中PFASs浓度和分布
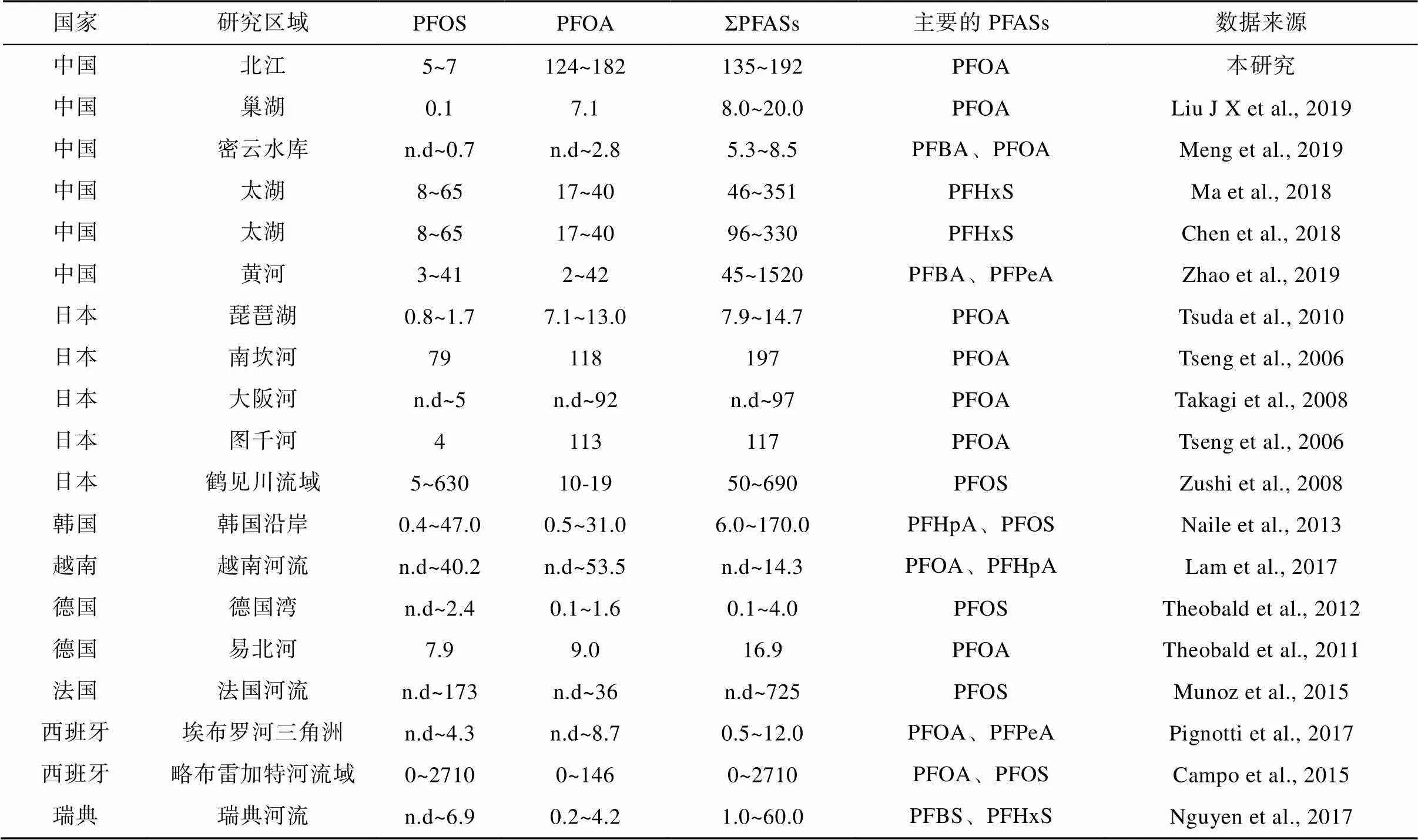
表3 国内外河流表层水中PFOA和PFOS浓度(ng/L)
注: n.d. 未检出。
本研究表层沉积物中PFASs的污染水平低于大多数其他淡水水体沉积物(Corsolini et al., 2012; Naile et al., 2013; Munoz et al., 2015; White et al., 2015; Zhao et al., 2016; Chen et al., 2018), 但与越南河流、中国长江与辽河流域等沉积物相近(Pan et al., 2014; Chen et al., 2015; Lam et al., 2017)。从全球角度看, 北江顺德水道表层沉积物中的PFASs处于较低污染水平。
2.2 北江顺德水道中PFASs的水生生态以及人类健康危害
Yang et al. (2014)根据美国环保局发布的水质标准计算方法推导中国水生系统中PFOA和PFOS的最大浓度基准值(criteria maximum concentration, CMC)和持续浓度基准值(criteria continuous concentration, CCC),PFOA的CMC和CCC分别为45.54和3.52 mg/L, PFOS的CMC和CCC分别为3.78和0.25 mg/L。本研究水体中PFOA和PFOS浓度远远低于其对应的基准值, 表明本次采样期间北江顺德水道中PFASs对区域水生生态系统危害较小。
PFASs主要存在于水相中, 通过直接饮用的方式从水环境进入人体, 然而目前的自来水处理工艺不能有效去除PFASs。很多国家和地区制定了饮用水中PFASs的健康参考浓度, 例如美国的明尼苏达州、新泽西州和新罕布什尔州对饮用水中PFASs的浓度要求最为严格, 设置的健康参考浓度低于其他地区和美国环保局的建议值。北江是周边地区的饮用水源地, 是居民日常用水的重要来源。本研究PFOS浓度低于表4中所有健康参考值, PFOA浓度低于英国、德国和加拿大的健康参考值, 高于美国明尼苏达州、新泽西州、新罕布什尔州和美国环保局设置的值。通过计算危害商评估PFASs对人体健康的风险, 发现根据严格的水质健康参考标准, 该区域水体的HI远超过1(表4), 表明北江顺德水道作为饮用水源地存在一定程度的健康风险。

图3 北江顺德水道SPM中PFASs浓度和分布
Fig.3 Concentrations and distribution of PFASs in the SPM from the Shunde Waterway of the Beijiang River
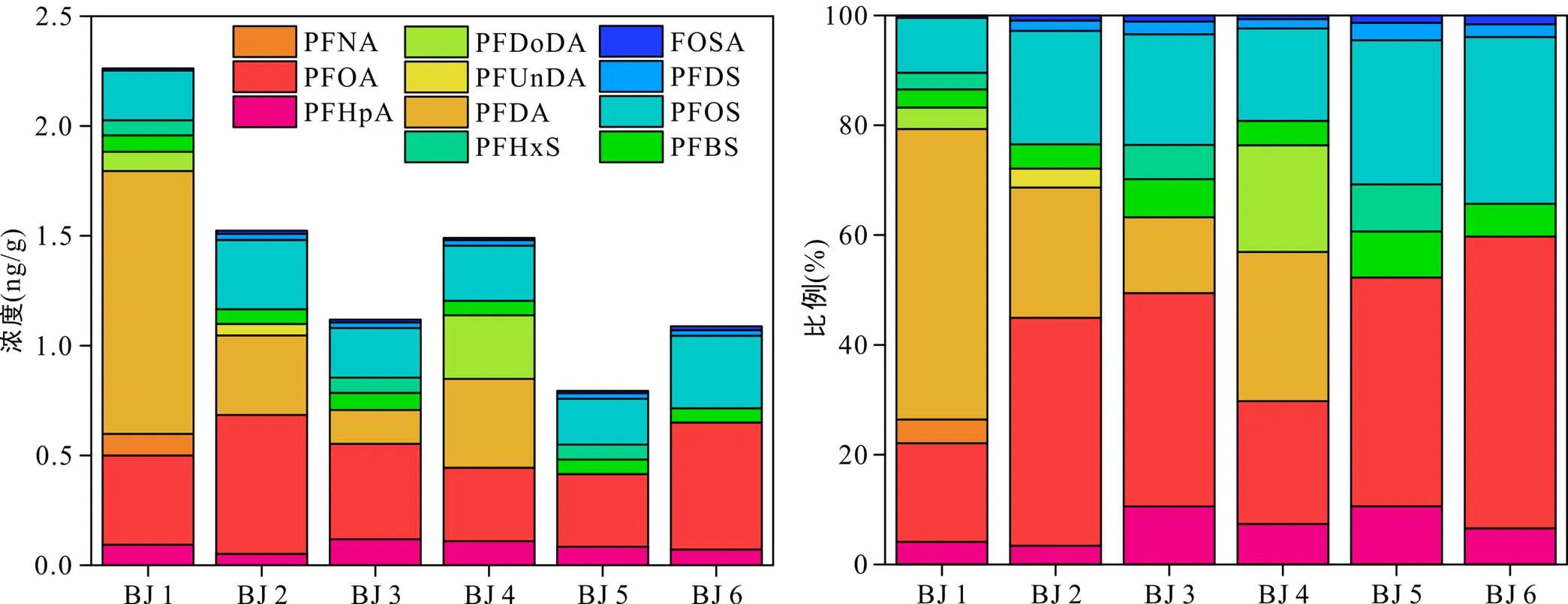
图4 北江顺德水道表层沉积物中PFASs浓度和分布

表4 PFASs在饮用水中的健康参考值以及表层水中的平均浓度(ng/L)和危害商
注: ND. 无数据。
3 结 论
(1) 北江顺德水道的溶解相和悬浮颗粒相中存在中等程度的PFASs污染, 但表层沉积物中PFASs的污染水平较低。其中, 中短链PFASs更多地存在于溶解相中, 长链则更易于悬浮颗粒物以及沉积物结合。
(2) 研究水域附近的电器工厂和货轮码头可能是水环境中PFASs的重要来源。
(3) 北江顺德水道中PFASs对区域水生生态系统危害较小。但是, 按照较严格的饮用水健康参考值, 该水域作为饮用水源地仍存在一定的健康风险。
致谢:感谢中国科学院广州地球化学研究所毕新慧研究员和另一位匿名审稿专家对本文提出的宝贵意见。
李玉娜. 2019. 全氟和多氟化合物在自来水中的污染特征及净水工艺的去除影响研究. 天津: 南开大学硕士学位论文: 109–110.
张鸿, 陈清武, 王鑫璇, 柴之芳, 沈金灿, 杨波. 2013. 自来水处理工艺对溶解相中全氟化合物残留的影响. 环境科学, 3467–3473.
Ahrens L, Siebert U, Ebinghaus R. 2009. Total body burden and tissue distribution of polyfluorinated compounds in harbor seals (Phoca vitulina) from the German Bight., 58(4): 520–525.
Ahrens L, Taniyasu S, Yeung L W Y, Yamashita N, Lam P K S, Ebinghaus R. 2010. Distribution of polyfluoroalkyl compounds in water, suspended particulate matter and sediment from Tokyo Bay, Japan., 79(3): 266–272.
Campo J, Perez F, Masia A, Pico Y, Farre M, Barcelo D. 2015. Perfluoroalkyl substance contamination of the Llobregat River ecosystem (Mediterranean area, NE Spain)., 503: 48–57.
Chen M, Wang Q, Shan G Q, Zhu L Y, Yang L P, Liu M L. 2018. Occurrence, partitioning and bioaccumulation of emerging and legacy per- and polyfluoroalkyl substances in Taihu Lake, China., 634: 251–259.
Chen X W, Zhu L Y, Pan X Y, Fang S H, Zhang Y F, Yang L P. 2015. Isomeric specific partitioning behaviors of perfluoroalkyl substances in water dissolved phase, suspended particulate matters and sediments in Liao River Basin and Taihu Lake, China., 80: 235–244.
Corsolini S, Sarkar S K, Guerranti C, Bhattacharya B D, Rakshit D, Jonathan M P, Godhantaraman N. 2012. Perfluorinated compounds in surficial sediments of the Ganges River and adjacent Sundarban mangrove wetland, India., 64(12): 2829–2833.
Lam N H, Cho C R, Kannan K, Cho H S. 2017. A nationwide survey of perfluorinated alkyl substances in waters, sediment and biota collected from aquatic environment in Vietnam: Distributions and bioconcentration profiles., 323: 116–127.
Liu J X, Zhong G W, Li W, Avendano S M. 2019. Isomer- specific biotransformation of perfluoroalkyl sulfonamidecompounds in aerobic soil., 651: 766–774.
Liu Y Q, Zhang Y, Li J F, Wu N, Li W P, Niu Z G. 2019. Distribution, partitioning behavior and positive matrix factorization-based source analysis of legacy and emerging polyfluorinated alkyl substances in the dissolved phase, surface sediment and suspended particulate matter aroundcoastal areas of Bohai Bay, China., 246: 34–44.
Ma X X, Shan G Q, Chen M, Zhao J Y, Zhu L Y. 2018. Riverine inputs and source tracing of perfluoroalkyl substances (PFASs) in Taihu Lake, China., 612: 18–25.
Meng J, Liu S F, Zhou Y Q, Wang T Y. 2019. Are perfluoroalkyl substances in water and fish from drinking water source the major pathways towards human health risk?, 181: 194–201.
Munoz G, Giraudel J L, Botta F, Lestremau F, Devier M H, Budzinski H, Labadie P. 2015. Spatial distribution and partitioning behavior of selected poly- and perfluoroalkylsubstances in freshwater ecosystems: A French nationwide survey., 517: 48–56.
Naile J E, Khim J S, Hong S, Park J, Kwon B O, Ryu J S, Hwang J H, Jones P D, Giesy J P. 2013. Distributions and bioconcentration characteristics of perfluorinated compounds in environmental samples collected from the west coast of Korea., 90(2): 387–394.
Naile J E, Khim J S, Wang T Y, Chen C L, Luo W, Kwond B-O, Park J, Koh C-H, Jones P D, Lu Y L, Giesy J P. 2010. Perfluorinated compounds in water, sediment, soil and biota from estuarine and coastal areas of Korea., 158(5): 1237–1244.
Nguyen M A, Wiberg K, Ribeli E, Josefsson S, Futter M, Gustavsson J, Ahrens L. 2017. Spatial distribution and source tracing of per- and polyfluoroalkyl substances (PFASs) in surface water in Northern Europe., 220: 1438–1446.
Pan C G, Ying G G, Zhao J L, Liu Y S, Jiang Y X, Zhang Q Q. 2014. Spatiotemporal distribution and mass loadings of perfluoroalkyl substances in the Yangtze River of China., 493: 580–587.
Pignotti E, Casas G, Llorca M, Tellbuscher A, Almeida D, Dinelli E, Farre M, Barcelo D. 2017. Seasonal variations in the occurrence of perfluoroalkyl substances in water, sediment and fish samples from Ebro Delta (Catalonia, Spain)., 607: 933–943.
Prevedouros K, Cusins I T, Buck R C, Korzeniowski S H. 2006. Sources, fate and transport of perfluorocarboxylates., 40(1): 32–44.
So M K, Miyake Y, Yeung W Y, Ho Y M, Taniyasu S, Rostkowski P, Yamashita N, Zhou B S, Shi X J, Wang J X, Giesy J P, Yu H, Lam P K S. 2007. Perfluorinated compounds in the Pearl River and Yangtze River of China., 68(11): 2085–2095.
Takagi S, Adachi F, Miyano K, Koizumi Y, Tanaka H, Mimura M, Watanabe I, Tanabe S, Kannan K. 2008. Perfluorooctanesulfonate and perfluorooctanoate in raw and treated tap water from Osaka, Japan., 72(10): 1409–1412.
Taniyasu S, Kannan K, So M K, Gulkowska A, Sinclair E, Okazawa T, Yamashita N. 2005. Analysis of fluorotelomeralcohols, fluorotelorner acids, and short- and long-chain perfluorinated acids in water and biota., 1093(1–2): 89–97.
Theobald N, Caliebe C, Gerwinski W, Huhnerfuss H, Lepom P. 2011. Occurrence of perfluorinated organic acids in the North and Baltic seas. Part 1: Distribution in sea water., 18(7): 1057–1069.
Theobald N, Caliebe C, Gerwinski W, Huhnerfuss H, Lepom P. 2012. Occurrence of perfluorinated organic acids in the North and Baltic Seas. Part 2: Distribution in sediments., 19(2): 313–324.
Tseng C L, Liu L L, Chen C M, Ding W H. 2006. Analysis of perfluorooctanesulfonate and related fluorochemicals in water and biological tissue samples by liquid chromatography-ion trap mass spectrometry., 1105(1–2): 119–126.
Tsuda T, Inoue A, Igawa T, Tanaka K. 2010. Seasonal Changes of PFOS and PFOA Concentrations in Lake Biwa Water., 85(6): 593–597.
White N D, Balthis L, Kannan K, De Silva A O, Wu Q, French K M, Daugomah J, Spencer C. Fair P A. 2015. Elevated levels of perfluoroalkyl substances in estuarine sediments of Charleston, SC., 521: 79–89.
Xie S W, Lu Y L, Wang T Y, Liu S J, Jones K, Sweetman A. 2013a. Estimation of PFOS emission from domestic sources in the eastern coastal region of China., 59: 336–343.
Xie S W, Wang T Y, Liu S J, Jones K C, Sweetman A J, Lu Y L. 2013b. Industrial source identification and emission estimation of perfluorooctane sulfonate in China., 52: 1–8.
Yang S W, Xu F F, Wu F C, Wang S R, Zheng B H. 2014. Development of PFOS and PFOA criteria for the protection of freshwater aquatic life in China., 470–471: 677–683.
Zhao J, Xia X H, Dong J W, Xia N, Jiang X M, Li Y, Zhu Y M. 2016. Short- and long-chain perfluoroalkyl substances in the water, suspended particulate matter, and surface sediment of a turbid river., 568: 57–65.
Zhuang P, Lu H P, Li Z H, Zou B, McBride M B. 2014. Multiple exposure and effects assessment of heavy metals in the population near mining area in South China., 9(4), e94484.
Zushi Y, Takeda T, Masunaga S. 2008. Existence of nonpoint source of perfluorinated compounds and their loads in the Tsurumi River basin, Japan., 71(8): 1566–1573.
Zushi Y, Ye F, Motegi M, Nojiri K, Hosono S, Suzuki T, Kosugi Y, Yaguchi K, Masunaga S. 2011. Spatially detailed survey on pollution by multiple perfluorinated compounds in the Tokyo Bay Basin of Japan., 45(7): 2887–2893.
Zushi Y, Ye F, Motegi M, Nojiri K, Hosono S, Suzuki T, Kosugi Y, Yaguchi K, Masunaga S. 2012. Spatial distribution and loading amounts of particle sorbed and dissolved perfluorinated compounds in the basin of Tokyo Bay., 88(11): 1353–1357.
Pollution characteristics and risk assessment of perfluoroalkyl substances in surface water, suspended particulate matter, and sediment in the Shunde Waterway of the Beijiang River
QIAO Lei1, 2, ZHANG Rupin1, 2, YANG Yu1, RAN Yong1*
(1. State Key Laboratory of Organic Geochemistry / Guangdong Key Laboratory of Environment and Resources, Guangzhou Institute of Geochemistry, Chinese Academy of Sciences, Guangzhou 510640, Guangdong, China; 2. University of Chinese Academy of Sciences, Beijing 100049, China)
To investigate the residual levels and pollution characteristics of 11 perfluoroalkyl substances (PFASs), water, suspended particulate matter (SPM), and sediment samples were collected from the Beijiang River (Shunde section).The results showed that the concentration ranges of ∑PFASs in dissolved phase, SPM, and sediment were 135–192 ng/L, 96.7–185 ng/g, and 0.794–2.26 ng/g, respectively. Perfluorooctanoic acid (PFOA) was the most frequently detected compound in the dissolved phases, and its contribution ratio was between 91.7% and 95.0%. SPM was dominated by PFOA and perfluorodecanoic acid (PFDA), while the sediments were dominated by PFOA and perfluorooctanesulfonicacid (PFOS). Short- and medium-chain PFASs are more abundant in the dissolved phase and can migrate with water flow, while long-chain PFASs bind more easily to SPM and sediments. Compared with other studies, PFASs in the Shunde Waterway of the Beijiang River had a moderate pollution level. The surrounding electrical factories and cargo terminals may be important sources of PFASs in this region. Additionally, the Shunde Waterway of the Beijiang River shows no aquatic ecological risk. However, according to the stricter drinking water health advisories, PFASs in the Shunde Waterway of the Beijiang River, a source of drinking water, may cause potential health problems.
perfluoroalkyl substances; Shunde Waterway of the Beijiang River; surface water; suspended particulate matter; sediment; pollution characteristics; hazard assessment
X142; X522
A
0379-1726(2022)06-0617-08
10.19700/j.0379-1726.2022.06.001
2020-10-12;
2020-11-04
国家自然科学基金和广东省的重点联合项目(U1701244)、国家自然科学基金项目(41473103)、广东省科学技术计划基金项目(2017B030314057)和国家重点实验室专项基金会项目(SKLOGA201603B)联合资助。
乔磊(1994–), 男, 硕士研究生, 环境科学专业。E-mail: 350554733@qq.com
冉勇(1963–), 男, 研究员, 主要从事有机污染物研究。E-mail: yran@gig.ac.cn

