阿比特龙联合泼尼松治疗mCRPC患者的疗效及安全性
周克斌,林佳伟,赵留存
西安市第九医院泌尿外科,陕西 西安 710054
前列腺癌是一种临床上常见的男性泌尿生殖系统疾病,该病早期通常无特异性的症状表现,导致大多数患者在就诊时已处于病情中晚期,失去了接受根治性手术的机会[1]。且有研究在实践中也发现,较多前列腺癌患者在接受去势治疗后,病情会出现复发或者持续性进展,此类患者被称作转移性去势抵抗性前列腺癌(mCRPC)[2]。目前针对mCRPC的确切发病机制仍不明确,尚未有特效的治疗方案,较为常用的药物包括泼尼松、多西他赛等,但它们在总体疗效方面尚有待提升[3]。阿比特龙属于一种CYP17抑制剂,是新型的抗雄激素药物,近年来关于其在前列腺癌患者中的疗效受到了较多临床关注[4-5]。本研究旨在探讨新型抗雄激素药物阿比特龙联合泼尼松治疗mCRPC患者的疗效及安全性,现报道如下:
1 资料与方法
1.1 一般资料选择2019年10月至2021年10月西安市第九医院泌尿外科收治的90例mCRPC患者为研究对象。纳入标准:(1)经过病理标本检查诊断为前列腺癌,且患者接受雄激素剥夺治疗失败,即雄激素剥夺治疗1周后,连续3次、间隔2周的前列腺特异性抗原(PSA)检查结果升高,则可确诊为mCRPC[6];(2)年龄50~80岁;(3)预计生存周期≥6个月。排除标准:(1)合并其余恶性肿瘤;(2)合并机体重要组织器官功能障碍;(3)合并垂体功能障碍、肾上腺皮质功能障碍;(4)血液系统功能异常、免疫功能障碍;(5)精神系统、认知功能异常。按照随机数表法将患者分为观察组和对照组,每组45例。两组患者的基线资料情况比较差异均无统计学意义(P>0.05),具有可比性,见表1。本研究经医院医学伦理委员会批准,所有患者均签署研究知情同意书。
表1 两组患者的基线资料比较[±s,例(%)]

表1 两组患者的基线资料比较[±s,例(%)]
组别观察组对照组χ2/t值P值例数45 45年龄(岁)70.94±6.72 71.62±5.88 0.511 0.611病程(年)2.48±0.52 2.55±0.47 0.670 0.505 Gleason评分(分)8.46±1.58 8.42±1.67 0.117 0.907骨转移36(80.00)34(75.56)0.257 0.612淋巴结转移13(28.89)14(31.11)0.053 0.818
1.2 治疗方法对照组患者采用泼尼松片(规格5 mg,厂家:浙江仙琚制药股份有限公司,国药准字H33021207)治疗,5 mg/次,2次/d。观察组患者在对照组治疗的基础上联合阿比特龙片(规格0.25 g,厂家:Patheon Inc.,批准文号H20150264)治疗,1 g/次,1次/d。两组患者均以21 d为一个疗程,连续治疗两个疗程。
1.3 观察指标与评价方法(1)临床疗效:比较两组患者治疗两个疗程后的临床疗效。疗效评价方法[7]:完全缓解,血清PSA水平正常,结果0~4 ng/mL;部分缓解,血清PSA水平和治疗前相比降低程度≥50%;稳定,血清PSA水平和治疗前相比降低≥25%且<50%;进展,血清PSA水平和治疗前相比降低程度不足25%或者升高;总有效率=完全缓解+部分缓解。(2)血清PSA、睾酮水平:采集治疗前、治疗两个疗程后两组患者的空腹静脉血标本5 mL,常规离心处理,转速3 500 r/min、半径10 cm,时间15 min,收集上层血清液,使用酶联免疫吸附法测定血清PSA水平,使用放射免疫法测定睾酮水平。(3)排尿情况:记录两组患者治疗前、治疗两个疗程后的最大尿流率(Qmax)和残余尿量,其中最大尿流率使用尿流率计测定,残余尿量指患者排尿后膀胱内所残余的尿量,使用导尿管导出后进行测定。(4)安全性:记录两组患者治疗过程中的不良反应,包括高血压、低钾血症、乏力、恶心呕吐、皮疹等。
1.4 统计学方法应用SPSS26.0软件包进行数据统计学分析。计量资料以均数±标准差(±s)表示,组间比较采用t检验,计数资料比较采用χ2检验。以P<0.05表示差异具有统计学意义。
2 结果
2.1 两组患者的临床疗效比较观察组患者的临床疗效总有效率为82.22%,明显高于对照组的62.22%,差异有统计学意义(χ2=4.486,P=0.034<0.05),见表2。

表2 两组患者的临床疗效比较(例)
2.2 两组患者治疗前后的血清PSA、睾酮水平比较治疗后,两组患者的血清PSA、睾酮水平明显低于治疗前,且观察组患者血清PSA、睾酮水平明显低于对照组,差异均有统计学意义(P<0.05),见表3。
表3 两组患者治疗前后的血清PSA、睾酮水平比较(±s,ng/mL)
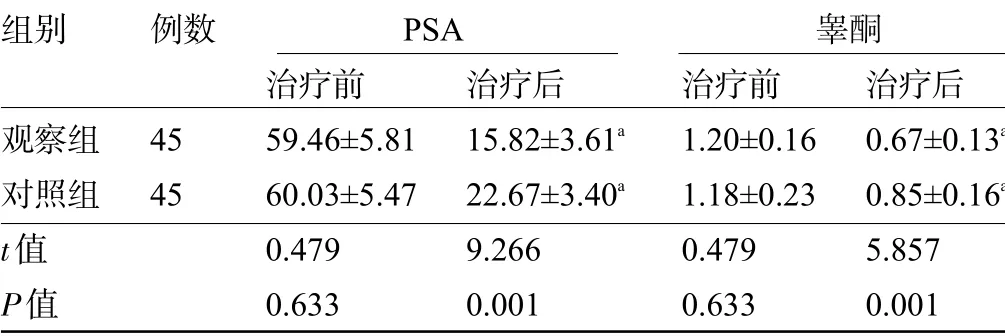
表3 两组患者治疗前后的血清PSA、睾酮水平比较(±s,ng/mL)
注:与本组治疗前比较,aP<0.05。
组别观察组对照组t值P值例数45 45治疗前59.46±5.81 60.03±5.47 0.479 0.633治疗后15.82±3.61a 22.67±3.40a 9.266 0.001治疗前1.20±0.16 1.18±0.23 0.479 0.633治疗后0.67±0.13a 0.85±0.16a 5.857 0.001 PSA 睾酮
2.3 两组患者治疗前后的排尿情况比较治疗后,两组患者的Qmax明显高于治疗前,残余尿量明显低于治疗前,且观察组患者的Qmax明显高于对照组,残余尿量明显低于对照组,差异均有统计学意义(P<0.05),见表4。
表4 两组患者治疗前后的排尿情况比较(±s)
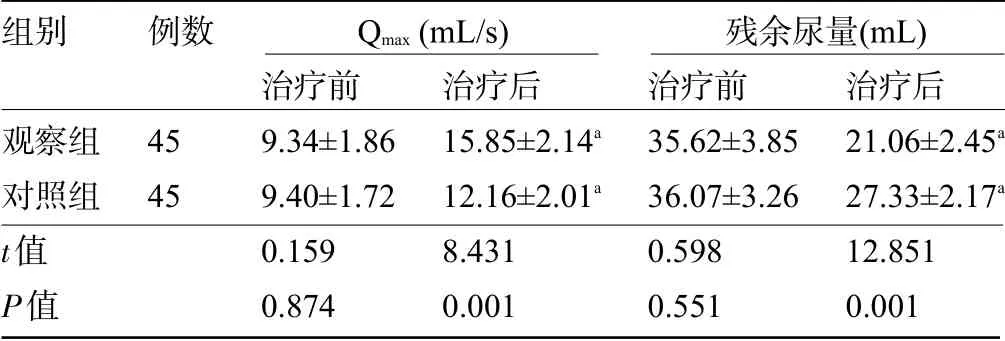
表4 两组患者治疗前后的排尿情况比较(±s)
注:与本组治疗前比较,aP<0.05。
组别观察组对照组t值P值例数45 45治疗前9.34±1.86 9.40±1.72 0.159 0.874治疗后15.85±2.14a 12.16±2.01a 8.431 0.001治疗前35.62±3.85 36.07±3.26 0.598 0.551治疗后21.06±2.45a 27.33±2.17a 12.851 0.001 Qmax(mL/s) 残余尿量(mL)
2.4 两组患者的不良反应比较观察组患者的不良反应总发生率为17.78%,略高于对照组的13.33%,但差异无统计学意义(χ2=0.338,P=0.561>0.05),见表5。

表5 两组患者的不良反应比较(例)
3 讨论
前列腺癌是一种对男性生殖健康有着严重威胁的恶性肿瘤,发病部位主要位于前列腺上皮组织,但多数患者在就诊时无法接受根治性手术治疗,只能选择去势治疗,然而mCRPC是前列腺癌患者去势治疗后难以避免的一个结局,可进一步增加临床治疗难度[8-9]。化疗是mCRPC患者较为常用的方案,虽然在延长生存时间上有较好的作用,但前列腺癌患者多数年龄较高、机体基础情况较差,化疗所带来的不良反应较多,部分患者可由于难以耐受不良反应而停药,导致总体疗效降低。因此在目前临床上多选择泼尼松治疗mCRPC,和化疗药物相比,化疗安全性更好,但单用的疗效尚有待提升[10-11]。由此可见,寻找一种疗效及安全性均较好的方案治疗mCRPC患者显得十分重要。
有研究认为,mCRPC患者血清睾酮在达到去势水平之后,仍然可通过肾上腺轴等性腺外的途径生成雄激素,在此过程中CYP17占据着重要地位。CYP17属于CYP/CYP450的家族成员,主要存在于肾上腺、睾丸、前列腺癌细胞之中,其能够催化孕激素、孕烯醇酮等物质,促使雄激素合成[12-13]。阿比特龙则是一种CYP17抑制剂,对CYP17具有选择性抑制作用,可直接抑制雄激素合成过程。国外有研究指出,mCRPC患者使用阿比特龙治疗后可明显获益,可作为患者化疗后的一种替代治疗方案或者二线治疗方案[14]。也有报道显示,1 000 mg/d的阿比特龙持续性治疗可降低50%~57%mCRPC患者的血清PSA水平,抑制疾病进展[15]。
本研究结果显示,联合阿比特龙治疗的患者血清PSA、睾酮水平、Qmax、残余尿量改善情况更明显,且临床疗效总有效率为82.22%,总体效果满意。主要原因是阿比特龙在进入机体后,能够水解成具有活性的代谢产物,并对CYP17A1酶的活性产生选择性抑制作用,积极阻断雄激素合成作用和睾酮向双氢睾酮的转化过程,且其对肿瘤合成、肾上腺来源的雄激素生成过程也能产生阻断作用,积极抑制雄激素生成,加上泼尼松抑制结缔组织增生的作用,两种药物之间相互协同,进一步发挥抗肿瘤目的,积极改善患者的排尿症状。此外,本研究结果也发现,联合阿比特龙治疗的患者在不良反应方面未明显增加,这和既往研究结果具有相似性[16],也显示出阿比特龙在mCRPC患者的应用中具有安全性。但由于本研究纳入的患者普遍年龄较高,考虑化疗所带来的不良反应,因此在治疗方案上面未选择多西他赛进行治疗,但在今后的试验中,还需继续开展更多组别、多用药方案的对比,且本研究时间较短,未能观察对患者更远期生存率的影响,今后也将持续性验证阿比特龙的疗效及安全性。
综上所述,新型抗雄激素药物阿比特龙联合泼尼松治疗mCRPC患者有助于促进疾病恢复,改善排尿情况,临床治疗效果满意,且安全性好。

